Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Medicina Experimental y Salud Publica
versión impresa ISSN 1726-4634
Rev. perú. med. exp. salud publica v.1 n.1-2 Lima oct. 1942
TRABAJOS ORIGINALES
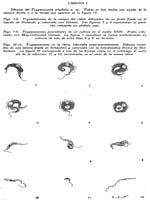
Trypanosoma Phyllotis n. sp. e infecciones asociadas en una titira, el Phlebotomus Noguchii Arístides Herrer A. 1 1 Departamento de Entomología Médica del Instituto Nacional de Higiene y Salud Pública, Lima. SUMARIO Se describe un nuevo trypanosoma, procedente de dos especies peruanas de Phyllotis, para el que se propone el nombre de Tripanosoma phyllotis. Se estudia su morfología, cultivo e inoculabilidad a la rata blanca, el cobayo y una tercer especie de Phyllotis. Se sabe que el Phlebotomus noguchii mantiene ciertas relaciones ecológicas con varios roedores salvajes, en especial con los del género Phyllotis, sobre los que se alimenta usualmente. Este insecto con frecuencia también es infectado al estado natural por el T. phyllotis n. sp. Las infecciones del P. noguchii se han reproducido experimentalmente en el laboratorio. INTRODUCCIÓN En tesis presentada en 1941 (7) ante la Facultad de Ciencias de la Universidad Mayor de San Marcos, se daba cuenta del hallazgo de dos especies de trypanosomas y varios otros hemoparásitos en roedores del género Phyllotis procedentes de las zonas verrucógenas de Santa Eulalia y el Rímac. Se trataba detenidamente acerca de las localidades donde se hallaron las tres especies de Phyllotis que se señalaba provisionalmente como Phyllotis sp., P. darwini limatus y P. amicus amicus (?). Se indicaba que solo uno de los citados trypanosomas habíase logrado cultivar, el que se estudiaba en cuanto a su morfología, cultivo e inoculación experimental, del mismo modo qué se hacía una ligera reseña sobre la infección del Phlebotomus noguchii por este hemoflagelado. Se decía entonces que cuando menos dos especies distintas de Phyllotis se habían encontrado naturalmente infectadas, el P. darwini limatus y el Phyllotis sp., encontrada esta última especialmente en la localidad de Tornamesa (kilómetro 63 de la Carretera Central; altura 1513 m.) Posteriores estudios nos han mostrado que las tres especies de Phyllotis señaladas anteriormente son sensibles al trypanosoma descrito entonces en forma preliminar. También ahora tenemos una idea mas exacta sobre la duración de la infección en su huésped vertebrado, la presencia del parásito en otros lugares, algunos pormenores sobre la infección del Phlebotomus noguchii por dicho flagelado, etc. Por tales razones y en vista de no haber encontrado la menor referencia sobre trypanosomiasis en Phyllotis, en esta ocasión lo vamos a describir como una especie nueva, utilizando gran parte de lo ya expuesto en la tesis mencionada. TRIPANOSOMA PHYLLOTIS n. sp. Descripción: Trypanosoma no patógeno encontrado en dos especies peruanas de Phyllotis, de 47µ de longitud y 6µ de ancho. Membrana ondulante y flagelo libre bien desarrollados. Núcleo voluminoso, esférica, y de posición ligeramente anterior; kinetoplasto de forma arriñonada o ligeramente ovoide. Escaso movimiento de traslación. Fácilmente cultivable y sin rosetas en los cultivos. Natural y experimentalmente infecta al Phlebotomus noguchii, en el que experimenta una notable tras formación morfológica, dando lugar como término final a una forma de critidia delgada y extensa, 35µ x 2µ. Localidad tipo: Tornamesa, provincia de Huarochirí, departamento de Lima, Perú. Infección natural en su huésped vertebrado. Dos especies de Phyllotis, que habitan lugares comprendidos entre 1000 y 1800 metros de altura, han sido encontradas infectadas en algunos de los sitiosdonde fueron capturadas: 1) el P. darwini limatus, únicamente en la localidad de Oscolla (kilómetro 61 de la Carretera; altura más o menos 1460 m.); y 2) el Phyllotis sp., se ha encontrado infectado en las siguientes localidades: Oscolla, Tornamesa, Puente Carrión (frente al kilómetro 67; altura 1760 m.), del Valle del Rímac; y en Huallanca (Km. 135 del Ferrocarril de. Chimbote, a Huallanca; altura, 1300 m.), en el Valle del Santa. Dos ejemplares de cada especie procedentes del Valle de Lurín (La Palma, altura 1250 m.), se mostraron negativos en observaciones fresco de la sangre, periférica. En 40 especímenes observados especialmente por medio de preparaciones frescas de la sangre del rabo o la oreja, se encontró infectados aproximadamente el 50 por ciento. La infección es sumamente ligera. En los casos de mayor parsitismo no se pudo contar mas de 10-12 trypanosomaspor preparación,hechas con laminillas de 20 x 20 mm. Muchas veces es necesario recurrir al hemocultivo para revelar la infección, ya que debido a su escasa intensidad se hace casi imposible ponerla de manifiesto por medio de frotises u observaciones frescas de sangre. El tiempo que dura la infección natural es relativamente largo. En varias ocasiones ratones conservados en el laboratorio durante 3-4 meses la mostraban todavía y en un caso se obtuvo cultivo positivo de un Phyllotis ocho meses después de su captura. Nunca se logró ver formas en división, por mas de haberlo buscado tanto en la sangre como también en los órganos internos. MORFOLOGÍA Forma. En frotises de sangre hemos conseguido con el Giemsa excelentes coloraciones del parásito, después de fijarse en el líquido de Hollande. Con el May-Grünwald Giemsa también se obtiene buenas preparaciones. De manera general conviene hacer los frotises no muy delgados y con frecuencia usar gotas gruesas de control ya que el trypanosoma se deforma fácilmente. En frotises coloreados se puede observar, a primera vista, la gran curvatura del parásito, con ambas extremidades terminadas en punta. El grado de curvatura es variable y una forma más o menos recta (Fig. 1) parece constituir excepción. Con frecuencia los dos extremos se cruzan, encerrando uno o dos glóbulos al centro (Figs. 5 y 6), actitud ésta mas frecuente y fácil de observarla en preparaciones frescas. Hay veces en las que todo el cuerpo sufre una doble curvatura dando al parásito una forma que podría asimilarse a una S, existiendo casos, también, en los que se nota, una triple curvatura, etc. Cuando las láminas son coloreadas con Giemsa, el protoplasma, se presenta azul oscuro, notándose algunas veces algo vacuolado. El núcleo, esférico u ovoide, es bastante voluminoso y por lo general se colorea de un rosado claro, muchas veces difícil de distinguirlo, siendo su posición ligeramente anterior. El kinetoplasto es relativamente pequeño, de forma ligeramente ovoide. Se colorea de azul intenso y siempre se encuentra pegado al borde externo, siendo a veces casi marginal y por lo general está mas cerca del núcleo que del extremo posterior. No se diferencia cuerpo parabasal y blefaroplasto y, alrededor del kinetoplasto, especialmente hacia el lado por donde se origina la membrana ondulante, se nota con nitidez un espacio claro o vacuola. La membrana ondulante es amplia, con un número considerable de ondulaciones, las que frecuentemente varían entre tres y ocho, y sólo excepcionalmente atraviesa el cuerpo de un lado a otro. En las muestras que están algo deformadas es frecuente ver la membrana ondulante casi pegada al borde del cuerpo. Dimensiones. Las dimensiones medias, obtenidas en 30 trypanosomas, son: longitud, incluyendo el flagelo libre, 47µ; ancho, 6 µ, sin tomar en cuenta la membrana ondulante y determinada a la altura del núcleo. Las dimensiones parciales son las siguientes: del extremo posterior al kinetoplasto 13.2 µ Movilidad. Observando una preparación fresca de sangre convenientemente infectada resulta por demás característico el escaso movimiento de traslación que se nota. Con aumentos bajos (100 x) el parásito puede ser localizado sin dificultad debido a su gran tamaño y al movimiento de la membrana ondulante y el del flagelo libre, pero, como se acaba de indicar, sin trasladarse de un campo microscópico a otro con la facilidad que lo hacen otros trypanosomas de roedores. Sucede con frecuencia, que un trypanosoma enfocado a inmersión (1000 x) suele permanecer en el mismo campo 8 ó 10 minutos. En tales preparaciones en fresco, corrientemente se les observa con ambas extremidades cruzadas formando el borde interno de su cuerpo un círculo dentro del cual muchas veces se encuentran encerrados algunos glóbulos (uno o dos, normalmente) al mismo tiempo que el movimiento de la membrana ondulante, la que en tales circunstancias se distingue con claridad, y el del flagelo libre, alborotan activamente los glóbulos adyacentes. Sólo al trasladarse a otro campo abandona, momentáneamente esta característica actitud, se endereza ligeramente y se desliza con lentitud ondulando todo el cuerpo. CULTIVO Es de fácil cultivo en los medios artificiales. En nuestros ensayos hemos encontrado que se desarrolla satisfactoriamente en los medios ZWF (26, 27), NNN, el semisólido de Noguchi para leptospira y el de Bonacci (1). Respecto al tejido embrionario para el medio ZWF, nos han dado igual resultado el embrión de ratón y el de pollo. Observaciones especiales sobre el cultivo se han realizado sólo en los medios leptospira y NNN. Cultivo en el medio NNN. Después de tres o cuatro días, a la temperatura de 28ºC., macroscópicamente ya se puede notar el desarrollo en este medio, distinguiéndose entonces las colonias sobre la superficie sólida del medio a manera de pequeños puntitos, ofreciendo un aspecto finamente granular si las colonias son abundantes. Después de los ocho o diez días se observa con facilidad que son circulares, de bordes lisos y superficie ligeramente convexa y brillante, parecidas a las colonias de Leishmania tropica en el mismo medio de cultivo. En los cultivos la coloración del parásito es más rápida y fácil que en la sangre. Dado el gran número de colonias que existen en la superficie sólida, es fácil preparar frotises casi únicamente de éstas, diluyéndolas con suero fisiológico. Coloreadas simplemente con May-Grünwald Giemsa muestran muy bien el flagelo libre, aunque Mejores resultados hemos obtenido exponiendo el frotis húmedo a los vapores de ácido ósmico (al 1 por ciento), y luego fijándolo en el alcohol metílico, el fijador de Hollande, de Schaudinn, etc. Si se usa este último fijador, la coloración con la hematoxilina férrica de Heidenhain dá excelentes resultados. Observando las preparaciones coloreadas con cualquiera de las técnicas indicadas, se ve que la mayoría de los trypanosomas se encuentran al estado de critidia. Son ligeramente curvos, con la extremidad, posterior delgada y terminada en punta y la anterior ancha y obtusa. (Fig. 7). Esta forma, que es la predominante en cultivos que tienen más de ocho días, es de un tamaño medio de 35.5µ de longitud por 3.5µ de ancho. Raramente se encuentran algunas de estas formas con dimensiones que suelen alcanzar 54 a 55µ, al lado de otras bastante chicas, inferiores a las 18µ. La principal forma de división parece ser la binaria, la que se realiza principalmente al estado de critidia (Fig. 9) o de leptomonas. Si se observan los cultivos del segundo al tercer día de hecha la resiembra, época en la que por lo general todavía no es posible distinguir las colonias ni con la ayuda de una lente de mano (10 x), el aspecto general es distinto, pues entonces predominan formas esféricas y ovoides, de varios tamaños, por lo general con un corto flagelo libre, frecuentemente agrupadas en número considerable. Junto a éstas también se encuentran formas de leishmania. Todas estas formas con frecuencia muestran dos núcleos y en casos raros hasta cuatro o cinco. Sin embargo, en ninguna ocasión se ha visto rosetas. La duración media de los cultivos es de 30 a 45 días. Cultivo en el medio semisólido de Noguchi. El desarrollo en este medio se manifiesta, corrientemente, en la parte superior en una zona de medio centímetro a uno de profundidad, a partir de la superficie donde se forman colonias microscópicas en enorme cantidad constituyendo una zona pálida o blanquecina que suele cambiar hasta amarillo oscuro, entretanto que debido al cambio que sufre la hemoglobina, la parte inferior del medio ofrece un color rojo violáceo, cambio de coloración que ya se nota al tercer o cuarto día. Al lado de esta forma de desarrollo suele también presentarse, con menor frecuencia, otra con colonias relativamente grandes, aisladas y blanquecinas, por lo general esféricas y con el centro más compacto que los bordes, logrando alcanzar en algunos casos un diámetro de 1.0 a 1.5 milímetros. Su número siempre es reducido y visto con aumentos de 20 a 25 diámetros parecen estar constituídas por colonias microscópicas. Al observar en láminas coloreadas los organismos que las constituyen se nota que casi todos tienen la forma de leishmania. Están agrupadas en masas de tamaño variable (Fig.16). Algunas de tales formas alcanzan un diámetro de 35µ y muestran por lo general varios núcleos, no siendo raro que presenten una gran vacuola al centro. Parece que la división de estas formas dá lugar a agrupaciones reducidas de trypanosomas, corrientemente de 4-8, con los flagelos dirigidos hacia el centro semejando pequeñas rosetas (Fig. 13). En trypanosomas libres, esto es, que no están agrupados en colonias, se nota también la división binaria al estado de critidia y de leptomonas como en el medio NNN. La duración de los cultivos es relativamente corta, por lo general de 15 a 20 días, llegando al mes sólo en casos excepcionales. INOCULABILIDAD Se ha inoculado: ratas blancas, cobayos y Phyllotis amicus amicus nacidos en el laboratorio. El inóculo en la mayoría de las veces ha procedido de cultivos, pero también en algunos casos se ha usado sangre infectada del huésped natural. Las observaciones después de inoculados los animales se han llevado a cabo por medio de exámenes en fresco de la sangre periférica y por medio de hemocultivos. Rata blanca. Parece no ser sensible a la inoculación experimental con cultivos. Sin embargo, si las ratas son inoculadas durante la primera semana de nacidas, muestran una infección transitoria. De un total de 13 ratas divididas en cuatro lotes de distintas edades -de 6, 10, 14 y 27 días- sólo en las dos que fueron inoculadas cuándo tenían apenas 6 días de nacidas, se pudo ver al parásito inoculado en la sangre periférica hasta el tercer día y se obtuvo un cultivo positivo a los 7 días de la inoculación. En cuatro ratas inoculadas a los 10 días de nacidas todos los resultados fueron negativos, inclusive cultivos, en las cuatro, a los 11 días. Resultados igualmente negativos se obtuvieron con animales de mayor edad. La inoculación de este trypanosoma en ratas tiernas no interfiere la marcha de una posterior infección por el T. lewisi. Cobayos. Este roedor tampoco es sensible a la inoculación experimental. Cuatro cobayos fueron inoculados, 2 de 2 días y 2 de 3 días de edad, obteniéndose en todos resultados negativos. En dos de ellos se hicieron cultivos a los 5, 10 y 25 días de la inoculación, sin lograr recoger el germen inoculado. Phyllotis amicus amicus (?). Este ratón, que al estado natural no se ha encontrado infectado, es sensible siempre que la inoculación se efectúe a temprana edad. Así en una serie de siete ratones inoculados los siete días de nacidos, todos fueron infectados. El parásito se logró ver en la sangre periférica hasta los tres meses y en uno de ellos se obtuvo cultivo positivo siete meses después de la inoculación. En cambio, otra serie de 5 Phyllotis inoculados a los 20 días de edad, ofreció en todos los casos resultados negativos; no se efectuó hemocultivos. De manera general parece que la infección experimental tampoco es patógena y en esta especie, el P. amicus amicus (?), ha sido mas ligera que las infecciones naturales en sus huéspedes conocidos, Phyllotis sp. y P. darwini limatus. INFECCIÓN DEL Phlebotomus noguchii Los trabajos de Hertiq (9) han puesto de manifiesto ciertas relaciones existentes entre el Phlebotomus noguchii y los roedores salvajes en general, indicando como esta titira parece alimentarse exclusivamente de sangre de roedores. Sucede así, por ejemplo, como hace notar el referido investigador, que en los nidos de Phyllotis situados a lo largo de las zonas verrucógenas, especialmente cuando la hembra tiene cría -lo que sucede durante los meses de febrero a julio- suele encontrarse números considerables de P. noguchii, las hembras frecuentemente con el abdomen repleto de sangre. Además este Phlebotomus no penetra a las casas y de preferencia se encuentra en cuevas, rajaduras de rocas, etc., por lo general en lugares alejados de ciudades o habitaciones humanas, sitios que son frecuentados por varios roedores salvajes, notándose el marcado contraste que hay en este sentido entre dicha titira y las otras dos especies más que existen en tales zonas, las que no se alimentan sobre roedores, prefiriendo en todo caso picar al hombre y algunos animales domésticos, para lo cual penetran a las habitaciones humanas. Al hacer disecciones de P. noguchii cazados en nidos de Phyllotis cuando todavía contenían sangre en el estómago, encontramos en la mayoría de ellas masivas infecciones de un flagelado al estado de critidia. En numerosas oportunidades pudimos relacionar tales infecciones del insecto con el trypanosoma que albergaba el ratón sobre el que se había alimentado, ya sea capturando el roedor y haciendo que sobre él se alimentasen titiras criadas en el laboratorio, para luego comparar estas infecciones experimentales con las encontradas en el insecto salvaje; o, también, obteniendo cultivos puros del flagelado a partir de las infecciones de titiras capturadas en el campo. Infección natural Las infecciones en titiras salvajes que retienen todavía siquiera parte de su alimentación con sangre son tan frecuentes que en muchas oportunidades nos hemos valido de ellas como un indicador de los lugares donde se encuentran Phyllotis infectados. En nuestras observaciones tales infecciones de titiras llegaron al 80 por ciento. No sucede lo mismo con aquellas cogidas en el campo y conservadas en el laboratorio hasta que hayan arrojado todo el contenido de su alimentación sanguínea, pues en tales circunstancias siempre nos ha sido imposible revelar la infección por medio de disecciones. En cuanto a la naturaleza de tales infecciones nuestras observaciones no han sido tan detenidas, habiéndonos limitado en la mayoría de las veces a la observación de cortes histológicos o a la constatación de la infección por medio de frotises, pero sin hacer un estudio detenido de la morfología del parásito, lo que se ha llevado a cabo, más bien, en las infecciones experimentales. En aquellas titiras cogidas en el campo que fueron observadas por medio de cortes histológicos, se logró ver que a los 4 ó 5 días de su alimentación sobre el ratón infectado, la infección del insecto comprendía a todo el intestino medio (cardia y estómago) y en algunos casos también a la faringe. En este estado de la infección es fácil recoger al flagelado en cultivo puro, ya que por lo general se presenta sin contaminación de otro germen. A medida que la sangre digerida pasa a través del recto, los trypanosomas siguen el mismo curso hasta ser arrojados con las heces, ofreciendo en general un cuadro idéntico al observado con más detenimiento en las infecciones experimentales que luego se exponen. Como nunca lográramos ver trypanosomas en frotises de titiras que habían arrojado todo el contenido de su alimentación con sangre, se llevó a cabo, por medio de cortes histológicos, detenidas observaciones en un total de 50 Phlebotomus que al capturarlas se encontraban en dicha condición, procedentes especialmente de las localidades de Tornamesa y Puente Carrión. De todas ellas, sólo una mostrábase infectada por un flagelado al estado de critidia. La infección comprendía al cardia y el estómago, ofreciendo un aspecto parecido a aquellas producidas experimentalmente. Infección experimental No obstante de haberse recogido varias veces en cultivo puro el trypanosoma partiendo de las infecciones naturales de titiras salvajes, siempre cabía la objeción de que al menos en algunas ocasiones dichas infecciones podían muy bien ser originadas por otro parásito, por lo cual tratamos de reproducirlas experimentalmente, valiéndonos de dos series distintas de experimentos: 1) exponiendo titiras criadas en el laboratorio a Phyllotis convenientemente infectados; y 2) dándoles a comer artificialmente cultivos puros de trypanosomas, también a titiras criadas en el laboratorio, por medio de la ingeniosa técnica de la pipeta de Hertig y Hertig (8). En ambos casos se usó un número conveniente de controles y los resultados fueron observados por medio de cortes histológicos y también por disecciones. 1. Titiras expuestas sobre Phyllotis infectados. Usando tres Phyllotis distintos realizamos una serie de 16 experimentos con un considerable número de titiras, logrando que 29 de ellas consiguiesen alimentarse sobre el ratón. De éstas, solamente 6 no mostraron tripanosomas durante las observaciones de que fueron objeto, correspondiendo este grupo a las dos primeras series llevadas a cabo con un Phyllotis que sufría una infección bastante ligera. Las 23 restantes, expuestas sobre ratones con fuerte infección, fueron infectadas en grados diversos. La infección del insecto es fácil de constatarla después de las 48 horas, simplemente por medio de disecciones. A los cuatro o cinco días la multiplicación del parásito es activísima, dando por resultado una enorme cantidad de trypanosomas que en los cortes histológicos parecen llenar por completo el estómago y el cardia (parte anterior del intestino medio), alcanzando algunas veces al esófago, (Fig. 14, E). Sólo en una oportunidad se ha visto trypanosomas en la faringe y en la cavidad bucal, pero jamás en la proboscis ni en las glándulas salivares. En el estómago del Phlebotomus la principal forma de división parece ser la binaria, ya sea al estado de critidia o de leptomonas y en cuanto a su morfología y dimensiones existe una notable diferencia entre los primeros días y los últimos de la infección. Al principio, durante el segundo y tercer día principalmente, predomina una forma de critidia con una longitud media de 24.5µ por 2.5µ de ancho, con la extremidad posterior terminada en punta, mostrando un núcleo esférico u ovoide de posición más o menos central. A medida que avanza la infección, esta forma va siendo reemplazada por otra sumamente delgada y extensa, alcanzando algunos una longitud de 40µ entretanto que el ancho se reduce a una o dos micras, con el núcleo alargado, la parte anterior del cuerpo mayor que la posterior, el kinetoplasto junto al núcleo y el axonema (porción no libre del flagelo) tan pegado al borde del cuerpo que casi no se nota la membrana ondulante (Fig. 12). Al lado de estas formas delgadas y largas, se encuentra otra que difiere notablemente por tener la extremidad posterior obtusa, el núcleo relativamente voluminoso, y en muchos casos toda la célula es piriforme, con una longitud que suele descender hasta 8-9µ (Fig. 11). Preferentemente en el recto y a los 6 ó 7 días, esta forma con frecuencia está en división. Antes del cuarto día, usualmente, el recto de la titira no muestra trypanosoma alguno y las heces que entonces son de un color blanco o gris, todavía no contienen al flagelado; pero después del quinto o sexto día, el recto está repleto de trypanosomas, únicamente de las dos últimas formas citadas, y cuando las heces que arroja tienen un color marrón o negro suelen contener masas compactas de los trypanosomas delgados y vistos en el estómago y el recto durante los últimos días de la infección (Fig. 12). Después que la titira había arrojado todos los restos de su alimentación, por medio de disecciones no hemos podido encontrar trypanosomas en ningún lugar del tubo digestivo. 2. Alimentación artificial. En esta serie se ha trabajado con un total de 35 titiras criadas en el laboratorio, 13 hembras y 22 machos. El contenido que se les administraba era una suspensión de trypanosomas procedentes de la superficie sólida de cultivos en medio NNN. La suspensión se hacía en suero fisiológico, en el líquido del mismo medio o en sangre citratada de Phyllotis. Las titiras sometidas a esta prueba por lo general no sobreviven mucho tiempo, debido principalmente a que se maltratan bastante durante el experimento. En nuestros ensayos solamente tres lograron sobrevivir hasta el séptimo día, siete hasta el quinto y las restantes murieron entre el segundo y tercer día de la alimentación artificial. En cambio, esta técnica ofrece la ventaja de que tanto las hembras como también los machos logren ingerir la suspensión. En 11 casos (4 hembras y 7 machos) de los 35 se logró ver trypanosomas en el tubo digestivo del insecto, entre el segundo y séptimo día. Siempre fueron escasos y por lo general se encontraban esparcidos frecuentemente adheridos al epitelio del cardia y el estómago, siendo muy raras las formas en división. Mientras vivían las titiras, sus heces fueron observadas diariamente, encontrándose en dos ocasiones que a partir del quinto día mostraban pequeñas masas de las formas delgadas ya descritas. La infección del recto era también sumamente ligera, aunque mostraba las mismas formas encontradas en las titiras que se alimentaron sobre Phyllotis infectados. De manera general, pues, parece que los trypanosomas procedentes de cultivos dados a comer artificialmente al P. noguchii, tanto en la hembra como en el macho, experimentan una trasformación morfológica que dá lugar a formas idénticas a las que se observan en las infecciones naturales. Pero por el momento no se podría precisar si existe una verdadera multiplicación del parásito en el tubo digestivo de la titira, al ser ésta infectada por medio de una alimentación artificial con cultivos. BIBLIOGRAFÍA 1. H. BONACCI: Rev. Inst. Bact., Buenos Aires, t. 6, p. 242-247 (abstracto del Trop. Dis. Bull., 1935, t. 32, p. 721-722), 1934. [ Links ] 2. E. BRUMPT: Bull. Soc. Path. Exot., t. 6, p. 167-71, 1913. 3. A. CARINI y J. MACIEL: Bull. Soc. Path. Exot., t. 8, p. 165-169, 1915. 4. J.T. CULBERTSON: Jour. Parasit., t. 27, p. 45-52, 1941. 5. P. DELANOE: Bull. Soc. Path. Exot., t. 8, p. 80-88, 1915. 6. C. J. GASTIABURÚ: Gaceta de los Hospitales, Lima, t. 1, p. 221-223, 1904. 7. A. HERRER: Rev. de Ciencias, Lima (en prensa), 1942. 8 A. HERTIG y M. HERTIG: Science, t. 65, p. 328-329, 1927. 9. M. HERTIG: Amer. Jour. Trop. Med., Suplemento t. 22, Nº 5, p.l-80, julio, 1942. 10. C. A. HOARE y F. COUTELEN: Ann. Parasit., t. 11, p. 196-200, 1933. 11. C. A. HOARE: Trans. R. Soc. Trop. Med. Hyg. t. 32, p. 333-342, 1938. 12. W. MAC NEAL: Jour. Infect. Dis., t. 1, p. 518-542, 1904. 13. F. NOVY, W. MAC NEAL y H. TORREY: Jour. Infect. Dis., t. 4, p. 223-276, 1907. 14. M. A. LAVERAN y F. MESNIL: Ann. Inst. Past., t. 15, p. 673-713, 1901. 15. M. LAVERAN y F. MESNIL: Trypanosomes et trypanosomiases, 2ª edición, París, 1912. 16. R. RIVEYRO y J. RAFFO: La Crónica Médica, Lima, p. 313-16, 1917. 17. J. RODHAIN: Bull Soc. Path. Exot., t. 8, p. 726-728, 1915. 18. A. RUIZ DEL RÍO: Bol. Soc. Biol. de Concepción, Chile, t. 13, p. 47-82, 1939. 19. J. SCHWETZ: Ann, Parasit., t. 11, p. 287-296, 1933. 20. L. SWINGI: Jour. Infect. Dis., t. 8, p. 125-146, 1911. 21. W. H. TALIAFERRO y L. C. TALIAFERRO: Am. Jour. Hyg., t. 2, p. 264-318, 1922. 22. THIROUX Ann. Inst. Pasteur., t. 19, p. 564-572, 1905. 23. J. YEPES: Rev. Chil, Hist. Nat., Santiago de Chile, t. 37, p. 46-49, 1933. 24. J. YEPES: Rev. Inst. Bact., Buenos Aires, t. 7, p. 213-269, 1935. 25. C. M. WENYON: Protozoology. Bailliere, Tindall and Cox, London, 1926. 26. H. ZINSSER, H. WEI y F. FITZPATRICK: Proc. Soc. Exp. Biol. and Med., t. 37, p. 604-606, 1937. 27. H. ZINSSER, F. FITZPATRICK y H. WEI: Jour. Exp. Med., t. 69, p. 179-190, 1939.
del kinetoplasto al núcleo 5.8 µ
del núcleo al extremo anterior 15.5 µ
núcleo (diámetro medio) 3.7 µ
flagelo libre 9.0 µ