Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Medicina Experimental y Salud Publica
versión impresa ISSN 1726-4634
Rev. perú. med. exp. salud publica v.1 n.1-2 Lima oct. 1942
TRABAJOS ORIGINALES
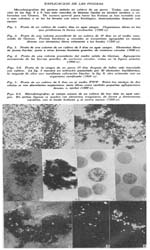
Microorganismo, posiblemente del grupo bartonella-grahamella, aislado de un perro Arístides Herrer A. 1 1 Departamento de Entomología Médica del Instituto Nacional de Higiene y Salud Pública, Lima. Después que NOGUCHI Y BATTISTINI (1926) cultivaran por primera vez la Bartonella bacilliformis, se ha logrado cultivar algunas especies más de bartonellas y grahamellas. [B. muris (BATTISTINI y WEISS, 1926;, MARMORSTON y PERLA, 1932; LAWKOWICZ, 1938), B tyzzeri (WEINMAN y PINKERTON, 1938), Haemobartonella microti (TYZZER y WEINMAN, 1939); y varias especies de grahamellas de pequeños roedores (TYZZER, 1941)] 1. En cambio la B. canis no se ha podido cultivar hasta la actualidad no obstante haberlo intentado varios investigadores (KNUTT1 y HAWKINS, 1935). Aprovechando de la experiencia que teníamos sobre el cultivo de la B. bacilliformis, en el Departamento de Entomología Médica de este Instituto en varias oportunidades hemos tratado de cultivar la B. canis. Recientemente nos fué posible realizar una serie de cultivos en cuatro perros esplenectomizados y con abundantes bartonellas en la sangre periférica. Estos animales fueron puestos a nuestra disposición debido a la gentileza del Profesor PEDRO WEISS, por lo que deseamos expresarle nuestros agradecimientos, del mismo modo que a sus Ayudantes del Departamento de Anatomía Patológica de la Facultad de Ciencias Médicas. En esta ocasión, además de los medios ZWF (Zinsser, Wei y Fitzpatrick, 1937) y el semisólido de Noguchi para leptospira usados en nuestros ensayos anteriores, empleamos los medios vitaminados recientemente ideados por GEIMAN (1941). La serie constó de cinco cultivos, cuatro de los cuales, correspondientes a tres perros, resultaron negativos y sólo en el del cuarto perro logramos recoger un gérmen que por su morfología, características de cultivo, propiedad de parasitar los glóbulos rojos de su huésped, etc., estaría posiblemente dentro del grupo Bartonella-Grahamella. En la actualidad se encuentra en su décimo segundo pasaje y en esta ocasión vamos a exponer en forma preliminar las observaciones que tenemos sobre él. Aislamiento El cultivo original fué hecho en el medio, semisólido de Geiman con sangre citratada obtenida de la vena yugular, incubándose a 28ºC. A los cuatro días, antes de verse todavía ningún desarrollo, con varias gotas de este cultivo se efectuó una resiembra en el mismo medio, la que se incubó a 37ºC. Los cultivos originales se descartaron a los 10 días, sin notarse en ellos desarrollo alguno. A las dos semanas, en las resiembras se vieron macroscópicamente pequeñas y compactas colonias blanquecinas de forma más o menos esférica y superficie irregular. Al principio su número era pequeño y se encontraban aisladas unas de las otras, pero posteriormente se iban haciendo cada vez más numerosas, al mismo tiempo que las colonias primitivas, después de haber aumentado un poco de tamaño, se fraccionaban dando lugar a numerosas colonias pequeñas que se esparcían desordenadamente. El desarrollo prácticamente alcanzaba a toda la extensión hasta donde había llegado el inóculo. Desde entonces las resiembras se efectuaron sin ninguna dificultad, especialmente en el agar sangre. En la actualidad esta cepa parece estar ya establecida, en cultivo en medios artificiales. Características del cultivo No se ha conseguido desarrollo en agar simple ni en caldo corriente y los medios que se han usado con éxito han sido el ZWF, el semisólido de Geiman y el agar sangre. Sólo en los dos últimos se ha hecho observaciones especiales. Desarrolla tanto a 28 como a 37ºC y carece de movilidad. Medio semisólido de Geiman Hasta el tercer pasaje se obtuvo fácil y abundante desarrollo, de los 8 a los 10 días en cultivos incubados a los 28ºC. Con frecuencia en estos cultivos primero se desarrollaban aisladamente colonias grandes, de más o menos 1 mm. de diámetro. Luego éstas daban lugar a numerosas colonias pequeñas que se esparcían a su alrededor, pero sin constituir halo como sucede en la B. bacilliformis. Ordinariamente después de los 20 ó 25 días el desarrollo de los cultivos había alcanzado su máximo. A partir del tercer pasaje se nos ha hecho difícil el cultivo en este medio y en aquellas pocas ocasiones que se consiguió desarrollo, el aspecto macroscópico era diferente del que ofrecieron las primeras resiembras. En estos casos el desarrollo generalmente se limitaba a una zona de más o menos 3-4 mm. de profundidad a partir de la superficie y estaba constituida casi únicamente por colonias pequeñas. Los cultivos en este medio nos han dado resiembras positivas solamente hasta los 30 días. Agar Sangre Durante el primer pasaje las colonias originales del inóculo a los 4-5 días se hacían ostensibles como puntos blancos, de borde circular y superficie convexa, un tanto más pronunciada que en las de la B. bacilliformis. Al tocarlas con agujas o con el asa de platino se deslizaban fácilmente, siendo casi imposible extraerlas solas. Fuera de estas colonias y en el líquido de condensación del medio generalmente no se encontraban organismos, al observar al microscopio. Después de varios pasajes el desarrollo se hacía cada vez más abundante y general a toda la superficie inoculada. En la actualidad a los tres o cuatro días las resiembras ofrecen un desarrollo magnífico, visible macroscópicamente, en cultivos incubados a 28ºC. Las colonias se ven como finos puntitos que cubren casi toda la superficie sólida del medio, dándole un aspecto granular. A partir de los 8 ó 10 días, con frecuencia algunas se destacan de las demás por sus dimensiones mayores y por que ofrecen un color blanco pronunciado, llegando unas pocas a alcanzar un diámetro de 1.5 a 2 mm. En este medio hemos obtenido resiembras positivas hasta los 60 días, sin notar descomposición de la hemoglobina o desprendimiento de algún olor particular. Morfología Se trata de un microorganismo de acentuado pleomorfismo Gram-negativo y que con el Giemsa se colorea de violeta rojizo. Al campo oscuro ofrecen el contorno brillante y el centro obscuro como las bartonellas, notándose un poco más grandes y de contornos mejor definidos que en láminas coloreadas especialmente aquellos que se encuentran libres. Parece que se podría considerar como forma típica la bacilar, ya que es la que predomina especialmente en los cultivos jóvenes, al lado de la que se encuentran también cocobacilos y aún formas francamente cocoides (Fig. 1). Los bacilos tienen dimensiones que varían entre 1-3 micras de longitud por 0.2-0.3 micras de ancho. Los de mayor longitud generalmente son algo curvos y algunos tienen uno de sus extremos más angosto que el otro, ofreciendo el aspecto de una porra. Las formas cocoides generalmente tienen un diámetro de 0.2-0.3 micras, aunque también las hay de dimensiones inferiores. Especialmente en cultivos de menos de una semana pueden verse algunas veces pequeñas cadenitas, usualmente de 4-12 organismos. En agar sangre durante los primeros días es frecuente encontrar formas irregulares de dimensiones variables, alcanzando algunas 3-4 micras de longitud por 0.5-1 micra de ancho (Fig. 8). Todas estas formas pueden estar libres o agrupadas en densas masas (Fig. 2), comparables a las de la B. bacilliformis. Al lado de los organismos libres o agrupaciones densas de los mismos, suelen encontrarse algunas formas de gran tamaño, por lo general de borde circular, con un diámetro que varía entre 1-5 micras. Se colorean de manera homogénea y no parecen individualizarse, sino muy raramente, en las formas ordinarias. Por lo general suelen hallarse mezcladas con organismos libres (Fig. 3), pero también se ven agrupaciones grandes constituidas únicamente por tales formas (Fig. 4). Al campo oscuro ofrecen también el contorno brillante y el centro oscuro (Fig. 9). Inoculaciones Se han efectuado inoculaciones en dos perros, cuyos protocolos son los siguientes: Perro 1. De 4-6 semanas de edad, peso 1200 grs. Marzo 20, 1942, esplenectomía. Abril 3-14, observaciones de control con dos hemocultivos y cuatro frotises de sangre negativos. Abril 14. Eritrocitos 3.2 millones. Inoculación, cultivo cuarto pasaje, agar sangre, 17 días: por vía endovenosa con 2 cc. e intradérmicamente en 7 puntos del abdomen. Abril 21. Eritrocitos 1.7 millones; Abril 24, 1.9 millones; Abril 30, 2.6 millones y Mayo 7, 3.2 millones. Desde entonces sólo ligeras variaciones. Después de tres o cuatro días de la inoculación algunos eritrocitos mostraban uno o dos puntitos azulados, sin poderse precisar que se tratasen de organismos. Fue a los 15 días que se vio un glóbulo rojo parasitado por 48-50 organismos bacilliformes (Fig. 5). Las inoculaciones intradérmicas al principio mostraron ligeras induraciones que desaparecieron a los 8-10 días. Abril 20 y Mayo 11. Hemocultivos positivos. Perro 2. Adulto, peso 5500 grs, Marzo 27, 1942, esplenectomía. Abril 10 y 17 inyección 0.15 grs. de Neosalvarsán. Abril l4-29, observaciones de control con 8 frotises de sangre negativos. Abril 30. Eritrocitos 6.4 millones. Inoculación, cultivo sexto pasaje, medio semisólido de Geiman, 10 días: con 4 cc. por vía endovenosa e intradérmicamente en 6 puntos del abdomen. Después de la inoculación los eritrocitos sufrieron solamente ligeras oscilaciones. Escasos eritrocitos mostraban uno o dos puntitos azulados; a veces comparables a organismos. Las inoculaciones intradérmicas dieron lugar a ligeras induraciones que desaparecieron a los 6-8 días. Mayo 19. Reinoculación por vía endovenosa con 3 cc., cultivo octavo pasaje, agar sangre, 33 días. A los cuatro días de la reinoculación se vio el primer glóbulo parasitado. La cifra de eritrocitos sigue más o menos igual. Mayo 20 y 26. Hemocultivos contaminados. Por lo general son sumamente escasos los glóbulos parasitados, siendo imposible señalar alguna proporción entre éstos y los demás glóbulos rojos. Se les ha encontrado en el primer perro hasta los 51 días después de la inoculación y en el segundo sólo hasta los 13 días de la reinoculación. El número de parásitos que se encuentran en un mismo glóbulo varía entre 1 y 70, siendo más frecuente las cifras comprendidas entre 10 y 30. El germen usualmente es de forma bacilar con dimensiones de 1.0-1.5 x 0.2-0.3 micras. También son frecuentes formas cocobacilares y aún en algunas ocasiones se pueden ver ciertos elementos que parecen simplemente granulaciones o pequeñas masas cromáticas. Sólo en una ocasión se ha encontrado organismos con ramificaciones (Fig. 6) semejantes a las que se ven con frecuencia en la B. canis. El aspecto general del animal infectado no muestra ningún trastorno o malestar aparente. Las inoculaciones parecen indicar, pues, que no se trata de la B. canis. Aunque no tenemos referencias sobre la existencia de grahamellas en el perro y nuestros experimentos de inoculación no son todavía de ninguna manera conclusivos, las características del cultivo y las infecciones experimentales obtenidas hasta ahora, probablemente colocarían al parásito en el grupo Bartonella Grahamella. REFERENCIAS 1. T. BATTISTINI & P. WEISS: Ann. de la Fac. de C. Med., Lima, 1926. 2. Q. M. GEIMAN: Proc. Soc. Exp. Biol. and Med., t. 47, p. 329, 1941. 3. R. E. KNUTT1 & W. B. HAWKINS: Jour. Exp. Med., t. 61, p. 115, 1935. 4. W. LAWKOWICZ: Off. Int. DHyg. Publ., t. 30, p. 1781, 1938. 5. J. MARMORSTON-GOTTESMAN & D. PERLA: Jour. Exp. Med., t. 56, p. 763, 1932. 6. H. NOGUCHI & T. BATTISTINI: Jour. Exp. Med., t. 43, p. 851, 1926. 7. E. E. TYZZER & D. WEINMAN: Am. Jour. of Hyg., t. 30, p. 141, 1939. 8. E. E. TYZZER: Proc. Nat. Aca. of Sc., t. 27, p. 158, 1941. 9. D. WEINMAN & H. PINKERTON: Ann. of Trop. Med. and Parasit., t. 32, p. 215, 1938. 10. H. ZINSSER, H. WEI & F. FITZPATRICK: Proc. Soc. Exp. Biol. and Med., t. 37, p. 604, 1937.
(Nota preliminar)