Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Medicina Experimental y Salud Publica
versión impresa ISSN 1726-4634
Rev. perú. med. exp. salud publica v.13 n.1-2 Lima 1960
Valoración del cloramfenicol y sus esteres en especialidades farmacéuticas
Julio Morales1 y Soledad Urquizo1
1 División de Control Técnico del Instituto Nacional de Salud, Lima-Perú.
SUMARIO
1. Hemos efectuado la valoración del cloramfenicol y cuatro de sus ésteres en especialidades farmacéuticas, por los métodos espectrofotométrico y microbiológico de la Placa-discocultivo, habiéndose obtenido en ambos casos resultados satisfactorios.
2. Para llevar a cabo la determinación espectrofotométrica se ha establecido primeramente el Coeficiente de Extinción Específico a la longitud de onda correspondiente a cada sustancia, a base de cuyo dato se realizaron los cálculos.
3. El cloramfenicol levógiro presenta su máxima absorción en la zona de luz ultravioleta a 277-278 mu; el palmitato y estearato a 271 mu; el cinamato a 278 mu. y el succinato a 276 mu.
4. Los coeficientes de extinción específicos obtenidos a las longitudes de onda mencionadas, son los siguientes: 298 para el cloramfenicol levógiro; 178 para el palmitato, 180 para el estearato, 760 para el cinamato y 231 para el succinato.
5. En cuanto al método microbiológico, anotamos que previamente se preparó una curva standard a base de cloramfenicol levógiro, la cual sirvió para efectuar por comparación, la valoración de los diversos ésteres presentes en las muestras analizadas.
6. Para obtener resultados satisfactorios en la determinación de la actividad de los ésteres presentes en especialidades, es necesario recurrir primero a la extracción de la sal y luego a la hidrólisis enzimática.
SUMMARY
1. We have carried out the assay of Chloramphenicol and four of his esters when they are present in pharmaceuticals. by spectrophotometric and microbiologic plate -disc- culture method; the results were satisfactory with two methods.
2. For spectrophotometric determinations we have found previously the absorptivity for each substance on the respective wave lenght, those absorptivities were used for calculations.
3. Chloramphenicol presents his absorbance at 277-278 mu, palmitate and stearate at 271 mu, cinnamate at 278 mu and succinate at 276 mu.
4. The absorptivities at those wave lengths are: 298 for chloramphenicol, 178 for palmitate, 180 for stearate, 760 for cinnamate and 231 for succinate.
5. Por microbiological method, we have established previously a standard curve in basis of chloramphenicol, this curve was used also in order to realize the esters assay that are present in pharmaceuticals, by comparison.
6. In order to obtain satisfactory results in the antibacterial action of esters when those are present in the samples, it is necessary after to take off them, and subsequently enzimatic hydrolisis is applied.
En la presente comunicación exponemos dos métodos utilizados para la valoración del cloramfenicol (CAF) y sus ésteres cuando ellos están presentes en especialidades farmacéuticas: uno el método espectrofotométrico, y otro el microbiológico de la Placa-disco-cultivo que requiere, para el caso de los ésteres, hidrólisis previa de las sales. Con ambos hemos obtenido resultados satisfactorios, teniendo el segundo, la ventaja de hacemos conocer, además de la concentración, la actividad antimicrobiana de los diversos compuestos, lo que no es posible precisar por el método espectrofotométrico.
MATERIALES y MÉTODOS
Materiales.
Espectrofotómetro Beckman Modelo DU; alcohol etílico de 95°; éter de petróleo, cloroformo, agua destilada; matraces aforados por 25, 50 y 100 c.c., embudos de separación y filtración; pipetas graduadas; medio de cultivo: agar-triptosa, placas Petri de 15 x 100 mm.; tubos de prueba de 16 x 125 mm.; solución tampón al 1% de fosfato con pH 6.0 preparado de acuerdo a la F. E. U.; discos antibióticos estandarizados; discos de papel de filtro estériles; pinzas rectas de extremo afilado; suero fisiológico al 9% estéril, cápsulas de Pantozyme "Wander" (concentrado de fermento de origen animal y vegetal: amilasa, celulasa, lipasa, pepsina y proteasas).
A. MÉTODO ESPECTROFOTOMÉTRICO
Se ha utilizado este método aprovechando la propiedad que tienen el clorámfenicol y sus ésteres de presentar su máxima absorción en determinada longitud de onda de luz ultravioleta (Fig. 3), para cada caso se ha hecho la determinación de la curva espectral, junto con la respectiva curva standard y el Coeficiente de Extinción Específico (E1%1cm).
Las lecturas fueron hechas en el espectrofotómetro Beckman Modelo DU.
Los cálculos se hicieron de acuerdo a la fórmula.

Preparación de las Curvas Standard.
Para el cloramfenicol levógiro se preparó una solución stock de 10 mg. en 100 c.c. de agua destilada. A partir de ella se hicieron las respectivas diluciones que se indican en el cuadro I.
En el caso de los ésteres, se tomó igualmente 10 mg. de cada una de las sales, se disolvió en cantidad suficiente de alcohol etílico 95% y se completó el volumen final a 100 c.c., las diluciones posteriores se hicieron también con alcohol utilizándose las concentraciones ya indicadas en el referido cuadro. Además las respectivas lecturas han sido trasladadas a papel milimetrado (Fig. 1 y 2).
Aplicación del método a las especialidades farmacéuticas.
Para las especialidades farmacéuticas de tipo cápsulas, grageas, pomadas o supositorios que tienen cloramfenicol levógiro, se procede a tomar una parte alícuota y luego de extraer el principio activo ya sea con alcohol etílico o utilizando éter de petróleo y agua cuando el vehículo graso no es miscible con esta última, como lo ha descrito uno de nosotros en trabajo anterior (URQUIZO, 1957). Extraído el principio activo, se hacen las diluciones convenientes con agua destilada la cual se utiliza también como blanco para hacer la lectura espectrotométrica.
En la preparación de jarabes y suspensiones para uso oral, se utilizan ésteres del cloramfenicol, debido al sabor amargo del antibiótico cuando está en su forma activa; para la valoración de estas sales, se procedió a su extracción utilizando el método indicado en las regulaciones del Food and Drug Administration de las Estados Unidos de Norte América (F.D.A.) para el palmitato (Compilation and Regulations for Test and Methods of Assay and Certifications of Antibiotic and Antibiotic Containing Drugs 1: D1-D15. 1957).
Ya que todos las ésteres que mencionamos son solubles en cloroformo, no se encontró dificultad en la aplicación del procedimiento. Las lecturas espectrofotométricas se hicieron a la longitud de onda correspondiente para cada caso.
B. MÉTODO MICROBIOLÓGICO
Obtención de la curva standard del cloramfenicol.
Utilizamos con este objeto cloramfenicol F.D.A. de 100% de potencia antibiótica, previamente secado en estufa a 60°C por tres horas; luego se pesó una parte alícuota, se disolvió en cantidad suficiente de alcohol etílico y se diluyó con fosfato buffer al 1% de pH 6.O hasta obtener una concentración de 10,000 mcg./c.c. A partir de esta solución se prepararon otras, a concentraciones de 32, 16, 8, 4, 2, 1 y 0.5 mcg./c.c. siempre con la ayuda de la solución de fosfato buffer de pH 6.0.
En la preparación de la curva standard (Fig. 4) usamos un total de 12 placas, dos placas par cada dilución, con excepción de la de 4 mcg./c.c. que está incluida en todas las placas y se le utiliza como punto de referencia; en cada una de las dos placas se colocan tres discos imbibidos de la dilución de 4 mcg./c.c. y las otras tres con otra concentración. La cepa usada fue la N° 7 I. N. S. (Estafiloccus aureus, coagulasa positiva).
Después de 16 a 18 horas de incubación a 37°C se hacen las lecturas de los halos de inhibición y los cálculos correspondientes, tal como se ha descrito en trabajos anteriores (MORALES y VELAZCO, 1957; MORALES, 1958).
Es sabido que los ésteres del cloramfenicol son inactivas si sobre ellos no actúa una hidrólisis previa, de ahí que para la valoración "in vitro" de estas sales hemos recurrido a la liberación del cloramfenicol activa por medio de la hidrólisis enzimática (CHIOVE, M. y col. 1956; PAULETTA, 1952; TROLLE-LASSEN, 1954). A continuación indicamos la técnica seguida por nosotros para cada caso.
Palmitato de CAF.
Se pesó 200 mg. de palmitato de CAF equivalente a 125 mg. de CAF levógiro, se disolvió en 10 c.c. de alcohol etílico, se agregó 200 mg. de Pantozyme "Wander" y luego se completó a 25 c.c. con solución tampón de pH 6.0 preparada de acuerdo a la edición XV Farmacopea de Estados Unidos (F.E.U.), se agitó hasta obtener una mezcla homogénea y se dejó a la temperatura ambiente. Se preparó otra solución en la misma forma, pero para su hidrólisis se le sometió a una temperatura de 37°C.
Con ambas soluciones se hicieron pruebas cada 30 minutos hasta las cinco horas, observándose que en la primera media hora ya se había producido una pequeña hidrólisis; de tres a cinco horas se obtuvo un 77.7% de actividad comparativamente con el standard de CAF levógiro; a las 24 horas se llegó a obtener un 97% de hidrólisis. Se siguieron haciendo ensayos después de las 24 horas, pero no se obtuvo modificación alguna.
Estearato de CAF.
Se preparó dos porciones de 228 mg. de estearato de CAF "Erba", equivalente cada una a 125 mg. de CAF levógiro, se procedió igual que para el palmitato. A las tres horas se obtuvo 83% de hidrólisis y a las 24 horas 87%. Después de éste tiempo no se observó modificación alguna.
Cinamato de CAF.
Se procedió como en los casos anteriores, variando sólo en la cantidad de sal tomada que fue de 180 mg. de cinamato de CAF equivalente a 125 mg. de CAF levógiro y se utilizó solución tampón de pH 8.0. A las tres horas se obtuvo un 40%, a las 24, 48 y 72 horas, 56.6%, a las 96 horas 71.6%. Después de este tiempo no hubo modificación.
Succinato de CAF.
Se preparó una solución madre disolviendo el contenido de un frasco de inyectable que contenía succinato sódico equivalente a 1 Gm. de CAF levógiro, en cantidad suficiente de solución tampón de pH 6.0 para hacer 10 c.c. Después de hallar su concentración exacta por el método espectrofotométrico, se tomó dos partes alícuotas equivalentes a 250 mg. de CAF levógiro, se agregó a cada una 400 mg. de Pantozyme "Wander" y se siguió el procedimiento como en los casos anteriores.
Después de 30 minutos se obtuvo un 34.2% de actividad, a las 24 horas 63.5%, a las 48 horas 70%, a las 72 horas 73.3%, a las 96 horas 83%, a las 120 horas, 85%; se siguió con las pruebas hasta obtener un máximo de hidrólisis lo cual se consiguió a los 8 días con un 92.5% de actividad; a partir de este tiempo, no se obtuvo aumento alguno.
Aplicación del método a las especialidades farmacéuticas.
Se tomó en todos los casos una cantidad de muestra equivalente a 125 mg. de CAF levógiro y se hizo la extracción del éster, agregando primero 20 c.c. de cloroformo, se agitó en un embudo de separación por varios minutos, luego se agregó 10 c.c. de solución de hidróxido de sodio al 10%; se volvió a agitar por un tiempo igual al anterior, cuidando de no emulsionar las dos capas; se separó la capa clorofórmica a un vaso de precipitado. La capa alcalina se volvió a agitar por dos veces más con porciones de 20 c.c. de cloroformo; reunidas las soluciones clorofórmicas, se evaporó el disolvente. El residuo se disolvió en 10 c.c. de alcohol etílico; se agregó 200 mg. de enzima y se completó a 25 c.c. con solución tampón de pH 6.0 para las muestras con palmitato y estearato, y con solución de pH 8.0 para las que llevaban cinamato.
Las concentraciones para las diluciones de los ensayos de actividad de los ésteres hidrolizados fueron: 32, 16, 8, 4, 2 y 1 mcg./c.c.
Para la valoración del CAF levógiro contenido en especialidades tales como cápsulas, grageas, pomadas, gotas o supositorios, se tomó una cantidad determinada de muestra; se disolvió en un volumen adecuado de alcohol y tampón de pH 6.0 para alcanzar una concentración de 10,000 mcg./c.c.; a partir de esta solución se hicieron las diluciones posteriores para obtener las concentraciones mencionadas más arriba. En caso de especialidades de tipo supositorio o pomada con vehículo no miscible con agua, se extrajo el antibiótico fundiendo la muestra en cantidad conveniente de la mezcla alcohol-tampón pH 6.0 a baja temperatura (50° a 60°C.).
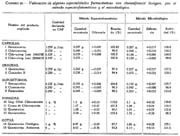
Los resultados obtenidos con ambos métodos aplicados a diferentes especialidades farmacéuticas se exponen en los cuadros Nos. II y III.
DISCUSIÓN
El método espectrofotométrico ha demostrado ser sencillo y sensible para hacer la valoración del cloramfenicol y sus ésteres. Mediante dicho método se pueden valorar soluciones cuyas concentraciones son menores de 60 mcg./c.c. para el cloramfenicol levógiro, 90 mcg./c.c. para el palmitato y estearato, y menores de 25 mcg./c.c. para el cinamato; concentraciones mayores que las indicadas no revelan sensibilidad al espectrofotómetro.
El método microbiológico utilizado manifiesta también gran sensibilidad, puesto que las determinaciones pueden hacerse hasta con concentraciones de 0.5 mcg./c.c.; además, es de fácil manipulación siendo su empleo muy práctico en los análisis de rutina.
La separación de los ésteres contenidos en las especialidades, se hizo debido a la dificultad que ofrecían las diversas combinaciones frente a la hidrólisis enzimática; sólo en el caso del jarabe de microcetina se obtuvo el mismo resultado haciendo la hidrólisis tanto con extracción como sin ella; el vehículo indicado en la fórmula del producto era el jarabe simple, a diferencia de los otros cuyos componentes eran más complejos.
El cloroformo empleado como solvente en la extracción, en la proporción indicada en el método operatorio, dio buen resultado.
Entre los ésteres, el más fácil de hidrolizar, y que por consiguiente, da mayor liberación de CAF activo, fue el palmitato; le siguen en orden decreciente, el estearato, cinamato y succinato. En la bibliografía consultada (CERIOTTI y col. 1954), indica que el cinamato tiene acción antimicrobiana aún sin hidrolizarse; nosotros no hemos llegado a obtener tal resultado.
Se ha comprobado también que la enzima empleada, no tiene efecto contrario sobre el desarrollo del germen utilizado en el ensayo. Se ha probado además la influencia que puede tener un aumento en la cantidad de enzima llegando a la conclusión de que no da lugar a variación alguna en la velocidad de la reacción hidrolítica.
Para el palmitato, estearato y succinato, se ha realizado la hidrólisis a un pH 5.5-6.0, lo que nos hace suponer que ha sido la pepsina, del producto utilizado como fuente hidrolizante, la que ha tenido acción preponderante; para el cinamato se obtuvo mejor resultado a un pH 7.5-8.0. En la bibliografía consultada (TROLLE-LASSEN, 1954) indican un margen de 3.0-8.0.
Entre las sales puras sometidas a digestión enzimática, fue el cinamato el que dio un porcentaje de actividad por debajo del requerimiento mínimo de potencia antibiótica (85%) exigida por la F.E.U. y las regulaciones del F.D.A., la causa podría ser la dificultad que ofrece para hidrolizarse; sin embargo, el cinamato obtenido por extracción a partir de jarabes dio mejor resultado en cuanto a actividad, pues se obtuvo con una de las muestras hasta 93.2 %, aunque este aumento podría deberse al mayor contenido de sal en las muestras, conforme se ve en el resultado obtenido por el método espectrofotométrico.
Las técnicas consultadas para llevar a cabo la hidrólisis enzimática (GHIONE y FIORETTI, 1956; PAULETTA, 1952: TROLLE-LASSEN, 1954) recomiendan no utilizar enzima de origen vegetal porque no da buen resultado. Esto lo hemos podido comprobar haciendo actuar papaina sobre el palmitato. En lo que respecta a la hidrólisis ácida (HC1) el rendimiento es muy bajo conforme indica PAULETTA (1952); se corre además el riesgo de escindir el grupo - NH-CO - de la molécula con la consiguiente pérdida de actividad.
Realizando la hidrólisis con Pantozyme "Wander", a 37°C, no se obtuvo incremento digno de tomarse en cuenta en la velocidad de la reacción, pues los resultados obtenidos fueron similares a los alcanzados a temperatura ambiente; TROLLE-LASSEN (1954) indica que la hidrólisis máxima se puede obtener a las 4 horas si la temperatura oscila entre 35°C y 40°C. En la realización del presente trabajo, el mayor porcentaje de actividad se ha obtenido con sales puras de palmitato y estearato a las 24 horas; y a las 48 horas para las mismas sales extraídas de especialidades farmacéuticas; 8 días para el succinto; para el cinamato extraído de los jarabes fueron necesarias 144 horas, mientras que para la sal pura de cinamato fueron 96 horas las empleadas, tanto a temperatura ambiente como a 37°C.
En las diferentes determinaciones se ha considerado tiempo suficiente aquel que dio lugar a la primera lectura no variable, pues se realizaron ensayos hasta obtener lecturas constantes en el diámetro de las zonas de inhibición de desarrollo del germen sensible empleado en la valoración.
Como se puede observar en los cuadros II y III, ambos métodos proporcionaron resultados satisfactorios, pero el método microbiológico es el que precisa la actividad antibacteriana que es lo que interesa desde el punto de vista terapéutico.
REFERENCIAS
1. CERIOTTI, G., DEFRANCESCHI, A., DE CARNERI, I. E ZAMBONI, V. Ricerche esperimentali su un Derivato Solubile in Acqua del Cloroamfenicolo: il Succinato de Cloroamfenicolo. II Farmaco. Ed. Cientifica, 9:21- 38. 1954. [ Links ]
2. FARMACOPEA FRANCESA, Ed. VII. Primer Suplemento: 24-25. 1954.
3. FOOD AND DRUG ADMINISTRATlON (EE.UU.) Compilations of Regulations for Tests and Methods of Assay and Certification of Antibiotic and Antibiotic-Containing Drugs. 1: D1-D15. 1957. [ Links ]
4. GHIONE, M. e FIORETTI, L. Titolazione Microbiologica di esteri insolubili del Cloroamfenicolo. II Farmaco. Ed. Cientifica, 11: 139-144. 1956. [ Links ]
5. MORALES, S., J. y VELAZCO, C. Curvas Standard y Determinación de Potencia Antibiótica. Rev. Med. exp., Lima, 11: 92-103. 1957. [ Links ]
6. MORALES, S. J. Control Microbiológico de Antibióticos. Rev. Med. exp., Lima, 11:1-64. 1958. [ Links ]
7. PAULETTA, G. Attivita di Alcuni Esteri del Cloroamfenicolo Suministrati per Via Orale.- II Farmaco Ed. Cientifica, 7:3-10. 1952. [ Links ]
8. TROLLE-LASSEN, C. Undersogelser over en Enzymatisk-Mikrobiologisk Analysemetode for Kloramfenicolestre.- Archiv. Phar. Chemi., Copenhagen, 61:435-452. 1954. [ Links ]
9. UNITED STATES PHARMACOPEIA. Ed. XV, 140-142 y 852-853. 1955.
10. URQUlZO B. SOLEDAD. Valoración del Cloramfenicol en especialidades farmacéuticas.- Tesis de Bachiller, Facultad de Farmacia y Bioquímica, Universidad Nacional Mayor de San Marcos, Lima-Perú. 1957.
[ Links ]