Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Medicina Experimental y Salud Publica
versión impresa ISSN 1726-4634
Rev. perú. med. exp. salud publica v.14 n.1 Lima ene./jul. 1997
ARTÍCULOS CIENTÍFICOS
Determinación de IgG y anticuerpos totales contra el Virus Dengue, en muestras obtenidas en papel filtro
García María1; Cabezas César1; Callahan Johny2; Yana Benedicta2; Gutiérrez Victoria1; Ortiz Ana1; Anaya Elizabeth1
1 Departamento de Virología, Centro Nacional de Laboratorios de Salud Pública, Instituto Nacional de Salud, A.P 451 Lima, Perú.
2 USA NAMRID. Naval Medical Research Institute Detachment, Unit 3800, APO AA 34031, Lima, Perú.
RESUMEN
Se propone como alternativa para la determinación de anticuerpos contra el virus del dengue, el uso de muestras de sangre total obtenidos en papel filtro, por ser un método sencillo y no requerir de muchos cuidados en el envío al laboratorio. Se evaluaron 100 muestras de suero obtenidas en tubos al vacío y sangre total en papel filtro respectivamente, de pacientes con diagnóstico clínico de Dengue clásico. Ambas muestras fueron evaluadas con los métodos serológicos de ELISA Indirecta para detectar IgG e Inhibición de la Hemoaglutinación para detectar anticuerpos totales.
Por ELISA indirecta se obtuvo un total de 51 positivos y 49 negativos en suero; 45 positivos y 48 negativos en papel filtro, con una concordancia por índice Kappa de 0.92, sensibilidad de 88% y especificidad de 98%. Por Inhibición de la Hemaglutinación se obtuvo un total de 45 positivos y 55 negativos en suero; 40 positivos y 50 negativos en papel filtro, con una concordancia por índice Kappa de 0,88, sensibilidad de 87% y especificidad de 91%.
Palabra clave: Anticuerpos IgG, Virus del Dengue, Papel Filtro
ABSTRACT
This present study suggest an alternative to determine dengue (DEN) antibodies from whole blood samples on filter paper because this method is simple and it requires less details for the shipment of samples to the laboratory. A total of 100 sera samples in vacutainers and total blood samples on filter paper were obtained from patients with clinical diagnosis of DEN ELISA for IgG and by hemagglutination Inhibition for total antibodies.
The Indirect ELISA results indicated 51 positive and 49 negative samples among the sera; 45 positive and 48 negative in filter paper samples. The test has a concordance 0,92 Kappa Index, 88% and 98% of sensitibity and specificity respectively. The Hemagglutation Inhibition test results indicated 45 positive and 55 negative samples among the sera; 40 positive and 50 negative results on filter paper. The test has 0,88 Kappa index, 87% and 91% of sensitibity and specificity respectively.
Key word: Antibodies, IgG, DEN viruses, filter paper.
INTRODUCCIÓN
El dengue constituye un serio problema de salud pública en las Américas1. En 1990 se produjo la primera epidemia de dengue clásico en el Perú, habiéndose registrado un total de 9 623 casos, en los departamentos de Loreto, San Martín, y Ucayali; el serotipo aislado fue el 1 hasta 1995; desde entonces se han presentado casos de dengue en 10 departamentos (Tumbes, Piura, Amazonas, San Martín, Loreto, Huánuco, Ucayali, Junín, Madre de Dios, y Cajamarca). En 1995 se aisló el serotipo 2 en Piura. La última localidad involucrada es Bagua Grande en Amazonas donde se ha aislado el serotipo 2 en enero de 1996.2
Si bien se estima que 2 747 891 personas que habitan en las localidades afectadas están en riesgo de desarrollar dengue hemorrágico,3 no se tiene información sobre la prevalencia de la infección previa y que esté basada en estudios de laboratorio, por lo que es importante realizar estudios de prevalencia adecuadamente diseñados y contar con técnicas de laboratorio, que sean de fácil realización desde la obtención de muestras en el campo y su procesamiento en el laboratorio. También es importante la detección precoz de casos de dengue durante los brotes de enfermedades febriles, con carácter epidémico.
Existen diversos métodos para la detección de anticuerpos circulantes tanto IgM como IgG utilizando muestras de suero;4,5,6 sin embargo, cuando se realizan pruebas de campo, se deben considerar las dificultades que pueden darse para la obtención de la muestra de sangre, la obtención del suero, su conservación y envío al laboratorio, y además otras como escasez de materiales e insuficiente capacitación del personal operativo.
Una alternativa para la determinación de anticuerpos para dengue es la obtención de la muestra de sangre en papel filtro, procedimiento que es sencillo y no requiere de muchos cuidados para su envío al laboratorio, además que reduce los costos. Hay estudios que muestran las bondades de esta técnica para detectar IgG y anticuerpos totales, sin embargo, es necesaria su estandarización en nuestro medio4,7,8.
La estandarización de este método, permitirá mejorar el diagnóstico y facilitar la realización de estudios seroepidemiológicos en el Perú con los beneficios de contribuir en el control y vigilancia del dengue.
MATERIALES Y MÉTODOS
El presente estudio se realizó después del brote epidémico ocurrido en Amazonas-Bagua Grande (noviembre de 1995 hasta enero de 1996).
Obtención de la muestra
La obtención de las muestras se efectuó en el mes de marzo de 1996, realizándose el muestreo serológico en 100 pacientes con diagnóstico clínico de Dengue clásico y el antecedente epidemiológico de residir en un área con presencia de Aedes aegypti.
Papel filtro
Para la obtención de muestras se utilizó papel filtro Whatman No 3 con un diámetro de 11mm, el cual adsorbe aproximadamente a 50 uL de sangre total.
La obtención de la muestra, se realizó mediante una punción en el pulpejo del dedo y se procedió a absorber la sangre directamente; la muestra debía cubrir el diámetro indicado por el círculo marcado, se dejó secar al medio ambiente en un lugar protegido de la luz solar directa. Se colocaron en bolsas de plástico para transportarlas al laboratorio. Se llenó una ficha clínica-epidemiológica para cada paciente.
Suero
Se obtuvieron 100 muestras de sangre venosa en tubos al vacío de las mismas personas a las que se habían obtenido muestras en papel filtro utilizando la técnica de tubos al vacío.
Las muestras de sangre fueron procesadas para la obtención de suero y mantenidas a -10oC hasta su envío al Laboratorio de Virología, Centro Nacional de Laboratorio de Salud Pública del Instituto Nacional de Salud (Lima, Perú).
Elución de la muestra
Prueba de ELISA Indirecta
En la prueba de ELISA Indirecta para detectar anticuerpos de tipo IgG; la elución de discos de papel filtro absorbidos con sangre se realizó con 2 ml de buffer fosfato salino (PBS) con albumina bovina fracción V al 0,5% pH 7,2 a 4oC durante toda la noche, obteniendo una dilución de 1:100 como lo requiere el método utilizado.
Las muestras de suero, se diluyeron siguiendo el protocolo del ELISA Indirecto estandarizado por el Naval Medical Research Institute Detachment (NAMRID).
El antígeno utilizado en la prueba ELISA Indirecto precede de células VERO infectadas con virus Dengue 1 cepa Hawaii lisadas por sonicación.
El conjugado empleado es una inmunoglobulina anti IgG marcada con peroxidasa (Affinity purified Antibody Peroxidase Labeled Goat Anti Human IgA + IgG + IgMH+L).
El Valor de corte se obtiene mediante XN+3DS.
Considerando en la prueba el valor de 0,2 como límite para la evaluación de los resultados:
Densidades ópticas < 0.2 : Negativo
Densidades ópticas > 0.2 : Positivo
Prueba de Inhibición de la Hemaglutinación
Para la prueba de Inhibición de la Hemaglutinación la elución del papel filtro se realizó con 450 uL de buffer borato salino 0,5 M pH 9,0 a 4oC durante toda la noche. Se eliminó el papel filtro y se agregó 500 uL de kaolin al 25% al eluido, con agitación ocasional x 30min. a temperatura ambiente para eliminar los inhibidores inespecíficos. Se centrifugó a 2,000 durante rpm 30min.
Luego cada muestra fué absorvida con 25ml de hematíes de ganso al 50% en solución salina fisiológica manteniendo a 4oC x 20min. con agitación ocasional. Se centrifugó a 1500 rpm durante 15min. a 4oC; obteniendo una dilución final de 1:20.
Las muestras de suero fueron tratadas con kaolin al 25% y hematíes al 0.5%; según el método convencional de Clark y Casals6.
Una vez obtenidas las muestras tratadas se realizó la detección de los anticuerpos utilizando la prueba de Inhibición de la Hemaglutinación (IHA) para detectar anticuerpos totales.
Los materiales que utiliza la prueba de Inhibición de la Hemaglutinación son los mismos descritos por Clark y Casals, modificado por el Instituto Pedro Kouri (IPK)5.
El antígeno utilizado para la prueba de Inhibición de la Hemaglutinación (IHA) fué obtenido a partir de cerebro de ratón lactante infectado tratado con sucrosa y acetona e inactivado con Beta-propiolactona.
Título >1: 20 : Anticuerpos detectables
Título <1: 20 : Anticuerpos no detectables
INTERPRETACIÓN DE RESULTADOS
Indice Kappa: es un test de concordancia que se basa en la comparación de índices de concordancia esperado (pe) con los índices de concordancia observados (po).9 Se clasificaron en 5 grupos:
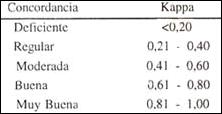
Positivo para ELISA: Cuando presentan densidad ópticas (DO) igual o superior al valor de corte (0,2) para la prueba ELISA Indirecta.
Positivo para IH: Si el título es mayor o igual a 1/20.
RESULTADOS
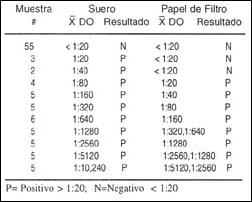
Los resultados de la prueba de ELISA Indirecta, comparando las muestras de suero y las muestras obtenidas en papel filtro se observan en la Tabla N l. La misma comparación cuando se utiliza la prueba de Inhibición de Hemaglutinación (IHA) se muestra en la Tabla 2.
Se observó que en 93 muestras los resultados de la prueba ELISA Indirecta fueron coincidentes (45 positivos y 48 negativos); 6 muestras positivas en el suero no fueron detectados en el papel filtro y una muestra fue considerada como falsa positiva.
En la prueba de Inhibición de la Hemaglutinación coincidieron 89 (39 positivos y 50 negativos) 6 muestras positivas en el suero no fueron detectadas en papel filtro y 5 muestras fueron consideradas falsas positivas.
Los resultados serológicos a partir de muestras de suero y muestras obtenidas en papel filtro, fueron sometidos a evaluación, presentando una sensibilidad para ELISA Indirecta e Inhibición de la Hemaglutinación de (88% y 87%) y una especificidad de 98% y 91% respectivamente. Así mismo se les aplicó la prueba de concordancia del Indice Kappa obteniendo un resultado de 0,92 para ELISA Indirecta y 0,88 para IHA.
La Tabla 3 muestra una diferencia entre las densidades ópticas de las muestras obtenidas en papel filtro y las densidades ópticas de las muestras de suero.
La Tabla 4 muestra una disminución en 1 y 2 diluciones entre el título de las muestras en papel filtro y el título de las muestras séricas.
Tabla 1. Resultado comparativo de IgG anti Dengue,
en suero y papel filtro, utilizando la prueba
de ELISA indirecta
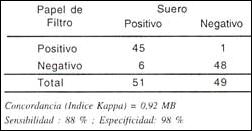
Tabla 2. Resultado comparativo de anticuerpos totales
anti-Dengue, en suero y papel filtro,
utilizando la prueba de IHA
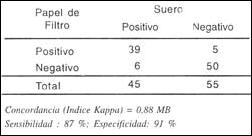
Tabla 3. Promedio de las densidades ópticas (DO)
obtenidas en suero y papel filtro,
por la prueba de Elisa indirecta
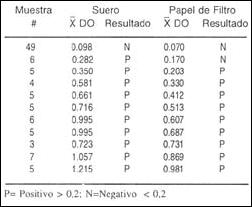
Tabla 4. Título en suero y papel filtro, en la prueba de inhibición
de hemaglutinación
DISCUSIÓN
Los resultados obtenidos en este estudio son comparables a otros realizados por Guzmán y col.7, Vásquez y col8 y Kuno y col.4; quienes emplearon papel filtro para la recolección de sangre, el método de Inhibición de la Hemaglutination7, ELISA de Inhibición8 y ELISA Indirecta para la evaluación serológica de las muestras recolectadas.
La sensibilidad obtenida en este estudio por el método de Inhibición de la Hemaglutination fue del 88%, siendo superior a la obtenida por otros autores2 quienes reportan una sensibilidad de 82% cuando las muestras en papel filtro fueron almacenadas a temperatura ambiente y procesadas a los 30 días.
La sensibilidad reportada para las pruebas de ELISA Indirecta y de Inhibición es de 96% a 99%4,8, mientras que en este estudio se encontró 88% utilizando ELISA Indirecta.
Hay variaciones en la sensibilidad cuando las muestras son procesadas en períodos diferentes luego de la obtención de la muestra, también es importante la conservación de los mismos10. La diferencia en la sensibilidad encontrada con la reportada podría estar relacionada a que nuestras muestras fueron almacenadas al medio ambiente, mientras que en los otros reportes fueron conservadas a 4oC. Consideramos importante evaluar la utilidad de las muestras conservadas al medio ambiente por las limitaciones de la cadena de frío en estudios epidemiológicos.
Cuando se estudiaron otras etiologías, algunos autores encontraron que al conservar sueros vidos en papel filtro y en bolsas de polietileno el de sílica a temperaturas menores o iguales oC durante un año los niveles de anticuerpos disminuyen sólo en un título10.
La diferencia entre las densidades ópticas (DO) de la muestra de suero y el obtenido en papel filtro en la prueba de ELISA Indirecta fue de 0,1 a 0,3 tal como se muestra en la tabla 3; de igual forma la diferencia de los títulos obtenidos en sueros y papel filtro por la prueba de Inhibición de la Hemaglutinación mostró una disminución de 1 a 4 diluciones tal como se observa en la Tabla 4. Estos resultados podrían también explicar la sensibilidad obtenida en este estudio con respecto a los reportados a otros trabajos4,7.
Al aplicar el Test de Concordancia mediante el Indice de Kappa9, se obtuvo un valor de 0,92 para ELISA Indirecta y un valor de 0,88 para Inhibición de la Hemaglutinación correspondiente a muy bueno.
La obtención de muestras de sangre para evaluar anticuerpos contra el dengue, utilizando papel filtro5,4,6 permitirá hacer encuestas seroepidemiológicas para delimitar zonas de riesgo y contar con cifras reales que orienten las programaciones considerando el riesgo del dengue hemorrágico, además de contribuir a la vigilancia epidemiológica con soporte laboratorial. La utilización de papel filtro trae consigo la facilidad de su realización, el bajo costo, aceptabilidad por parte de la población y facilidad para el transporte, con un margen de error poco significativo.
De acuerdo a los resultados obtenidos en este estudio consideramos que pueden utilizarse muestras de sangre colectadas en papel filtro para la detección de anticuerpos IgG y anticuerpos totales contra dengue por ELISA Indirecta e Inhibición de la Hemaglutinación respectivamente debiéndose continuar con las evaluaciones considerando otras variables como tipo de papel filtro, temperatura, tiempo de conservación de las muestras colectadas en papel filtro y dilución final de la elución, así como su aplicación a otras etiologías de interés para el país.
Nota
Las opiniones aquí vertidas constituyen opiniones particulares de los autores y no deben ser interpretadas como opiniones oficiales o que reflejen el parecer del Departamento de Marina de los Estados Unidos.
BIBLIOGRAFÍA
1. Publicación Científica No 548. OPS: Dengue y Dengue Hemorrágico en las Américas: Guía para su Prevención y Control. [ Links ]
2. Boletín INS, Año 2,3 Instituto Nacional de Salud, 1996. [ Links ]
3, Ministerio de Salud, Situación actual del Dengue. Programa Nacional de Control de Malaria y otras enfermedades, Lima 1996. [ Links ]
4. Kuno G, Gómez I, and Gubler DJ. An ELISA procedure for the diagnosis of dengue infections . Journal of Virological Methods, 1991; 33: 101-113. [ Links ]
5. Manual de procedimientos para el Diagnóstico de Arbovirus. IPK-Cuba; 1990. [ Links ]
6. Clark DH, Casals J.Techniques for hemagglutination and hemagglutination inhibition with arthropodborne viruses. Am J Trop Med Hyg 1958; 7: 561-573, [ Links ]
7. Guzmán M, Kouri G, y Bravo J, Normalización de la toma de muestra de sangre en papel de filtro para la serología del dengue. Rev. Cub. Trop. 1982; 34: 114-118. [ Links ]
8 Vásquez S, Fernández R, Lorente C, Utilidad de sangre almacenada en papel filtro para estudios serológicos por ELISA de inhibición. Revista del Instituto de Medicina Tropical. Sao Paulo 1991; 33:309-11. [ Links ]
9. Cura E, Mendel S. Manual de Procedimientos de Control de Calidad para los Laboratorios de Serología de los Bancos de Sangre. Organización Panamericana de la Salud (OPS). 1994. [ Links ]
10. Marinkelle CJ, De Sánchez N, Grogl M, y Gurl F. Recomendaciones para el almacenamiento de sueros absorvidos en papel filtro bajo condiciones rurales, para el diagnóstico de infección chagásica con la prueba de inmunofluorescencia. Revista del Instituto de Medicina Tropical. Sao Paulo. 1978.20 (2):112-114. [ Links ]














