Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Medicina Experimental y Salud Publica
versión impresa ISSN 1726-4634
Rev. perú. med. exp. salud publica v.17 n.1-4 Lima 2000
TEMA DE REVISIÓN
Diagnóstico Parasitológico de la Leishmaniasis Tegumentaria Americana
César Augusto Cuba Cuba1
1 Departamento de Patología, Universidad de Brasilia, Brasil.
RESUMEN
La demostración directa o indirecta de Leishmania en las muestras patológicas continúa siendo un importante desafío en el diagnóstico parasitológico de esta protozoosis. A pesar de los avances significativos surgidos en investigaciones de biología molecular, muchas de sus técnicas con potencial aplicación diagnóstica, continúan siendo solamente herramientas de los laboratorios de investigación científica. Pocas de ellas se encuentran en fase de valorización clínica y epidemiológica en áreas endémicas, y quizás, de manera optimista, muy pocas estarían a disposición de los laboratorios de diagnóstico de salud pública en la próxima década. Mientras tanto, seguiremos contando con el auxilio de los llamados métodos clásicos de la Parasitología básica que todavía, en las manos de individuos experimentados, diagnostican la gran mayoría de los casos.
Este artículo identifica los métodos recomendados por los especialistas del tema, describe los procedimientos consagrados por su sensibilidad y reproductibilidad, concluyendo que éstos continuarán vigentes, siempre que sean correctamente ejecutados.
Palabras clave: Leishmaniasis cutánea/diagnóstico; Leishmaniasis mucotánea/diagnóstico; Parasitología/métodos (fuente: BIREME).
ABSTRACT
Direct or indirect demonstration of Leishmania in pathological samples still constitutes a critical challenge when it comes to the parasitological diagnosis of this protozoose. In spite of significant and novel advances in the field of molecular biology of Leishmania, many of the techniques with a real potential diagnostic application, still continue to be the tools for laboratory scientific investigation. Few methods are in the stage of clinical and epidemiological application in endemic areas. Being optimistic, very few techniques would be available at public health laboratories in the next decade in developing countries, where these parasites are prevalent. Meanwhile, we will have to continue to rely on the so called classical methods of Basic Protozoology, which under the supervision of experienced professionals will provide a diagnosis for the great majority of the cases.
This overview identifies the methods recommended by experts in this field, it also describes the procedures widely recognized by its sensitiveness and reproducibility, and it demonstrates that these methods will continue to be used if they are appropriately performed.
Key words: Leishmaniasis cutaneous/diagnosis; Leishmaniasis mucotaneus/diagnosis; Parasitology/methods (source: BIREME).
INTRODUCCIÓN
El género Leishmania comprende protozoarios parásitos pertenecientes a la Familia Trypanosomatidae y al Orden Kinetoplastida, cuya principal característica estructural es la de poseer un orgánulo citoplasmático: el kinetoplasto. La presencia de este último, es de capital importancia en la identificación morfológica de las fases evolutivas del género Leishmania.
El ciclo evolutivo, aparentemente simple, transcurre en dos huéspedes: un vertebrado (el hombre y otros mamíferos susceptibles), y un invertebrado (un insecto, la hembra hematófaga de un flebótomo del género Lutzomyia (Diptera, Psychodiidae). En el flebótomo, dos formas evolutivas se desarrollan en el tubo digestivo: una forma fiagelada, las promastigotes, con capacidad de multiplicarse asexualmente por división binaria longitudinal; y otra forma, que se diferencia morfológica y fisiológicamente para pre-adaptarse al parasitismo intracelular en el hospedero mamífero, éstas son las formas de promastigotas metacíclicas o formas infectantes 1. Cuando el insecto pica un vertebrado susceptible, las formas metacíclicas son inoculadas en la piel y dermis, y son fagocitadas por las células del Sistema Fagocitario Mononuclear (SFM). Las células invadidas permiten la transformación de las formas flageladas en formas amastigotes, en el interior de las vacuolas parasitóforas. Los amastigotes de Leishmania tienen la capacidad de evadir la acción parasiticida de las células del SFM y además, de multiplicarse por división binaria simple asexuada. Muchas de esas células liberan los amastigotes, en tanto que otras células, fagocitan los parásitos diseminando así el parasitismo en los tejidos, nódulos linfáticos y otras localizaciones tegumentarias. El resultado del proceso referido es la configuración de cuadros cutáneos y mucosos polifacéticos. Sumariamente, son vistas lesiones de tipo ulceroso, nodular, necrótico, vegetante, plaquetiforme, etc. Este polimorfismo clínico de las leishmaniasis cutáneas y mucosas influencian substancialmente los procedimientos empleados en el diagnóstico parasitológico.
Lamentablemente, cierto porcentaje de los individuos parasitados con algunas especies del sub-género Viannia (ver Tabla 1) desarrollan lesiones metastásicas con localizaciones subcutáneas linfonodulares, llamadas formas «esporotricoides» causadas por L.(V). guyanensis2, y localización en ganglios linfáticos3.4 y mucosa del tracto respiratorio naso-buco-faríngeo-laringeos provocadas por L. braziliensis y, menos frecuentemente, por L. panamensis6,7.
Un cuadro clínico caracterizado por una anergia selectiva en la inmunidad celular del individuo afectado, es la entidad nosológica conocida como Leishmaniasis Cutánea Difusa (LCD). En América, los infectados con L. amazonensis presentan un parasitismo extremamente agresivo e incurable: nódulos subcutáneos, y/o placas coalescentes, no ulceradas, que contienen un número impresionante de amastigotes y que, generalmente, respetan las mucosas. En individuos inmunocompetentes, parasitados por L. (L) amazonensis, las lesiones son delimitadas, curables, pero interesantemente, presentan un porcentaje elevado de pacientes reactores negativos a la reacción de Montenegro8.
La preocupación de varios investigadores con relación a la etiopatogenia de las leishmanias es la comprobación de las vías probables de diseminación del parasitismo por Leishmania. La comprobación de la hipótesis de difusión hematógena y/o linfática ha producido resultados contradictorios. Los cultivos de la llamada «crema leucocitaria» de un paciente mucoso resultaron positivos según lo reportado por Bowdre 9, en tanto que, los aislamientos de Leishmania de linfonódulos vecinos a las lesiones, refuerzan la hipótesis de diseminación hematogénica y/o linfática 3. Nosotros fracasamos en los intentos de aislar L. (V) braziliensis en cultivos de monocitos circulantes, en pacientes cutáneos y mucocutáneos 10,11. Recientemente, Silveira no logró demostrar, en sangre periférica de pacientes parasitados por L. (L) Amazonensis, amastigotes circulantes usando hemocultivo 12 ; y últimamente, el asunto ha sido actualizado por Martínez quien refiere haber aislado L.(V) braziliensis de dos pacientes con lesiones mucosas: los parásitos fueron evidenciados por centrifugación diferencial de células mononucleares de sangre circulante 13. Todo esto no quiere decir que pensemos incluir como rutina diagnóstica, al hemocultivo, ya que consideramos este fenómeno un hecho esporádico y de difícil reproducibilidad.
Las leishmaniasis tegumentarias son diagnosticadas, en conclusión, cuando se demuestra la presencia de amastigotes en las lesiones sugestivas de este parasitismo. Igualmente, si por cultivo «in vitro», comprobamos la evolución de formas promastigotes derivadas de las respectivas formas intracelulares.
Es bien conocido que, las leishmaniasis tegumentarias son causadas por una variedad de diferentes miembros del género Leishmania. Se sabe también que la patogenicidad, abordaje terapéutico y los posibles métodos de control de este complejo síndrome de enfermedades son determinados, en gran parte, por la especie de Leishmania. Es, por lo tanto, extremadamente importante que en cualquier caso de leishmaniasis el agente etiológico sea identificado. En ese sentido, los científicos vienen desplegando considerables esfuerzos para conseguir métodos que asocien diagnóstico e identificación en forma simultánea. La sonda ideal sería aquella de sensibilidad, especificidad y reproducibilidad total, aplicada directamente en las muestras retiradas de las heridas de los pacientes. Aparentemente los biólogos moleculares estarían próximos a proporcionarnos estas herramientas.
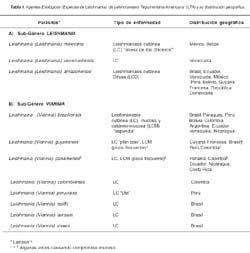
La Tabla 1 nos muestra las especies de Leishmania descritas que parasitan al hombre, así como su distribución geográfica en América. La especie predominante en la gran mayoría de focos endémicos y brotes epidémicos 14 de Leishmaniasis Tegumentaria Americana (LTA) es L. V. braziliensis 15-17, lamentablemente, esta es la especie más difícil de diagnosticar y tratar.
MÉTODOS Y TÉCNICAS DE DIAGNÓSTICO PARASITOLÓGICO DE LTA
Debemos siempre tener en cuenta que los procedimientos empleados en el diagnóstico de LTA dependerán, en gran parte, de la finalidad e infraestructura del laboratorio en que actuemos. Si se trata de un laboratorio de investigación, que apoya logísticamente estudios epidemiológicos en áreas endémicas, la metodología será más compleja; sin embargo, si se trata de un laboratorio hospitalario o de una posta médica de salud, escogeremos las técnicas que por su simplicidad, costo y reproducibilidad sean las más efectivas y sensibles.
Por otro lado, sabemos que, debido al polimorfismo clínico de la LTA, los métodos de demostración y aislamiento de los parásitos variarán en la obtención de las muestras.
La Tabla 2 presenta una revisión parcial de la literatura recientemente publicada, y en el que pretendemos mostrar la interdependencia que existe entre el tipo de procedimiento utilizado en la colecta de las muestras clínicas y la sensibilidad del diagnóstico parasitológico.
Dos alternativas surgen en el diagnóstico parasitológico. La primera será demostrar que el paciente está albergando Leishmania: lo haremos visualizando los amastigotes en los tejidos infectados. La segunda opción, será intentar aislar directamente de las lesiones sospechosas, en cultivos «in vitro» los promastigotes. Ambas son las más recomendadas, aunque en la práctica, en los servicios de salud pública solamente los frotices de material de las lesiones son ejecutados. Sin embargo, ambos procedimientos son aplicados de rutina en los estudios epidemiológicos, en muchos focos endémicos de América.
En la siguiente secuencia de este artículo discutiremos algunas dificultades encontradas en la investigación de Leishmania en pacientes. Se formularán recomendaciones y se señalarán pequeños detalles para reforzar la habilidad de diagnosticar los parásitos.
COLECCIÓN DE MUESTRAS PATOLÓGICAS
1. Investigación de Amastigotes
1.1. De lesiones cutáneas:
La úlcera es la más frecuente presentación clínica de LTA. Independientemente de la especie de Leishmania causante del cuadro dermatológico, estas lesiones ulcerosas francas generalmente se encuentran contaminadas secundariamente con diversos patógenos. Pueden estar presentes hongos como Paracoccidiodes braziliensis, y Histoplasma capsulatum, Sporothrix schenckii y bacterias piogénicas, tipo Staphylococcus y Streptococcus, o también Mycobacterium.
Es práctica universal proceder a ejecutar una buena tarea aséptica previa, a la toma de la muestra. Se usan líquidos antisépticos como agua oxigenada (10 volúmenes), Furacin (0,22 mg/ml), alcohol al 95% o alcohol al 70%. La finalidad es remover el material costroso, tejidos necrotizados, pus y otros detritos de las lesiones. Incluso, algunos han realizado estudios comparativos entre el uso de la solución iodada con una solución de agua y jabón en la optimización de la asepsia de las heridas, previas al cultivo de Leishmania, concluyendo que no existía diferencias en la utilización de uno u otro elemento en cuanto a su potencial interferencia en la viabilidad del parásito.
Esta primera etapa del trabajo diagnóstico es importante y ha recibido la atención de muchos investigadores, quienes, dependiendo del método de recolección utilizado, han encontrado una eficiencia en sus resultados que varía entre 18,0% y 52,0%. El porcentaje encontrado por Navin 19 en 65 lesiones de pacientes infectados, supuestamente, por L. (V) braziliensis y/o L. (L) mexicana, es sorprendentemente elevado con relación a otras observaciones y a las nuestras. Pensamos que los autores diagnosticaron pacientes infectados predominantemente por L. (L) mexicana, sub-género caracterizado por su elevada densidad parasitaria.
Cuando, por el contrario, los parásitos circulantes en áreas endémicas pertenecen al sub-género Viannia, la eficiencia de visualización y aislamiento de Leishmania es menor. Los resultados por frotices se sitúan en un índice de alrededor de 30,0% - 40,0% de los pacientes infectados.
Los datos de la literatura que mejor se comparan son los de Brasil y Colombia, esto debido al empleo de protocolos similares de diagnóstico parasitológico. En Brasil, desde el inicio de nuestros estudios, observamos que visualizar amastigotes de Leishmania en nuestros pacientes era tarea difícil. Esa dificultad, está relacionada con la biología del parasitismo que cada especie exhibe en el hospedero humano: en 1981, diagnosticamos en los frotices directos de las lesiones 25,0% de resultados positivos, quince años después, esta figura mejoró a 44,0%.
Sobre el aporte de la histopatología, siempre fue y continúa siendo difícil para un patólogo visualizar amastigotes de Leishmania en los cortes de tejido rutinariamente coloreados por hematoxilina-eosina (H&E). Nosotros afirmamos esto porque frecuentemente observamos que fragmentos de las mismas biopsias presentaban parásitos en los frotices coloreados por Giemsa. En nuestra casuística inicial, nuestro patólogo describió un 27,0% de histología positiva, similar a otras series de 28,0% 22 y muy parecidas a las de Weigle (21, 0%) 23, Navin (18,0%) 19 y Dimier-David (26,6%) 24.
Es digno de mencionar el comentario de Ridley25, que dice que la mayoría de patólogos están de acuerdo que un diagnóstico histológico confiable de leishmaniasis es imposible sin la identificación del parásito. En este contexto, una alternativa sería el empleo de la técnica de Giemsa-colophonium 26, empleada en la coloración de los parásitos tisulares de malaria. En nuestra experiencia, limitada a observaciones de leishmaniasis experimental en hamsters, los amastigotes de L.(V) braziliensis son bien evidenciados, especialmente por una nitidez mayor del kinetoplasto que se colorea de rojo intenso en los cortes clarificados por el colophonium. De acuerdo a nuestro conocimiento, esta técnica no ha sido evaluada en muestras humanas clínicas de LTA.
Un avance importante en este campo ha sido la introducción de técnicas inmunocitoquímicas. Sells 27 utilizó con éxito relativo la técnica de inmunoperoxidasa indirecta (IMPI) con un antisuero policlonal de conejo para marcar amastigotes en dos pacientes con leishmaniasis. La IMPI fue también evaluada en 265 biopsias de lesiones tegumentarias causadas por L. (V) braziliensis y L. (V) panamensis en Colombia; en este último estudio, la observación y localización de los parásitos fue más eficiente usando el método de IMPI (61,0% de positividad, en 181 pacientes) que lo obtenido con la histopatología convencional con H&E (34,8%), la eficiencia del método de IMPI fue mayor en lesiones precoces (75% de los casos con menos de 3 meses de evolución), 37,5% (6 meses) y 21% en los de 12 meses a más. Asímismo, el uso combinado del examen directo e IMPI permitió un diagnóstico etiológico de 72.0%28.
De otro lado, Lynch 29 y Anthony30 usaron anticuerpos monoclonales en la detección de amastigotes de lesiones cutáneas.
1.2 De lesiones Mucosas:
En relación con las formas mucosas únicas o múltiples, los procedimientos generalmente utilizados para el diagnóstico de amastigotes son:
- La biopsia obtenida con la ayuda de pinzas cortantes especiales (Cutting biopsy punch), después de la infiltración con un anestésico local (xylocaina al 10%, por ejemplo). Se retira un número variable de fragmentos de tejido en la dependencia de la extensión del granuloma y de su accesibilidad.
- Los frotices de las biopsias que, fijados con alcohol metílico o mejor, con líquido de Bouin, son coloreados por el método de Giemsa.
- Biopsias para estudios histopatológicos, fijadas con Formol-Zenker (neutro) al 10%, y cortes de Slim coloreadas por H&E.
Los datos parasitológicos cuantitativos de la infección mucosa son extremamente escasos. Muy pocas son las publicaciones que localizan la eficacia y sensibilidad de los procedimientos empleados. Generalmente el análisis del parasitismo se realiza en las formas cutáneomucosas. Todos sabemos que L. (V) braziliensis es difícil de diagnosticar en los granulomas mucosos31.
En 1981, nosotros informamos que de 27 pacientes, 5 (19,9%) fueron amastigotes positivos en los frotices de biopsias. En otra serie de pacientes, en 1984, publicamos los siguientes resultados para nuestros 51 pacientes evaluados: 27,4% de positividad en los frotices de las biopsias y 16,0% para los hallazgos histopatológicos. Estos resultados son opuestos a los de Dimier-David 24 que publicaron una positividad de 17,7% en 112 frotices de individuos con lesiones mucosas. Ellos describieron también que, en su casuística de 116 pacientes mucosos, la histopatología fue positiva en 28,4% constituyéndose ésta última, en su opinión, en la técnica más eficiente para la demostración parasitológica de L. (V) braziliensis.
Marsden 32 llama la atención que es más fácil detectar los parásitos en lesiones mucosas múltiples, que en lesiones únicas de L. (V) braziliensis; Dimier-David 24, en Bolivia, trabajando con infecciones causadas por L. (V) braziliensis en pacientes con lesiones mucosas múltiples y únicas, encontró similar información: 57,7% y 42,2% de positividad, respectivamente.
2. Investigación de Promastigotes
De las fases evolutivas de Leishmania, la forma promastigote es la más fácil de ser cultivada «in vitro», en ella se hacen la mayoría de las investigaciones parasitológicas. Enfatizando los aspectos médicos y epidemiológicos, los principales objetivos del cultivo de Leishmania son:
- El diagnóstico de la infección por los laboratorios de Salud Pública y de hospitales.
- El aislamiento primario del parásito del hombre, flebótomos y otros reservorios mamíferos, en los estudios epidemiológicos.
- La preparación de «stocks» de Leishmania, para estudios bioquímicos e inmunológicos de identificación, o la elaboración de antígenos convencionales no purificados.
- El clonaje de «stocks» y cepas representativas para tests «in vitro» de susceptibilidad o resistencia a los quimioterapéuticos.
No es nuestra intención revisar la extensa literatura publicada por diversos investigadores en relación al cultivo «in vitro» de Leishmania. Los lectores interesados pueden remitirse a las revisiones del tema hechas por Hendricks 33, Jaffe 34, y Evans 35. Se dará énfasis a los procedimientos y medios que, en nuestro concepto, han contribuido al mejor diagnóstico de LTA. Muchos de esos métodos han sido empleados por nuestro grupo a lo largo de los últimos 18 años de investigaciones en L. (V) braziliensis.
Ya en la década del 70, era opinión generalizada que los parásitos pertenecientes al hoy, sub-género Viannía (braziliensis complex), eran difíciles de cultivar. Este hecho era completamente opuesto a la facilidad con que se cultivaban las leishmanias del sub-género Leishmania (mexicana complex) en cualquier medio de agar sangre. Hoy sabemos que no existe un único medio de cultivo artificial capaz de reunir características tales que consiga cumplir los objetivos enunciados. Lo ideal sería un medio universal que sea sensible, líquido, liofilizable, que mantenga un tiempo de validez para su uso relativamente largo y, finalmente, sea protegido por antibióticos y antimicóticos36. Podemos afirmar que, continuamos aguardando la formulación de tal medio ideal, el que sería una gran contribución para los laboratorios de las áreas endémicas.
Diversos autores 37-39 han abordado el tema empleando diversos medios líquidos, normalmente utilizados en el cultivo de células de insectos, y también de células de mamíferos, en Leishmania del Nuevo y Viejo Mundo. Sin embargo, la regla básica es que se requieren diferentes medios de cultivo para cumplir diferentes finalidades, es decir, no existe un medio universal que sirva para aislar, multiplicar el parásito y mantenerlo por largo tiempo en subinóculos sucesivos y para obtener gran masa de células. Si bien existen medios que sirven para el transporte y mantenimiento prolongado de los parásitos ya adaptados artificialmente, ellos no son tan eficientes para propiciar la transformación de amastigotes en promastigotes, paso indispensable para un eficiente aislamiento primario del parásito en los pacientes de leishmaniasis. Además, el crecimiento de las diversas especies de Leishmania y de los diversos «stocks» aislados en puntos geográficos distintos es variable, por lo que se necesita del uso de varios tipos de medios.
Por lo tanto, es recomendable que cada área endémica de LTA ensaye primero algunos medios conocidos por su sensibilidad. Esto permitirá una mayor eficiencia futura en el aislamiento de los parásitos que circulan en el foco de transmisión.
3. Medios de Cultivo
3.1 Monofásicos (líquidos)
En el cultivo de Leishmania se han empleado medios de cultivo de células de mamíferos, suplementados con porcentajes variables de Suero Bovino Fetal (SBF). Algunos ejemplos de ellos, reportados en la literatura con eficacia variable, son: el medio de Eagle, el medio MEM (Mínimal Essential Medium, 20%, SBF), el medio 199 TC, y el Medio RPMI 1640. Estos medios son de difícil aplicación y uso en las áreas endémicas de los países pobres, ya que el costo y la necesidad de importación dificultan su aprovechamiento.
También se utilizan medios líquidos empleados en el cultivo de células de insectos, como por ejemplo el medio de Schneider (muy empleado en el cultivo de células de Drosophila y que ha tenido mayor difusión en nuestros países), el medio Grace y el medio de Mitsuhashi-Maramosch, estos dos últimos utilizados en aspectos biológicos moleculares de Leishmanial. Es oportuno comentar que la concentración del SBF empleada, reviste mucha importancia en el éxito del cultivo de Leishmania: todos los medios líquidos citados emplean concentraciones variables de SBF que fluctúan entre 10,0% y 20,0%.
3.2 Medios Bifásicos
Diversos autores han publicado listas detalladas de medios de cultivo sólidos, semisólidos y bifásicos empleados en el cultivo de los promastigotes y la cinética de crecimiento de Leishmania 33,35. Citaremos únicamente los más utilizados por los investigadores latinoamericanos:
- Medio Bifásico de Agar Sangre, NNN, 3N (Medio de Novy, McNeal, Nicolle)40: constituye el más antiguo y conocido medio empleado para el cultivo de parásitos hemáticos y tisulares.
- Medio de Agar Sangre USAMRU38: medio de composición simple, preparado con un agar base enriquecido, consagrado por la mayoría de los investigadores, en América.
- Medio de Senekjie: enriquecido con Bacto-peptona y Bacto-beef, ha sido constantemente utilizado en Panamá y Colombia con éxito en el diagnóstico de LTA.
Entre algunas de las ventajas prácticas de la adopción de medios bifásicos de agar sangre para el diagnóstico primario se mencionan las siguientes:
- Son particularmente valiosos para el aislamiento primario y el mantenimiento, por largo tiempo, de los «stocks» de Leishmania.
- Permiten la morfogénesis celular de amastigotes en promastigotes, en la gran mayoría de los aislados de L. (V) braziliensis, y de otras especies del sub-género Viannia, así como del sub-género Leishmania.
- Son apropiados para los estudios de curvas de crecimiento, lográndose densidades de 107-108 promastigotes por mL de cultivo «in vitro». El medio permite también el establecimiento de la fase estacionaria de crecimiento, en aproximadamente 6-7 días (ver Figura 2), característica importante para la mayor eficiencia de la infectividad de las cepas de Leishmania.
- Son de fácil preparación y de bajo costo, sobre todo en nuestro medio.
Entretanto, existen también algunos inconvenientes entre los cuales podríamos citar:
- La dificultad de poder estandarizarse, por ser químicamente complejos y no definidos.
- No son apropiados para el crecimiento en masa de los flagelados por la presencia del agar, por lo que es necesario utilizar mejor los medios líquidos para la preparación de antígenos convencionales y células para estudios bioquímicos.
Un medio bastante empleado y de eficiencia comprobada en el aislamiento primario y conservación de «stocks» es el agar sangre USAMRU (agar enriquecido de la DIFCO). Diversos autores lo emplean validando su buena actuación y sensibilidad 10,42-45 y nosotros lo adoptamos como medio de rutina para el diagnóstico de LTA. Nuestro laboratorio en Brasilia, ha cultivado en los últimos años más de 500 aislados de L. (V) braziliensis, y este medio ha servido para formar el Banco de Criopreservación de la Unidad de leishmaniasis con cepas criopreservadas por más de 18 años que sirven para realizar modernos estudios de genética y de biología molecular en L. (V) braziliensis. Un ejemplo de ello es la MHOM/BR/83/LTB-300, cepa de referencia internacional de la Organización Mundial de la Salud (OMS), producto del criobanco de Brasilia 46.
Sin embargo, algunos autores prefieren el medio bifásico de Senekjie modificado por la adición de medio líquido RPMI-1640 y con 30,0% de sangre desfibrinada de conejo 47-48 . El aislamiento primario de L. (V) guyanensis ha sido logrado exitosamente en éste medio por Santrich6.
4. Métodos de Cultivo
4.1 Aislamiento primario de las lesiones cutáneas
Constituye el paso más importante del proceso diagnóstico, ya que de este procedimiento dependerá el futuro establecimiento del parásito y su crecimiento «in vitro».
La sensibilidad del método está directamente relacionada con la correcta selección que hagamos del medio más apropiado. Asimismo, la habilidad del investigador para escoger el local de la lesión que sea la de mayor actividad parasitaria, solo surge después de varios años de experiencia y práctica.
En el contexto anterior, se aconseja un estudio piloto empleando algunos medios conocidos. Este estudio servirá de marco referencial para saber con que parásitos estamos trabajando en la región. Este abordaje establecerá, en corto período de tiempo, el medio apropiado para el aislamiento primario. Posteriormente, si estamos interesados en estudios más profundos de la biología o epidemiología de las leishmanias, usaremos otros medios existentes en la literatura18.
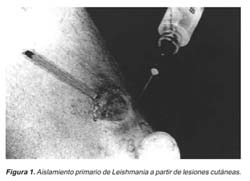
Para la realización de los cultivos, nosotros preferimos la técnica de aspiración de las lesiones, por el procedimiento descrito inicialmente por Hendricks38, ligeramente modificado. Preferimos utilizar una jeringa más potente, de 5mL, y una aguja de mayor calibre, 22G. El vehículo será 0,2- 0,3 mL de suero fisiológico estéril (Figura 1).
Previamente, y conforme ya fue discutido, es crucial un riguroso proceso de asepsia y limpieza de las lesiones. Esto va íntimamente relacionado con los problemas de contaminación por otros microorganismos 45,49. La superficie del área a ser trabajada es limpiada, de manera sistemática y en forma secuencial, con: agua oxigenada, agua estéril con detergente, alcohol iodado, alcohol al 95%, y finalmente agua estéril. Este ritual ayudará a disminuir significativamente la contaminación bacteriana y fúngica. La muestra también puede ser obtenida a través de una biopsia («punch»), y posteriormente triturada con la ayuda de un «tissues grinder», en una solución de suero fisiológico y antibióticos (Garamicina, 200 mg/ml; S-Fluorocytosine, 250 mg/mL). Algunas gotas de este homogenizado serán inoculadas en los tubos de cultivo. Es importante señalar que la excesiva presencia de sangre en las muestras colectadas es perjudicial para el desarrollo del parásito. Según Evans35, la sangre contiene proteínas séricas; altamente inhibitorias para el crecimiento de los promastigotes de Leishmania.
4.2 Aislamiento primario de las lesiones mucosas
Es bastante difícil aislar Leishmania de los granulomas mucosos, en medios de cultivo. La razón principal es la elevada contaminación de los tubos de cultivo, ya que tanto bacterias como hongos ambientales y del huésped crecen rápidamente en los medios eliminando la posibilidad del crecimiento del parásito. Nosotros hemos empleado algunos procedimientos para aliviar el problema, como el descrito por Herrer50. De manera similar, incubamos fragmentos de las biopsias de los tejidos mucosos en altas concentraciones de antifúngicos (5-Fluorocytosine) y antibióticos (Gentamicina y Estreptomicina), a 4°C, durante 24 horas. Esto lo realizamos previamente a la inoculación de los tubos de cultivo. Sin embargo la eficacia es poco significativa.
Nuestro mejor hallazgo ha sido de 30,0% de positividad en pacientes mucosos en área endémica de L. (V) braziliensis22: Dimier-David 24 en 94 pacientes bolivianos con lesiones mucosas consiguió 23,0% de positividad diagnóstica en medio NNN complementado con Schneider y antibióticos, como fase líquida. Los parásitos aislados fueron identificados por Revollo como L. (V) braziliensis 51.
DEMOSTRACIÓN DEL PARASITISMO POR LEISHMANIA MEDIANTE LA INOCULACIÓN DE ANIMALES DE LABORATORIO
1. EN RATONES ISOGÉNICOS Y NO ISOGÉNICOS
La utilización de animales de laboratorio en infecciones experimentales por diversas especies de Leishmania ha permitido el establecimiento de algunos modelos en leishmaniasis. Estudios de nuevos agentes terapéuticos 52-54, investigaciones sobre los mecanismos que gobiernan la patogenicidad del parásito, tanto humoral como celular durante el curso de la infección experimental han sido descritos en la literatura 55-58. El curso de la infección en los ratones y, probablemente, en otros animales de laboratorio, es considerablemente influenciado tanto por la especie del parásito, como por los factores genéticos del hospedero.
Diferentes cepas de ratones isogénicos varían en su comportamiento frente a la infección por L. (L) tropica, L. (L) mexicana, L. (V) braziliensis, L. (V), panamensis, etc. La innata susceptibilidad o resistencia al parásito es genéticamente controlada59.
El conjunto de todas esas observaciones ha llevado a la conclusión que, existen disponibles importantes modelos murinos experimentales que reproducen parcialmente la biología del parasitismo por Leishmania. Lamentablemente, la utilidad diagnóstica de esos modelos es limitada sólo para la gran mayoría de las especies del subgénero Leishmania. Muy pocas son las especies del subgénero Viannia que han sido adaptadas a alguna cepa de ratón «in bred». Hasta el presente no tenemos, todavía, un animal experimental de laboratorio que reproduzca la enfermedad mucosa provocada por L. (V) braziliensis. Estrictamente, hablando de diagnóstico parasitológico, sólo contamos con el concurso valioso del hamster dorado, Mesocriectus auratus.
Para ilustración de nuestros lectores, a continuación citaremos algunas líneas de ratones isogénicos más comúnmente utilizados por los investigadores con cepas de Leishmania del Nuevo Mundo (Tabla 3).
Otro roedor utilizado para estudios por su potencial como modelo experimental con L. (V) panamensis es Mystromys albicaudatus. En él, las lesiones nodulares son de lenta evolución (se tornan visibles a los 9-12 meses pos-inoculación), y desaparecen posteriormente espontáneamente, demostrando su poca sensibilidad a Leishmania; lógicamente, no es útil en el diagnóstico.
2. EN HAMSTERS DORADOS Mesocriectus auratus
Fue Adler quien relató que la primera vez que éstos cricétidos fueron empleados en la investigación de leishmaniasis ocurrió en el Mediterráneo (en la investigación de Kala-azar). Eso fue en 1930, por el equipo del Departamento de Parasitología de la Universidad Hebrea de Jerusalem. Después, este roedor fue distribuido por el citado autor a diversos centros de investigación de Europa y América; aunque Rey 63 ya estudiaba, en Estados Unidos, una cepa que él llamó L. (V) braziliensis inoculada en hamsters.
Sin embargo, se atribuye a los investigadores ingleses 64, el mérito de introducir el uso del hamster como parámetro esencial de la caracterización biológica de las leishmaniasis del Nuevo Mundo. Por lo que, consideramos que la crianza de los cricétidos es condición indispensable en todo laboratorio de investigación en leishmaniasis.
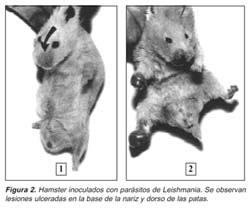
El procedimiento más adecuado para el aislamiento primario de Leishmania utilizando los hamsters es por medio de las biopsias practicadas en las lesiones de los pacientes sospechosos de leishmaniasis. Estas son obtenidas con la ayuda del «punch» de 4mm de diámetro o de una navaja de bisturí. Las biopsias son entonces trituradas utilizándose un «tissues grinder plain» de 15 mL y suero fisiológico estéril. La suspensión de los tejidos es luego inoculada intradérmicamente (0,1 mL) en la base de la nariz (dorso), patas posteriores (dorso) o ambos lugares del hamster (Figura 2), aunque también se acostumbra inocular intraperitonealmente, pues muchos de estos parásitos tienden a visceralizar. Normalmente, se inyectan dos animales por paciente, los animales pasan a ser examinados semanalmente, y permanecen en una sala de mantenimiento a temperatura adecuada (25°C). A la primera señal clínica de infección, se procede al trabajo de aislamiento y comprobación parasitológica.
Los siguientes datos deben ser sistemáticamente anotados:
- Período de incubación aproximado en el aislamiento primario del parásito.
- Período de incubación aproximado en las inoculaciones subsecuentes (hamster-hamster).
- Características evolutivas de las lesiones (tamaño, ulceración, necrosis de patas, etc.).
- Densidad parasitaria relativa en el local de inoculación.
- Metástasis: tiempo aproximado - locales observados.
- Visceralización: tiempo aproximado, órganos comprometidos, densidad parasitaria relativa.
Las cepas de L. (V) panamensis, L. (V) guyanensis y algunas L. (V) braziliensis visceralizan, colonizando principalmente ganglios regionales, bazo e hígado del hamsters 51,65,66. Este comportamiento de la L. (V) braziliensis ha sido también documentado en cepas aisladas en los focos endémicos de LTA, de Santiago del Estero y Salta, Argentina 67. Curiosamente, esto no se registra con las cepas colombianas de L. (V) braziliensis66, y tampoco en los parásitos aislados en Pará (Lainson, comunicación personal). De manera muy esporádica, es posible observar un foco metastásico cutáneo con L. (V) braziliensis68, ya que esta especie puede visceralizar y luego producir lesiones metastásicas cutáneas, cuando inyectamos formas metacíclicas del parásito69.
Concordamos con las observaciones de otros autores que afirman que la técnica de inoculación del hamster con el triturado de las biopsias de las lesiones, la mejor y más eficiente manera de aislar Leishmania. Esto último es especialmente cierto tratándose de lesiones de «espundia», la forma más grave y mutilante del parasitismo por L. (v) braziliensis22,23,70 .
Con relación a la ruta y lugar de inoculación existen discrepancias pero, es la base de la nariz y el dorso de las patas inyectadas con las formas amastigotes y promastigotes, intradérmicamente, las más usadas 71
3. EL USO DE LA INOCULACIÓN DE HAMSTERS EN EL DIAGNÓSTICO DE LTA
Nuestra eficiencia con este método es de 60% de éxito en la positividad de los animales inoculados con la suspensión de la biopsia triturada y, de solo aproximadamente 35%, cuando procedemos a aspirar, con aguja y jeringa las lesiones e inmediatamente inoculamos los animales. Ambos procesos son complementarios al proceso de aislamiento de Leishmania. Para comprobar el parasitismo del hamster inoculado no basta hacer un simple frotis del lugar clínicamente positivo, es necesario cultivar; ello porque el frotis apenas demostrará 25% de animales con amastigotes.
El cultivo efectuado hasta las primeras 3 semanas de inyectado el animal será significativamente más eficiente72. Esto debe ser hecho toda vez que los lugares inyectados no presenten evidencia de infección. Por otro lado, sabemos que existe un espectro de infección cuando trabajamos con las cepas de Leishmania en el hamster: ciertos aislados primarios solo infectan el lugar de inoculación pero no producen señal de inflamación evidente, esto ocurre en la presencia de amastigotes comprobados por cultivo; otros producen lesiones nodulares que rápidamente crecen y ulceran; y por último, algunos aislados provocan lesiones evidentes y, concomitantemente compromiso visceral. Se debe pues prestar atención a todas estas posibilidades y evitar perder cepas que impidan hacer el diagnóstico.
A pesar que el empleo de este método de diagnóstico «in vivo» es lento con relación al cultivo directo y a la impronta, la ventaja práctica esencial es que el animal «limpia» de contaminantes bacterianos y fúngicos las muestras patológicas. Esto es importante en las biopsias obtenidas de las heridas mucosas.
Con relación a L. (V) braziliensis, Llanos-Cuentas 73 trabajando con 71 pacientes cutáneos observó que el método con mejor rendimiento para diagnosticar Leishmania fue la inoculación en el hamster (69,9% de positividad), seguidamente de la histología (48,0%), el cultivo «in vitro» (33,0%), y el frotis coloreado por Giemsa (31,5%). Lógicamente, la demostración del parásito aumentó con el empleo de un mayor número de métodos, así, solamente frotices obtuvo 31,0% de positividad, adicionando la histología 58,0%, y más la inoculación en hamster se alcanzó 80,0% de positividad acumulada. Esto constituye el mejor rendimiento en el diagnóstico de LTA forma cutánea. En contraste, en 55 pacientes mucosos los parásitos fueron demostrados sólo en 48,0%, llamando la atención que, en pacientes con lesiones mucosas múltiples, el parasitismo fue comprobado en 72,7%.
COMENTARIOS FINALES
El diagnóstico parasitológico de LTA es parte fundamental del estudio de la enfermedad. Es condición obligatoria cuando se desea probar la acción de un nuevo medicamento y difundir el esquema terapéutico de un paciente parasitado, entre otras utilidades clínicoepidemiológicas. Pensamos que muchas de las infecciones causadas por las diversas especies de Leishmania son difíciles de diagnosticar. Sin embargo, es el parasitismo por L. (V) braziliensis el que presenta el mayor desafío al profesional de salud. Marsden revisa, más de una vez el asunto, y enfatiza la dificultad encontrada por un clínico para demostrar el parasitismo por L. (V) braziliensis en pacientes con lesiones mucosas crónicas y mutilantes3.
De los métodos diagnósticos descritos, dos son los que merecen ser destacados por su eficiencia y sensibilidad: el cultivo «in vitro» y la inoculación en hamsters. Entretanto, en los estudios de investigación parasitológica hecha por diversos autores, comprobamos una gran variación en la sensibilidad, pues los índices fluctúan entre 19,0% y 83,0%. Esto sería explicado por diferencias en la metodología empleada, tiempo de la enfermedad y la forma clínica de los pacientes estudiados.
En leishmaniasis, tanto cutánea como mucosa, el éxito en el aislamiento es inversamente proporcional al tiempo de duración de la enfermedad. Además que el tratamiento específico previo disminuye la eficiencia de demostración del parásito. Sin embargo, nosotros observamos que existe un parasitismo residual en individuos que han completado series regulares de Glucantime, siendo posible pues aislar parásitos viables en espacio de tiempo relativamente corto, después del tratamiento.
Debemos admitir que no existe una técnica de aislamiento que reúna todas las características necesarias a fin de diagnosticar parasitológicamente 100% de los pacientes con LTA, siendo de opinión generalizada, que el máximo rendimiento se consigue con la combinación de 2 ó 3 de ellas. Si a esto se asocian, la prueba de Montenegro y la serología por ELISA, el diagnóstico laboratorial de LTA puede llegar a más de 90,0%.
Cuando queremos no sólo diagnosticar, sino también aislar el parásito del paciente, los métodos de cultivo son muy eficientes, si se trabajan con los cuidados sugeridos en esta revisión. No existe a disposición de los estudiosos de leishmaniasis un único medio de cultivo «in vitro» que tenga aplicación universal y soporte el crecimiento de todas las especies de Leishmania humanas. Esto implica la necesidad de estudios previos de evaluación que informen cual es el más apropiado para las 6 especies de parásitos que circulan en la región endémica.
Tratándose de infecciones causadas por L. (V) braziliensis, el esfuerzo siempre tenderá a encontrar un método ideal, rápido, sencillo y barato para la diferenciación del agente etiológico de esta entidad, con el resto de infecciones causadas por otras leishmanias menos patogénicas y de mejor pronóstico. Un diagnóstico precoz es pues obligatorio en la leishmaniasis mucosa de fase inicial, para quizá prevenir el compromiso más grave: el síndrome de «espundia».
Como resultado de lo descrito anteriormente, recientemente ha surgido una estrecha colaboración entre los laboratorios de investigación de campo en leishmaniasis y los puestos de salud de áreas endémicas. Nuevas herramientas diagnósticas han surgido de la investigación efectuada en biología y genética moleculares. Se han identificado antígenos con potencial diagnóstico, producto del clonaje de genes que los codifican y, como resultado de la tecnología de ADN recombinante, han surgido proteínas. Todo esto nos lleva a creer en un futuro mejor en el campo del diagnóstico de LTA 74.
Actualmente las técnicas de hibridización de los ácidos nucleicos permiten establecer relaciones nucleotídicas entre las leishmanias. Él ADN-K de Leishmania tiene características singulares que han permitido desarrollar métodos basados en la detección de secuencias de nucleótidos del ADN-K pertenecientes a un organismo desconocido que resultan ser complementarios a las secuencias de una cepa de referencia internacional. Esto ha llevado a la descripción de un número considerable de sondas altamente sensibles en el diagnóstico de LTA. En el inicio de la década de 1980 estas sondas empleaban material radioactivo, eran sondas isotópicas, y los parásitos detectados provenían de cultivos y de animales experimentales, y la detección era por una hibridización «in situ»74,75; sin embargo, las sondas radioactivas de ADN-K no proporcionaron adecuada sensibilidad diagnóstica y fueron poco populares entre los investigadores de los países endémicos por razones obvias.
Posteriormente, De Bruijn 76 presentó resultados muy promisorios cuando asoció la técnica del PCR (Polymerase Chain Reaction) a una hibridización «in situ» realizada en láminas de pacientes de Colombia, Venezuela y Perú, y que llevaron al autor a declarar que la sonda desarrollada era Leishmania complex específica y serviría para el diagnóstico de LTA. A su vez, Lópes77 publicó sus estudios realizados en Perú con pacientes cutáneos y mucosos aplicando PCR directamente en material de biopsia. A fin de validar clínicamente la sonda desarrollada en laboratorio, se tomaron muestras de pacientes de ambientes rurales, las cuales fueron comparativamente estudiadas mediante PCR-hibridización con los métodos clásicos de frotices y cultivos «in vitro». Los autores relataron una sensibilidad significativamente mayor en el método de amplificación e hibridizacion del ADN en el diagnóstico de campo.
Concluimos diciendo que todo este potencial para el diagnóstico de LTA que surge del campo de la biología molecular requiere mayores estudios clínicos y de campo para su validación definitiva.
REFERENCIAS
1. Almeida MC, Cuba CA, Pharoah M, Howard KM, Miles MA. Metacyclogenesis of Leishmania (Viannia) braziliensis «in vitro» evidence that lentil lectin is a marker of complement resistance and enhanced infectivity. Trans R Soc Med Hyg 1983; 87: 335-9. [ Links ]
2. Dedet JP. Cutaneous leishmaniasis in French Guiana: A review. Am J Trop Med Hyg 1990; 43(1): 25-8. [ Links ]
3. Marsden PD. Mucosal leishmaniasis due to Leishmania (Viannia) braziliensis , LVb in Três Braςos , Bahia, Brasil. Rev Soc Brasil Méd Trop1994; 27(2): 93-101. [ Links ]
4. Marsden PD. Personal experience with diagnostic and therapeutic aspects of human Leishmania (Viannia) braziliensis in Três Braςos , Bahia, Brasil. Mem Inst Oswaldo Cruz 1994; 89(3): 485-7. [ Links ]
5. Marsden PD. Eustachian tube blockage with consequent middle ear infection in mucosal leishmaniasis. Rev Soc Brasil Méd Trop 1994; 27:103. [ Links ]
6. Santrich C, Segura E, Armas A, Saravia N. Mucosal disease caused by Leishmania (Viannia) braziliensis panamensis. Am J Trop Med Hyg 1990; 42: 51-5. [ Links ]
7. Naiff RD, Talhari S, Barrett TV. Isolation of Leishmania guyanensis from lesions of the nasal mucosa. Mem Inst Oswaldo Cruz 1986; 83: 529-30. [ Links ]
8. Silvera FT, Lainson R, Shaw JJ, De Souza AA, Ishikawa EA, Braga RR. Cutaneous leishmaniasis due to Leishmania (Leishmania) amazonensis in Amazonian Brazil and the significance of a negative Montenegro skin test in human infections. Trans R Soc Trop Med Hyg 1991; 85: 735-8. [ Links ]
9. Bowder JH, Campbell JL, Walker DH, Tart DE. American mucocutaneous leishmaniasis: culture of a Leishmania species from peripheral blood leukocytes. Am J Clin Pathol 1981; 75: 435-8. [ Links ]
10. Cuba CA, Llanos-Cuentas EA, Marsden PD. Failure to detect circulating Leishmania in human cutaneous leishmaniasis due to Leishmania braziliensis braziliensis. Trans R Soc Trop Med Hyg 1986; 80: 346. [ Links ]
11. Llanos-Cuentas EA, Arana M, Cuba CA, Rosa AC, Marsden PD. Leishmaniasis cutanea diseminada asociada a metastasis en mucosas causada por Leishmania braziliensis: fracaso en el hallazgo de parásitos circulantes. Rev Soc Brasil Med Trop 18: 271-2. [ Links ]
12. Silvera FT, Lainson R, Shaw JJ, De Souza AA, Ishikawa EA, Braga RR. Sobre a sensiblidade de cultura de leucocitos circulantes na detecςão de Leishmania no sangue periferico de pacientes com Leishmaniose tegumentar. Rev Soc Brasil Med Trop 1989; 22:143-6. [ Links ]
13. Martínez JE, Alba L, Arias M, Escobar A, Saravia N. Haemoculture of Leishmania (Viannia) braziliensis from two cases of mucosal leishmaniasis:re-examination of haematogenus dissemination. Trans R Soc Trop Med Hyg 1992; 86: 392-4. [ Links ]
14. Franca F, Lago EL, Tada S, Costa JML, Vale K, Oliveira J, et al. An outbreak of human Leishmania (Viannia) braziliensis infection. Mem Inst Oswaldo Cruz; 86:164-74. [ Links ]
15. Grimaldi G, Tesh RB, McMahon-Pratt D. A review of the geographic distribution and epidemiology of leishmaniasis in the New World. Am J Trop Med Hyg 1989; 41: 687-725. [ Links ]
16. Rosa AC, Cuba CA, Vexenat A, Barreto AC, Marsden PD. Predominance of Leishmania braziliensis braziliensis in the regions of Três Braços and Corte de Pedra, Bahia, Brazil. Trans R Soc Trop Med Hyg 1988; 82: 409-10. [ Links ]
17. Evans DA, Lanham SM, Baldwin C, Peters W. The isolation and isoenzyme characterization of Leishmania braziliensis sbsp. From patients with cutaneous leishmaniasis acquired in Belize. Trans R Soc Trop Med Hyg 1984; 78: 35-42. [ Links ]
18. Lainson R, Shaw JJ. Some problems in studies on parasites of the Leishmania braziliensis complex. In: Ecologie des leishmaniases. Colloques Internationaux au CNRS. 239 Montpellier, 1967. p. 83-6. [ Links ]
19. Navin TR, Arana FA, Mérida AM, Arana BA, Castillo AL, Silvers N. Cutanoeus leishmaniasis in Guatemala: comparison of diagnostic methods. Am J Trop Med Hyg 1990; 42:36-42. [ Links ]
20. Weigle KA, Dávalos M, Heredia P, Molineros R, Saravia N, D'Alesandro A. Diagnosis of cutaneous and mucocutaneous leishmaniasis in Colombia: a comparison of seven methods. Am J Trop Med Hyg 1987; 36: 489-96. [ Links ]
21. Urjel R, Recacochea M, L a Fuente C, Orellana A. A simple method for the collection of material from cutaneous and mucocutaneous leishmaniasis. Trans R Soc Trop Med Hyg 1983; 77: 882-90. [ Links ]
22. Cuba CA, Llanos-Cuentas EA, Barreto AC, Lago EL, Reed SG, Marsden PD. Human mucocutaneous leishmaniasis in Três Braços, Bahia, Brasil, an area of Leishmania braziliensis braziliensis transmission. 1. Laboratory diagnosis. Rev Soc Brasil Med Trop 1984; 17: 161-7. [ Links ]
23. Dimier-David L, David C, Ravisse P, Bustillos R, Revollo S, Lyevre P, et al. Parasitological diagnosis of mucocutaneous leishmaniasis due to Leishmania (Viannia) braziliensis in Bolivia. Rev Soc Brasil Med Trop 1991; 24: 231-4. [ Links ]
24. Ridley DS. Pathology. In: The Leishmaniasis in Biology and Medicine Vol. II. Clinical aspects and control. Peters, W & Killick-Kendrick eds. 1997. Academic press, London. [ Links ]
25. Shortt HE, Cooper W. Staining of microscopical sections containing protozoan parasites by modification of McNamara's method. Trans R Soc Trop Med Hyg 1948; 41: 427-8. [ Links ]
26. Sells PG, Burton M. ldentification of Leishmania amastigotes and their antigens formalin fixed tissue by inmunoperoxidase staining. Trans R Soc Trop Med Hyg 1981; 75: 461-8. [ Links ]
27. Salinas GL, Valderrama G, Palma G, Montes G, Saravia NC. Detección de amastigotas en leishmaniasis cutánea y mucocutánea por el método de inmunoperoxidasa, usando anticuerpo policlonal: sensibilidad y especificidad comparadas con métodos convencionais de diagnóstico. Mem Inst Oswaldo Cruz 1989; 84: 53-60. [ Links ]
28. Lynch NR, Malave C, Infante BR, Modlin RI, Convit J. In situ detection of amastigotes in American Cutaneous Leishmaniasis using monoclonal antibodies. Trans R Soc Trop Med Hyg 1986; 80: 6-9. [ Links ]
29. Anthony RL, Grogl M, Sacci JB, Ballou RN. Rapid detection of Leishmania amastigotes in fluid aspirates and biopsies of human tissues. Am J Trop Med Hyg 1987; 37: 271-6. [ Links ]
30. Ridley DS, Magalhaes AV, Marsden PD. Histological analysis and pathogenesis of mucocutaneous leishmaniasis. J Pathol 1989; 159: 293-9. [ Links ]
31. Marsden PD. Mucosal leishmaniasis (Espundia, Escomel, 1911). Trans R Soc Trop Med Hyg 1986; 80: 859-76. [ Links ]
32. Hendricks LD, Childs GE. Present knowledge of the in vitro" cultivation of the pathogens of tropical diseases. Tropical Disease Research. Serie 2, 1980, Schwabe, Bassel. [ Links ]
33. Jaffe CL, Grimaldi G, MacMahon-Pratt D. Cultivation and cloning of Leishmania. In: Genes and Antigens of Parasites: A laboratory Manual. C. M., Morel edt. 2nd edition. UNDP/WORLD BANK/STDR. Fiocruz, Rio de Janeiro, 1984, pp.47-91. [ Links ]
34. Evans DA. Leishmania. In vitro" Methods for parasite cultivation . Taylor, A.E.R. & Baker, JR. eds. Academic Press, New York. 1987. p. 52-75. [ Links ]
35. Miles MA. Leishmania-culture and biochemical comparisons - some difficulties. In: Chance, M.L. & Walton, B.C. eds. Biochemical characterization of Leishmania. Proceedings of a workshop held the Pan. Am. Health Org., Washington D.C. 1980. Undp/World Bank/ WHO/TDR, STDR.Geneve, Switzerland, 1982. p.123-37. [ Links ]
36. Hendricks LD, Wood DE, Hajduk ME. Heamoflagellates: Commercially available liquid media for rapid cultivation. Parasitol 1978; 76: 309-16. [ Links ]
37. Hendricks LD, Wright N. Diagnosis of cutaneous leishmaniasis by "in vitro" cultivation of saline aspirates in Schneider's Drosophila medium. Am J Trop Med Hyg 1979; 28: 962-4. [ Links ]
38. Childs GE, Foster KL, Mc Roberts MJ. Insect cell culture media for the cultivation of New World Leishmania. Int J Parasitol 1978; 8:255-8. [ Links ]
39. Pessoa SB, martins AV. Leishmaniose Tegumentar Americana. Imprensa Nacional 1982. p. 243. [ Links ]
40. Walton BC, Shaw JJ, Lainson R. Observations on the "in vitro" cultivation of Leishmania braziliensis. J Parasitol 1977; 63: 1118-9. [ Links ]
41. Walton BC, Intermill RW, Hayduk ME. Differences in biological characteristics of three Leishmania isolates from patients with espundia. Am J Trop Med Hyg 1977; 26: 850 -5. [ Links ]
42. Shaw JJ, Lainson R. The "in vitro» cultivation of members of the Leishmania braziliensis complex.Trans R Soc Trop Med Hyg 1981; 75: 461-8. [ Links ]
43. Cuba CA, Neetto ME, Marsden PD, Llanos-Cuentas EA, Costa JLM. Cultivation of Leishmania braziliensis braziliensis from skin ulcers in man under field conditions. Trans R Soc Trop Med Hyg 1986; 80: 456-7. [ Links ]
44. Cuba CA, Neetto ME, Costa JLM, Barretto AC, Marsden PD. El método de cultivo "in vitro"como instrumeno práctico en el diagnóstico y el aislamiento primario de Leishmania braziliensis braziliensis II. Estudios en pacientes de areas endémicas. Rev Inst Med Trop São Paulo 1986; 28: 317-24. [ Links ]
45. Lainson R, Strangways-Dixon. Leishmaniasis mexicana: the epidemiology of dermal leishmaniasis in British Honduras. Trans R Soc Med Hyg 1963; 57: 242-5. [ Links ]
46. Saravia N, Holguín AF, McMahon-Pratt D, D´Alessandro A. Mucocutaneous leishmaniasis in Colombia: Leishmania braziliensis diversity. Am J Trop Med Hyg 1985; 34: 714-20. [ Links ]
47. Melby PC, Kreutzer RD, McMahon Pratt D, Gam A, Neva FA. Cutaneous leishmaniasis: Review of 59 cases seen at the National Institutes of Health. Clin Infect Dis 1992; 15:924-37. [ Links ]
48. Netto EM, Cuba CA, Marsden PD, Barretto AC. El método de cultivo "in vitro" como instrumento práctico en el diagnóstico y el aislamiento primario de Leishmania braziliensis braziliensis . I. Observaciones de laboratorio. Rev Soc Brasil Med Trop 1986; 19: 79-84. [ Links ]
49. Herrer A, Thatcher VE, Johnson CA. Natural infections of Leishmania and Trypanosomas demonstrated by skin cultures. J Parasitol 1966; 52: 954-7. [ Links ]
50. Trotter ER, Peters W, Robinson BL. The experimental chemotherapy of Leishmaniasis. VI. The development of rodent models for cutaneous infection with L. major and L. mexicana amazonensis. Ann Trop Med Parasitol 1980; 74: 299-319. [ Links ]
51. Revollo S, Dimiers-David L, David C, Lyevre P, Camacho C, Dedet JP. lsoenzymatic characterization of Leishmania braziliensis braziliensis isolates obtained from Bolivian and Peruvian patients. Trans R Soc Trop Med Hyg 1992; 86:388-91. [ Links ]
52. Neal RA. Effect of sodium stibogluconate and pyrimethamine on mouse infections with Leishmania mexicana. Ann Trop Med Parasitol 1976; 70: 252. [ Links ]
53. Peters W, Trotter ER, Robinson RL. The experimental chemotherapy of Leishmaniasis VII. Drug responses of L. tropica and L. mexicana amazonensis with an analysis of promising chemicals leads to new leishmanial agents. Ann Trop Med Parasitol 1980; 74: 321-36. [ Links ]
54. Behin R, Mauel I, Sordat B. Leishmania tropica. Pathogenicity an "in vitro" macrophage function in strains of inbred mice. Exo Parasitol 1979, 48:81-91. [ Links ]
55. Preston MP. The immunology, immunopathology and immunoprofilaxis of Leishmanía infections.In: Immune responses in parasitic infections. Immunology, Immunopathology and Immunoprofilaxis . Vo. III. Protozoa. E. J.L.Soulsby ed. Cambridge, England. CRC Pres Inc. Florida. 1987. p. 169-70. [ Links ]
56. Pearson RD, Wheeler DA, Harrison LH, Kay DH. The immunobiology of Leishmaniasis. Rev Infect Dis 1983; 5: 907-27. [ Links ]
57. Peres H, Arredondo L, Gonzáles M. Comparative study of American cutaneous leishmaniasis and diffuse cutaneous leishmaniasis in two strains of inbred mice. Infect Immun 1978; 22: 301-7. [ Links ]
58. Bradley DJ. Introduction and genetics of susceptibility to Leishmania donovani. In: Genetics of resistance to infection with special reference to Leishmaniasis. Meeting Roy Soc Trop Med Hyg. Trans R Soc Trop Med Hyg 1982; 76: 143-6. [ Links ]
59. Moriearty PL, Grimaldi G. Host and parasite factors influencing outcome of Leishmania mexicana mexicana infection in mice. VIII. Reunião annual de Pesquisa Básica em Doença de Chagas. Caxambú. 1980. Brasil. 1-44. [ Links ]
60. Childs GE, Foster KL, Mc Roberts MJ. Insect cell culture media for the cultivation of New World Leishmania. Int J Parasitol 1978; 8: 255-8. [ Links ]
61. Grimaldi G, Moriearty PL, Hoff R. Leishmania mexicana immunology and histopathology in C3H mice. Exp Parasitol 1980; 50: 45-56. [ Links ]
62. Rey H. Cellular reactions in the dermal connective tissues of the hamster to Leishmania braziliensis J Infect Dis 1943; 72: 117-24 . [ Links ]
63. Lainson R, Shaw JJ. Leishmania and Leishmaniasis of the New World with particular reference to Brazil. Bull Pan Am Health Org 1973; 7:1-19. [ Links ]
64. Pearson RD, Harrinson LU, Kay DU. The immunobiology of Leishmaniasis. Rev Infect Dis 1983; 5: 907-27. [ Links ]
65. Travi B, Rey Ladino J, Saravia N. Behaviour of Leishmania braziliensis s.l. in golden hamsters evolution of infection under different experimental conditions. J Parasitol 1988; 74: 1059-62. [ Links ]
66. Cuba CA, Torno O, Ledesma O, Barbieri L, Visciarelli E, Pratt MI, et al. Human cutaneous leishmaniasis caused by Leishmania (Viannia) braziliensis (LVb) in Santiago del estero, Province of Argentina: Identification of parasites by Monoclonal Antibodies and isoenzymes. Mem Inst Oswaldo Cruz 1993; Suppl. 88: 120. [ Links ]
67. Brazil R. Metastatic spread of Leishmania braziliensis braziliensis to the extremities of hamsters Trans R Soc Med Hyg 1976; 70: 89. [ Links ]
68. Almeida MC, Cuba CA, Miles MA. The ability of Leishmania (Viannia) braziliensis in the hamster to primarily infect visceral sites and develop secondary metastasic cutaneous lesions. Rev Soc Brasil Med Trop 1992; 25. Suppl.: 85. [ Links ]
69. Cuba CA, Marsden PD, Barretto AC, Rocha R, Sampaio R, Patzlaff L. Parasitologic and Immunologic diagnosis of American (mucocutaneous) leishmaniasis Bull Pan Am Health Org 1981; 15: 249-59. [ Links ]
70. Wilson HR, Diekman BS, Childs GE. Leishmania braziliensis and Leishmania mexicana: Experimenatl cutaneous infections in golden hamsters Exp Parasitol 1979; 47: 270-83. [ Links ]
71. Grimaldi G, Jaffe CL, Mc Mahon Pratt D, Falqueto A. A simple procedure for the isolation of leishmanial parasites and for the recovery of parasite virulence in avirulent stocks. Trans R Soc Trop Med Hyg 1984; 78: 560. [ Links ]
72. Llanos-Cuentas EA. Estudo clínico evolutivo da Leishmaniose em area endêmica de Leishmania braziliensis braziliensis Três Braços, Bahía, Brasil.Tese Mestrado. 1984. Universidade de Brasilia, Brasil. p. 166. [ Links ]
73. Barker DC. DNA diagnosis of human leishmaniasis. Parasitol Today 1987; 3: 177-84. [ Links ]
74. Barker DC, Butcher J, Gibson LJ, Kennedy WP, Williams RH, Cuba CA, et al. Sequence homology of kinetoplast DNA in Leishmania studied by endonuclease digested fragments and in situ hybridization of individual organisms. In: Leishmania taxonomie et phylogenese. Applications ecoepidemiologiques I.M.E.E., 1 986; 41:55. [ Links ]
75. De Bruijn MHL, Barker DC. Diagnosis of New World Leishmaniasis: specific detection of species of the Leishmania braziliensis complex by amplification of kinetoplast. Act Trop 1992; 52: 45-58. [ Links ]
76. López M, Inga R, Cangalaya M, Echevarría J, Llanos-Cuentas AE, Orrego C, et al. Diagnosis of Leishmania using Polymerase chain reaction: A simplified procedure for field work. Am J Trop Med Hyg 1993; 49: 348-56. [ Links ]