Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Medicina Experimental y Salud Publica
versión impresa ISSN 1726-4634
Rev. perú. med. exp. salud publica v.20 n.2 Lima abr./jun. 2003
TRABAJOS ORIGINALES
Perfiles genéticos (RFLP-IS6110) y resistencia a drogas en aislamientos de M. tuberculosis de pacientes internados en un hospital referencial del Callao, Perú.
Christian Baldeviano V1; Neyda Quispe T1; César Bonilla A2; Dauma Gastiaburu3; José Pro C3; Luis F. Llanos–Zavalaga1.
1 Grupo Multifuncional de Tuberculosis. Centro Nacional de Salud Pública, Instituto Nacional de Salud. Lima, Perú.
2 Servicio de Neumología, Hospital Nacional Daniel A. Carrión. Bellavista. Callao, Perú.
3 Facultad de Medicina Alberto Hurtado, Universidad Peruana Cayetano Heredia. Lima, Perú.
RESUMEN
Objetivo: evaluar la frecuencia y el agrupamiento de los perfiles genéticos (RFLP-IS6110) y los niveles de resistencia a drogas en aislamientos de M. tuberculosis de pacientes hospitalizados con tuberculosis pulmonar frotis positivo (TBP-FP) en un hospital general de la provincia del Callao, Lima, Perú. Materiales y métodos: se incluyeron pacientes con TBP-FP hospitalizados en el Hospital Nacional Daniel A. Carrión entre agosto de 2000 y febrero de 2001. Se realizó la prueba de sensibilidad a las cuatro drogas de primera linea (INH, RIF, SM, EMB) por el método de las proporciones y la genotipificación mediante el método estándar de RFLP-IS6110. Se recolectó la información de los pacientes de los registros de laboratorio e historias clínicas. Resultados: en 74 aislamientos, el número de bandas en los perfiles genéticos variaron entre 2 y 16, 4 perfiles (5,5%) mostraron menos de 5 bandas. En total 50 perfiles genéticos fueron obtenidos de 70 pacientes. 34 aislamientos (48,6 %) se agruparon en 14 clusters y 36 tuvieron ocurrencia única. La resistencia a drogas en pacientes nunca y antes tratados fue 45,2% y 71,1%, respectivamente. La multidrogorresistencia fue 16,1% y 36,8%, respectivamente. 10 de los 14 clusters incluyeron por lo menos un aislamiento resistente y un cluster agrupó 6 aislamientos resistentes. Conclusiones: No se encontró evidencia de algún genotipo predominante en la población estudiada. Sin embargo, se observaron «clusters» agrupando pacientes con TB sensible y resistente. Nuestros resultados sugieren que existen genotipos asociados a resistencia lo cual indicaría transmisión activa de cepas resistentes en la provincia del Callao. Es necesario llevar a cabo un estudio poblacional para confirmar nuestros resultados.
Palabras clave: Tuberculosis; M. tuberculosis; Resistencia a las drogas; Códigos genéticos; Polimorfismo de longitud del fragmento de restricción; Callao; Perú (Fuente: BIREME)
ABSTRACT
Objective: To assess the frequency and clustering of DNA fingerprinting (RFLP-IS6110), and to determine levels of drug-resistance among M. tuberculosis isolates from smear-positive pulmonary tuberculosis patients (SP-PTB) from a general hospital in Callao. Materials and methods: Patients with SP-PTB hospitalized in the Hospital Nacional Daniel A Carrión from August 2000 to February 2001were included in the study. Drug-susceptibilty testing to the four first-line drugs (INH, RIF, SM, EMB) was performed using the proportion method, and DNA fingerprinting analysis was performed using the standard IS6110-RFLP technique. Patient information was collected from clinical and laboratory records. Results: From 74 isolates, the number of IS6110-bands varied from 2 to 16, 4 isolates (5,5%) showed less than 5 bands. Overall, 50 DNA fingerprinting profiles were observed in 70 patients. 34 isolates (48,6 %) were grouped in 14 clusters and 36 isolates were isolated ocurrences. Drug resistance in never treated and previoulsy treated patients was 45,2% and 71,1%, respectively. Multidrug-resistance was 16,1% and 36,8%, respectively. 10 out of 14 clusters had at least one drug-resistant isolate. One cluster involved 6 drug-resistant isolates. Conclusion: No evidence of clonal spread of a particular strain was observed. However, we found clusters grouping drug-resistant and drug-susceptible patients. Our results suggests that there are genotypes associated with drug resistance, which could indicates ongoing transmission of drug-resistant M. tuberculosis strains in Callao. A population-based study is necessary to confirm our results.
Key words: Tuberculosis; M. Tuberculosis; Drug resistanse; Genetic code; polymorphism, restriction fragment length; Callao; Perú (Source: BIREME)
INTRODUCCIÓN
La tuberculosis (TB) es responsable de 3 millones de muertes al año y de la presentación de aproximadamente 8 millones de nuevos casos; se calcula que un tercio de la población mundial se encuentra infectado con esta enfermedad 1,2 . La situación es aún más dramática en países en vías de desarrollo, en los cuales ocurren 95 a 98% de los casos y las muertes por esta enfermedad 3 . En el Perú, luego de la implementación de la terapia corta directamente suministrada (DOTS/TAES), los niveles de incidencia han disminuido de manera importante; aunque todavía se encuentre entre las más alta en América. En el año 2000 se diagnosticaron un total de 39 918 pacientes con TB en todas sus formas, 58% de los cuales fueron reportados sólo en Lima y Callao 4 . Además, de acuerdo con el último estudio nacional de vigilancia, los niveles de resistencia a drogas antituberculosas se han incrementado. En este contexto, es de vital importancia la búsqueda de nuevas herramientas experimentales para delinear mejor las estrategias de intervención y prevenir la transmisión de la tuberculosis en la comunidad.
El desarrollo de nuevos métodos moleculares para caracterizar genéticamente aislamientos de Mycobacterium tuberculosis ha contribuido enormemente en entender mejor la dinámica de transmisión y la patogénesis de la TB en el mundo 5,6,8,9,20 . El Polimorfismo en la longitud de los fragmentos de restricción (RFLP, por sus iniciales en inglés) de la secuencia de inserción IS6110 ha sido hasta la fecha el método más aceptado 7 . El RFLP es capaz de discriminar entre cepas relacionadas y no relacionadas clonalmente; y así, proporciona perfiles genéticos idénticos en cepas que provienen de pacientes relacionados epidemiológicamante, y proporciona perfiles genéticos diferentes en cepas provenientes de pacientes sin relación de contagio 5,6 . Estudios de epidemiología molecular, empleando procedimientos moleculares como el RFLP combinado con métodos epidemiológicos convencionales, han logrado identificar fuentes de infección y nuevos focos de transmisión no detectados por los métodos clásicos de estudio de contactos, estudiar la magnitud de la transmisión reciente e identificar factores de riesgo asociados a la transmisión activa 5,6, 8-10,19,20 .
El primer paso para implementar un estudio poblacional de epidemiología molecular y, posteriormente, un sistema de vigilancia de la transmisión mediante RFLP en los llamados bolsones de TB, es caracterizar los aislamientos, identificar patrones predominantes y evaluar la diversidad clonal de las cepas que ocasionan enfermedad tuberculosa en una determinada área geográfica. En ese sentido, el objetivo del presente estudio fue de evaluar preliminarmente la frecuencia y el agrupamiento de los perfiles genéticos basados en el marcador genético IS6110 (RFLP-IS6110), y determinar los niveles y patrones de resistencia a drogas en una población de pacientes hospitalizados en un hospital referencial del Callao durante un periodo de seis meses entre el año 2000 y el año 2001.
MATERIALES Y MÉTODOS
POBLACIÓN DE PACIENTES Y AISLAMIENTOS CLÍNICOS.
Entre agosto de 2000 y febrero de 2001 se obtuvieron muestras clínicas de todos los pacientes con TB pulmonar con baciloscopía positiva (TBP-FP). Los pacientes fueron nunca y antes tratados que fueron hospitalizados (al menos un día de hospitalización) en los servicios de neumología y medicina interna del Hospital Nacional Daniel A. Carrión. Los pacientes nunca tratados fueron hospitalizados por algún otro motivo. Las muestras de esputo se transportaron de manera adecuada al Laboratorio Nacional de Referencia de Micobacterias (LNRM)11. Se utilizó una ficha estandarizada para la recolección de la información demográfica (edad, sexo, procedencia) y la información clínico-epidemiológica (fecha de diagnóstico, antecedentes de tratamiento, infección VIH, historia previa de TB), las cuales fueron obtenidas a partir de los registros del laboratorio y mediante revisión de historias clínicas.
CULTIVO Y PRUEBA DE SENSIBILIDAD A DROGAS ANTITUBERCULOSAS.
Las muestras de esputo se procesaron de acuerdo con el método de Ogawa para el aislamiento de micobacterias 11 . La prueba de susceptibilidad a drogas de primera línea: rifampicina (RIF), isoniacida (INH), estreptomicina (SM), y etambutol (EMB) fueron desarrolladas por el método de las proporciones de acuerdo con Canetti, Rist y Grosset 11 . Para ello, se emplearon las siguientes concentraciones críticas de las drogas antes mencionadas: RIF: 40,0; INH: 0,2; SM: 4,0 y EMB: 2,0 mg/mL. Se definió resistencia a drogas (TB-R) como resistencia por lo menos a una de las cuatro drogas estudiadas y multidrogorresistencia (TB-MDR) como resistencia por lo menos a RIF e INH.
CARACTERIZACIÓN GENÉTICA POR RFLP-IS6110
Para caracterizar las cepas de M. tuberculosis, fue empleado el método estándar de RFLP-IS6110 reportado por van Embden (1993)7,12 . Para ello, el ADN se extrajo mediante la técnica basada en CTAB/NaCl (SIGMA) y cloroformo:alcohol isoamílico (24:1). Luego, 4,5 mg de ADN genómico fue cortado con la enzima de restricción PvuII (New England Biolabs), y los fragmentos de restricción fueron separados mediante electroforesis en 0,8% agarosa (SIGMA) durante toda la noche a 25 V. Posteriormente, el ADN fue transferido a una membrana de nylon (Hybond+, Amersham Pharmacia, Biotech) por el método de capilaridad y la membrana fue hibridizado con una sonda de 245 pb de una región de la secuencia de inserción IS6110. El marcaje y detección se realizaron usando el Kit ECL (Amersham Pharmacia, Biotech) de acuerdo con las instrucciones del fabricante. Una cepa de referencia (M. tuberculosis 14323) se incluyó en cada corrida como control externo de normalización 7,12 .
ANÁLISIS DE LOS PERFILES GENÉTICOS
Los perfiles genéticos RFLP-IS6110 generados en base al número y posición de IS6110 en el genoma de M. tuberculosis fueron analizados con la ayuda del programa GelCompare II versión 4,0 (Window 98, Applied Maths, Kortrijk, Bélgica). Los tamaños de los fragmentos que contienen la secuencia de inserción fueron normalizados empleando el patrón conocido de la cepa de referencia M. tuberculosis 14323. Para estudiar la diversidad clonal de los aislamientos se generó un dendrograma de similitud basado en el algoritmo UPGMA y el coeficiente de Dice. Para el análisis de agrupamiento se incluyeron únicamente los perfiles RFLP-IS6110 que presentaron al menos 5 bandas 13 . Se definieron clusters de perfiles genéticos relacionados si dos o más aislamientos tuvieron más de 4 bandas y compartieron idénticos perfiles RFLP-IS6110 o ellos difirieron únicamente en la adición o ausencia de una única banda 13. Todos los patrones fueron inspeccionados visualmente para detectar posibles errores.
RESULTADOS
De los 90 pacientes reclutados para el presente estudio, 9 fueron excluidos por presentar cultivo negativo. Los 81 restantes fueron elegibles para la prueba de sensibilidad y el análisis de RFLP-IS6110. Sin embargo, 12 fueron excluidos para este análisis porque en 7 se obtuvo ADN genómico degradado y en 4 el perfil genético mostró menos de 5 copias de IS6110 (población final = 70). Los 4 perfiles genéticos con menos de 5 bandas IS6110 fueron incluidos en el dendrograma, pero fueron posteriormente excluidos del análisis de agrupamiento. Por otro lado, únicamente en 69 de 81 (85,2%) pacientes se realizó la prueba de sensibilidad porque en 7 pacientes se obtuvieron menos de 10 colonias (criterio de exclusión para prueba de sensibilidad)11 y 5 de los cultivos se contaminaron (población final = 69). Todos los paciente provinieron de los distritos de Callao, La Perla, Bellavista, y Ventanilla (7 pacientes fueron posteriormente transferidos fuera del Callao). Las muestras clínicas procesadas fueron: esputo en su mayoría (77), y aspirado bronquial (4). La edad de los pacientes varió entre 13 y 88 (34,7 ±15,2). 51,8% de los pacientes tuvieron entre 20 y 33 años. La mayoría de los pacientes fueron del sexo masculino (masculino / femenino = 1,18:1). 40 pacientes (49,4%) recibieron tratamiento antituberculoso por más de 3 semanas, 9 pacientes (11,1 %) tuvieron un diagnóstico positivo para VIH, 27 (33,3%) fueron VIH negativo y en 45 (55,6%) pacientes no se encontró registros de prueba para diagnóstico de infección por VIH. Se encontró evidencia de historia previa de TB en 36 pacientes (44,4 %).
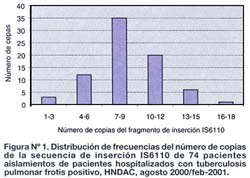
El número de copias de IS6110 en 70 aislamientos (70 pacientes) varió entre 5 y 16, 35% de los aislamientos tuvieron entre 7 a 9 copias, y 55% entre 7 a 12 copias de IS6110 (Figura N°1).
La moda fue de 8. No se observó ningún aislamiento sin la secuencia de inserción IS6110; sin embargo, 4 aislamientos (5,4%) tuvieron menos de 5 segmentos de inserción IS6110 y fueron incluidos en la elaboración del dendrograma; pero no fueron considerados en el análisis de agrupamiento. En total 50 perfiles genéticos RFLP-IS6110 diferentes fueron obtenidos de 70 aislamientos. 34 (48,6 %) perfiles genéticos se agruparon en 14 clusters, y 36 perfiles RFLP-IS6110 tuvieron ocurrencia única (Figura Nº 2).
Los tres clusters más grandes estuvieron conformados por uno que agrupó 6 pacientes (cluster I), y dos que agruparon 3 pacientes (cluster II y III). Los 11 clusters restantes agruparon únicamente a dos pacientes (cluster IV, V, ..., XIV). El cluster I estuvo caracterizado por un perfil de 9 bandas (similitud = 92,7%), 4 fueron nunca tratados y dos antes tratados, dos de los pacientes eran positivo para VIH. El cluster II agrupó pacientes con aislamientos que presentaron un perfil genético de 6 y 7 bandas (similitud = 92,3%) e incluyeron 2 pacientes nunca tratados. El cluster III estuvo caracterizado por perfiles de 6 y 7 bandas (similitud = 90,8%) y los tres pacientes que lo conformaron fueron nunca tratados. 84,3 % (59/70) de los pacientes estudiados mostraron aislamientos cuyo perfil genético RFLP-IS6110 presentó mayor o igual a 75% de similitud (Figura N°2, 3 y Tabla Nº 1).
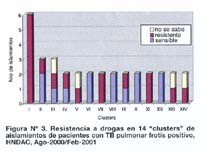
Por otro lado, en cifras globales, la resistencia a drogas (TB-R) y la multidrogorresistencia global (TB-MDR) en pacientes hospitalizados para el periodo estudiado fue 59,4 % y 27,5 %, respectivamente. La resistencia por lo menos a H fue 43,5 % y por lo menos a R fue 31,9%. La TB-R y la TB-MDR fueron mayores en pacientes antes tratados con respecto a los pacientes nunca tratados (71,1% frente a 45,2%, p = 0,026; y 36,8% frente a 16,1%, p = 0,049, respectivamente). Asimismo, la resistencia por lo menos a R y por lo menos a H fueron mayores en pacientes antes tratados respecto de los pacientes que nunca recibieron tratamiento (45,5 % frente a 19,4 %, p = 0,021; y 63,6 % frente a 25 %, p = 0,001). El 10,1% de la población en estudio tuvo resistencia a las cuatro drogas (H, R, S y E) y ello fue observado únicamente en pacientes antes tratados (Tabla Nº 1).
En 10 de 14 clusters (cluster I-V, VII, IX, XI, XIII y XIV) se observó la ocurrencia de por lo menos un paciente TB-R y en un cluster grande (cluster I) se observó 6 pacientes TB-R, 5 de los cuales fueron TB-MDR.
DISCUSIÓN
En el Perú, luego de más de 10 años del establecimiento de la estrategia de tratamiento acortado directamente supervisado (DOTS/TAES) recomendado por la Organización Mundial de la Salud, la tasa de notificación de casos y la incidencia de tuberculosis está disminuyendo en los últimos años 14 . Sin embargo, como en muchos países del mundo, la emergencia de la resistencia a drogas, y en particular de la multidrogorresistencia (MDR) es una grave amenaza para el control de la TB. El último estudio nacional de vigilancia mostró un incremento en la resistencia global primaria y la multidrogorresistencia primaria 15 .
En el presente estudio se identificaron un total de 34 pacientes que se agruparon en 14 «clusters», haciendo un total de 48,6% de agrupamiento. El porcentaje de agrupamiento de los patrones genéticos en una determinada población de pacientes ha sido empleado de forma grosera para estimar el grado de transmisión activa en esa población 8,9 . Esto se basa en que pacientes con reciente enfermedad relacionada epidemiológicamente presentan cepas de un mismo origen clonal y, por ende, proporcionan un patrón genético de RFLP idéntico o muy similar; mientras que pacientes con TB rocedentes de una reactivación endógena de una infección pasada son independientes, por lo tanto, presentan patrones genéticos de RFLP distintos entre sí 6.
Varios autores emplean la definición de agrupamiento como aquellos aislamientos que se relacionan por presentar patrones genéticos idénticos; es decir, con un 100% de similitud. Sin embargo, se ha reportado que pacientes con relación epidemiológica comprobada podrían presentar pequeñas diferencias en sus perfiles genéticos, como por ejemplo la ausencia o presencia de una banda adicional 16-18 . Por ello, nosotros empleamos como definición de agrupamiento patrones idénticos (100% de similitud) o patrones muy similares (una banda adicional o una banda ausente a lo mucho). Si bien el objetivo del presente trabajo no fue estimar transmisión activa en la población en estudio, de acuerdo con la definición de agrupamiento que usamos en el presente estudio, nosotros encontramos que cerca de la mitad (48,6%) de los pacientes se agruparon en «clusters» de patrones genéticos relacionados, sugiriendo transmisión reciente. Este valor es superior a estudios similares en países desarrollados con baja y moderada prevalencia de TB 8, 9, 19, 20 . Creemos, sin embargo, que este valor no refleja una estimación real del grado de agrupamiento en el Callao debido a dos razones principales: Primero, el corto periodo de muestreo (6 meses) fue probablemente insuficiente para captar el desarrollo de enfermedad TB en pacientes infectados con una cepa de alguno de los clusters 21 . Segundo, la fracción muestral, que se define como la proporción de casos estudiados con relación al total de casos reportado para una determinada región y lapso de tiempo, fue muy reducida. Recientes reportes demuestran que una reducida fracción muestral subestima enormemente el agrupamiento 22, 23 .
Aunque la fracción muestral del presente estudio fue reducida, no se encontró la presencia de alguna cepa predominante o altamente diseminada en la población estudiada; como se ha observado en varios países del mundo, en donde existe la predominancia de determinados genotipos asociados a una mayor transmisibilidad o a altos niveles de resistencia a drogas. Por ejemplo, las cepas beijing en gran parte del Asia 24,25 ; las cepas de la familia W y W1 en Estados Unidos 26 ; o la cepa M en Argentina 27 .
En el presente estudio se determinaron también los niveles y patrones de resistencia a medicamentos antituberculosos. Se observó elevados niveles de resistencia global (59,4 %), resistencia en pacientes nunca tratados (45,2 %) y antes tratados (71,1%), así como altos niveles de TB-MDR global (27,5%) y TB-MDR en pacientes nunca tratados (16,1 %) y en antes tratados (36,8%). Sin embargo, no se debe asumir que estos valores de resistencia sean extrapolables a la población del Callao, debido a que la población estudiada corresponde a pacientes hospitalizados y ellos fueron reclutados de un hospital de nivel terciario, los cuales probablemente tienen un mayor riesgo de presentar drogoresistencia 28 . Existe poca literatura sobre niveles de resistencia a drogas en pacientes hospitalizados. Fandinho 28 investigó 265 pacientes hospitalizados en dos hospitales terciarios en Río de Janeiro (incidencia TB = 160 casos/100 000 hab; y 17,2 % de resistencia en población general) y encontraron que 16,6 % fueron resistentes por lo menos a una droga y el 10% fueron TB-MDR. Asimismo, Baptista29 encontró 42,6% y 13% de resistencia y TB-MDR, respectivamente en un hospital general de Sao Paulo (incidencia = 55 casos/100 000 hab y 42% de resistencia en el población general); mientras que, Harrow (1998) halló 30% y 15% de resistencia y TB-MDR en un hospital de Guatemala 30.
Los niveles de resistencia encontrados en el presente estudio concuerdan con los hallazgos de Willingham 31 quien llevó a cabo un estudio en un hospital de Lima y encontró que 58% (23/40) fueron resistentes por lo menos a una droga y 20% (8/40) fueron TB- MDR. Los alarmantes niveles de resistencia y multidrogorresistencia observados en hospitales de Lima y Callao son preocupantes dadas las precarias condiciones de bioseguridad y la carencia de apropiadas políticas de manejo intrahospitalaria en los hospitales del país. Willingham investigó el riesgo potencial de transmisión intrahospitalaria y encontró que 75% de los pacientes con TB MDR no había tenido sospecha de TB al ingreso de hospitalización 31.
En conclusión, el método de RFLP- IS6110 fue útil para caracterizar la diversidad clonal de las cepas y logró definir grupos de perfiles genéticos asociados a cepas resistentes y sensibles Por otro lado, se encontraron altos niveles de resistencia y multidrogorresistencia en pacientes TBP-FP hospitalizados, lo cual es alarmante dado las precarias condiciones de bioseguridad en los hospitales de Lima y Callao. Aunque no se encontró la presencia de alguna cepa predominante, se observaron «clusters» agrupando pacientes con TB MDR, lo cual podría sugerir transmisión activa de TB resistente y multidrogorresistente. Son necesarios estudios adicionales en la población para determinar la magnitud de la transmisión activa y su impacto en la emergencia de la resistencia a drogas.
AGRADECIMIENTOS
Agradecemos al personal técnico del Laboratorio Nacional de Referencia de Micobacterias, al Sr. Lino Gómez y al Sr. Hugo Miranda. Al personal técnico del Laboratorio Central del Hospital Nacional Daniel A. Carrión (HNDAC) y al equipo de enfermeras del Programa de Control de Tuberculosis del HNDAC.
REFERENCIAS
1. World Health Organization. Global Tuberculosis Control. WHO Report 2001. [ Links ]
2. Dye C, Scheele S, Dolin P, Pathania V, Raviglioni MC. Concensus Statement Global burden of tuberculosis, estimeted incidence, prevalence, and mortality by country. WHO Global Surveillance and Monitoring Project. JAMA 1999; 282(7): 677- 86. [ Links ]
3. Zumla A, Grange JM. Doing something about tuberculosis. BMJ 1999; 318 (7189):956. [ Links ]
4. Ministerio de Salud. Tuberculosis en el Perú. Informe 2000. Dirección General de Salud de las Personas / Programa de Control de Enfermedades Transmisibles / Control de Tuberculosis. Informe 2000. 322pp. [ Links ]
5. Kato-Maeda M, Small PM. How molecular epidemiology has changed what we know about tuberculosis. West J Med 2000; 172(4):256-9. [ Links ]
6. Van Soolingen. Molecular epidemiology of tuberculosis and other mycobacterial infections: main methodologies and achievements. J Inter Med 2001; 249(1): 1-26. [ Links ]
7. Van Embden JD, Cave MD, Crawford JT, Dale JW, Eisenach KD, Gicquel B, et al. Strain identification of Mycobacterium tuberculosis by DNA fingerprinting: recommendations for a standardized methodology. J Clin Microbiol. 1993; 31(2): 406-9. [ Links ]
8. Small PM, Hopewell PC, Singh SP, Paz A, Parsonnet J, Ruston DC, et al. The epidemiology of tuberculosis in San Francisco. A population-based study using conventional and molecular methods. N Engl J Med. 1994; 330(24):1703-9. [ Links ]
9. Alland D, Kalkut GE, Moss AR, McAdam RA, Hahn JA, Bosworth W, et al. Transmission of tuberculosis in New York City. An analysis by DNA fingerprinting and conventional epidemiologic methods. N Engl J Med. 1994; 330(24): 1710-6. [ Links ]
10. Barnes PF, Yang Z, Pogoda JM, Preston-Martin S, Jones BE, Otaya M, et al. Foci of tuberculosis transmission in central Los Angeles. Am J Respir Crit Care Med. 1999; 159(4 Pt 1): 1081-6. [ Links ]
11. Instituto Nacional de Salud. Manual de normas y procedimientos en bacteriología de tuberculosis. Lima: INS; 1995. Serie de Normas Técnicas N10. [ Links ]
12. Van Soolingen D, De Hass PE, Hermans PW, van Embden JD. RFLP analysis of Mycobacteria. In: RFLP analysis of Mycobacteria. Bilthoven, The Netherlands, National Institute of Public Heath and Environmental Protection 1995, 63 pp. [ Links ]
13. Soini H, Pan X, Teeter L, Musser JM, Graviss EA. Transmission dynamics and molecular characterization of Mycobacterium tuberculosis isolates with low copy numbers of IS6110. J Clin Microbiol. 2001; 39(1): 217-21. [ Links ]
14. Suarez PG, Watt CJ, Alarcon E, Portocarrero J, Zavala D, Canales R, et al. The dynamics of tuberculosis in response to 10 years of intensive control effort in Peru. J Infect Dis 2001; 184(4): 473-8. [ Links ]
15. Ministerio de Salud. Vigilancia de la resistencia a los medicamentos antituberculosos en el Perú. 1999. En: Informe 2000. Dirección General de Salud de las Personas / Programa de Control de Enfermedades Transmisibles / Control de Tuberculosis. MINSA 2000. [ Links ]
16. Yeh RW, Ponce de Leon A, Agasino CB, Hahn JA, Daley CL, Hopewell PC, et al. Stability of Mycobacterium tuberculosis DNA genotypes. J Infect Dis 1998; 177(4): 1107- 11. [ Links ]
17. Alito A, Morcillo N, Scipioni S, Dolmann A, Romano MI, Cataldi A, et al. The IS6110 restriction fragment length polymorphism in particular multidrug- resistant Mycobacterium tuberculosis strains may evolve too fast for reliable use in outbreak investigation. J Clin Microbiol 1999; 37(3): 788-91. [ Links ]
18. Cave MD, Eisenach KD, Templeton G, Salfinger M, Mazurek G, Bates JH. Stability of DNA fingerprint pattern produced with IS6110 in strains of Mycobacterium tuberculosis. J Clin Microbiol 1994; 32(1): 262-6. [ Links ]
19. Ferrazoli L, Palaci M, Marques LR, Jamal LF, Afiune JB, Chimara E, et al. Transmission of tuberculosis in an endemic urban setting in Brazil. Int J Tuberc Lung Dis 2000; 4(1): 18-25 [ Links ]
20. Van Deutekom H, Gerritsen JJ, van Soolingen D, van Ameijden EJ, van Embden JD, Coutinho RA. A molecular epidemiological approach to studying the transmission of tuberculosis in Amsterdam. Clin Infect Dis 1997; 25(5): 1071–7. [ Links ]
21. Warren R, Richardson M, van der Spuy G, Victor T, Sampson S, Beyers N, et al. DNA fingerprinting and molecular epidemiology of tuberculosis: use and interpretation in an epidemic setting. Electrophoresis 1999; 20(8): 1807-12. [ Links ]
22. Murray M. Sampling bias in the molecular epidemiology of tuberculosis. Emerg Infect Dis 2002; 8(4): 363-9. [ Links ]
23. Glynn JR, Vynnycky E, Fine PE. Influence of sampling on estimates of clustering and recent transmission of Mycobacterium tuberculosis derived from DNA fingerprinting techniques. Am J Epidemiol 1999; 149(4): 366-71. [ Links ]
24. Glynn JR, Whiteley J, Bifani PJ, Kremer K, van Soolingen D. Worldwide occurrence of Beijing/W strains of Mycobacterium tuberculosis: a systematic review. Emerg Infect Dis 2002; 8(8): 843-9. [ Links ]
25. Kruuner A, Hoffner SE, Sillastu H, Danilovits M, Levina K, Svenson SB, et al. Spread of drug-resistant pulmonary tuberculosis in Estonia. J Clin Microbiol 2001; 39(9): 3339-45. [ Links ]
26 Bifani PJ, Mathema B, Liu Z, Moghazeh SL, Shopsin B, Tempalski B, et al. Identification of a W variant outbreak of Mycobacterium tuberculosis via population- based molecular epidemiology. JAMA 1999; 282(24): 2321-7. [ Links ]
27. Ritacco V, Di Lonardo M, Reniero A, Ambroggi M, Barrera L, Dambrosi A, et al. Nosocomial spread of human immunodeficiency virus-related multidrug- resistant tuberculosis in Buenos Aires. J Infect Dis 1997; 176(3): 637-42. [ Links ]
28. Fandinho F, Kritski A, Hofer C, Conde H Jr, Ferreira R, Silva M, et al. Drug resistance patterns among hospitalised tuberculous patients in Rio de Janeiro, Brazil, 1993-1994. Mem Inst Oswaldo Cruz 1999; 94(4): 543-7. [ Links ]
29. Baptista IM, Oelemann MC, Opromolla DV, Suffys PN. Drug resistance and genotypes of strains of Mycobacterium tuberculosis isolated from human immunodeficiency virus-infected and non-infected tuberculosis patients in Bauru, Sao Paulo, Brazil. Mem Inst Oswaldo Cruz 2002; 97(8): 1147-52. [ Links ]
30. Harrow EM, Rangel JM, Arriega JM, Cohen I, Regil Ruiz MI, DeRiemer K, et al. Epidemiology and clinical consequences of drug-resistant tuberculosis in a Guatemalan hospital. Chest 1998; 113(6): 1452-8. [ Links ]
31. Willingham FF, Schmitz TL, Contreras M, Kalangi SE, Vivar AM, Caviedes L, et al. Hospital control and multidrug-resistant pulmonary tuberculosis in female patients, Lima, Perú. Emerg Infect Dis 2001; 7(1): 123-7. [ Links ]
Correspondencia: Christian Baldeviano Vidalón. Centro Nacional de Salud Pública. Instituto Nacional de Salud. Dirección: Calle Cápac Yupanqui 1400. Lima 11, Perú.
Telf.: (511) 471-9920 anexo 149 Fax: (511) 471-0179.
Correo electrónico: cvaldeviano@ins.gob.pe, chrisbal2001@yahoo.es