Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Medicina Experimental y Salud Publica
versión impresa ISSN 1726-4634
Rev. perú. med. exp. salud publica v.23 n.1 Lima ene.-mar. 2006
TRABAJO ORIGINAL
Administración de vacunas y casos de muerte súbita del lactante en el Perú, 2001. ¿asociación o coincidencia temporal?
Javier Vargas H1; Magna Suárez J1; Alejandro Llamoga S1; Neyda Quispe T1; Fernando Alva R2; Julia Chu C3; Héctor Pereyra S4; María Ticona Z4; Jorge Medrano G5; Carolina Cerna D5
1 Centro Nacional de Salud Pública, Instituto Nacional de Salud. Lima, Perú.
2 Centro Nacional de Control de Calidad, Instituto Nacional de Salud. Lima Perú.
3 Centro Nacional de Producción de Biológicos, Instituto Nacional de Salud. Lima Perú.
4 Oficina General de Epidemiología, Ministerio de Salud. Lima, Perú.
5 Dirección General de Salud de las Personas, Ministerio de Salud. Lima, Perú.
RESUMEN
Objetivos: Describir las características clínicas, socioeconómicas, y patológicas de nueve casos de lactantes que fallecieron horas después de administrárseles vacunas antipolio y DPT junto con anti Haemophilus influenzae b o asociada con antihepatitis B o BCG. Materiales y métodos: Revisión de la historia clínica, entrevista con el equipo de salud a cargo de la vacunación y con los padres del lactante fallecido. Revisión de los informes del protocolo de autopsia e informes de anatomía patológica y entrevista con los médicos legistas y patólogos. Evaluación de control de calidad de las vacunas administradas. Realización de exámenes de inmunohistoquímica de tejidos pulmonares para el diagnóstico de virus. Resultados: Entre agosto y diciembre de 2001 se notificaron en el Perú, nueve casos de fallecimiento de lactantes entre ocho horas y tres días después de la aplicación de vacunas DPT y antipolio. Después de la vacunación, los síntomas iniciaron entre 30 minutos a tres horas y la muerte se produjo entre ocho a 78 horas. Los síntomas más frecuentes fueron irritabilidad 8/9, llanto persistente 6/9, somnolencia 5/9, sangrado por nariz y boca 5/9. Todos los casos procedieron de familias pobres o muy pobres. El control de calidad se corroboró que las vacunas cumplieron con los estándares establecidos por la OMS. Las causas de la muerte reportadas en las necropsias fueron neumonía en dos casos y edema pulmonar en cinco casos, los informes de anatomía patológica mostraron una neumonitis intersticial y meningitis linfocitaria. No se observaron efectos citopáticos virales en los tejidos pulmonares y los estudios toxicológicos fueron negativos. Conclusiones: No existe evidencia de una asociación causal entre los eventos fatales y la administración de las vacunas.
Palabras clave: Vacuna contra difteria, tétanos y tos ferina; /efectos adversos; Muerte súbita infantil; Perú (Fuente: DeCS BIREME).
ABSTRACT
Objectives: To describe clinical, socio-economic, and pathological characteristics of nine infants who died hours after receiving anti-polio and DPT vaccines, together with anti-Haemophilus influenzae b or in association to anti-hepatitis B vaccine or BCG. Materials and methods: Review of the clinical record, interview with the healthcare team in charge of immunization, and with parents of the deceased infant. Review the autopsy and pathology reports, as well as an interview with pathologists and forensic physicians. Quality control assessment of vaccines used immunohistochemistry examinations for virus diagnosis. Results: Between August and December 2001, nine cases of infant death were reported in Peru, between 8 hours and 3 days after receiving DPT and anti-polio vaccines. After immunization, symptoms appeared from thirty minutes to three hours, and death occurred between 8 to 78 hours. Most frequently reported symptoms were: irritability (8/9), persistent weeping (6/9), somnolence (5/9), nose and mouth bleeding (5/9). All cases occurred in poor or very poor families. Quality control assessments corroborated that vaccines complied with standards set by the World Health Organization. Causes of death reported in autopsies were pneumonia in 2 cases and pulmonary edema in 5 cases; pathology reports indicated the presence of interstitial pneumonitis and lymphocyte meningitis. No viral cytopathic effects in pulmonary tissues were found, and toxicological studies were reported as negative. Conclusions: There is no evidence of a causal relationship between fatal events and vaccine administration.
Keywords: Diphteria-Tetanus-Pertussis Vaccine; /adverse effects; Sudden Infant Death; Peru (source: DeCS BIREME).
INTRODUCCIÓN
La inmunización contra las enfermedades infecciosas es reconocida como uno de los más importantes logros de la salud pública en los últimos doscientos años. Ha permitido la erradicación de la viruela, la eliminación de la poliomielitis del hemisferio occidental y ha contribuido a reducir de manera importante la incidencia de otras enfermedades1. Sin embargo, se reconoce que la vacunación puede causar raramente efectos secundarios serios2.
En los países desarrollados, el incremento de las coberturas de vacunación se acompañó de un mayor crecimiento de los eventos adversos, que incluyen a las reacciones realmente causadas por las vacunas y acontecimientos que pueden coincidir en el tiempo en que se realizó la vacunación, especialmente considerando que el periodo de mayor vulnerabilidad a las enfermedades corresponden a los primeros meses de vida, periodo en el que los niños empiezan a recibir las vacunas2,3. A pesar de todo, es consenso generalizado que la vacunación es más segura y beneficiosa, que los riesgos de enfermar o morir por las enfermedades que éstas previenen4.
Una de las vacunas más reactogénicas que existen es la DPT, compuesta por células íntegras de Bordetella pertussis, y los toxoides tetánico y diftérico. Se considera que de éstos, el componente pertusis es el responsable de la mayoría de las reacciones indeseables esperadasdespués de la vacunación, debido a los efectos de las toxinas que contiene5. La vinculación entre DPT y efectos indeseables está bien documentada e incluso se han clasificado y ordenado para establecer o rechazar una asociación causal según el grado de evidencia existente2,3.
La posible relación entre la vacunación con DPT y muerte súbita del lactante ha sido objeto de varias publicaciones6-9; sin embargo, la mayoría de estudios recientes, concluyen que es una coincidencia temporal y no una asociación causal, ya que la probabilidad de que un lactante presente muerte súbita es mayor en los primeros meses de vida, periodo en el que se aplican las vacunas10-14.
El síndrome de muerte súbita del lactante (SMSL) se define como muerte repentina de un lactante menor de un año de edad, que permanece sin explicación después de una investigación minuciosa del caso, incluyendo la práctica de una autopsia completa, examen del escenario de la muerte y repaso de la historia clínica15. Se incluyen los casos en que se encuentran infiltrados inflamatorios u otras anormalidades en la autopsia que no expliquen la muerte16.
Las tasas de mortalidad por SMSL varían considerablemente de un país a otro, pueden ser bajas como en Hong Kong (0,3 defunciones por 1000 hab. 1987) o muy altas como Nueva Zelandia (4,4 defunciones por 1000 hab. 1988)17, en Estados Unidos se notifican anualmente más de 5000 casos de muerte súbita infantil2,3, en el Perú carecemos de esa información con exactitud.
Casi todos los niños peruanos, entre los dos y seis meses, reciben como parte del calendario regular de vacunación, la vacuna DPT (denominada comúnmente triple), o vacuna DPT en combinación con vacuna contra el Hemophilus influenzae serotipo B y vacuna contra la hepatitis B (pentavalente), aplicada según el área geográfica en donde resida1.
Durante el segundo semestre del año 2001 se notificaron en diferentes departamentos del Perú, nueve casos de muerte súbita del lactante, poco tiempo después de recibir vacunas DPT y otras. El presente artículo describe los resultados de las investigaciones de campo realizadas acerca de estos casos.
MATERIALES Y MÉTODOS
POBLACIÓN DE ESTUDIO
Se realizó un estudio descriptivo, tipo serie de casos, con los lactantes que fallecieron en un lapso de 8 a 78 horas después de recibir vacunas DPT, antipolio y BCG del Programa de Inmunizaciones del Ministerio de Salud (MINSA) en los departamentos de Lima, La Libertad, San Martín, Lambayeque, Arequipa y Cusco entre agosto y diciembre de 2001.
RECOLECCIÓN DE INFORMACIÓN
Para dilucidar las causas de la muerte de estos lactantes, se conformaron, para cada uno de los casos, equipos de investigación, en un trabajo conjunto realizado por el Instituto Nacional de Salud, la Oficina General de Epidemiología y el Programa de Inmunizaciones de la Dirección General de Salud de las Personas del MINSA, la Organización Panamericana de la Salud y las direcciones regionales de salud. Estos equipos viajaron a cada una de las ciudades en donde se produjeron los eventos para obtener la mayor cantidad de información del caso, se regresó a Lambayeque y La Libertad para completar datos inicialmente omitidos o pendientes. Para cada uno de los casos se realizó in situ las siguientes actividades:
- Revisión de la historia clínica del lactante fallecido, del establecimiento de salud en donde nació,en donde fue vacunado y, eventualmente, donde recibió su última atención.
- Entrevista con el equipo de salud a cargo de la vacunación y de la última atención recibida. Inventario de los insumos y materiales de las salas de vacunación.
- Entrevista con los padres del lactante fallecido. La madre fue la principal informante.
- Recolección de muestras de vacunas, jeringas y agujas en el establecimiento de salud en donde se vacunó el lactante y de la red de abastecimiento intrarregional de biológicos, de los mismos lotes involucrados en los casos, los cuales fueron enviados al Centro Nacional de Control de Calidad del Instituto Nacional de Salud en Lima.
- Revisión de los informes del protocolo de autopsia y entrevista con el médico legista que realizó la autopsia del lactante fallecido; además se tomaron muestras de órganos y tejidos que fueron enviadas a la Morgue Central de Lima.
CONTROL DE CALIDAD
Se realizó el control de calidad de las vacunas DPT, antipolio y BCG, según procedencia (así fuesen del mismo lote) y de acuerdo con el tamaño de la muestra, verificando la integridad del envase, esterilidad, inocuidad (toxicidad inespecífica, prueba de ganancia de peso del ratón), niveles de timerosal y aluminio, según correspondiera, en el Centro Nacional de Control de Calidad del Instituto Nacional de Salud en coordinación con un comité técnicoad hoc, siguiendo los protocolos recomendados por la Organización Mundial de la Salud.
Las prueba realizadas para las jeringas fueron integridad del envase, esterilidad e inyección sistémica (reactividadbiológica). Adicionalmente, se enviaron muestras de dos lotes de vacuna DPT al Instituto Nacional de Control de Calidad de la Salud de la Fundación Oswaldo Cruz del Brasil para que se realicen pruebas de toxicidad específica y potencia.
ANATOMÍA PATOLÓGICA
Se revisaron los informes de anatomía patológica de la Morgue Central de Lima e informes toxicológicos, así como la entrevista con los médicos patólogos responsables. Se enviaron los bloques de muestras fijadas de cerebro y pulmones que estuvieron disponibles al Instituto de Patología de las Fuerzas Armadas de los Estados Unidos. En donde se realizaron pruebas de coloración de metamina de plata de Grocott, Brown-Hopps, ácido peryódico de Schiff y Warthin Satrry, así como pruebas de inmunohistoquímica para la identificación de los siguientes agentes virales: Epstein Barr, citomegalovirus, adenovirus, herpes simpIe I y II. ReSULtAdoS Se investigaron nueve casos de lactantes (siete varones / dos mujeres) de dos meses (7) y tres meses (2) que fallecieron entre ocho horas y tres días después de la aplicación de vacunas que les correspondía recibir de acuerdo con la edad y con el esquema oficial de vacunación para menores de cinco años del Ministerio de Salud entre los meses de agosto y diciembre, la mayoría de ellos (6/9) se presentaron en septiembre y octubre.
En todos los casos los niños recibieron vacuna DPT y antipolio. A excepción del caso seis, todos los demás recibieron vacuna DPT de cuatro lotes diferentes delmismo productor. El caso cinco recibió además BCG, el caso cuatro el componente anti Haemophilus influenzae B de una vacuna pentavalente y el caso seis la vacuna pentavalente completamente reconstituida (DPT + anti Haemophilus influenzae B + Anti Hepatitis B) (Tabla 1).
La distribución de los casos fue geográficamente homogénea en todo el país. Se presentaron casos tanto en la zona norte (dos en La Libertad, dos en Lambayeque y uno en San Martín), como en la zona centro (dos en Lima) y en la zona sur (uno en Arequipa y uno en Cusco) del país. Ocho de los casos fueron reportados por los establecimientos de salud en donde fueron vacunados y uno fue descubierto durante la investigación de un caso reportado por uno de los establecimientos de salud. (Tabla 1)
Más de la mitad de los niños 5/9, presentaron una evaluación de control de crecimiento y desarrollo del niño, el mismo día de la vacunación, siendo calificados como niños sanos, mientras que el resto, se calificaron como niños sanos por el personal a cargo de la vacunación. Sin embargo, se ha verificado en al menos la tercera parte de ellos, 3/9 presentaron antecedentes de enfermedades o riesgos previos (uno nació pretérmino y con bajo peso, uno nació de parto gemelar y uno presentó diagnóstico de neumonía por criterios del programa).
Ocho de los nueve casos presentaron síntomas después de recibir la vacunación, no se tienen datos de la enfermedad en el caso siete. El tiempo de inicio de los síntomas varió de 30 minutos a 17 horas después de servacunados. El tiempo transcurrido desde la aplicación de la vacuna hasta la muerte varió entre 8 y 78 horas, con una mediana de 20 horas.
Los síntomas sistémicos más frecuentemente reportados fueron irritabilidad 8/9, llanto persistente 6/9, somnolencia 5/9, sangrado o espuma por nariz y boca 5/9, hiporexia (disminución de la lactancia) 4/9. La fiebre elevada fue reportada sólo en tres de los nueve casos. En uno de los casos se reportó cianosis. Entre los síntomas locales fueron frecuentes dolor y enrojecimiento en el lugar de la aplicación (Tabla 2).
En pocos niños, vacunados de los mismos viales con que se vacunaron los niños que fallecieron, se presentaron eventos adversos asociados con la vacunación. En Trujillo, dos de los seis niños a quienes se les administró la vacuna del mismo vial presentaron abscesos subcutáneos. Este evento estuvo relacionado con la utilización de una aguja (aguja de 25 G por 1¨) no recomendada para la aplicación de esta vacuna. En Lambayeque, uno de los nueve niños que recibieron la vacuna del mismo vial presentó una convulsión (Tabla 3).
Todos los casos procedieron de familias pobres o muy pobres, ocho de los nueve casos procedieron de zonas urbanas marginales y sólo un caso, el que fue descubierto en la investigación de campo, procedía de un área rural. La mayoría de los casos 7/9, compartían la misma cama con los padres. La edad de la madre se encontró en un rango de 15 a 25 años con una mediana de 20 años. Cinco madres informaron tener estudios secundarios, tres primaria y sólo una informó ser analfabeta (Tabla 4).
Los estudios de esterilidad, inocuidad, timerosal, aluminio, pH, características físicas, inspección y verificación de los envases realizados en el Instituto Nacional de Salud indicaron que las diferentes vacunas y lotes empleados en la inmunización de los niños, cumplieron criterios de conformidad con los estándares establecidos por la Organización Mundial de la Salud. Del mismo modo, las pruebas de toxicidad específica y de potencia de dos de los lotes de vacuna, realizadas en el Instituto de Control de Calidad de la Fundación Oswaldo Cruz en el Brasil, cumplieron criterios de conformidad con los estándares establecidos por la Organización Mundial de la Salud.
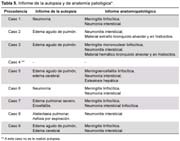
En casi todos los casos 8/9, se practicó una autopsia de ley. Las causas de la muerte reportadas por los médicoslegistas de acuerdo con las necropsias realizadas fueron neumonía en dos casos y edema pulmonar o edema agudo de pulmón en cinco casos. En un caso se reportó asfixia por aspiración y atelectasia. En dos casos se reportó además edema cerebral y en uno encefalitis. Sin embargo, los informes de anatomía patológica realizados en la Morgue Central de Lima, coincidieron en todos los casos en reportar una neumonitis intersticial y en la mayoría de ellos meningitis o meningoencefalitis linfocitaria (Tabla 5). La falta de uniformidad en la presentación de los resultados se debe a que no se enviaron las mismas muestras de órganos y tejidos en todos los casos.
En opinión de los patólogos que examinaron las muestras, los tejidos disponibles mostraron un componente inflamatorio multifocal, multivisceral, parenquimal, intersticial y de tejidos blandos periféricos con predominio perivascular y mononuclear linfocítico, el cual podríacorresponder a una infección viral. Sobre la base de esta opinión se remitieron muestras de tejido pulmonar disponibles al Instituto de Patología de las Fuerzas Armadas de los Estados Unidos (AFIP) solicitando la identificación de agentes virales, los tejidos enviados correspondieron a los casos 1, 2, 3, 5, 6, 7 y 8.
Para todas las muestras remitidas, la AFIP informó que en las secciones de pulmón examinadas observaron congestión e inflamación crónica en el intersticio, así como la presencia de cocos y bacilos Gram positivos que probablemente representan crecimiento post mórtem de la flora normal. No se observaron otros microorganismos en tinciones especiales, ni efectos citopáticos virales. Las tinciones de inmunohistoquímica para citomegalovirus, virus de Epstein Barr, virus de herpes simple tipo I y II y adenovirus fueron no reactivos, sin embargo, los patólogos de la AFIP consideran que dichos hallazgos son sugerentes de una infección viral.
Los estudios toxicológicos de muestras de contenido gástrico e hígado incluyeron la determinación de: ácido clorhídrico, insecticidas órgano clorados / órgano fosforados / carbámicos, ácidos orgánicos, salicilatos, alcaloides, sulfamidados, alcaloides, psicofármacos barbitúricos / fenotiazínicos / benzodiazipinas, marihuana, anfetaminas, y carboxihemoglobina. Todos los exámenes fueron negativos.
DISCUSIÓN
Es completamente inusual, aun en el Perú donde se carece de información básica, que se notifiquen en un periodo tan corto (cinco meses), nueve casos de muerte en lactantes entre dos y tres meses de edad, con una mediana de veinte horas después de administrárseles vacunas DPT y antipolio, entre otras. En varios países se han reportado casos de esta asociación9,11, sin embargo, la variación en el periodo que siguió desde la vacunación hasta la muerte, así como las circunstancias en las que se produjeron, es bastante variable13,18.
Una serie de casos de muerte súbita del lactante asociada temporalmente a vacunación con DPT, frecuentemente citada ocurrió en Tennessee, Estados Unidos, a fines de 1978 y comienzos de 1979, donde se registraron ocho casos de muerte después de la vacunación3, de los cuales, cuatro murieron antes de cumplirse 24 horas después de ser vacunados. Este episodio culminó con la suspensión del lote de vacuna involucrado en las muertes, pese a no haberse comprobado mediante los estudios de control de calidad de la vacuna, que ésta estuviera fuera de los patrones recomendados.
Inicialmente, algunos estudios encontraron un mayor riesgo de presentar síndrome de muerte súbita del lactante en niños que se vacunaron con DPT6,8. Walker etal., reportaron que la tasa de síndrome de muerte súbita en los niños que se vacunaron con DPT entre cero y tres días antes de morir fue siete veces mayor que en los niños que se vacunaron 30 ó más días antes de morir6. Por su parte, Baraff et al. encontraron que el número de muertes observadas fue significativamente mayor que el número de muertes esperadas entre los siete días después de la inmunización con DPT8. Estas observaciones fueron cuestionadas2,5, sus críticos afirman que los autores asumieron que la presentación del síndrome de muerte súbita infantil sigue una distribución similar en cada semana, desconociendo que los casos de muerte súbita infantil alcanzan su pico en el segundo mes de vida, periodo en el que los niños se vacunan14.
Sin embargo estudios posteriores descartan definitivamente la existencia de una asociación entre vacunación con DPT y muerte súbita infantil. Un estudio de seguimiento durante 12 años publicado en 1987 en los Estados Unidos reportó sólo cuatro muertes hasta tres días después de la aplicación de vacuna DPT; éstas se produjeron en un intervalo de un año de los 12 que duró el estudio2.
El Instituto de Medicina de los Estados Unidos3, después de revisar en 1991, toda la información publicada hasta entonces referida a la vacunación contra la tos ferina y las muertes clasificadas como SMSL, mediante la técnica del meta análisis para comparar los resultados de estudios controlados, concluyó que: Los estudios que muestran una relación temporal entre estos eventos son consistentes con la ocurrencia esperada de SMSI en el rango de edad en los cuales la vacunación con DPT comúnmente ocurre. Los únicos eventos adversos que presentan una evidencia aceptable de asociación con la administración de DPT son anafilaxis y llanto prolongado e inconsolable. Esta falta de asociación ha sido corroborada con estudios tipo casos y controles19,20, así como un metaanálisis posterior18.
Incluso Fleming et al. después de realizar un estudio de casos y controles de niños fallecidos con diagnóstico de muerte súbita en el Reino Unido de Gran Bretaña concluye que la vacunación con DPT incluso actuaría como un factor protector frente al SMSL12.
No hay información suficiente para juzgar adecuadamente el SMSL en el Perú, ya que muchos de los factores de riesgo reconocidos de muerte súbita infantil21-23, tales como bajo nivel socioeconómico, mayor número de partos, madre adolescente, niños prematuros o de bajo peso, dormir con los padres, etc. son tan prevalentes en nuestro medio, a tal punto que la mayoría de los casos presentados en este reporte a pesar de su escaso número, no dejan de tener alguno.
Una hipótesis que se manejó con respecto a la asociación temporal entre la aplicación de vacunas y las muertes, fue que si la vacuna está involucrada en la muerte de estos niños, era de esperarse que la frecuencia de reacciones adversas en los niños vacunados sea superior a las reconocidas y esperadas. La Oficina General de Epidemiología llevó a cabo varios estudios de prevalencia de eventos adversos asociados con la vacunación en los lugares donde se notificaron fallecidos después de la administración de vacuna DPT y antipolio, encontrando que la frecuencia de los eventos adversos postvacunales correspondía a las tasas esperadas de eventos adversos que siguen a la vacunación con DPT (comunicación personal, OGE).
No se ha encontrado reportes de casos acerca del curso clínico antes del fallecimiento o de los hallazgos de la anatomía patológica en casos similares. Aunque no se pudo establecer el agente etiológico de la muerte, patólogos de la Morgue Central de Lima y del Instituto de Patología de las Fuerzas Armadas de los Estados Unidos coincidieron en señalar que los hallazgos parecen corresponder a una infección viral. A juzgar por el periodo estacional en que se presentaron estos casos, es posible que haya coincidido con un incremento en la incidencia de infecciones respiratorias de origen viral, pero carecemos de datos exactos al respecto.
La presencia de hallazgos patológicos pulmonares que pudieran explicar la causa de muerte en niños con SMSL son similares a otras series, como en Uruguay en la que se atribuyó como causa respiratoria a 48,2% de los casos24, sin embargo, también es frecuente la presencia de infiltrado y probable infección respiratoria que no explican el deceso24,25.
Aunque este estudio sea descriptivo, sin análisis estadístico y sin grupo control, la información recogida y analizada permite plantear que no existe evidencia de una asociación causal entre los eventos fatales estudiados y la administración de las vacunas; conclusión que se sustenta principalmente en los resultados de control de calidad practicados en las vacunas demostrando que cumplieron los estándares recomendados, la opinión coincidente de patólogos nacionales y de EEUU, acerca del patrón histopatológico en pulmones de presunto origen viral, y el respaldo de estudios controlados que descartan esta asociación.
Sin embargo, es importante que el Programa de Inmunizaciones del Ministerio de Salud del Perú, continúe manteniendo la calidad de las vacunas administradas e investigando los eventos adversos graves seguidos a la inmunización. Vargas J. et al.
AGRADECIMIENTOS
A la Dra. Tanis Batsel y al Armed Forces Institute of Pathology (AFIP) de los Estados Unidos por el procesamiento y análisis de las láminas histopatológicas; a la Dra. Lucía de Oliveira, al Dr. Washington Toledo y al Dr. Carlos Castillo-Solorzano de la Organización Panamericana de la Salud, por su colaboración en la realización del estudio así como las sugerencias en la redacción del manuscrito.
REFERENCIAS BIBLIOGRÁFICAS
1. Ministerio de Salud del Perú / Organización Panamericana de la Salud. Evaluación Multidisciplinaria del componente Inmunización en el Perú. Lima Agosto del 2002. [ Links ]
2. Advisory Committee on immunization Practices. Update: Vaccine side effects, adverse, reactions, contraindications and precautions. Recommendations of the Advisory Committee on Immunization Practices (ACIP) MMWR Recomm Rep 1996; 45(RR-12): 1-35. [ Links ]
3. Howson CP; Howe CJ; Fineberg HV. Adverse effects of pertussis and rubella vaccines. A report of the committee to review the adverse consequences of pertussis and rubella vaccines. Washington DC: National Academy Press; 1991. [ Links ]
4. Francois G, Duclos P, Margolis H, Lavanchy D, SiegristCA, Meheus A, et al. Vaccine safety controversies and the future of vaccination programs. Pediatr Infect Dis J 2005; 24(11): 953-61. [ Links ]
5. Mortimer EA. Pertussis Vaccine. In: Plotkin SA, Mortimer EA, eds. Vaccines. 2nd ed. Philadelphia: WA Saunders Co; 1994. p. 91-135. [ Links ]
6. Walker AM, Jick H, Perera DR, Thompson RS, Knauss TA. Diphtheria-tetanus-pertussis immunization and sudden infant death syndrome. Am J Public Health 1987; 77(8): 945–51. [ Links ]
7. Griffin MR, Ray WA, Livengood JR, Schaffner W. Risk of sudden infant death syndrome after immunization with the diphtheria-tetanus-pertussis vaccine. N Engl J Med 1988; 319(10): 618-23. [ Links ]
8. Baraff LJ, Ablon WJ, Weiss RC. Possible temporal association between diphtheria-tetanus toxoid-pertussis vaccination and sudden infant death syndrome. Pediatr Infect Dis 1983; 2(1): 7-11. [ Links ]
9. Torch W. Diphteria-Pertussis-Tetanus (DPT) immunization: A potential cause of sudden infant death syndrome (SIDS). Neurology 1982; 32: 169-70. [ Links ]
10. Hoffman HJ, Hunter JC, Damus K, Pakter J, Peterson DR, van Belle g, et al. Diphtheria-tetanus-pertussis immunization and sudden infant death: results of the National Institute of Child Health and Human Development Cooperative Epidemiological Study of Sudden infant death syndrome risk factors. Pediatrics 1987; 79(4): 598-611. [ Links ]
11. Bouvier-Colle MH, Flahaut A, Messiah A, Jougla E, Hatton F. Sudden infant death and immunization: an extensive epidemiological approach to the problem in France-Winter 1986. Int J Epidemiol 1989; 18(1): 121-26. [ Links ]
12. Fleming P, Blair P, Platt M, Tripp J, Smith I, Golding J. The UK accelerated immunization programme and suddenunexpected death in infancy: casecontrol study. BMJ 2001; 322(7290): 822. [ Links ]
13. Brotherton JM, Hull BP, Hayen A, Gidding HF, Burgess MA. Probability of coincident vaccination in the 24 or 48 hours preceding sudden infant death syndrome death in Australia. Pediatrics 2005; 115(6): e643-46. [ Links ]
14. Mortimer EA Jr, Jones PK, Adelson L. DTP and SIDS. Correspondence. Pediatr Infect Dis 1983; 2(6): 492-93. [ Links ]
15. Willinger M, James LS, Catz C. Defining the sudden infant death syndrome (SIDS): deliberations of an expert panel convened by the National Institute of Child Health and Human Development. Pediatr Patol 1991; 11(5): 677-84. [ Links ]
16. Beckwith JB. Defining the sudden infant death syndrome. Arch Pediatr Adolesc Med 2003; 157(3): 286-90. [ Links ]
17. Mitchell EA, Becroft dM. Comparison of sudden infant death syndrome mortality over time and among countries. Acta Paediatr 1997; 86(8): 789-90. [ Links ]
18. Carvajal A, Caro-Patón T, Martin de diego I, Martin Arias LH, Alvarez Requejo A, Lobato A. Vacuna DTP y syndrome de muerte súbita del lactante. Med Clin (Barc) 1996; 106(17): 649-52. [ Links ]
19. Jonville-Bera AP, Autret-Leca E, Barbeillon F, Paris- Llado J, French Reference Centers for SidS. Sudden unexpected death in infants under 3 month of age and vaccination status. A case-control study. Br J Clin Pharmacol 2001; 51(3): 271-76. [ Links ]
20. Heininger U, Kleemann WJ, Cherry JD, Sudden infant death Syndrome Study group. A controlled study of the relationship between Bordetella pertussis infections and sudden unexpected deaths among German infants. Pediatrics 2004; 114(1): e9-15. [ Links ]
21. Leach CE, Blair P, Fleming P, Smith I; Platt M; Berry P, et al. Epidemiology of SIDS and explained sudden infant deaths. Pediatrics 1999; 104(4): e43.
22. Pérez E; Hernández M; Marrero A. Principales hipótesis y teorías patogénicas del SMSL. En: Grupo de Trabajo para el Estudio y Prevención de la Muerte Súbita Infantil de la Asociación Española de Pediatría. Síndrome de Muerte Súbita del Lactante (SMSL). Libro Blanco. 2ª ed. Madrid: Ergón; 2003. p. 46-56. [ Links ]
23. Asociación Latinoamericana de Pediatría, Comité en síndrome de muerte súbita del lactante. Consenso para la reducción del riesgo en el síndrome de muerte súbita del lactante. Arch Pediatr Urug 2003; 74(4): 275-77. [ Links ]
24. Gutiérrez C, Siminovich M. Enfermedad pulmonar en 238 casos de muerte inesperada del lactante. Arch Pediatr Urug 2003; 74(4): 255-58. [ Links ]
25. Krous HF, Nadeau JM, Silva PD, Blackbourne Bd. A comparison of respiratory symptoms and inflammation in sudden infant death syndrome and in accidental or inflicted infant death. Am J Forensic Med Pathol 2003; 24(1): 1-8. [ Links ]
Correspondencia: Dr. Javier Vargas Herrera, Centro Nacional de Salud Pública, Instituto Nacional de Salud. Lima, Perú.
Dirección: Jirón Cápac Yupanqui 1400, Jesús María, Lima 11.
Teléfono: (511) 471-9920
Correo electrónico: jvargas@ins.gob.pe