Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Medicina Experimental y Salud Publica
versión impresa ISSN 1726-4634
Rev. perú. med. exp. salud publica v.23 n.2 Lima abr. 2006
TRABAJOS ORIGINALES
Niveles de resistencia a drogas antituberculosas en pacientes con infección VIH / Tuberculosis, Lima, 1998-2001.
Luis Asencios S1; Lucy Vásquez C1; Elena Leo H1; Neyda Quispe T1; Luz Huaroto V 2; César Cabezas S1
1 Laboratorio de Referencia Nacional de Micobacterias, Centro Nacional de Salud Pública, Instituto Nacional de Salud. Lima, Perú.
2 Hospital Nacional Dos de Mayo. Lima, Perú.
RESUMEN
Objetivos: Determinar los niveles de resistencia a drogas antituberculosas de primera línea en muestras clínicas de pacientes con coinfección por el virus de la inmunodeficiencia humana y tuberculosis (VIH-TB) en cinco hospitales de Lima en el periodo 1998-2000. Materiales y métodos: Estudio descriptivo que incluyó las muestras de cultivos de Mycobacterium tuberculosis de pacientes con coinfección VIH-TB, a los que se realizó las pruebas de sensibilidad por el método de las proporciones para isoniacida (H), estreptomicina (S), etambutol (E) y rifampicina (R), y el método de Wayne para pirazinamida (H). Resultados: De 523 muestras de pacientes incluidos, 78,2% correspondieron a varones, 72,7% fueron de pacientes sin antecedentes de tratamiento previo. Los valores de resistencia global primaria y multidrogorresistencia (MDR) primaria fueron 55,8% y 32,1%, respectivamente; en tanto que los valores de resistencia global adquirida y MDR adquirida fueron 93,0% y 74,8%. La resistencia primaria por drogas fue H (42,1%), R (35,0%), S (35,3%), E (19,0%) y Z (24,5%) respectivamente; y la resistencia adquirida por drogas fueron H (85,3%), R (78,3%), S (64,4%), E (42,0%) y Z (46,2%). Conclusión: Los niveles resistencia a drogas antituberculosas y la MDR en pacientes con coinfección VIH-TB provenientes de hospitales de Lima son elevados.
Palabras clave: Mycobacterium tuberculosis; VIH; Resistencia a drogas; Perú (fuente: DeCS BIREME).
ABSTRACT
Objective: To determine resistance rates to first-line antituberculous drugs in clinical samples from patients co-infected with the human immunodeficiency virus (HIV) and M. tuberculosis (TB) in five hospitals in Lima between 1998–2000. Materials and methods: A descriptive study including samples sent for culturing Mycobacterium tuberculosis in patients co-infected with HIV-TB. Susceptibility tests for isoniazid (H), streptomycin (S), ethambutol (E), and rifampin (R) were performed using the proportion method and Waynes method for pyrazinamide (Z). Results: Out of 523 samples, 78,2% were from male patients, and 72,7% were from naive patients. Overall primary resistance and multidrug-resistance (MDR) rates were 55,8% and 32,1%, respectively; and overall acquired resistance and MDR rates were 93,0% and 74,8%, respectively. Primary resistance rates were: H, 42,1%; R, 35,0%; S, 35,3%; E, 19.0%, and Z, 24,5%, respectively; and acquired resistance rates were: h, 85,3%; R, 78,3%; S, 64,4%; E, 42,0%; and Z, 46,2%. Conclusion: There are high resistance rates to antituberculous drugs and MDR TB in patients co-infected with HIV and TB in Lima hospitals.
Key words: Mycobacterium tuberculosis; HIV; Drug resistance; Peru (source: DeCS BIREME).
INTRODUCCIÓN
La coinfección tuberculosis (TB) – virus de inmunodeficiencia humana (VIH) se ha convertido en un grave problema de salud pública. La Organización Mundial de la Salud (OMS) estima que de los más de dos mil millones de personas infectadas por Mycobacterium tuberculosis en el año 2000, 8,3 millones fueron casos nuevos de TB y 11 millones de personas presentan coinfección VIH-TB1-3.
El resurgimiento de la TB viene siendo influenciado por factores como el incremento de la población marginal con problemas de pobreza y hacinamiento, el deterioro de los programas de control de la enfermedad, la epidemia VIH/SIDA y la aparición de cepas resistentes a los medicamentos antituberculosos4. En el caso del VIH, se reporta que esta infección es responsable de 4,2% de los casos nuevos de tuberculosis1.
En los EE.UU., entre 1993 y 1996, de acuerdo con los Center for Disease Control (CDC), el riesgo de presentar TB resistente es mayor en los pacientes con infección por VIH. Además, se informó un aumento de las tasas de resistencia a rifampicina (R) en personas con infección por VIH asociada a una mala adhesión al tratamiento antituberculoso. Según CDC, las resistencias globales han aumentado hasta 14% y las resistencias a isoniacida (H) y rifampicina (R) hasta 3,5%5; en tanto que un estudio mundial reveló cifras de resistencia primaria del 1,7-36,9%, y entre 5,3-93,8% en aquellos que habían recibido tratamiento antituberculoso6.
En el Perú, los niveles de resistencia de las drogas antituberculosas también se han visto incrementados. Si bien se demostró que la combinación 2RHZE/4R2H2 (dos meses de isoniacida + rifampicina + estreptomicina + etambutol, seguido de cuatro meses de isoniacida + rifampicina) logró en un inicio disminuir la tasa de fracasos en pacientes con tuberculosis sin antecedente de tratamiento, entre los años 1996 y 2000, se ha observado una tendencia en aumento progresivo, año por año, de los porcentajes de fracasos al tratamiento en los enfermos con TB que recibieron este esquema7.
En los dos estudios nacionales de vigilancia de resistencia a las drogas antituberculosas de primera línea (1995-96 y 1999)8,9, se evidencia un incremento en los niveles de resistencia primaria global (de 15,4% a 17,8%) y de multidrogorresistencia primaria (de 2,5% a 3%), situación que podría tener relación con los casos cada vez mayores de personas portadores de la infección por VIH, y que podrían estar contribuyendo con el aumento de los fracasos y la mayor morbimortalidad por TB9.
Dado que en nuestro país es escasa la información sobre la resistencia a drogas antituberculosas en pacientes con coinfección VIH-TB, se realizó el presente trabajo con el objetivo de conocer los niveles de resistencia a los medicamentos antituberculosos de primera línea en pacientes con esta coinfección durante el año 1998 al año 2001.
MATERIALES Y MÉTODOS
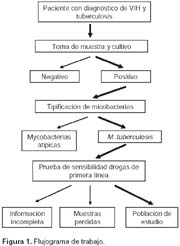
Se realizó un estudio observacional, descriptivo, y prospectivo, en el cual se incluyeron todos los cultivos positivos para Mycobacterium tuberculosis de pacientes con infección por VIH diagnosticada con ELISA positivo y confirmado por Western Blot provenientes de cinco hospitales generales de Lima y Callao, captados entre enero de 1998 a diciembre de 2001 por el Programa de Control de Tuberculosis (PCT) del Perú (Figura 1).
Los laboratorios intermedios y regionales de Lima realizaron el cultivo para M. tuberculosis de todos los pacientes incluidos en el PCT, las muestras fueron tratadas con solución acuosa estéril de hidróxido de sodio al 4% por 20 minutos, inoculando luego 0,1 mL de muestra en dos tubos con medio de Ogawa, procediendo finalmente a incubar a 37 °C durante tres a cuatro semanas.
Los cultivos positivos fueron enviados al Laboratorio de Referencia Nacional de Micobacterias (Centro Nacional de Salud Pública, Instituto Nacional de Salud), donde se realizó la prueba de sensibilidad para drogas antituberculosas de primera línea. Se realizó el método de las proporciones de Canetti, Rist y Grosset para isoniacida (H), rifampicina (R), estreptomicina (S) y etambutol (E), se usaron en concentraciones de 0,2 μg/mL (H), 40,0 μg/mL (R), 4,0 μg/mL (S) y 2,0 μg/mL (E), y los criterios de resistencia para las cuatro drogas mencionadas fue 1%10.
La prueba de sensibilidad para pirazinamida (Z) se realizó por el método de Wayne, incorporando 100 mg (100 μg/mL) de la droga, 6,5g medio base Dubos, para 1 L de medio11. Se consideró multidrogoresistencia (MDR) cuando presentaba resistencia en forma simultánea a isoniacida, rifampicina y pirazinamida.La información fue ingresada a la base de datos creada en el software PHLIS (Public Health Laboratory Information System) usado por el Sistema de Información de la Red Nacional de Laboratorios en Salud Pública. Los resultados fueron expresados en frecuencias absolutas y relativas. Mediante análisis bivariado a través de pruebas no paramétricas (Chi-cuadrado, test de Fisher, Kruskal Wallis, según correspondía) se evaluó la existencia de asociación entre los perfiles de resistencia encontrados y las variables registradas, considerándose un p < 0,05 como significativo. En el procesamiento y análisis de los datos se utilizó el paquete estadístico STATA 7,0 para Windows.
RESULTADOS
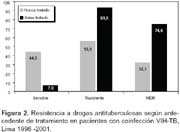
Se incluyeron 523 muestras clínicas, 87% correspondieron a muestras de esputo y 13% fueron muestras extrapulmonares (orina, heces, secreción ganglionar, biopsia ganglionar, líquido pleural, absceso subcutáneo, aspirado gástrico y líquido cefalorraquídeo). La edad promedio de los pacientes fue 31,75 ±8,99 años (rango: 1-75 años), 409 (78,2%) fueron varones; 380 (72,7%) cultivos correspondieron a pacientes sin antecedente de tratamiento antituberculoso previo (nunca tratados o NT) y 143 (27,3%) a pacientes antes tratados (AT).La resistencia a una o más drogas en el grupo de pacientes NT y AT fue 55,8% (52,6% - 60,2%) y 93,0% (88,6% - 97,3%), respectivamente; en tanto que la multidrogorresistencia (MDR) para estos grupos de pacientes fue 32,1% (25,0% - 41,6%) y 74,8% (70,3% - 81,5%), respectivamente (p<0,001) (Tabla 1, Figura 2).
Los valores de resistencia por droga individual se muestran en las tablas 2 y 3. En el caso de los pacientes nunca tratados (Tabla 3), el mayor valor de resistencia primaria a drogas individuales correspondió a H (42,1%) y el menor a E (19%). No se encontró diferencias significativas entre los valores de resistencia individual al comparar los diferentes años evaluados.
Asimismo, en el caso de los pacientes antes tratados (Tabla 4), el mayor valor de resistencia adquirida a drogas individuales correspondió a H (85,3%) y el menor a E (42,0%). Resalta que a lo largo de los años se identificó un aumento significativo de los valores de resistencia por drogas individuales, tanto para H (77,3% en 1998 a 92,6% en 2001) como para R (de 77,3% a 81,5%).
Finalmente, en la tabla 4 se muestran los diferentes perfiles de resistencia encontrados, destacando una mayor frecuencia de resistencia a una sola droga en los casos NT (16,1%), en tanto que conforme aumentó el número de drogas resistentes, estas combinaciones fueron más frecuentes en los AT (19,6% para dos drogas, 16,1% para tres drogas, 31,5% para cuatro drogas y 18,9% para cinco drogas)(p<0,05).
DISCUSIÓN
Nuestro estudio muestra los niveles de resistencia de las drogas antituberculosas de primera línea en un grupo particular de pacientes (VIH-TB). Si bien no se realizó un muestreo representativo del departamento de Lima, creemos que los casos incluidos en este estudio son un buen indicador de los índices de resistencia a las drogas antituberculosas de los casos VIH-TB de Lima y Callao, pues los datos se recogieron de sus principales hospitales, los cuales concentran el manejo de los pacientes con esta coinfección; además es de tener en cuenta que en esta región del país se notifica 58% de los casos7.
En el caso del grupo de pacientes nunca tratados, la resistencia primaria global fue 55,8% y la MDR 32,1%, siendo estos valores superiores a los informados en los diferentes estudios nacionales de vigilancia de resistencia a drogas antituberculosas (1995-968: 15,3% y 2,5% de resistencia primaria y MDR, respectivamente; y 19999: 17,8% y 3,0% de resistencia primaria y MDR, respectivamente), y al reportado por Vásquez12 para Lima y Callao en 1999(17,6% y 3,7% de resistencia primaria y MDR, respectivamente).
Asimismo, en el caso del grupo de pacientes antes tratados, la resistencia a una o más drogas fue 93,0% y la MDR 74,8%, cifras también muy superiores a los valores informados a nivel nacional en 1995-968 con 36,0% y 15,7% de resistencia adquirida y MDR, respectivamente; en 19999 con 23,5% de resistencia adquirida y 12,3% de MDR y para Lima y Callao en 1999 (22,4% y 15,9% de resistencia primaria y MDR, respectivamente).
En otro estudio realizado en Lima, se encontró una prevalencia de 43%(35/81) de MDR en pacientes con HIV13, muy similar al hallado en el presente estudio 43,8% (229/523); así mismo, encontramos que la resistencia a drogas es mayor en los pacientes previamente tratados (93%) con HIV que en la población general (57,4%)14, como se ha demostrado en otros países15; por lo que el VIH se estaría comportando en nuestro medio como un factor asociado de resistencia16.
La prevalencia de MDR en pacientes con HIV reportados en otros países como en Italia 2,6% en casos nuevos y 12,5% en antes tratados17, y en India 3,4% (NT) y 13,5%(AT)18, son menores a los que mostramos en el estudio, esto puede ser debido al alto riesgo de contagio de cepas resistentes en los pacientes en estadio SIDA19, situación frecuente en nuestros pacientes antes de la implementación del tratamiento antirretroviral20; así como a un tratamiento inadecuado posiblemente asociado con la falta de adherencia.
Dado los altos niveles de resistencia y de MDR encontrado en este grupo de pacientes, podemos presumir que este grupo podrían tener factores asociados, como probables fuentes comunes de infección, siendo necesarios nuevos estudios en que se comparen con población no infectada con HIV, así como en grupos no hospitalarios y en pacientes con TB en los que se busque activamente HIV21; asimismo es importante realizar estudios moleculares para la diferenciación genética de cepas de M. tuberculosis22.
REFERENCIAS BIBLIOGRÁFICAS
1. Organización Panamericana de la Salud. Asociación de VIH y tuberculosis: Guía técnica. Bol Oficina Sanit Panam 1993; 115(4): 357-69. [ Links ]
2. Corbett EL, Watt CJ, Walker N, Maher D, Williams BG, Raviglione MC, et al. The growing burden of tuberculosis: global trends and interactions with the HIV epidemic. Arch Intern Med 2003; 163(9): 1009-21. [ Links ]
3. OnUSida. La tuberculosis y el SIDA: Punto de vista del ONUSIDA. Ginebra: ONUSIDA; 1997. [ Links ]
4. Aaron L, Saadoun D, Calatroni I, Launay O, Mémain N, Vincent V, et al. Tuberculosis in HIV-infected patients: a comprehensive review. Clin Microbiol Infect 2004; 10(5): 388-98. [ Links ]
5. Bloch AB, Cauthen GM, Honorato IM, Dansbury KG, Kelly GD, Driver CR, et al. Nationwide survey of drug resistant tuberculosis in the United State. JAMA 1994; 271: 665-71. [ Links ]
6. Espinal MA, Laszlo A, Simonsen L, Boulahbal F, Kim SJ, Reniero A, Hoffner S, et al. Global trends in resistance to antituberculosis drugs. N Eng J Med 2001; 344(17): 1294- 303. [ Links ]
7. Perú, Ministerio de Salud. Tuberculosis en el Perú: Informe 2000. Lima: Programa de Control de Tuberculosis / MINSA; 2001. [ Links ]
8. Vásquez L, Asencios L, Quispe N, Diaz S, Carrillo C, Portocarrero J, et al. Vigilancia de la resistencia a los medicamentos antituberculosos en el Perú, 1995-96. Rev Med Exp 1997; 14(1): 5-14. [ Links ]
9. Instituto nacional de Salud. Vigilancia de la resistencia a los medicamentos antituberculosos en el Perú, 1999. Lima: INS; 2000. [ Links ]
10. Organización Panamericana de la Salud. Manual de normas y procedimientos técnicos para la bacteriología de la tuberculosis. Parte III. Sensibilidad del Mycobacterium tuberculosis a las drogas: identificación de Micobacterias. Washington D.C.: OPS/OMS; 1986. Nota Técnica N°28. [ Links ]
11. Wayne LG. Simple pyrazinamidase and urease test for routine identification of mycobacteria. Am Rev Respir Dis 1974; 109(1): 147-51. [ Links ]
12. Vásquez L, Asencios L, Leo E, Quispe N, Lecca L, Llanos F. Trends for drug-resistant Mycobacterium tuberculosis in Lima and Callao, 1995-96 and 1999. Int J Tuberc Lung Dis 2002; 6(10): S201. [ Links ]
13. Campos P, Suarez P, Sanchez J, Zavala D, Arevalo J, Ticona E, et al. Multidrug-resistant Mycobacterium tuberculosis in HIV-infected persons, Peru. Emerging Infect Dis 2003; 9(12): 1571-77. [ Links ]
14. Vasquez-Campos L, Asencios-Solis L, Leo-Hurtado E, Quispe-Torres N, Salazar-Lindo E, Bayona J, et al. Drug resistance trends among previously treated tuberculosis patients in a national registry in Peru, 1994-2001. Int j Tuberc Lung Dis 2004; 8(4): 465-72. [ Links ]
15. Pereira M, Tripathy S, Inamdar V, Ramesh K, Bhavsar M, Date A, et al. Drug resistance pattern of Mycobacterium tuberculosis in seropositive and seronegative HIV-TB patients in Pune, India. Indian J Med Res 2005; 121(4): 235-39. [ Links ]
16. Gordin FM, Nelson ET, Matts JP, Cohn DL, Ernst J, Bernator D, et al. The impact of human immunodeficiency infection on drug-resistant tuberculosis. Am J Respir Crit Care Med 1996; 154(5): 1478-83. [ Links ]
17. Vanacore P, Koehler B, Carbonara S, Zacchini F, Bassetti D, Antonucci G, et al. Drug-resistant tuberculosis in HIV-infected person: Italy 1999-2000. Infection 2004; 32(6): 328-32. [ Links ]
18. Swaminathan S, Paramasivan CN, Ponnuraja C, Iliayas S, Rajasekaran S, Narayanam PR. Anti-tuberculosis drug resistance in patients with HIV and tuberculosis in South India. Int J Tuberc Lung Dis 2005; 9(8): 896-900. [ Links ]
19. Cobo J, Asensio A, Moreno S, Navas E, Pintado V, Oliva J, et al. Risk factors for nosocomial transmission of multidrug-resistant tuberculosis due to Mycobacterium bovis among HIV-infected patients. Int J Tuberc Lung Dis 2001; 5(5): 413-18. [ Links ]
20. López R. Acceso a tratamiento antirretroviral en el Perú. Boletín Regional sobre Derechos Sexuales. Ciudadanía sexual. 2003; 1(1). [ Links ]
21. Nelson L, Talbot E, Mwasekaga M, Ngirubiu P, Mwansa R, Notha M, et al. Antituberculosis drug resistance and anonymous HIV surveillance in tuberculosis patients in Botswana, 2002. Lancet 2005; 366: 488-500. [ Links ]
22. Baptista IM, Oelemann MC, Opromolla DV, Suffys PN. Drug resistance and genotypes of strains of Mycobacterium tuberculosis isolated from human immunodeficiency virusinfected and non-infected tuberculosis patients in Bauru, Sao Paulo, Brazil. Mem Inst Oswaldo Cruz 2002; 97(8): 1147-52. [ Links ]
Correspondencia: Luis Asencios Solis. Laboratorio de Referencia Nacional de Micobacterias, Centro Nacional de Salud Pública, Instituto Nacional de Salud.
Dirección: Jirón Capac Yupanqui 1400, Jesús María, Lima, Perú.
Teléfono: (511) 471-9920 anexo:
Correo electrónico: lasensios@ins.gob.pe3.