Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Medicina Experimental y Salud Publica
versión impresa ISSN 1726-4634
Rev. perú. med. exp. salud publica v.24 n.2 Lima abr./jun. 2007
ARTICULOS ORIGINALES
Evaluación de campo del efecto residual de la deltametrina sobre la mortalidad y knockdown en Triatoma infestans, según tipo de superficie en Arequipa, Perú
Field evaluation of the deltametrin residual effect on mortality and knockdown for triatoma infestans, on three types of substrates in Arequipa, Peru
Miriam Palomino S1a ; Walter León C1a ; Pedro Valencia V1,2b ; Fanny Cárdenas1,3a ; Jenny Ancca J3a
1 Centro Nacional de Salud Pública, Instituto Nacional de Salud. Lima, Perú.
2 Facultad de Medicina, Universidad Nacional Mayor de San Marcos. Lima, Perú.
3 Laboratorio de Referencia Regional Arequipa, Dirección Regional de Salud Arequipa. Arequipa, Perú.
a Biólogo entomóloga
b Médico infectólogo
Estudio financiado por el Instituto Nacional de Salud del Perú
RESUMEN
Objetivos: Determinar el efecto de volteo (knockdown) y mortalidad en la medición de la eficacia residual del insecticida deltametrina 5% SC usado en el control vectorial de la enfermedad de Chagas sobre tres tipos de substratos (sillar, ladrillo y concreto) a dosis de 25 mg/m2. Materiales y métodos: Se aplicó la deltametrina en casas de diferente material en una zona endémica de Arequipa, Perú, luego fueron expuestas por 72 horas entre 87 a 120 ninfas V de Triatoma infestans en las paredes tratadas, posteriormente las ninfas fueron transferidas a recipientes limpios para determinar el knockdown, la mortalidad a 15 días y la recuperación. Este experimento fue realizado a las 24 horas, 30, 60, 90 y 120 días posttratamiento. Resultados: La mortalidad de la deltametrina se fue reduciendo de 95% en las 24 primeras horas a 34% en el cuarto mes posterior a la exposición, independientemente del tipo de substrato, a un ritmo de 14,5% mensual (p<0,001; r2=0,79), el knockdown se mantuvo por encima de 75% al cuarto mes y la recuperación fue aumentando con el tiempo (p<0,001; r2=0,77). Según substrato, se evidencia una persistencia de la mortalidad >50% hasta los 60 días para sillar, y 90 días para el ladrillo y concreto. Conclusiones: Se demostró una baja efectividad de deltametrina 5% SC a cuatro meses después del tratamiento sobre diferentes superficie (sillar, ladrillo y concreto). Es necesario tener en cuenta estos resultados para calcular los tiempos de aplicación de este insecticida en los programas de control vectorial.
Palabras clave: Triatoma infestans; Control vectorial; Insecticidas; Eficacia (fuente: DeCS BIREME).
ABSTRACT
Objectives: To determine knockdown and mortality in the measurement of the residual efficacy of deltamethrin formulated insecticide 5% SC used in Chagas disease vector control on three types of substrates (sillar [white local volcanic rock], brick and concrete) to doses of 25mg/m2. Material and methods: We applied the deltamethrin in house with different construction material in an endemic zone of Arequipa, Peru, 87 to 120 third-stage nymphs V of Triatoma infestans was exposed by 72 hours to the treated surfaces, the nymphs were transferred to clean containers to determine mortality to 15 days, as well as knockdown and recovery. This experiment was carried out at 24 hours, 30, 60, 90 and 120 days post-treatment. Results: The mortality of the deltamethrin was reduced from 95% in the fist 24 hours to 34% in the fourth month after exposure, regardless of the type of substrate, to a monthly rate of 14,5% (p<0,001; r2=0,79), the knockdown was maintained above 75% in the fourth month recovery was increased over time (p<0,001; r2=0,77). According substrate, we found a persistent mortality >50% to 60 days for sillar, and 90 days for the brick and concrete. Conclusions: We showed the low effectiveness of deltamethrin 5% SC to four months after the treatment on different substrates (sillar, brick and concrete). It is necessary to take into account these results to calculate the time of application of this pesticide on vector control programmes.
Key words: Triatoma infestans, Vector control; Insecticides; Efficacy (source: DeCS BIREME).
INTRODUCCIÓN
La enfermedad de Chagas es endémica de las Américas y se extiende desde México hasta la Argentina1, es causada por el Trypanosoma cruzi, parásito transmitido por insectos de la familia Reduviidae2. La zona rural de Latinoamérica tiene características geográficas y socioeconómicas ideales para la presencia y difusión de este parasitismo3. En el Perú, la enfermedad de Chagas presenta dos áreas endémicas principales, la zona Nor – Oriental con Panstrongylus herreri como vector principal y la zona Sur – Occidental con Triatoma infestans como único vector, abarcando los departamentos de Ica, Arequipa, Moquegua, Tacna, Apurímac y Ayacucho4,5.
El Triatoma infestans se caracteriza por su adaptación a la vivienda humana, encontrándose casi exclusivamente en ambientes domiciliarios y peridomiciliariarios de áreas rurales y recientemente urbanos6,7, aunque excepcionalmente se le ha hallado en ambientes silvestres8 y selváticos9.
El T. infestans se encuentra en altas densidades en viviendas que no han sido tratadas con insecticidas, manteniendo tamaños poblacionales similares de año en año, en los que el máximo número de insectos adultos se reconoce al final del verano. Esta especie puede completar dos generaciones por año en Brasil10 y sólo una en la región semiárida de Argentina, debido al frío invernal11.
Debido a las características de la transmisión de la enfermedad de Chagas, la alternativa de lucha contra la endemia esta centrada en el mejoramiento de vivienda, la educación sanitaria y el control de vectores con utilización de insecticidas4. De estas tres últimas, la que ha tenido mayor continuidad y éxito en toda Latinoamérica es el tratamiento de viviendas y sus peridomicilios con insecticidas sintéticos1. En la región de las Américas son diez los países (Argentina, Bolivia, Brasil, Colombia, Guatemala, Honduras, Paraguay, Perú, Uruguay y Venezuela) que han reportado al WHOPES12, el uso de insecticidas para el control vectorial de la enfermedad de Chagas en el periodo comprendido entre los años 2000 a 200213. Los insecticidas más usados son los organofosforados y los piretroides (fenitrotion, alfacipermetrina, betaciflutrina, ciflutrina, cipermetrina, etofenprox y lambdacihalotrina)12.
Las herramientas de control químico más exitosas en el control de triatominos y utilizadas en forma casi exclusiva por las campañas gubernamentales, son los insecticidas piretroides14. Dentro de esta familia de compuestos químicos, los de mayor efectividad y uso son los llamados de tercera generación. Entre los piretroides de este grupo, los que han resultado más exitosos en evaluaciones de laboratorio y campo, y que actualmente están en uso en campañas nacionales de control de vectores de Chagas, son la deltametrina, la lambdacihalotrina y la beta-cipermetrina15.
La deltametrina [(S)-ß-cyano-3-phenoxybenzyl (1R)-cis-3- (2,2-dibromovynil)-2,2-dimetilcyclopropanecarboxylate], es un insecticida sintético piretroide, clasificado como moderadamente peligroso14. Los cianopiretroides son considerados altamente selectivos y tóxicos para los mamíferos, sin embargo, su toxicidad para los insectos es 5000 veces mayor que para los mamíferos (deltametrina). Esta característica permite controlar a las plagas con dosis tan bajas de piretroides, que su aplicación no constituye un riesgo importante para los mamíferos16.
La primera manifestación de la intoxicación con piretroides en el insecto, es la parálisis del tercer par de patas, seguido por temblores y otros efectos de incoordinación al caminar. Los piretroides no producen una muerte rápida, sino que se caracterizan por producir un efecto de volteo o knockdown: el insecto recostado sobre su dorso no puede volver a su posición normal, es una parálisis muy rápida y reversible. Los insectos pueden permanecer volteados varias horas o días (según la dosis y la especie) y luego se recuperan16. La eficacia de los insecticidas es medida con la mortalidad de los individuos sometidos a ensayos con concentraciones formuladas de éstos y la residualidad se define como la persistencia del insecticida (eficacia) en superficies de material de la vivienda en el tiempo. Los factores que limitan la actividad de los insecticidas incluyen las dosis iniciales, la naturaleza de la superficie rociada, así como la edad de los depósitos de insecticidas y las condiciones ambientales como la temperatura y humedad relativa. El tipo de substrato, en lo que se refiere a su porosidad, es de importancia particular. En las superficies porosas como el barro, el depósito de insecticida parece perder actividad más rápidamente que en superficies tales como madera, cerámica y azulejos. En el caso de piretroides, la interrupción química se puede también esperar en superficies altamente alcalinas o expuestas a la luz del sol17.
Para conocer la interacción de insecticida/substrato, es necesario evaluar la eficacia residual de las formulaciones piretroides comerciales usadas actualmente en el control de triatominos. El presente estudio, evalúa la eficacia y residualidad en condiciones de campo del insecticida deltametrina, usado en el control de Triatoma infestans en una zona endémica del sur del Perú, los datos obtenidos contribuirán a un mejor conocimiento de la efectividad de este insecticida sobre los materiales de construcción usados predominantemente en este distrito y en la planificación de futuras actividades de control vectorial.
MATERIALES Y MÉTODOS
TIPO DE ESTUDIO
Estudio experimental longitudinal, realizado en la localidad Ampliación Pampas del Cusco, distrito Hunter, provincia y departamento de Arequipa (Sur del Perú), en el periodo comprendido entre octubre 2003 a febrero de 2004.
ÁREA DE ESTUDIO
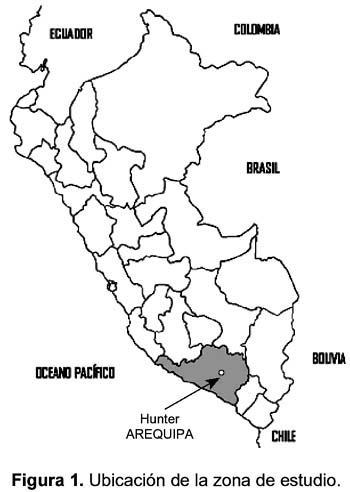
El distrito de Hunter está ubicado al suroeste de la provincia de Arequipa, sobre una explanada intermedia, al pie del cerro Kcaccllinca, con una extensión de 20,37 Km2 (Figura 1). Su topografía es accidentada y heterogénea, está conformado por 53 localidades distribuidas en siete sectores. Cuenta con una población total de 60 489 habitantes, 94,2% es netamente urbana y 5,8% rural. De acuerdo a las líneas de pobreza, el 32% de familias están en extrema pobreza y el 53% en pobreza, 97% de viviendas tiene agua potable, el 98% desagüe y el 99% servicio de energía eléctrica. La población se dedica a la agricultura y a la ganadería.
Las viviendas en Arequipa, están construidas principalmente de sillar (roca volcánica blanca), ladrillo (bloque de adobe horneado), concreto (ladrillo cubierto con cemento) y en menor proporción piedra con barro. El peridomicilio está circunscrito con pircas de piedra y barro, donde crían cuyes y aves de corral.
INSECTICIDA
Se evaluó el insecticida piretroide de principio activo deltametrina [(S)-D-cyano-3-phenoxybenzyl (1R)-cis-3- (2,2-dibromovynil)-2,2-dimetilcyclopropanecarboxylate] de formulación suspensión acuosa en solución concentrada (SC) al 5%.
Para el ensayo se seleccionaron por muestreo aletorio simple del almacén de la Micro Red Javier Llosa García Hunter, 78 envases originales (frascos de 100 mL) de deltametrina SC 5%, los cuales se utilizan en las intervenciones de control vectorial del Centro de Salud Hunter.
Adicionalmente, se realizó la evaluación físico-química del insecticida a utilizar, en el Laboratorio de Química del Centro Nacional de Control de Calidad del Instituto Nacional de Salud (Lima, Perú). La muestra analizada de deltametrina 5% SC, lote N° 1001/03 - 17040, cumple con las especificaciones señaladas por el fabricante (Tabla 1).
SELECCIÓN DE LAS VIVIENDAS Y ROCIAMIENTO
Las viviendas estaban ubicadas en la localidad Ampliación Pampas del Cusco del distrito Hunter y se eligieron teniendo en cuenta 1) la aceptación de los jefes de familia al rociado de las viviendas 2) la autorización a visitas periódica para la realización de los bioensayos y 3) al tipo de material de construcción de la vivienda. Se seleccionaron tres tipos de material de construcción (substrato) representativos de los disponibles en el área: sillar (S), ladrillo (L) y concreto (C).
El personal encargado de la aplicación residual (jefe de brigada y brigadistas) fue provisto con la indumentaria adecuada18 (mamelucos de manga larga, casco con visera, mascarilla con filtro, guantes y botas) para reducir el riesgo de la exposición al piretroide. Adicionalmente se consideraron como medidas de bioseguridad: no comer, beber ni fumar durante el proceso de aplicación y al final de la jornada tomar un baño con abundante agua y jabón y, mudarse de ropa antes del consumo de los alimentos.
Para la aplicación del insecticida en la vivienda se usó el método clásico de fajas verticales para rociar todas las superficies internas con reforzamiento en grietas y fisuras de la pared; además del intradomicilio se roció el peridomicilio19. Se usó 5/15 bombas aspersoras manuales Hudson-X-Pert adaptadas con pico tipo Teejet 8002 que produjeron una descarga entre 790 a 840 mL/ min (media: 808,2 mL/min) a 50 psi.
En octubre de 2003, se roció 16/162 viviendas, cinco de sillar, cinco de ladrillo y seis de concreto, con un depósito aproximado de 25 mg/m2. La solución insecticida se preparó en ocho litros de agua y se usaron 34 cargas (2,13 cargas/vivienda). De las 16 viviendas tratadas químicamente, se seleccionaron al azar tres de cada tipo de substrato para evaluar la efectividad residual a 1, 30, 60, 90 y 120 días postratamiento.
Para evitar la posible agresión de las superficies tratadas, se recomendó a los moradores no limpiar, pintar o pegar objetos en las paredes. Los moradores realizaron sus actividades cotidianas de una forma habitual.
BIOENSAYOS DE PARED CON TRIATOMINOS
Para cada evaluación se obtuvieron los triatominos por búsqueda activa y captura manual en el intra y peridomicilio de viviendas no rociadas del distrito de Hunter. Los triatominos capturados fueron trasladados al Laboratorio de Referencia Regional Arequipa, donde se seleccionaron las ninfas de V estadio, fueron alimentadas con sangre de conejo y mantenidas en el laboratorio hasta cuatro días antes de la aplicación de los bioensayos postratamiento.
Los bioensayos de pared se realizaron 24 horas después del rociamiento, durante las primeras horas de la mañana (06:00 a 10:00 horas) y cuando las superficies internas de las viviendas estuvieron secas. Por cada substrato (S, L y C) se utilizaron cuatro viviendas (tres tratadas químicamente y una sin tratar para el control [B]); en cada vivienda se usaron entre dos a tres placas de vidrio (12 cm de diámetro y 1,5 cm de altura), conteniendo entre 9 a 12 ninfas V de Triatoma infestans (Klug) (Hemiptera: Reduviidae).
En los bioensayos de pared al primer día se usaron 230 (60S, 70L, 70C y 30B) ninfas V, a los 30 días se usaron 285 (90S, 80L, 85C, 30 control), a los 60 días se usaron 244 (84S, 70L, 60C y 30B), a los 90 días se usaron 207 (57S, 60L, 60C y 30B) y a los 120 días se usaron 249 (70S, 69L, 80C y 30B).
Las placas fueron adheridas a las paredes con una cinta engomada a las alturas de 0,5, 1,0 y 1,5 metros sobre el nivel del suelo; estas fueron colocadas en posiciones adyacentes a la superficie ocupada en la evaluación anterior19. El tiempo de exposición fue 72 horas en cada substrato, durante este periodo se cubrieron las placas con una tela negra.
Después del periodo de exposición se transfirieron todos los insectos a recipientes limpios acondicionados con tul a manera de tapa y papel filtro plegado; luego fueron transportados y mantenidos en el laboratorio por 15 días20, en condiciones de temperatura de 19 a 27 °C y humedad relativa de 23 a 69% registrados con termohigrómetros digitales a lo largo de todo el tiempo de evaluación.
El mismo tipo de bioensayo se utilizó para evaluar la efectividad residual cada 30 días, basada en el tiempo que ocasionan los residuos del insecticida a insectos nuevos. Los bioensayos se realizaron a 30 días (noviembre 2003), a 60 días (diciembre 2003), a 90 días (enero 2004) y 120 días (febrero 2004) postratamiento21.
DEFINICIONES
El efecto de volteo (knockdown) se definió como la incapacidad que tiene un insecto de caminar normalmente (aunque puede parecer que esta vivo), su lectura se realizó 72 horas después de la exposición18. Los insectos volteados o moribundos con síntomas de incoordinación fueron mantenidos durante 15 días con el fin de observar la recuperación de las actividades locomotoras del insecto15.
La mortalidad se definió como la incapacidad de un insecto de colgarse sobre un pedazo de papel de filtro inclinado19, ausencia de actividad locomotora propia sobre un papel de filtro o espontáneamente cuando es estimulado, su lectura se realizó a los 15 días después de la exposición (período de recuperación)20.
Se consideraron como insectos recuperados del efecto de volteo, a todos aquellos que fueron catalogados como knockdown a las 72 horas después de la exposición y en la observación posterior durante 15 días no fueron catalogados como muertos22.
Los resultados de los bioensayos de pared se expresaron como el porcentaje de knockdown o de mortalidad (número de ninfas con el efecto x 100 / total de ninfas expuestas) para cada una de las evaluaciones posteriores a la aplicación de la deltametrina.
ANÁLISIS DE DATOS
Los datos fueron ingresados a una base de datos y procesados con el paquete estadístico Stata 9,0 y Epidat 3,1. Se calculó la variación del efecto de la deltametrina sobre la mortalidad, knockdown y recuperación en relación al tiempo (en meses) ajustado por el tipo de substrato usando la regresión lineal múltiple. Para evaluar las diferencias de los efectos de la deltametrina según cada sustrato en determinado tiempo posterior a la aplicación del insecticida, se comparó los porcentajes en tablas de contingencia usando la prueba exacta de Fisher o Chi2 con corrección de Yates según corresponda. Se consideró un p<0,05 como significativo.
RESULTADOS
EFECTO RESIDUAL DE LA DELTAMETRINA: MORTALIDAD, KNOCKDOWN Y RECUPERACIÓN
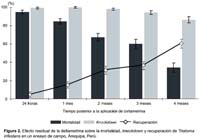
Evaluando en forma global (independientemente del substrato), la deltametrina es muy eficaz para matar a los Triatoma infestans en las primeras horas de aplicación (Figura 2); sin embargo su efecto disminuye progresivamente de 95% en las 24 horas a 34% en el cuarto mes posterior a la exposición; sólo pudo eliminar más del 50% de triatominos hasta el tercer mes. La mortalidad fue disminuyendo desde la aplicación de la deltametrina en 14,5% mensual (IC95% ß: 10,3-18,8; p<0,001; r2 ajustado: 0,79).
Para el caso de knockdown, se mantiene entre 100 y 98% hasta el segundo mes de aplicación, donde se va reduciendo a un ritmo mensual de 6,5% desde el segundo mes (p>0,05; r2 ajustado: 0,1) para luego caer hasta 86% al cuarto mes. El grupo que se recuperó del knockdown varió de 4% a las 24 horas a 60% en el cuarto mes posterior a la exposición, aumentando 13,3% mensual (IC95% ß: 9,2-17,4; p<0,001; r2 ajustado: 0,77).
DIFERENCIAS SEGÚN SUBSTRATO
En el grupo control no se observó mortalidad, ni efecto de volteo, por lo que no se pudo evaluar la recuperación. No hubo diferencias en la acción de la deltametrina sobre la mortalidad, knockdown y recuperación hasta el primer mes después de la aplicación en los tres substratos.
Hasta el tercer mes posterior a la aplicación del insecticida el knockdown de los triatominos expuestos en superficies de sillar y ladrillo fue del 100% (Tabla 2). En el cuarto mes, se observa una menor proporción de afectados en superficie de concreto, en relación con los expuestos en superficie de sillar (75 vs 88%; p>0,05) y ladrillo (75 vs 97%; p<0,01).
En la comparación de la mortalidad de triatominos a 1, 30, 60, 90 y 120 días postratamiento, se observa pérdida de la eficacia y residualidad en todos los substratos. En la primera evaluación la efectividad de deltametrina en todos los substratos fue alta (>91%). En la evaluación residual se observa una menor persistencia en sillar en relación con ladrillo y concreto. La persistencia de deltametrina hasta los 90 días postratamiento, sobre los substratos ladrillo y cemento es >50% y en el substrato sillar, lo es solo hasta los 60 días postratamiento. A los 120 días la persistencia del insecticida sobre ladrillo y concreto es <50% (Tabla 3).
A partir del segundo mes se observó una mayor recuperación en los triatominos con knockdown expuestos en superficie de sillar, en el cuarto mes se observa que prácticamente uno de cada dos insectos volteados se recuperan (Tabla 4). No se encontró diferencias según la altura en que fueron colocadas las placas (0,5; 1 y 1,5 metros).
DISCUSIÓN
Los resultados encontrados en esta evaluación de campo, reafirman la necesidad de una observación por largo tiempo cuando se quiere evaluar la mortalidad, particularmente con insecticidas piretroides, ya que es frecuente confundir el knockdown con la mortalidad16, estos hallazgos son concordantes con lo que encontraron Casabé et al. quienes observaron recuperación del insecto después de 15 días de intoxicación con deltametrina22.
El knockdown es una parte importante de la acción de los insecticidas piretroides, es rápido en el inicio, a veces muy duradero, y asociado no necesariamente a la acción mortal23. Clements y May, sugirieron que el efecto de volteo de los piretroides resulta de un tipo particular de acción fisiológica, y la capacidad de inducir la acción es dependiente de la estructura molecular. Estos autores demostraron que ß-cyano realiza la actividad del efecto de volteo de los piretroides24. Burt y Goodchild, determinaron que el sistema nervioso central es el sitio de acción de los piretroides para inducir la incoordinación en los insectos expuestos25.
El volteo ocurre pocos minutos después de la aplicación de los insecticidas; sin embargo no esta claro si el volteo y la muerte o las diferentes manifestaciones tienen el mismo mecanismo subyacente16. Briggs et al. concluyeron que la incoordinación rápida debe implicar la penetración rápida y eficiente al sistema nervioso central. Esto fue puesto en contraste con la mortalidad, que puede ocurrir dos días o más después de la aplicación26. Los eventos de incoordinación y recuperación presentan una cinética muy diversa en T. infestans, entre los síntomas de incoordinación se enumeran, 1) leves temblores; (2) dislocación posterior o lateral; (3) contracción de los tres pares de patas; (4) elevación sobre el plano del cuerpo; (5) parálisis del tercer par de patas; (6) movimientos convulsivos violentos; (7) parálisis de los tres pares de patas; (8) movimientos lentos u ocasionales; (9) carencia de movimientos16.
Los resultados obtenidos, son similares a los hallados por Arias et al., quienes demostraron que deltametrina 2,5% SC, registró la mortalidad mas alta durante los primeros 30 días postratamiento. Los rangos más altos de mortalidad (sobre el 50%) fueron observadas en bloques de madera hasta tres meses posrociado20.
La capacitación al personal que realizó el rociado de las superficies, permitió obtener una uniformidad en el rociado por lo cual no se encontraron diferencias en las acciones de la deltametrina según altura.
Los datos de los análisis determinan la baja efectividad (mortalidad <50%) de deltametrina 5% SC después de los 90 días de la aplicación residual sobre los substratos de sillar, ladrillo y concreto; evidenciándose que durante los primeros 30 días la formulación suspensión concentrada fue efectiva, pero a más largo plazo mostró bajos niveles de persistencia debido probablemente a la absorción excesiva del insecticida en estructuras porosas (sillar, concreto y ladrillo), que pueden ocasionar la retención inadecuada del insecticida por periodos largos, lo que facilitaría su degradación20. Sin embargo, el buen funcionamiento de los piretroides no depende enteramente del efecto residual del insecticida que esta relacionado a la cantidad de insecticida restante en la superficie tratada. La eficacia de los piretroides en su impacto inicial es más relevante que el efecto residual que disminuye puntualmente en todos los tipos de superficies20.
Los resultados obtenidos, nos dan evidencias para ser tomadas en cuenta en las actividades de control de triatominos; siendo muy importante conocer la eficacia y residualidad de una determinada formulación de insecticida sobre un substrato, pues depende de la interacción, de las condiciones medioambientales y factores externos que influyen en la efectividad de un plaguicida.
AGRADECIMIENTOS
A Maritza Pinto, Cecilia Motta y Elizabeth Laime, por el apoyo en la captura y mantenimiento de triatominos; a los brigadistas y jefes de brigada por el rociamiento de las viviendas; asimismo a la Dirección Regional de Salud Arequipa, al Laboratorio de Referencia Regional Arequipa y al Centro de Salud de Hunter Javier Llosa García por las facilidades brindadas para la ejecución del estudio. A Máximo Vergaray y Norma García por el apoyo en el control de calidad de la deltametrina. Al Dr. César Náquira por la revisión y sugerencias al manuscrito.
REFERENCIAS BIBLIOGRÁFICAS
1. Dias JC, Silveira AC, Schofield CJ. The impact of Chagas disease control in Latin America: a review. Mem Inst Oswaldo Cruz. 2002; 97(5): 603-12. [ Links ]
2. Zeledon R, Rabinovich JE. Chagas disease: an ecological appraisal with special emphasis on its insect vectors. Ann Rev Entomol. 1981; 26: 101-33. [ Links ]
3. Zerba EN. Evolución del control químico de los insectos vectores de la Enfermedad de Chagas. Ann Soc Cient Arg. 1997; 227: 35-39. [ Links ]
4. Perú, Ministerio de Salud. Doctrina, normas y procedimientos para el control de la Tripanosomiasis o enfermedad de Chagas en el Perú. Lima: MINSA; 1998. p. 7-8. [ Links ]
5. Chávez J. Contribución al estudio de los triatominos del Perú: distribución geográfica, nomenclatura y notas taxonómicas. An Fac Med. 2006; 67(1): 65-76. [ Links ]
6. Rabinovich JE. Vital statistics of Triatominae (Hemiptera: Reduviidae) under laboratory conditions. I. Triatoma infestans Klug. J Med Entomol. 1972; 9(4): 331-70. [ Links ]
7. Levy MZ, Bowman NM, Hawai V, Waller LA, Cornejo del Carpio JG, Cordova Benzaquen E, et al. Periurban Trypanosoma cruzi-infected Triatoma infestans, Arequipa, Peru. Emerg Infect Dis. 2006; 12(9): 1345-52. [ Links ]
8. Lent H, Wygodzinsky P. Revision of the Triatominae (Hemiptera, Reduviidae), and their significance as vectors of Chagas disease. Bull Am Mus Nat Hist. 1979; 163: 124- 520. [ Links ]
9. Noireau F, Bastrenta B, Catala S, Dujardin JP, Panzera F, Torres M, et al. Sylvatic population of Triatoma infestans from the Bolivian Chaco: from field collection to characterization. Mem Inst Oswaldo Cruz. 2000; 9(Suppl 1): 119-22. [ Links ]
10. Schofield CJ. Density regulation of domestic populations of Triatoma infestans in Brazil. Trans R Soc Trop Med Hyg. 1980; 74(6): 761-69. [ Links ]
11. Gorla DE, Schofield CJ. Analysis of egg mortality in experimental populations of Triatoma infestans under natural climatic conditions in Argentina. Bull Soc Vector Ecol. 1985; 10(2): 107-17. [ Links ]
12. Organización Panamericana de la Salud. Relevamiento de insecticidas empleados por los Programas Nacionales de Control de la enfermedad de Chagas del Cono Sur de América. 2ª edición. Washington: OPS; 2002. OPS/HCP/ HCT/231/03. [ Links ]
13. Picollo MI. Avances en el monitoreo de resistencia a insecticidas en triatominos y necesidades futuras. En: Monitoreo de la resistencia a insecticidas en triatominos en América Latina. Buenos Aires: Fundación Mundo Sano; 2001. p. 13-21. [ Links ]
14. World Health Organization. The WHO recommended classification of pesticides by hazard and guidelines to classification 2000–2002. Geneva: WHO; 2001. WHO/ PCS/01.5. [ Links ]
15. World Health Organization. Control of Chagas diseases. Report of a WHO Expert Committee. Geneva: WHO; 1991. Technical Report Series 811. [ Links ]
16. Alzogaray RA, Zerba EN. Incoordination, paralysis and recovery after pyrethroid treatment on nymphs III of Triatoma infestans (Hemiptera: Reduviidae). Mem Inst Oswaldo Cruz. 1997; 92(3): 431-35. [ Links ]
17. Leahey JP. The pyrethroid insecticides. London: Taylor & Francis; 1985. [ Links ]
18. Ramsey J, Arias J, Frederickson C, Salvatella R. Manual para el rociado residual intradomiciliario: aplicación del rociado residual para el control de vectores. Washington: Organización Panamericana de la Salud; 2002. WHO/CDS/ WHOPES/GCDPP. [ Links ]
19. Schofield CJ. Field testing and evaluation of insecticides for indoor residual spraying against domestic vector of Chagas disease. Geneva: World Health Organization; 2001. WHO/CDS/WHOPES/GCDPP/2001.1. [ Links ]
20. De Arias AR, Lehane MJ, Schofield CJ, Fournet A. Comparative evaluation of pyrethroid insecticide formulations against Triatoma infestans (Klug): residual efficacy on four substrates. Mem Inst Oswaldo Cruz. 2003; 98(7): 975-80. [ Links ]
21. World Health Organization. Protocolo de evaluación de efecto insecticida sobre triatominos. WHO/UNDP/WB/TDR. Acta Toxic Argent. 1994; 2(1-2): 29-31. [ Links ]
22. Casabé N, Melgar F, Wood EJ, Zerba EN. Insecticidal activity of pyrethroids against Triatoma infestans. Insect Sci Applic. 1988; 9(2): 233-36. [ Links ]
23. Naumann K. Synthetic pyrethroid insecticides: structures and properties. Berlin: Springer-Verlag; 1990. [ Links ]
24. Clements AN, May TE. The actions of pyrethroids upon the peripheral nervous system and associated organs in the locust. Pestic Sci. 1977, 8(6): 661-80. [ Links ]
25. Burt PE, Goodchild RE. Knockdown by pyrethroids: its role in the intoxication process. Pestic Sci. 1974; 5(5): 625- 33. [ Links ]
26. Briggs GG, Elliot M, Farnham AW, Janes NF, Needham PH, Pulman DA, et al. Insecticidal activity of the pyrethrins and related compounds. VIII. Relation of polarity with activity in pyrethroids. Pestic Sci. 1976; 7(3): 236-40. [ Links ]
Correspondencia:
Blga. Miriam Palomino Salcedo
Laboratorio de Entomología, Centro Nacional de Salud Pública, Instituto Nacional de Salud. Lima, Perú.
Dirección: Cápac Yupanqui 1400, Lima 11.
Teléfono: (511) 471-9920
Correo electrónico: mpalomino@ins.gob.pe