Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Peruana de Medicina Experimental y Salud Publica
Print version ISSN 1726-4634
Rev. perú. med. exp. salud publica vol.24 no.3 Lima July/set 2007
ARTÍCULO ORIGINAL
Incidencia y factores asociados con las reacciones adversas del tratamiento antirretroviral inicial en pacientes con VIH
Incidence and associated factors to adverse reactions of the initial antiretroviral treatment in patients with HIV
Juan Astuvilca1,2a ; Yanet Arce-Villavicencio1,2a ; Raúl Sotelo1,2a ; José Quispe1,2a ; Regina Guillén1a ; Lillian Peralta1a ; Jorge Huaringa1a ; César Gutiérrez3b
1 Facultad de Medicina, Universidad Nacional Mayor de San Marcos. Lima, Perú.
2 Sociedad Científica de San Fernando. Lima, Perú.
3 Departamento Académico de Medicina Preventiva y Salud Pública, Facultad de Medicina, Universidad Nacional Mayor de San Marcos. Lima-Perú.
ª Estudiantes de medicina
b Médico epidemiólogo
RESUMEN
La alta incidencia de reacciones adversas medicamentosas (RAMA) al tratamiento antirretroviral de gran actividad (TARGA) en pacientes con VIH/SIDA puede afectar la calidad de vida y adherencia al tratamiento. Objetivos: Determinar la incidencia de RAMA del TARGA inicial e identificar los factores asociados con la ocurrencia de RAMA al recibir dicha terapia. Materiales y métodos: Se realizó un estudio de cohorte histórica con todos los pacientes VIH (+) mayores de 18 años que recibieron TARGA por primera vez en el Hospital Nacional Arzobispo Loayza, con un seguimiento de 360 días desde la primera prescripción. Se recabó las RAMA de las historias clínicas y tarjetas de control. Resultados: Se incluyeron 353 pacientes, se encontró una incidencia acumulada de 66,7% de efectos adversos al TARGA inicial y una densidad de incidencia de 9,1 eventos de RAMA por 10 personas año de seguimiento (IC95%: 8,1-10,1). Anemia (23,4%), náuseas (20,6%) y rash (17,2%) fueron las RAMA más frecuentes. El uso de drogas (OR 2,40; IC95% 1,01-5,67); consumo de alcohol (OR 0.32; IC95%: 0,19-0,55) y estadio SIDA (OR 0,20; IC95%: 0,04-0,95) estuvieron asociadas con la presencia de RAMA. Conclusiones: Existe un alta incidencia de RAMA, siendo la anemia la más frecuente. El uso de drogas es un factor de riesgo para presentar RAMA.
Palabras clave: VIH/SIDA; Terapia de alta actividad antirretroviral/ efectos adversos; Sistemas de registro de reacción adversa a medicamentos; Incidencia (fuente: DeCS BIREME).
ABSTRACT
The high incidence of adverse reactions to the high activity antiretroviral treatment (HAART) in patients with HIV/AIDS, can affect their quality of life and adherence to the treatment. Objectives: To determinate the incidence of adverse reactions to the initial HAART and to identify the factors associated to the occurrence of adverse reactions when receiving this therapy. Material and methods: Historic cohort study. The population was conformed by all the HIV-infected adult patients (≥18 years old) receiving HAART for the first time in Arzobispo Loayza National Hospital. 353 clinic histories were reviewed and their respective control cards. The following for 360 days alter the first prescription was realized. Results: It was found an accumulated incidence of 66,7% adverse reactions to initial HAART and an incidence density of 9,1 events of adverse reactions for 10 persons-year of follow-up (95%CI: 8,1-10,1); being anemia (23,4%), nausea (20,6%) and rash (17,2%) the most frequent adverse reactions. It was found significant associations with the following factors: drug use (OR 2,40; 95%CI: 1,01-5,67); alcohol consume (OR 0,32; 95%CI: 0,19-0,55) and AIDS stadium (OR 0,20; 95%CI: 0,04-0,95). Conclusions: There is a high incidence of adverse reactions to initial HAART, being anemia the most frequent. The drug consume is a risk factor to present adverse reactions.
Key words: HIV/AIDS; Highly active antiretroviral therapy; Adverse drug reaction reporting system; Incidence (source: DeCS BIREME).
INTRODUCCIÓN
Desde el año 2004, el Ministerio de Salud del Perú brinda un acceso universal al tratamiento antirretroviral de gran actividad (TARGA). Desde entonces se observa un cambio perceptible en el patrón de morbilidad y mortalidad de los pacientes con infección por el virus de la inmunodeficiencia humana (VIH) y síndrome de inmunodeficiencia adquirida (SIDA), con una notable disminución del riesgo de padecer infecciones oportunistas y un aumento de la calidad de vida. Sin embargo, tales ventajas, sólo pueden ser posibles con un alto nivel de adherencia1.
Diversos estudios confirman que las reacciones adversas a los medicamentos antirretrovirales (RAMA) forman parte de los factores que contribuyen a la descontinuación del tratamiento y a la no adherencia2-4. Los pacientes reconocen y atribuyen a los antirretrovirales como los causantes de sus molestias, de tal modo que interfieren con sus actividades diarias y conducen a la interrupción del tratamiento.
El TARGA plantea problemas tanto a corto como a largo plazo. Se sabe que la incidencia de las RAMA es alta en el momento inicial de la terapia, y que la principal causa de suspensión al inicio del tratamiento es la toxicidad, sobre todo la gastrointestinal5,6. Los efectos a largo plazo son en cambio, de tipo sistémicos y metabólicos, como lipodistrofia, parestesias, insuficiencia renal, osteoporosis, etc7,8.
Los factores que se asocian positivamente a las RAMA incluyen el sexo femenino, el uso de ritonavir comparado a otro inhibidor de la proteasa, el aumento progresivo de la edad, comorbilidades, bajo conteo de linfocitos y carga viral más alta al iniciar la terapia5,9-13 .
Los pacientes que reciben el TARGA son sometidos a una evaluación clínica, virológica e inmunológica en forma periódica; estos son parámetros imprescindibles para el monitoreo de la eficacia, adherencia y efectos adversos del TARGA. Es este continuo seguimiento y registro, lo que permite estudiar de forma idónea la ocurrencia de las RAMA y los factores que influyen en ellas14.
En el Perú, a pesar de existir una política nacional de acceso universal al TARGA, hay pocos estudios al respecto. La determinación de la incidencia de RAMA, nos daría a conocer la magnitud del problema, y la identificación de sus factores asociados, permitiría una mejor elección de la terapia inicial, que se adapte cada vez más a las características del paciente, contribuyendo a una mejor adherencia al tratamiento.
Por ello, se decidió desarrollar la presente investigación con el objetivo de determinar la incidencia de RAMA del TARGA inicial en pacientes VIH/SIDA, así como identificar los factores asociados a la ocurrencia de RAMA al recibir este tipo de tratamiento.
MATERIALES Y MÉTODOS
TIPO DE ESTUDIO
Se realizó un estudio analítico observacional, cuyo diseño fue de una cohorte histórica.
MUESTRA Y RECOLECCIÓN DE DATOS
La muestra estuvo conformada por todos los pacientes del Hospital Nacional Arzobispo Loayza de Lima, Perú, VIH positivos, mayores de 18 años que recibieron TARGA por primera vez (498 pacientes) en el periodo abril 2004 – abril 2006. Fueron excluidos las gestantes y los pacientes que durante el seguimiento, antes de completar el año, se retiraron del tratamiento, fallecieron o se derivaron a otros hospitales.
Para la recolección de datos se revisaron las historias clínicas, las tarjetas de control de cada paciente y los registros de reacciones adversas. La tarjeta de control es una ficha estandarizada, diseñada por la estrategia de control del VIH y otras ITS del Ministerio de Salud, donde el personal de salud que evalúa a los pacientes VIH/SIDA que reciben TARGA debe registrar todas las ocurrencias del paciente en cada consulta de control. Los registros de RAMA, elaborados por la Dirección General de Medicamentos, Insumos y Drogas (DIGEMID)1, es llenado sólo por el médico tratante cuando éste considere que las molestias del paciente son atribuibles a los antirretrovirales.
Se hizo un seguimiento de 360 días a partir del primer día de prescripción. Se obtuvo información sobre reacciones adversas reportadas y otras variables clínicas y sociodemográficas.
VARIABLES DE ESTUDIO Y SEGUIMIENTO
La reacción adversa medicamentosa a antirretrovirales (RAMA) inicial fue definida como el efecto o síntoma indeseable que coloca en la historia clínica, tarjeta de control o registro de RAMA, el médico responsable del paciente y que ocurrieron hasta 360 días después de la primera prescripción de TARGA.
Se tomaron en cuenta para el análisis, todas las reacciones adversas encontradas durante el seguimiento. Se usó una lista estandarizada para describir los efectos gastrointestinales (diarrea, náuseas, vómitos), dermatológicos (rash), neurológicos (insomnios, parestesias) y otras reacciones adversas. La gravedad de las RAMA fue determinada en base al requerimiento de hospitalización, al cambio en el régimen o al ajuste de las dosis terapéuticas.
Adicionalmente, se consideraron variables sociodemográficas (edad, sexo, procedencia), conductuales (consumo de alcohol, consumo de drogas ilícitas y tabaquismo actual) y clínicas (estadio clínico inicial, conteo de linfocitos T-CD4+, carga viral al iniciar la terapia, comorbilidades y hospitalizaciones durante el tratamiento).
ASPECTOS ÉTICOS
EL protocolo fue revisado y aprobado por el Comité de Ética e Investigación del Hospital Nacional Arzobispo Loayza (HNAL). Se obtuvo la autorización del HNAL para recabar la información de las historias clínicas, se garantizó la protección de la confidencialidad de los datos utilizados.
ANÁLISIS ESTADÍSTICO
El análisis descriptivo fue realizado para caracterizar el número y el tipo de las RAMA. Se estimó la incidencia acumulada y la densidad de incidencia (número de RAMA presentadas en un paciente que ingresa por primera vez al TARGA, durante un año de seguimiento) general y por esquemas de TARGA. El cálculo de la densidad de incidencia, tuvo como numerador a la cantidad total de RAMA registradas y como denominador a la sumatoria de tiempo contribuido por cada paciente en el intervalo entre la fecha de inicio de TARGA y los registros de todos las RAMA presentadas.
En el análisis bivariado se estimó la fuerza de asociación mediante el riesgo relativo, calculando intervalos de confianza del 95%. Se realizó luego un análisis multivariado de regresión logística, con el que se estimó los OR ajustados. Todos los datos fueron almacenados en una base de datos (Microsoft Excel 2003) y después analizados en el programa estadístico SPSS v.12.0 para Windows y Epidat v.3.1.
RESULTADOS
CARACTERÍSTICAS DE LA POBLACIÓN ESTUDIADA
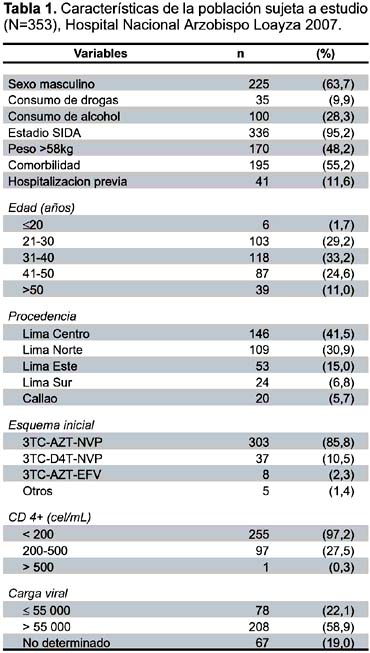
El estudio incluyó la totalidad de pacientes VIH (+) que reciben TARGA del Hospital Nacional Arzobispo Loayza, de los cuales sólo 353 cumplieron los criterios de inclusión para iniciar el seguimiento. El 63,7% de la cohorte estudiada, fueron hombres y el grupo etario más prevalente al iniciar el seguimiento fue el de 31 a 40 años (33,2%). La mayoría procedía de Lima Centro (41,5%), los otros participantes provinieron del Callao y de los conos de Lima.
Respecto a sus características clínicas, casi la totalidad (95,2%) de pacientes ingresan al TARGA presentando estadio SIDA. En 72,2% de pacientes, se inició el seguimiento con un conteo de CD4+ menor de 200 células/mL, y en 58,9% con una carga viral mayor de 55 000 copias/mL.
En 55,2% de los casos, se presentó alguna comorbilidad durante el TARGA, característica importante en el diagnóstico del síndrome de reconstitución inmune (SRI), caracterizado por infecciones oportunistas, producto de una adaptación del sistema inmune al tratamiento inicial. Al menos uno de cada diez pacientes (11,6%) de la cohorte estudiada presentó por lo menos una hospitalización antes de iniciar el tratamiento (Tabla 1).
INCIDENCIA Y CARACTERÍSTICAS DE LAS RAMA
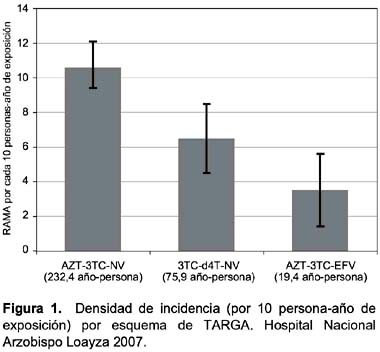
El número de reacciones adversas registradas durante el seguimiento fue 253, arrojando una incidencia acumulada de 66,6 % (IC 95%: 61,4-71,5). La densidad de incidencia hallada para la presentación de una RAMA fue de 9,1 por 10 personas-año de exposición (IC 95%: 8,1 - 10,1). Las densidades de incidencia halladas para cada uno de los esquemas de TARGA se aprecian en la Figura 1.
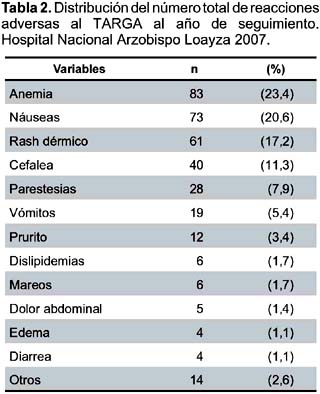
De las reacciones adversas reportadas (Tabla 2), la más frecuente fue anemia (23,4%), seguida de náuseas (20,6%) y rash dérmico (17,2%).
FACTORES ASOCIADOS A LA PRESENTACIÓN DE RAMA
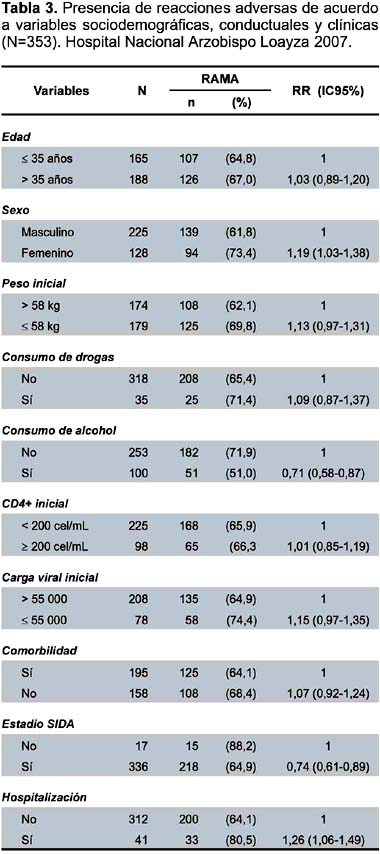
Análisis bivariado: Se pudo comprobar que existe asociación significativa con los siguientes factores: el sexo femenino con un RR de 1,19 (IC95% 1,03-1,38) se comportó como un factor de riesgo leve; mientras que el consumo de alcohol con un RR de 0,71 (IC95% 0,58-0,87) y el estadio SIDA con un RR de 0,74 (IC 95% 0,61-0,89) se comportaron como factores protectores moderados (Tabla 3).
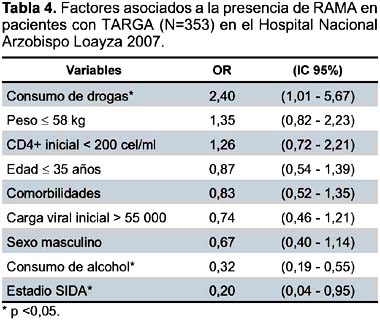
Análisis multivariado. Se incluyeron nueve variables en el modelo, se encontró que el consumo de alcohol y el estadio SIDA disminuyen el riesgo de RAMA independientemente de los otros factores, mientras que el consumo de drogas lo aumenta (Tabla 4).
DISCUSIÓN
Se encontró una alta incidencia acumulada de RAMA (66,7%) en el grupo estudiado, aproximadamente el doble a la observada por otros investigadores5. Una incidencia mayor a la nuestra fue encontrada en un estudio brasileño (88.9%), la cual, según sus propios autores, pudo haberse sobreestimado debido a la dificultad de discriminar dichas reacciones de las propias producto de la enfermedad de fondo5. En relación a la densidad de incidencia general, ésta nos indica una posibilidad de presentar 9,1 RAMA (IC 95%: 8,1-10,1) en diez pacientes al estar en TARGA durante un año de seguimiento, es decir, que se tiene esa posibilidad independientemente de los esquemas que se reciban.
Tras el análisis por esquema de tratamiento, encontramos que para el primer esquema (AZT-3TC-NV) la densidad de incidencia fue mayor en relación a las demás, ya que al ser el esquema inicial de tratamiento en nuestro estudio y el de mayor tiempo de exposición (232,4 añopersona), se producirá durante este tiempo la mayor probabilidad de presentar una RAMA (10,6 RAMA por 10 persona-año de exposición; IC95%: 9,4-12,1).
La mayor parte de las reacciones adversas ocurrieron durante los primeros cuatro meses de tratamiento, siendo éstas de tipo aguda, comunes y no específicas. La mayoría, fueron leves y moderadas, siendo las graves, aquellas que motivaron un cambio de esquema.
De acuerdo con investigaciones anteriores5,9,10, los síntomas gastrointestinales eran las reacciones más frecuentemente registradas, teniendo a las náuseas y vómitos como las reacciones adversas más frecuentes, con una incidencia de 14,5 y 13,1% respectivamente; sin embargo, en nuestro estudio encontramos a la anemia como la reacción adversa más frecuente (23,4%), seguida de náuseas (20,6%), rash dérmico (17,2%), cefalea (11,3%), parestesias (7,9%) y vómitos (5,4%). Cabe precisar, que las definiciones de cada una de las reacciones adversas y su diagnóstico, no se han estandarizado totalmente en la práctica rutinaria en el Perú, a pesar de su alta frecuencia al principio de la terapia, constituyendo ésta una de las limitaciones del estudio.
Es importante resaltar que en el estudio no se registraron reacciones adversas como la lipodistrofia o la enfermedad cardiovascular, porque éstas se suelen presentar a largo plazo, con un tiempo de administración del TARGA mayor a un año, como se han encontrado en otras series18-20.
En cuanto a los factores asociados, a diferencia de otros estudios similares9,10,13, no encontramos asociación de un mayor riesgo de desarrollar RAMA con factores como la edad, linfocitos CD4+ de 200 a 500 células/mL, comorbilidades, pero sí con el consumo de drogas. No se pudo corroborar al sexo femenino como factor de riesgo para la presentación de RAMA al igual que otros estudios5,11.
Existen pocos estudios en relación con la incidencia de RAMA en pacientes con estadio SIDA o sin éste21. En un estudio, se señala que existe mayor probabilidad de eventos adversos graves y amenazantes contra la vida, en pacientes que reciben TARGA y tienen un CD4 <200, y estadio SIDA antes del tratamiento22,23; en nuestro estudio, no se encontró una asociación entre el nivel de CD4 y la incidencia de RAMA, así mismo no se encontró una mayor incidencia de RAMA en relación a la carga viral; sin embargo, se encontró con el análisis multivariado que el estadio SIDA fue un factor protector (OR: 0,20; IC95: 0,04-0,95).
Se sabe que el TARGA tiene el potencial de generar algún grado de toxicidad, característica que está relacionada con la no adherencia al tratamiento24. El abuso de alcohol también ha sido asociado con una pobre adherencia en individuos infectados con HIV25, incluso Samet et al. 26 demuestran que el consumo de alcohol es el factor más fuertemente asociado con una adherencia disminuida. Esto podría explicar el aparente efecto protector que presentó el alcohol en este estudio, ya que es posible que los pacientes con mayor consumo de alcohol, al no cumplir el tratamiento (mayor riesgo de no adherencia25,26) no hayan podido cumplir el año de seguimiento y por tanto, no ser incluidos en el estudio.
En nuestro medio, se utiliza como registro de reacciones adversas, hojas de reporte elaboradas por la Dirección General de Medicamentos, Insumos y Drogas (DIGEMID) del MINSA1, donde no se detallan muchas de las quejas de los pacientes, que por la literatura revisada7,8,16, serían atribuidas a los antirretrovirales, generando así una subestimación de la verdadera incidencia en la población estudiada. Sin embargo, los datos basados sólo en historias clínicas pueden carecer de confiabilidad, ya que los médicos pueden registrar de forma inadecuada los síntomas o efectos nocivos divulgados por los pacientes; es por ello, que en nuestro estudio consultamos las historias clínicas apoyadas de sus exámenes auxiliares, además de las hojas de registro de RAMA del DIGEMID. El instrumento adecuado para el estudio de la ocurrencia de RAMA aún genera confusión, por lo que consideramos que se debería explorar más a fondo en estudios futuros.
Finalmente, debemos recalcar la importancia de la instauración, en los centros dispensadores de TARGA, de protocolos estandarizados para reacciones adversas. Ello, podría ayudar a los profesionales de salud a mejorar el reconocimiento y prevención de estos eventos, con el fin de mejorar la adherencia entre los pacientes que inician terapia con antirretrovirales.
En conclusión, se encontró una alta incidencia de RAMA durante el tratamiento inicial del TARGA (66,6%). Así también se concluye que, por cada diez pacientes que por primera vez se adhieren al TARGA en el Servicio de Infectología del Hospital Nacional Arzobispo Loayza, se tiene la posibilidad de presentación de 9,1 reacciones adversas durante un año de tratamiento. El consumo de alcohol y el estadio SIDA se asocian con una menor incidencia de RAMA; mientras que el consumo de drogas, a una mayor incidencia. La anemia fue la RAMA más frecuente en la población estudiada.
AGRADECIMIENTOS
Al Dr. Carlos Benites Villafane, médico asistente del servicio de infectología del Hospital Nacional Arzobispo Loayza, por el apoyo brindado. De igual forma, agradecemos a nuestros compañeros Miguel Salinas Vergaray, Nataly Aramburú Miranda, Jorge Ávalos Gómez, Juan José Olaya Llerena, William Poma Hullcapuri, Renzo Andrade González y Armando Villanueva Álvarez por su importante aporte en el protocolo de investigación y en la recolección de datos.
REFERENCIAS BIBLIOGRÁFICAS
1. Perú, Ministerio de Salud. Análisis de la situación epidemiológica del VIH/SIDA en el Perú. Lima: Dirección General de Epidemiología, MINSA; 2006. [ Links ]
2. Pinheiro CA, de Carvalho Leite JC, Drachler ML, Silveira VL. Factors associated with adherence to antiretroviral therapy in HIV/AIDS patients: a cross-sectional study in Southern Brazil. Braz J Med Biol Res. 2002; 35(10): 1173-81.
3. da Silveira VL, Drachler ML, Leite JC, Pinheiro CA. Characteristics of HIV antiretroviral regimen and treatment adherence. Braz J Infect Dis. 2003; 7(3): 194-201.
4. Bonolo F, César CC, Acurcio FA, Ceccato MG, de Pádua CA, Alvares J, et al. Non-adherence among patients initiating antiretroviral therapy: a challenge for health professionals in Brazil. AIDS. 2005; 19 (Suppl 4): S5-13.
5. Pádua CA, César CC, Bonolo PF, Acurcio FA, Guimarães MD. High incidence of adverse reactions to initial antiretroviral therapy in Brazil. Braz J Med Biol Res. 2006; 39(4): 495-505.
6. Galindo Puerto MJ, von Wichmann MA, Roca B, Téllez MJ, Blázquez R, Grupo de estudio del SIDA (GeSIDA). La comorbilidad como factor limitante del TARGA. Enferm Infecc Microbiol Clin. 2006; 24(Suppl 2): 1-12.
7. Carr A, Cooper DA. Adverse effects of antiretroviral therapy. Lancet. 2000; 356: 1423-30.
8. Montessori V, Press N, Harris M, Akagi L, Montaner JS. Adverse effects of antiretroviral therapy for HIV infection. CMAJ. 2004; 170(2): 229-38
9. Pádua CA, César CC, Bonolo PF, Acurcio FA, Guimarães MD. Self-reported adverse reactions among patients initiating antiretroviral therapy in Brazil. Braz J Infect Dis. 2007; 11(1): 20-26.
10. Fellay J, Boubaker K, Ledergerber B, Bernasconi E, Furrer H, Battegay M, et al. Prevalence of adverse events associated with potent antiretroviral treatment: Swiss HIV Cohort study. Lancet. 2001; 358: 1322-28.
11. Silverberg MJ, Gore ME, French AL, Gandhi M, Glesby MJ, Kovacs A, et al. Prevalence of clinical symptoms associated with highly active antiretroviral therapy in the Womens Interagency HIV study. Clin Infect Dis. 2005; 40(3): 491-2.
12. Bonfanti P, Ricci E, Landonio S, Valsecchi L, Timillero L, Faggion I, et al. Predictors of protease inhibitor-associated adverse events. Biomed Pharmacother. 2001; 55(6): 321- 23.
13. Lucas GM, Chaisson RE, Moore RD. Highly active antiretroviral therapy in a large urban clinic: risk factors for virologic failure and adverse drug reactions. Ann Intern Med. 1999; 131(2): 81-87.
14. Perú, Ministerio de Salud. Norma Técnica para el TARGA en Adultos infectados por el VIH. Lima: MINSA; 2004. NT Nº 004-MINSA/DGSP-V.02
15. Friis-Møller N, Sabin CA, Weber R, d`Arminiio Monforte A,El-Sadr WM, Reiss P, et al. Combination antiretroviral therapy and the risk of myocardial infarction. N Engl J Med. 2004; 350(9): 955.
16. Mocroft A, Lundgren JD. Starting highly active antiretroviral therapy: why, when and response to HAART. J Antimicrob Chemother. 2004; 54(1): 10-13.
17. d`Arminiio Monforte A, Sabin CA, Phillips A, Sterne J, May M, Justice A, et al. The changing incidence of AIDS events in patients receiving highly active antiretroviral therapy. Arch Intern Med. 2005; 165(4): 416-23.
18. Pujari SN, Dravid A, Naik E, Bhagat S, Tash K, Nadler JP, et al. Lipodystrophy and dyslipidemia among patients taking first-line, World Health Organization-recommended highly active antiretroviral therapy regimens in Western India. J Acquir Immune Defic Syndr. 2005; 39(2): 199-202.
19. Friis-Møller N, Weber R, Reiss P, Thiebaut R, Kirk O, dArminiio Monforte A, et al. Cardiovascular disease risk factors in HIV patients -- association with antiretroviral therapy. Results from the DAD study. AIDS. 2003, 17(8): 1179-93.
20. Martínez E, Mocroft A, García-Viejo MA, Pérez-Cuevas JB, Blanco JL, Mallolas J, et al. Risk of lipodystrophy in HIV-1 infected patients treated with protease inhibitors: a prospective cohort study. Lancet. 2001; 357: 592-98.
21. Carter M. HAART patients at greater risk of severe side effects than AIDS. IAPAC Mon. 2003, 9(12): 314.
22. Geijo Martínez MP, Maciá Martínez MA, Solera Santos J, Barberá Farré JR, Rodríguez Zapata M, Marcos Sánchez F, et al. Ensayo clínico comparativo de eficacia y seguridad de cuatro pautas de tratamiento antirretroviral de alta eficacia (TARGA) en pacientes naive con infección por VIH avanzada. Rev Clin Esp. 2006; 206(2): 67-76.
23. Keiser O, Fellay J, Opravil M, Hirsch HH, Hirschel B, Bernasconi E, et al. Adverse events to antiretrovirals in the Swiss HIV Cohort Study: effect on mortality and treatment modification. Antiv Ther. 2007; 12(8): 1157-64.
24. Heath KV, Singer J, OShaughnessy MV, Montaner JS, Hogg RS. Intentional nonadherence due to adverse symptoms associated with antiretroviral therapy. J Acquir Immune Defic Syndr. 2002; 31(2): 211-17.
25. Cook RL, Sereika SM, Hunt SC, Woodward WC, Erlen JA, Conigliaro J. Problem drinking and medication adherence among persons with HIV infection. J Gen Intern Med. 2001; 16(2): 83-88.
26. Samet JH, Horton NJ, Meli S, Freedberg KA, Palepu A. Alcohol consumption and antiretroviral adherence among HIV-infected persons with alcohol problems. Alcohol Clin Exp Res. 2004; 28(4): 572-77.
Correspondencia:
Juan Astuvilca Cupe.
Sociedad Científica de San Fernando, Universidad Nacional Mayor de San Marcos. Lima, Perú.
Dirección: Jr. Las Lateritas 2020 Urb. Inca Manco Cápac. Lima 36, Perú.
Teléfono: (511) 92031581
Correo electrónico: astuvilcajr1706@hotmail.com














