Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Medicina Experimental y Salud Publica
versión impresa ISSN 1726-4634
Rev. perú. med. exp. salud publica v.24 n.4 Lima oct./dic. 2007
ARTÍCULOS DE REVISIÓN
Hepatitis viral B y Delta en el Perú: epidemiología y bases para su control.
Viral hepatitis B and Delta in Perú: epidemiology and basis for control
César Cabezas1,2,a
1 Instituto Nacional de Salud. Lima, Perú.
2 Instituto de Medicina Tropical Daniel A Carrión, Facultad de Medicina, Universidad Nacional Mayor de San Marcos. Lima, Perú.
a Médico infectólogo tropicalista
Resumen
El Perú está catalogado como un país de mediana endemicidad para la infección por la hepatitis B (HBV), sin embargo, esta enfermedad se está dispersando en el país por la intensa migración de áreas de alta endemicidad a zonas de baja que endemicidad. Además de los mecanismos clásicos de transmisión de la infección como la vía parenteral y la vía sexual, debe destacarse la transmisión horizontal sobre todo en población infantil de áreas hiperendémicas y la limitada ocurrencia de transmisión vertical a diferencia de Asia. Desde que se cuenta con una vacuna segura y eficaz contra la HBV, se ha desarrollado programas de vacunación piloto en el país, luego de lo cual se ha generalizado la inmunización de la población infantil primero de áreas endémicas y luego a todo el país, según la prioridad y disponibilidad de vacunas. Dada la dispersión de la infección, y para lograr un efectivo control del problema en personas susceptibles, en un menor tiempo, es necesaria la inmunización contra HBV de adolescentes, jóvenes y grupos de riesgo, intervención que es una de las más costo-efectivas en salud pública, mereciendo en el mediano y largo plazo la evaluación de su real impacto. Estos temas son los que se desarrollan en la presente revisión.
Palabras clave: Hepatitis B/epidemiología, /transmisión, /prevención & control; Hepatitis D/epidemiología, /transmisión, /prevención & control; Perú (fuente: DeCS BIREME).
Abstract
Peru is catalogued as a middle-endemic country for hepatitis B infection (HVB), however, this disease is spreading in the country, by intense migration of highly endemic to low endemic areas. In addition to the classical mechanisms of transmission as the parenteral and sexually, it should be noted the horizontal transmission among children especially in hiperendemic areas and limited occurrence of vertical transmission. Since there is a safe and effective vaccine against HBV, the Peruvian Ministry of Health has developed a pilot vaccination programs in the country, after which has been widespread immunization to children first and then in endemic areas throughout the country, according the priority and availability of vaccines. Given the spread of infection, and to achieve an effective control of the problem in susceptible people, in less time is needed against HBV immunization of adolescents, young people and risk groups, that intervention is one of the most cost-effective public health, is needed in the medium and long term the evaluation of its real impact. These issues were development in this review.
Key words: Hepatitis B/epidemiology, /transmission, /prevention & control; Hepatitis D/epidemiology, /transmission, /prevention & control; Peru (source: DeCS BIREME).
EPIDEMIOLOGÍA DE LA HEPATITIS B Y DELTA EN EL PERÚ
DISTRIBUCIÓN DE LA INFECCIÓN
La hepatitis viral, es una de las principales causas de enfermedad aguda, crónica y de mortalidad en el mundo1,2, de la cual se ha identificado a cinco virus como responsables de hepatitis (A,B,C,D,E), con características epidemiológicas bien definidas en las diversas zonas y poblaciones del mundo3, además, existe evidencias epidemiológicas y virológicas de otros virus que causan hepatitis como G, TTV(Transmitted Transfusión Virus) y SEN4-7.
El virus de la hepatitis B (HBV) es de la familia Hepadnaviridae que primariamente infecta al hígado, es cien veces más infeccioso que el VIH, se le encuentra en sangre y fluidos corporales y es capaz de permanecer más de una semana en sangre desecada que queda en la superficie8,9.
La Organización Mundial de la Salud (OMS) estima que más de dos billones de habitantes en el mundo han sido infectados por el virus de la hepatitis B, de los cuales 350 millones serán portadores crónicos del antígeno de superficie (HBsAg) y cinco millones tienen hepatitis aguda10,11. De otro lado, tres cuartas partes de la población mundial viven en zonas hiperendémicas y aproximadamente un millón de muertes en un año están relacionadas directamente con la infección por el virus de la HVB1,12.
La infección aguda de HBV puede tener manifestaciones subclínicas, hepatitis ictérica o como hepatitis fulminante. La infección crónica de HBV puede manifestarse a manera de portador asintomático, hepatitis crónica, cirrosis o como carcinoma hepatocellular9,13. Por otro lado, hay evidencias de la asociación etiológica entre la infección por HBV crónica y el carcinoma hepatocelular14-18.
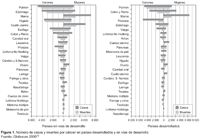
El virus de hepatitis B causa de 60 a 80% de cánceres de hígado en el mundo, que es una de las primeras causas de muerte por cáncer en hombres del este y sudeste de Asia, la Cuenca del Amazonas y África Subsahariana19,20. De otro lado, el cáncer de hígado es la cuarta causa de muerte debida a cánceres en países en vías de desarrollo donde la prevalencia de HBV es mayor que en países desarrollados (Figura 1)21,22.
En localidades donde el estado de portador del antígeno de superficie (HBsAg) excede al 10%, la infección por HBV produce hasta 3% de la mortalidad total20, aunque en áreas hiperendémicas como Huanta (Ayacucho) y Abancay (Apurímac) en el Perú, este porcentaje llega a 7%23,24. El 30% de los portadores crónicos del virus que sobreviven hasta los 30 años, están expuestos a morir de complicaciones como hepatitis crónica, cirrosis o cáncer primario de hígado12,25,26.
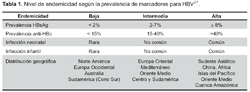
Los niveles de prevalencia y endemicidad la HBV, pueden determinarse tomando como índice a marcadores serológicos como el antígeno de superficie (HBsAg) y anticuerpos anti HBsAg o a los anticuerpos anti-HBcAg. De acuerdo con ello se pueden ubicar a las diferentes zonas endémicas (Tabla 1).
El predominio de infección de HBV varía según las áreas geográficas (Figura 2). El antecedente de infección de HBV se estima en 5% en los Estados Unidos y países de baja prevalencia y cerca de 100% entre los adultos en algunas partes del Sudeste de Asia, Africa y la Cuenca Amazónica, áreas que son de alta endemicidad.Hay un predominio creciente de infección de HBV en general, con la edad. En los Estados Unidos, el predominio de infección de HBV es más alto entre los afro-americanos, hispanos y asiáticos que en la población blanca, sin embargo, se conoce de varias comunidades con mayores tasas de portadores crónicos de HBsAg que sus regiones vecinas, en los esquimales de Alaska, en las Islas Asiático-Pacífico, y los aborígenes australianos28.
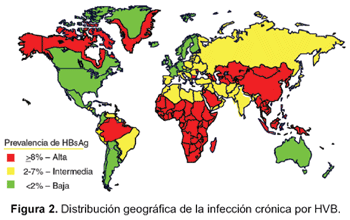
Las Américas, tienen regiones con diferentes niveles de prevalencia para hepatitis virales B y Delta. En Sudamérica el número de portadores de HBsAg se incrementa de sur a norte. Se ha observado elevada prevalencia en la zona central y oeste de la región Amazónica del Brasil y ciertas zonas adyacentes de Colombia y Venezuela, estimándose que entre 140 000 a 400 000 nuevos casos de hepatitis B pueden estar ocurriendo anualmente en Latinoamérica, dos tercios de ellos en América del Sur, incluyendo 440 a 1000 casos de hepatitis fulminante29.
Se estima que anualmente las secuelas de infección por el virus de la HBV ascienden a 2965 casos de hepatitis crónica, entre 12 782 a 44 737 casos de cirrosis y de 3271 a 11 449 casos de hepatocarcinoma. Adicionalmente, se conoce una elevada prevalencia de hepatitis viral Delta (HDV) en las mismas áreas de elevada prevalencia de HBV, particularmente en la Cuenca Amazónica, incluyendo algunas otras áreas de Colombia y Venezuela30.
HEPATITIS DELTA
El virus de la hepatitis Delta (HDV), está asociado al de la HBV y cumple un papel importante en la evolución del compromiso hepático; se adquiere bajo dos formas, como una coinfección primaria junto con la HBV, o como una superinfección en portadores crónicos del HBsAg, ambas formas de asociación pueden estar relacionadas con hepatitis fulminante y las formas crónicas de hepatitis, además de la cirrosis y el hepatocarcinoma31.
Se estima que en todo el mundo la proporción de portadores del HBsAg, infectados por el virus Delta, supera el cinco por ciento31. La hepatitis Delta que tiene una distribución mundial, también tiene dos patrones epidemiológicos, uno asociado con difusión no parenteral del virus, como en el sur de Italia, el área Amazónica y algunas partes de África, postulándose en este caso, la transmisión de persona a persona, en ausencia de exposición percutánea32 y el otro patrón asociado a transmisión parenteral como el caso de hemofílicos, politransfundidos y drogadictos endovenosos, como ocurre en EEUU y en el Oeste de Europa. Cerca de 25% de casos de HBV fulminante, están asociados a coinfección con HVD31,32, además, la infección por virus Delta agrava la enfermedad hepática crónica en los portadores del HBsAg33, así, aquéllos portadores que tienen además anticuerpos anti-Delta, tienen cuatro veces más riesgo de enfermedad crónica que aquéllos que no presentan dichos anticuerpos34.
En general, al Perú se le ha ubicado entre los países de endemicidad intermedia para HBV, tomando como promedio la prevalencia de marcadores determinados en diferentes regiones del país35,36; sin embargo, es importante destacar que esos mismos estudios y otros posteriores, nos indican que las prevalencias son significativamente diferentes entre las tres regiones geográficas y aún dentro de ellas en los diferentes poblados, así, en la selva la endemicidad está entre media y alta35-41 con prevalencias que van de 2,5% en población de Iquitos, hasta 83% en población indígena35,40,41y en la costa, prevalencias entre 1 y 3,5%36,38,42.
En la sierra los estudios son coincidentes en cuanto a la prevalencia en esta región, siendo baja en las localidades de la vertiente occidental de los andes y de media a alta en valles interandinos de la vertiente oriental de los Andes, particularmente en los valles interandinos de Huanta y Abancay, Huánuco y en el Río Pampas (Ayacucho-Apurímac) ubicados cerca a los 2400 msnm43-46.
En el Perú se ha evidenciado la presencia de infección por el virus Delta, en la región de la selva, especialmente en comunidades rurales y nativas, así como en algunos valles interandinos como Abancay, Cuenca del Río Pampas y Huanta, donde se ha encontrado una prevalencia de 14% de HDV en escolares aparentemente sanos, además, 17% de los que tuvieron infección por HBV tiene infección por el virus Delta, y 56,5% de los portadores de HBsAg también tiene marcador de HDV43. En un estudio que incluyó 870 pobladores de 37 comunidades indígenas de la Amazonía Peruana, distribuidas en 12 cuencas hidrográficas, encontramos antecedentes de infección por HBV que varía entre 24 a 83%, portadores de HBsAg entre 2,7 a 18%, e infección por el virus de hepatitis Delta de 6,2 a 13% entre aquellos con antecedente de infección por HBV y de 14 a 53,3% entre los portadores de HBsAg40.
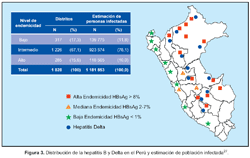
Con la información disponible se ha elaborado un mapa de la distribución de la prevalencia de infección por HBV, el cual está sujeto a cambios dada la dinámica poblacional, acentuada por la intensa migración de las dos últimas décadas debido a factores sociales, políticos y violencia. Se ha estimado, que de los 1828 distritos existentes en el país para el 2005, 67,1% está en riesgo intermedio y se estima que habría más de un millón de personas infectadas con el HBV (Figura 3).
En razón a la información recogida de los estudios seroepidemiológicos en población general aparentemente sana, se puede concluir que entre 8 a 86% de esta población tienen algún marcador de infección para HBV, esta marcada diferencia estaría en relación al año, a la zona de estudio, al diseño, a marcadores y técnicas de laboratorio usadas. Estudios recientes muestran cambios en el patrón epidemiológico, así, en el primer estudio seroepidemiológico realizado entre 1965 y1972 por Madalengoitia48 en población urbana y rural de la selva, encontró 1,8% de portadores del HBsAg en promedio, con prevalencias máximas de 6,4%, mientras que los estudios realizados en la década del 80, muestran prevalencia de 3 a 4% en poblaciones urbanas de la selva, y mayor a 10% en áreas rurales de esta región35,36.
Adicionalmente, la acentuada migración en las últimas dos décadas, por problemas económicos y socio-políticos, de zonas hiperendémicas a zonas de baja endemicidad, agrega focos de transmisión al mozaico que desde ya constituye la distribución de las HBV y HDV en el país. Un ejemplo de ello es que en una población residente en una localidad periurbana de Lima, luego de siete años de convivencia con migrantes de áreas hiperdendémicas, la prevalencia de portadores crónicos de HBsAg ascendió de 2 a 3,5%, indicando un importante cambio que muestra la dispersión de la infección42.
MECANISMOS DE TRANSMISIÓN
Transfusión sanguínea.
En los años 60, el riesgo de hepatitis por la infección HBV por transfusión de sangre comercial, era tan alto como 50% y el HBsAg fue detectado en 60% de pacientes con hepatitis postransfusión de sangre. La exclusión de donantes pagados y la aplicación de tamizaje de marcadores para HBV, redujo dramáticamente en los años 70 la incidencia de HBV postransfusión, al menos en los países desarrollados48.
En Estados Unidos se usa para el tamizaje tanto de HBsAg como anticuerpos anti Core (anti-HBc). El anti HBc permite detectar la infección por HBV en la fase de la ventana durante la recuperación de las hepatitis agudas B o en aquellos casos en los que la infección crónica HBV es de bajo nivel. Cuando se determine el uso de marcadores de infección como el anti HBc, hay que tener en cuenta la sensibilidad y especificidad de la prueba49,50. Igualmente, se debe considerar la incidencia de infección de HBV asociada con transfusión, en áreas de baja prevalencia donde sólo se usa el HBsAg como marcador de tamizaje51 y la necesidad de excluir más de 22% de la población de donantes en áreas hiperendémicas52.
Hace falta la evaluación de otros marcadores de infecciocidad como el DNA del virus, para definir los niveles reales del riesgo de infección por HBV, pues hay hallazgos de que en personas con anticuerpos anti HBc positivos y HBsAg negativos en el país, hasta 14% de ellos pueden ser positivos para DNA de HBV (G Hijar comunicación personal).
En el Perú, los niveles de prevalencia en donantes de sangre son coincidentes con los niveles de prevalencia en la población general, así, en Chiclayo (Lambayeque) encontramos 0,5% de portadores de HBsAg, en Ica 2,2%, Arequipa 0,4%, Huancayo (Junín) 1,8%, Tarapoto (San Martín) 3,8%, Pucallpa (Ucayali) 3,2%53. En el caso de las áreas urbanas de las ciudades de la selva, encontramos prevalencias intermedias. Un hallazgo que llama la atención es la de Ica, que está en transición de endemicidad baja a intermedia, probablemente por la intensa migración receptora de áreas hiperendémicas del departamento de Ayacucho. También en el Perú esta forma de transmisión se está limitando al ser obligatorio el tamizaje para HBsAg y anti HBc en donantes de sangre, sin embargo, aún constituye un serio problema la disponibilidad de donantes aptos en áreas hiperendémicas de HBV, donde 80 a 90% de la población en condiciones de donante, tiene marcadores positivo para anti HBc.
Transfusión percutánea.
La inoculación de sangre o fluidos corporales a través de la vía percutánea sigue constituyendo una forma de transmisión importante. El compartir agujas, como lo hacen los drogadictos endovenosos, son una ruta importante para la transmisión de hepatitis B54, igualmente el reuso de agujas contaminadas para los tatuajes, extracciones o curaciones dentales, inyectables, acupuntura e implantación de adornos a través de la piel. Estas rutas son válidas prácticamente en todos los países, aunque estas prácticas son más frecuentes en países en vías de desarrollo como el nuestro, donde la práctica de la medicina no tiene un control adecuado. En poblaciones indígenas de la amazonía peruana, donde la prevalencia de HBV es alta, el tatuaje probablemente constituye uno de los factores que contribuye a la alta transmisión, además de las otras formas como el consumo de masato, mordedura por murciélagos, picadura de mosquitos y la transmisión horizontal40.
Transmisión sexual.
En los países desarrollados, la vía sexual es la más importante forma de transmisión de HBV. La transmisión sexual corresponde a aproximadamente 30% de las infecciones agudas de HBV en los Estados Unidos54. Se observa una elevada prevalencia de portadores crónicos de HBV en homosexuales y en heterosexuales con múltiples parejas, de modo que a fines de los 70 se estimó una tasa de incidencia anual de infección por HBV del 20% entre los homosexuales54.
A fines de los años 80, esta proporción ha caído a menos de 10%, probablemente como resultado de la modificación de conducta sexual de alto riesgo de infección por el VIH. Desgraciadamente, la incidencia de transmisión heterosexual permanece alta.
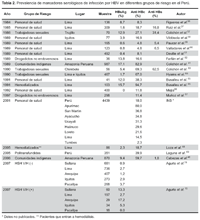
El riesgo de transmisión sexual de infección de HBV se relaciona directamente con el número de compañeros sexuales, el nivel de educación logrado, ocurrencia de sexo pagado, e historia anterior de enfermedades sexualmente transmitidas. En el Perú, la información disponible también muestra una elevada prevalencia de HBsAg en trabajadoras sexuales y homosexuales, con tendencia a disminuir en los últimos años en las trabajadoras sexuales, probablemente debido a las medidas de prevención adoptadas por estos grupos contra las ITS y el VIH/SIDA. Sin embargo, la tendencia es similar o creciente con relación a anteriores prevalencias en los HSH. Los niveles de prevalencia de HBsAg en estos grupos de riesgo se pueden observar en la Tabla 2.
Transmisión perinatal.
La proporción de transmisión perinatal de HBV desde las madres infectadas a sus hijos, es menor a 10% en los países occidentales. Se estima que 20 000 niños nacen anualmente de mujeres portadoras del HBsAg en los Estados Unidos71. En las áreas hiperendémicas como China, la proporción de infección perinatal puede ser tan alta como 90%, particularmente cuando las mujeres embarazadas son HBeAg positivas o tienen DNA para HBV positivo en el suero. La transmisión de la madre al infante tiene lugar en el momento de la gestación, por transfusión en la circulación materno-fetal o por exposición a la sangre materna durante el pasaje a través del canal del parto y posterior al nacimiento a través del contacto íntimo entre la madre y el niño. La transmisión intrauterina es rara porque la detección del HBsAg en los infantes frecuentemente es tardía. Adicionalmente, la inmunización pasiva y activa al momento del nacimiento ha demostrado tener una eficacia mayor a 90% en la prevención de HBV72.
La cesárea no ha mostrado eliminar el riesgo de adquirir infección perinatal por HBV73. Aunque el HBsAg puede encontrarse en la leche materna, no hay evidencia que la infección de HBV puede transmitirse a través de la lactancia materna74. La vacunación universal de todos los recién nacidos y administración adicional de inmunoglobulina hiperinmune contra HBV (HBIg) a recién nacidos de madres portadoras de HBsAg se comenzó a dar en muchos países del Sudeste Asiático, como Hong Kong, Taiwán, Singapur, y Japón en los años 80.
Estos programas han llevado a reducciones significativas en las tasas de portadores de HBsAg, así como en la disminución en la incidencia del carcinoma hepatocelular (HCC) en niños75. En los Estados Unidos, la vacunación universal de todos los recién nacidos se empezó a partir de 1992, luego de probar otras estrategias que no dieron resultados respecto a las coberturas.
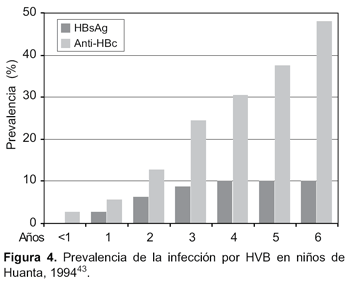
En el Perú los estudios realizados en población infantil de áreas hiperendémicas como Huanta, muestran una baja prevalencia de HBsAg en menores de un año (menor al 0,1%), lo cual indica que la infección no ocurre en el periodo perinatal, sino después, en los primeros años de la vida, cuando el niño empieza la etapa de socialización y además tiene un mayor tiempo de exposición a portadores crónicos, sea dentro o fuera del hogar43 (Figura 4). Igualmente, la mayor prevalencia del HBeAg en portadores crónicos de HBV en niños, tanto en poblaciones nativas de la Amazonía, como en poblaciones mestizas de áreas hiperendémicas, explicaría que la transmisión ocurre principalmente en los primeros años de vida, para ir reduciéndose progresivamente en la edad adulta, esto vinculado a una menor presencia del HBeAg, el cual es un marcador de mayor infecciosidad40.
Por otro lado, estudios realizados en gestantes en localidades de las tres regiones geográficas del Perú, y al margen de los niveles de endemicidad, han mostrado una baja prevalencia de antígeno e (HBeAg) en mujeres portadoras del HBsAg, lo cual también corrobora el hallazgo de la baja prevalencia en niños, no siendo por lo tanto muy importante la forma de transmisión perinatal76,77. A diferencia de lo que ve en países asiáticos, probablemente debido a las variantes genotípicas entre los virus de HBV de nuestra región con las de los que circulan en Asia.
Riesgos de infección en áreas de cuidado de pacientes.
El virus de la hepatitis B es el agente más común responsable de las infecciones virales nosocomiales78. Durante el seguimiento de una cohorte en diez años, se encontró que la incidencia de infección por el virus de la hepatitis B era 55 veces mayor que la del virus de inmunodeficiencia humana (VIH), y 38 veces mayor que la del virus de la hepatitis C (HCV)79.
El CDC (Centers for Disease Control and Prevention) calculó que de 6500 a 9000 nuevas infecciones ocurrieron en trabajadores de salud en 199080. Siguiendo el curso natural de la infección por el HBV, entre 300 a 950 de estos trabajadores (5 a 10%) eventualmente, desarrollarían infección crónica, la que llevaría a la muerte por cirrosis entre 100 a 150 personas y carcinoma hepatocelular fatal en 25 a 40 sujetos80. Mundialmente la hepatitis B representa la principal causa de incapacidad prolongada del personal de salud como consecuencia de exposición laboral81.
El común denominador de la exposición ocupacional del personal de salud es el contacto frecuente y sistemático con sangre o líquidos serosos. Los grupos de trabajadores que están expuestos a un frecuente contacto con sangre, en vez de un tiempo de exposición prolongado, define a aquellos con mayor riesgo de exposición al virus B, sin diferencias con respecto al contacto con pacientes, con una incidencia de nuevas infecciones del 1% por año en aquellos con contacto frecuente con sangre frente a 0% por año en aquellos con contacto limitado82.
Además, se reporta que la exposición al virus B estaba en función a una historia previa de hepatitis, duración de la exposición ocupacional y la edad. Sin embargo, otros autores demuestran que el riesgo de infección por HBV cambia en el tiempo65,82, es mayor durante los primeros años de trabajo y varía en los distintos servicios de un hospital83. El sistema de rotación del personal auxiliar por los diferentes servicios, practica acostumbrada en nuestros hospitales, aumenta el número de personas expuestas61.
En el Perú, los estudios también muestran que los trabajadores de salud de áreas con baja endemicidad par HBV tienen un mayor riesgo, particularmente los que manipulan material contaminado con sangre y secreciones, así como aquellos que desarrollan procedimientos invasivos (Tabla 2). Sin embargo, en áreas hiperendémicas, el ser trabajador, no es un riesgo adicional para contraer HBV, pues han adquirido la infección en edades tempranas de la vida, como se mostró en un estudio en Huanta, donde los niveles de infección entre trabajadores de salud de un hospital general y profesores, eran similares84. En ese sentido los trabajadores de salud de áreas de mediana y baja endemicidad deben beneficiarse con la vacunación contra HBV por ser un grupo de riesgo importante. Por otro lado, es conocido que los estudiantes de medicina y otras ciencias de la salud, en sus prácticas tienen un alto nivel de exposición a accidentes biológicos; sin embargo, se encontró que sólo 34% tenía completo su esquema de vacunación85.
Transplante de hígado.
Actualmente a los donantes de órganos, de modo rutinario se les hace un tamizaje para HBsAg. Se ha reportado casos de infección secundaria a transplantes de órganos extrahepáticos, como riñones en personas portadoras de HBsAg. Esto puede relacionarse a sangre residual en los vasos sanguíneos de estos órganos, que contienen partículas virales.
También puede ocurrir luego de transplantes de tejido avascular como la córnea86. El rol del tamizaje de anticuerpos anti HBc puede tener incovenientes, debido a la posibilidad de resultados falso positivos, la pérdida potencial de 5% de donantes87 y la incertidumbre sobre el infectividad de los órganos de donantes en lo que se encuentra el anti HBc88. La incidencia de infección de HBV de los donantes con anti HBc positivo es muy bajo (0 a 2%) en receptores de transplantes de corazón y riñón, pero varía de 0 a 78% en receptores de hígado87,89. En el Perú, los transplantes aún están limitados a aquellas personas que tienen hepatopatías no relacionadas con hepatitis viral, y en todos los donantes se realiza tamizaje para marcadores serológicos de HBV y HCV. Los riesgos de transmisión a través de este procedimiento son similares al de los países desarrollados, aunque si consideramos una mayor prevalencia de infección por HBV en población general, el riesgo puede ser mayor.
Transmisión horizontal.
En áreas endémicas, la transmisión horizontal en niños es un mecanismo muy común90, y está en razón al contacto directo de portadores del virus de HBV con susceptibles, a través de solución de continuidad en la piel o mucosas, pudiendo ser la saliva un vehículo importante, pues se han encontrado el virus de la hepatitis B en concentraciones infectantes. En las áreas estudiadas en el Perú, como en Huanta y en la Amazonía, los mecanismos clásicos de transmisión como el de agujas, relaciones sexuales, tatuajes, o transfusiones de sangre, no se dan en la medida que podrían explicar las altas tasas de prevalencia40,41, particularmente en población infantil, por lo que consideramos que la transmisión horizontal cumple un papel importante en estas poblaciones. De otro lado, la migración de personas portadoras del HBV hacia áreas no endémicas, con una gran cantidad de susceptibles, condiciona la transmisión a través de este mecanismo horizontal, como se ha mostrado en un estudio donde la tasa de portadores de 2,3% se incrementó a 4,5% en un periodo de siete años, habiendo mediado sólo la presencia de migrantes portadores del HBsAg en un área de susceptibles42.
En las áreas endémicas, la transmisión horizontal entre los niños puede ser el resultado de contacto corporal íntimo que lleva para transferir del virus por pequeñas erosiones de la piel y las membranas mucosas. Se ha informado que varias secreciones del cuerpo pueden contener el HBsAg, pero sólo se ha mostrado en forma consistente que el semen, secreción vaginal y saliva de personas infectadas, pueden albergar el virus de la HBV91,92. Aunque el DNA de HBV se ha descubierto en la saliva de algunas hepatitis, los portadores de B, y se asume que puedan cumplir un papel importante en la transmisión, hace falta más estudios que apoyen la transmisión mediante esta ruta93, aunque con la existencia de la vacuna contra HBV y por cuestiones éticas estos estudios estarán limitados.
El virus de la HBV puede permanecer durante mucho tiempo fuera del cuerpo humano, contaminando superficies medioambientales y los artículos de uso cotidiano, como cepillos de dientes, navajas de afeitar, e incluso juguetes donde es posible que persistan. En un estudio realizado en comunidades indígenas de la Amazonía, encontramos una asociación importante (OR: 4,98; IC95%: 3,4-7,4) entre estado de portador crónico de HBsAg y el consumo de masato, que es una bebida preparada mediante la premasticación de la yuca, la cual luego es fermentada40.
Por otro lado, existe la costumbre en estas comunidades, que la madre ofrece directamente a la boca de los lactantes alimentos premasticados. Si consideramos la elevada prevalencia de lesiones en mucosa oral y el estado de portador del virus, este puede constituir un mecanismo adicional a los descritos.
Otros mecanismos propuestos.
Se ha demostrado que algunos insectos hematófagos pueden ser vectores al menos mecánicos para la transmisión de HBV, sin embargo, es necesario contar con mayores evidencias al respecto. En estudios realizados en poblaciones indígenas, como en militares, se ha encontrado asociación epidemiológica entre infección aguda o crónica por HBV y la mordedura de murciélagos hematófagos (Desmodus rotundus). En indígenas de la Amazonía40 se encontró, que aquellos mordidos por murciélagos tenían casi dos veces más riesgo de infección que aquellas no mordidas (OR: 1,69; IC95%: 1,2-2,4), mientras que en población militar94 80% de los que tuvieron HBV, habían sido mordidos por murciélagos. Se viene complementando estos hallazgos con estudios de inmunohistoquímica y biología molecular para evidenciar esta forma de transmisión.
Se ha descrito la posibilidad de que algunos insectos puedan participar en la transmisión de la HBV95,96, pero no había evidencias de este mecanismo de transmisión. Se han descrito experimentos en chinches (Cimex lectularius L)97,98, mosquitos (Anopheles stephensi y Ochlerotatys triseriatus)99 y chirimachas (Rodnius prolixus)98; sólo con el Cimex lectularius se ha descrito que el virus de HBV inoculado puede sobrevivir y encontrarse en sus heces hasta 21 días postinoculación, planteándose la hipótesis de que el chinche abre una solución de continuidad en la piel de la persona, deja el virus en las inmediaciones y al rascarse la persona puede introducir el virus, conllevando a la infección.
GRUPOS DE ALTO RIESGO
El personal que cuida directamente la salud de personas, tienen un mayor riesgo de tener infección por el virus de la HBV, que la población en general. Este riesgo es particularmente alto entre cirujanos, patólogos, odontólogos, laboratoristas, además de médicos y personal que labora en las unidades de hemodiálisis y unidades de oncología. Las laceraciones de la piel, los cortes pequeños, y los accidentes con objetos punzocortantes en general, abren la puerta de entrada para el virus.
Las personas con retraso mental que viven en hospicios, así como el personal que los cuida y miembros de la familia también tienen una proporción alta de hepatitis B. A pesar de que los productos hemoderivados son tamizados, los pacientes que reciben múltiples transfusiones tienen mayor riesgo de infección, entre ellos los hemodializados, hemofílicos y talasémicos69. Los pacientes en hemodiálisis, pueden infectarse a través de las transfusiones de sangre o por contaminación de máquinas de la diálisis o equipos, así como la transmisión horizontal interpersonal en las unidades de la diálisis, constituyendo un serio problema en el Perú100. Los cuidados de la infección y la disponibilidad de vacunas han reducido la incidencia de infección de HBV. Otros grupos de alto riesgo incluyen a los usuarios de droga por vía endovenosa, particularmente aquéllos que usan jeringas, los homosexuales y los heterosexuales promiscuos.
Aunque en el Perú no es frecuente el uso de drogas por vía endovenosa, los consumidores de droga por inhalación suelen ser promiscuos, lo cual también los pone en riesgo de infección. Se ha realizado varios estudios en el Perú, respecto a la prevalencia de infección por HBV en grupos de riesgo (Tabla 4), donde en promedio hay mayor riego de infección entre los trabajadores más expuestos a sangre o secreciones. Así mismo se muestra una mayor prevalencia que en población general, en hemodializados, prostitutas y drogadictos de PBC, en estos últimos en relación a su promiscuidad más que al uso de drogas por vía endovenosa. En zonas hiperendémicas, donde la infección ocurre en los primeros años de vida, no se encuentra mayor prevalencia en trabajadores de salud que en población general, aunque debe considerarse que los susceptibles a la infección, mantienen un mayor riesgo en estas zonas por razones vinculadas a su ocupación, como mostramos en un estudio efectuado en Huanta84.
Población militar.
La prevalencia de HBV en población militar ha ido variando de 1961 a 1997, registrándose un incremento de 55,67 a 230 por cada 100 000. Asimismo, entre 1977 y 1981 se registraron dos brotes en Loreto, en guarniciones militares fronterizas, con una letalidad de 12,9 y 27,7% respectivamente35. En 1985, se notificó siete casos en una guarnición militar en Amazonas, identificando HBsAg en seis muestras, con una tasa de letalidad de 21,4%. Ese mismo año, Ruiz et al.37 investigaron una población mixta de 164 individuos (98 civiles y 66 militares), residentes de Ampama, departamento de Amazonas, identificando HBsAg en 43,2% y anti HBc en 50,6%; el 10,3% de estos últimos presentaron reactividad IgM (indicador de infección actual de la hepatitis B). Además menciona en una de sus conclusiones que la hepatitis podría transmitirse a través de vectores naturales, lo cual sin embargo, no ha sido comprobado en estudios posteriores. Brotes recurrentes de hepatitis aguda se han dado en la Amazonía Peruana, entre 1992 y 1993, determinándose en 88 militares, una tasa de infección del 95% y 64% para HBV y HDV respectivamente. Adicionalmente, en este brote la genotipificación viral determinó la presencia de genotipo F para el virus de hepatitis B y genotipo III para el virus Delta100.
Durante el conflicto con el Ecuador se presentó un brote debido a hepatitis B y Delta, durante el cual se hospitalizaron 234 militares con diagnóstico de HBV en el Hospital Militar de Lima. Entre enero y agosto de ese año ocurrieron 652 casos, teniendo una morbilidad de 8,5% y una mortalidad de 2,9% en la población afectada. Entre 84 soldados que fueron evaluados se encontró infección aguda por el virus de hepatitis B en 47 (56%) y 4,8% de infección por el virus Delta94. Estos hallazgos justifican largamente la inmunización de los integrantes de las fuerzas armadas y policiales, desde su ingreso a estas instituciones. Igualmente el personal civil que por diferentes motivos se desplaza a zonas endémicas de hepatitis B y Delta.
HISTORIA NATURAL DE LA HBV
El curso natural de infección de HBV está determinada por la interacción entre la replicación del virus y la respuesta inmune. Otros factores que pueden contribuir en la progresión de enfermedad hepática debido a HBV, están relacionadas con el sexo, consumo del alcohol, e infección concomitante con otros virus de hepatitis. El resultado de infección de HBV crónica depende de la gravedad de enfermedad hepática en el momento de la replicación viral9.
La edad a la que ocurre la infección es gravitante para el desarrollo de infección crónica. Si la infección ocurre al nacimiento la probabilidad de quedar como portador crónico es de 90%, si la infección ocurre entre 1 – 4 años esta probabilidad está entre 30-50% y si ocurre en la edad adulta se reduce a menos del 5%101. Por otro lado, la infección en niños pequeños cursa asintomática, de modo que sólo 10% de niños menores de diez años presentan síntomas que clínicamente orienten a una infección por hepatitis B102 (Figura 5).
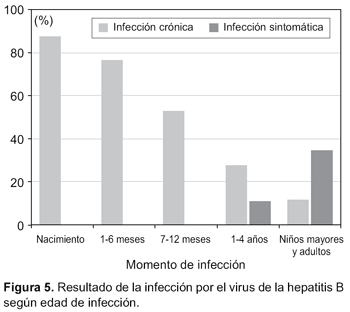
En general, la infección de HBV crónica pasa por dos fases, una fase replicativa temprana relacionada con la enfermedad activa del hígado y una fase no replicativa más tardía, relacionada con la remisión de la enfermedad hepática103,104. Sin embargo, en los pacientes que adquirieron la infección en el periodo perinatal, se cree que hay una fase adicional en la que la replicación del virus no se acompaña de enfermedad hepática activa105. Esto es debido a la tolerancia inmune secundaria a la exposición a HBV o a los antígenos HBV-relacionados, en etapas tempranas de la vida.
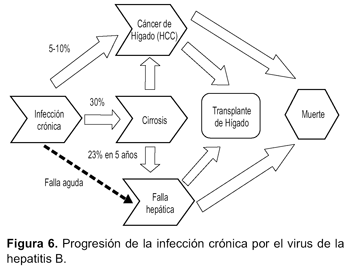
La progresión de la infección crónica por HBV se puede mostrar en la figura 6. La HBV aguda y la coinfección con el HDV tiende a ser más grave que la infección de HBV aguda sola y más probablemente produce hepatitis fulminante106,107. La superinfección con HDV en los pacientes con la infección crónica por HBV crónica se acompaña por la supresión de la replicación de HBV108. La mayoría de los investigadores ha encontrado que la superinfección por HDV está asociada con la enfermedad hepática más grave y la progresión acelerada a cirrosis109,110.
INFECCIÓN DE HBV Y HEPATOCARCINOMA (HCC)
A nivel mundial el HCC es la tercera causa de muertes por cáncer en los hombres, y la séptima causa más común de muertes de cáncer en las mujeres, reportándose aproximadamente 500 000 muertes cada año111,112. La inmensa mayoría (85%) de HCC se concentra en Asia oriental y del sudeste y África Subsahariana113 donde la infección de HBV es endémica. Hay varios estudios, que evidencian la asociación de la infección crónica por HBV y HCC. Hay una correlación muy cercana entre la distribución geográfica de portadores de HBsAg y la ocurrencia de HCC. El HCC es la cuarta malignidad más común con una incidencia de mayor en las áreas endémicas como China y África Subsahariana donde la HBsAg portador proporción es 10 a 15%, a 150 casos de HCC por 100,000 por año114 en contraste con los Estados Unidos donde la tasa de portadore de HBsAg es menor a 1%, donde hay cuatro casos de HCC por 100 000 por año y ocupa el puesto 22 como causa de cáncer en general.
El predominio de HBsAg entre los pacientes con HCC varía de 85 a 95% en Asia y África a 10 a 25% en los Estados Unidos y Europa occidental114. La evidencia más fuerte para una asociación etiológica entre la infección de HBV crónica y el desarrollo de HCC deriva de un estudio en 22 707 hombres taiwaneses que fueron seguidos por un periodo de 8,9 años115. La incidencia de HCC fue de 495 por 100 000 por año para HBsAgpositivo y 5 por 100 000 por año para los hombres HBsAg-negativos, con un riesgo relativo de 98. Ninguno de los 1 272 hombres que eran los seronegativos para los marcadores de HBV desarrolló HCC.
En el Perú, es evidente que en las áreas hiperendémicas de HBV también es prevalente la presencia de HCC, como se ha mostrado en los estudios de Abancay y Huanta donde alrededor de 7% del total de fallecimientos corresponden a enfermedades hepáticas relacionadas con infección por el virus de la hepatitis B, como HCC, cirrosis y hepatitis fulminante23,24 , debiendo destacar que en estas áreas, del total de fallecidos por enfermedades hepáticas 50% corresponden a hepatitis fulminante (asociado con infección por el virus Delta), 10% a cáncer de hígado y 40% a cirrosis hepática. De otro lado, 73% de los que fallecen por hepatitis fulminante son menores de 20 años, en este mismo grupo de edad están 18% de los que fallecen por cirrosis hepática y 35% del los que fallecen por cáncer de hígado, que al igual que en otras series, más de 60% son varones. Otros estudios hechos en el Perú, en pacientes con HCC y cirrosis, utilizando técnicas inmunohistoquímica y marcadores de infección por HBV en suero, han mostrado también asociación importante116-121.
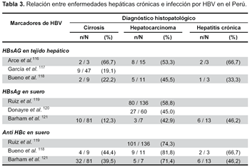
Los estudios en el Perú, que tratan de correlacionar la infección por HBV con cirrosis y hepatocarcinoma, se han realizado utilizando diferentes metodologías, entre ellas, la búsqueda del antígeno de superficie (HBsAg) en tejido hepático por inmunohistoquímica o la determinación de marcadores serológicos para HBV (HBsAg o anti-HBc) en pacientes con cirrosis, hepatitis crónica o hepatocarcinoma (Tabla 3) .
Mortalidad debida a cirrosis y hepatocarcinoma
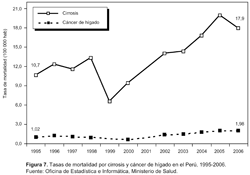
Según información de la Oficina de Estadística e Informática del Ministerio de Salud, ajustada al nivel de subregistro existente, anualmente han muerto, en promedio, 4399 personas por cirrosis y 419 por hepatocarcinoma en el Perú entre los años 1995 al 2006; así mismo, se ha visto un incremento en las tasas de mortalidad de ambas enfermedades (Figura 7).
PREVENCIÓN Y CONTROL DE LA HE PATITIS B
POBLACIÓN SUJETA A VACUNACIÓN Y BENEFICIOS DEL PROGRAMA DE VACUNACIÓN
En áreas de alta y mediana endemicidad de HBV se recomienda la inmunización de población infantil, particularmente a menores de un año, y progresivamente ir incorporando a otros grupos poblacionales de mayor edad y grupos de riesgo para la infección. Una de las ventajas de la vacunación infantil son las altas coberturas de vacunación que a su vez conlleva a la protección contra la infección; sin embargo en áreas como nuestro país donde existen áreas de alta, mediana y baja endemicidad con intensa migración que contribuye a la diseminación de la infección, es necesaria la inmunización de grupos de mayor edad, como adolescentes y jóvenes, además de grupos de riesgo (trabajadores y estudiantes de áreas de la salud, población policial y militar, pacientes que serán politransfundidos como hemodializados y hemofílicos) para limitar al máximo al grupo de susceptibles y obtener impactos de intervención en periodos menores que si sólo se mantiene la vacunación infantil.
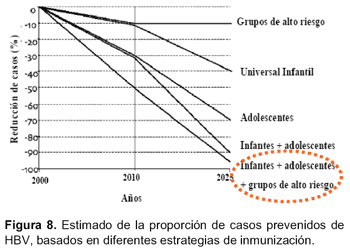
Hace 15 años los elevados costos de la vacuna limitaban intervenciones masivas, aun sabiendo de sus beneficios, sin embargo actualmente la disponibilidad de vacunas contra HBV seguras, eficaces y de bajo costo permiten no sólo plantear, si no desarrollar intervenciones en grupos de mayor edad como la población general menor de 20 años, además de grupos de riesgo. La justificación para incluir a la mayor población susceptible posible es que se reduce el número de infectados a través del tiempo y se reduce el periodo en el cual se eliminaría la infección en la población general. Así, si quisiéramos reducir la tasa de portadores de HBV de 10% a 0,2%, si la estrategia fuera sólo vacunar a los menores de un año, se requerirían 70 años para lograrlo. Si se realiza una vacunación masiva a población susceptible el periodo necesario para lograr la eliminación será mucho menor, dependiendo de la protección a la población de susceptibles122 (Figura 8).
Adicionalmente, es necesario tener en cuenta el costo beneficio de la vacunación, que ahorra al país una gran inversión en el tratamiento de personas con infección aguda o sus complicaciones crónicas como la cirrosis y cáncer de hígado, en comparación con la inversión que significa proteger a la población susceptible. Diferentes estudios muestran costos anuales por paciente de $ US 142,24 para hepatitis crónica, $ US 185,11 para cirrosis compensada, $ US 1701,58 para cirrosis descompensada y $ US 4 740,53123 para carcinoma hepatocelular.
Si hacemos una aproximación a los portadores crónicos de HBV calculados en el Perú, tendríamos que 56 517 desarrollarían hepatocarcinoma, cuyo costo de tratamiento anual ascendería a $US 96 132 015. De otro lado 169 546 portadores desarrollarían cirrosis hepática, que si consideramos las cirrosis compensada, el tratamiento tendría un costo anual de $US 31 384 660 y si fueran estas cirrosis descompensadas, este costo ascendería a US $ 803 737 899.
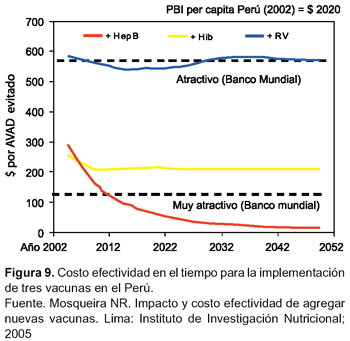
El costo efectividad de la incorporación de la vacunación contra HBV en el Perú124, comparada con otras vacunas como la de rotavirus y Haemophilus influenza B, se puede observar en la figura 9.
PROGRAMAS DE INMUNIZACIÓN CONTRA HBV EN EL PERÚ
Desde 1991, se iniciaron estudios piloto para la incorporación de la vacuna contra HBV en el programa ampliado de inmunizaciones (PAI), como en Abancay125, localidad ubicada a 2395 msnm, en la sierra del Perú, la cual es hiperendémica para HBV y HDV, donde 7% de las defunciones son relacionadas con infección por HBV. Se programó para la vacunación a 1 301 niños menores de un año y 3 488 niños entre 1-4 años. Se utilizaron tres dosis de vacuna recombinante de DNA contra HBV para cada niño. El esquema de vacunación fue adecuado al calendario de vacunación del PAI, y en el grupo de 1 a 4 años el esquema fue 0, 1 y 6 meses. Al año de iniciado el programa se inmunizaron 1 262 (97,0%) menores de un año y 2 529 (72,5%) en el grupo de 1-4 años. No se registró efectos adversos importantes por el uso de la vacuna HBV. Ocurrieron ocho defunciones debidas a infección respiratoria aguda y enfermedad diarreica aguda, las cuales son las principales causas de defunción en la zona. Se objetivó una mejora en las coberturas de vacunación del PAI en menores de un año, mostrándose para la DPT una cobertura de 97,0% en 1991, en comparación a años previos: 63,0% (1988), 26,9% (1989) y 61,9% (1990).
En 1994, se realizó una intervención similar en Huanta126, un valle interandino ubicado a 2400 msnm, considerada una zona hiperendémica de HBV y HDV, donde cerca de 8% del total de fallecidos corresponden a enfermedades hepáticas como hepatitis fulminante, cirrosis o hepatocarcinoma. Se incluyó para la vacunación 1 412 niños menores de un año y 5 175 niños entre 1-4 años. Se aplicó a cada niño tres dosis de una vacuna recombinante de DNA contra HBV. El esquema fue adaptado al del PAI en niños menores de un año y de 0, 1 y 6 meses en el grupo de 1-4 años.
Al año de iniciado el programa, recibieron tres dosis de la vacuna 1 386 (98,1%) niños menores de un año y 4 353 (84,1%) niños de 1 a 4 años. No se reportaron reacciones adversas importantes. El objetivo de mejorar las coberturas de vacunación del PAI, fue alcanzado, así las coberturas de vacunación en menores de un año con DPT en 1991 fue de 75% en 1992 de 64,5%, en 1993 del 55,2%, mientras que en 1994 en el que se incluyó la vacuna contra HVB, la cobertura fue de 98,1%.
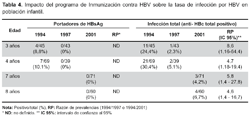
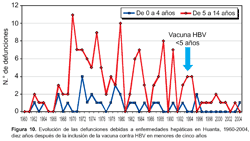
En 1997 se evaluó la vacunación contra HBV en Huanta, lo cual mostró una significativa reducción de las tasas de infección en niños de 3-4 años en 1994 (24,4%- 30,4%) comparado con las tasas de infección en niños de la misma edad en 1997 (2,3- 5,1%), concluyendo que la inclusión de la vacuna contra HBV en el PAI en una zona hiperendémica de HVB/HVD, es segura, eficaz y mejora las coberturas del PAI. Una posterior evaluación en el 2001, muestra que las tasas de infección permanecen tan bajas como en el 1997 (Tabla 4). Últimamente al revisar las causas de defunción debidas a enfermedades hepáticas en menores de 14 años, beneficiados en 1994 con la inmunización contra HBV en un área hiperendémica como Huanta, se observa una significativa reducción, en comparación a años previos a la inmunización (Figura 10).
Basados en estas dos experiencias nacionales y la experiencia internacional, el Ministerio de Salud127, en 1996, decidió incorporar la vacuna contra HBV en el Programa Ampliado de Inmunizaciones para niños menores de un año residentes en áreas de mediana y alta endemicidad, que al inicio de la vacunación constituían alrededor de 120 430 niños menores de un año. Esta medida se tomó considerando el mayor riesgo de los niños de estas áreas y la disponibilidad de recursos en ese momento. Posteriormente, el MINSA ha implementado la inmunización universal contra la HBV a nivel nacional para menores de un año, desde el año 2003. Sin embargo, es pertinente avanzar hacia la universalización de la vacunación contra HBV a todo el país, que incluya además de los niños, adolescentes, jóvenes y grupos de riesgo, para reducir al máximo posible el número de susceptibles a la infección128,129, considerando la intensa migración que hay entre áreas de alta, mediana y baja endemicidad; lo cual nos llevaría a la eliminación de la HBV y sus secuelas como la cirrosis y el cáncer de hígado en un periodo menor al que si solamente se incluye a menores de un año.
VIGILANCIA EPIDEMIOLÓGICA DE LA HBV Y EVALUACIÓN DEL IMPACTO DE LAS INTERVENCIONES
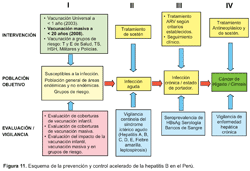
Para continuar las actividades de prevención y control de la HBV y Delta en el Perú es necesaria la sistematización de las estrategias y actividades de intervención, evaluación y vigilancia de la enfermedad e infección por HBV en los diferentes grupos poblacionales, como se muestra en la Figura 11.
Para la población susceptible a la infección, residente en áreas endémicas y no endémicas de HBV y los grupos de riesgo, el Ministerio de Salud del Perú, viene realizando la inmunización a menores de un año de áreas de alta y mediana endemicidad para HBV desde 1996 y desde el año 2003 paulatinamente se ha universalizado la vacunación dentro del Programa Ampliado de Inmunizaciones y actualmente la vacuna contra HBV está incluida dentro de la vacuna pentavalente, conjuntamente con la DPT y la HBi.
A fin de reducir el número de susceptibles a la infección y teniendo en cuenta el costo efectividad de la intervención, el MINSA ha considerado pertinente la inmunización a la población nacional menor de 20 años de edad y grupos de riesgo como trabajadores de salud, estudiantes de áreas de la salud, politransfundidos, trabajadoras sexuales y hombres que tienen sexo con hombres (HSH).
Estas intervenciones requieren ser evaluadas para medir su impacto, por lo que se considera una evaluación de las coberturas de vacunación a menores de un año y también de la vacunación masiva a ser realizada en el 2008, para lo cual se requiere un sistema de información confiable y en tiempo real, considerando las tres dosis de vacuna requeridas.
Para evaluar el cambio sobre los niveles de infección es necesario tener un corte transversal de la prevalencia de infección por HBV y luego evaluar las tasas de infección haciendo otro corte transversal a los tres años de la intervención masiva y también desarrollar vigilancia centinela del síndrome ictérico en establecimientos elegidos en las tres regiones geográficas del Perú. De este modo tendremos la opción de conocer el impacto de las intervenciones que en relación a la HBV se vienen haciendo.
REFERENCIAS BIBLIOGRÁFICAS
1. Lavanchy D. Worldwide epidemiology of HBV infection, disease burden, and vaccine prevention. J Clin Virol. 2005; 34(Suppl 1): S1-3.
2. B arazani Y, Hiatt JR, Tong MJ, Busuttil RW. Chronic viral hepatitis and hepatocellular carcinoma. World J Surg. 2007; 31(6): 1243-48.
3. E chevarría-Mayo JM. Etiología y patogenia de las hepatitis víricas. Enferm Infecc Microbiol Clin. 2006; 24(1): 45-56.
4. Quirós-Roldán E, Torti C, Carosi G. Los nuevo virus de la hepatitis no-A no-E y su efecto patógeno. Med Clin (Barcelona). 2004; 122(14): 552-54.
5. Irshad M, Joshi YK, Sharma Y, Dhar I. Transfusion transmitted virus: a review on its molecular characteristics and role in medicine. World J Gastroenterol. 2006; 12(32): 5122-34.
6. Akiba J, Umemura T, Alter HJ, Kojiro M, Tabor E. SEN virus: epidemiology and characteristics of a transfusion transmitted virus. Transfusion. 2005; 45(7): 1084-88.
7. Sehgal R, Sharma A. Hepatitis G virus (HGV): current perspectives. Indian J Pathol Microbiol. 2002; 45(1): 123- 28.
8. Ribeiro RM, Lo A, Perelson AS. Dynamics of hepatitis B virus infection. Microbes Infect. 2002; 4(8): 829-35.
9. Lai CL, Yuen MF. The natural history of chronic hepatitis B. J Viral Hepatol. 2007; 14(Suppl 1): 6-10.
10. World Health Organization. Hepatitis B fact sheet Nº 204 (revised October 2000). Geneva: WHO; 2000. Disponible en: http://www.who.int/mediacentre/factsheets/fs204/en/index.html
11. Kane A, Lloyd J, Zaffran M, Simonsen L, Kane M. Transmission of hepatitis B, hepatitis C and immunodeficiency viruses through unsafe injections in the developing world: model-base regional estimates. Bull World Health Organ. 1999; 77(10): 801-7.
12. World Health Organization. Expanded Programme on Immunization. Protocol for assessing prevalence of hepatitis B infection in antenatal patients. Geneva: WHO; 1990. WHO/EPI/GEN/90.6
13. Alegre F, Moreno D, Quiroga J. Infección aguda por el VHB. An Sist Sanit Navar. 2004; 27(Suppl 2): 17-25.
14. Chen CJ, Yang HI, Su J, Jen CL, You SL, Lu SN, et al. Risk of hepatocellular carcinoma across a biological gradient of serum hepatitis B virus DNA level. JAMA. 2006; 295(1): 65-73.
15. Iloeje UH, Yang HI, Jen CL, Su J, Wang LY, You SL, et al. Risk and predictors of mortality associated with chronic hepatitis B infection. Clin Gastroenterol Hepatol. 2007; 5(8): 921-31.
16. Ikeda K, Saitoh S, Susuki Y, Kobayashi M, Tsubota A, Koida I, et al. Disease progression and hepatocellular carcinogenesis in patients with chronic viral hepatitis: a prospective observation of 2215 patients. J Hepatol. 1998; 28(6): 930-38.
17. Amin J, O´Connell D, Bartlett M, Tracey E, Kaldor J, Law M, et al. Liver cancer and hepatitis B and C in New South Wales, 1990-2002: a linkage study. Aust N Z J Public Health. 2007; 31(5): 475-82.
18. Amin J, Law MG, Bartlett M, Kaldor JM, Dore GJ. Causes of death after diagnosis of hepatitis B or hepatitis C infection: a large community-based linkage study. Lancet. 2006; 368: 938-45.
19. Szmuness W. Hepatocellular carcinoma and the hepatitis virus: evidence for a causal association. Prog Med Virol. 1978; 24: 40-69.
20. Kew MC. The development of hepatocellular cancer in humans. Cancer Surv. 1986; 5: 719-39.
21. B rown ML, Goldie SJ, Draisma G, Harford J, Lipscomb J. Health service interventions for cancer control in developing countries in: priorities in developing countries. In: Jamison DT, Breman JG, Measham AR, Alleyne G, Claeson M, Evans DB, et al (editors). Diseases control priorities in developing countries. 2nd ed. New York: Oxford University Press; 2006.
22. Ferlay J, Bray F, Pisani P, Parkin DM. GLOBOCAN 2000: Cancer incidence, mortality, and prevalence worldwide, Version 1.0, IARC Cancer Base Nº 5. Lyon: IARC Press; 2001.
23. Cabezas C, Miranda J. A 38 year evaluation of death causes related to liver diseases in Huanta – Peru. Am J Trop Med Hyg. 1999; 61(Suppl 3): 370.
24. Indacochea S, Gotuzzo E, De la Fuente J, Phillips I, Whignal S. Elevada prevalencia de marcadores de hepatitis B y Delta en el valle interandino de Abancay. Rev Med Hered. 1991; 2(4): 168-72.
25. Maynard JE, Kane MA, Hadler SC. Global Control of hepatitis B vaccine in the Expanded Programme on Immunization. Rev Infect Dis. 1989, 2(Suppl 3): S574-75.
26. B easley RP, Hwang LY, Lin CC, Chien CS. Hepatocellular carcinoma and hepatitis B virus. A prospective study of 22 707 men in Taiwan. Lancet. 1981; 2: 1129-33.
27. Cabezas C. Hepatitis virales B y Delta: epidemiología y prevención en el Perú. Rev Peru Med Exp Salud Publica. 2002; 19(3): 150-61.
28. Szmuness W, Harley EJ, Ikran H, Stevens CE. Sociodemographic aspects of the epidemiology of hepatitis B. In: Vyas GN, Cohen SN, Schmid R, eds. Viral Hepatitis. Philadelphia: Franklin Institute Press; 1978. p. 279-320.
29. Paraná R, Almeida D. HBV epidemiology in Latin America. J Clin Virol. 2005; 34(Suppl 1): S130-33.
30. E chevarría JM, León P. Epidemiology of viruses causing chronic hepatitis among populations from the Amazon Basin and related ecosystems. Cad Saude Publica. 2003; 19(6): 1583-91.
31. H sieh TH, Liu CJ, Chen DS, Chen PJ. Natural course and treatment of hepatitis D virus infection. J Formos Med Assoc. 2006; 105(11): 869-91.
32. B ensabath G, Hadler SC, Soares MC, Fields H, Maynard JE. Epidemiologic and serologic studies of acute viral hepatitis in Brazils Amazon Basin. Bull Pan Am Health Organ. 1987; 21(1): 16-27.
33. Tanaka T, Nagai M, Yoshihara S, Imai S, Ishiguro H, Seto S, et al. Changing pattern of age specific prevalence of hepatitis B surface antigen and corresponding antibody in Japan. Am J Epidemiol. 1986; 124(3): 368-71.
34. Arico S, Aragona M, Rizzetto M, Caredda F, Zanetti A, Marinucci G, et al. Clinical significance of antibody to the hepatitis delta virus in symptomless HBsAg carriers. Lancet. 1985; 2: 356-58.
35. Méndez M, Arce M, Kruger H, Sánchez S. Prevalencia de marcadores serológicos de hepatitis vírica en diversos grupos de población del Perú. Bol Oficina Sanit Panam. 1989; 106(2): 127-38.
36. Vildósola H, Farfán G, Colan E, Delgado G, Mendoza L, Pineda R, et al. Prevalencia del antígeno de superficie del virus de hepatitis B en población general de costa sierra y selva del Perú. Reporte preliminar. Rev Gastroenterol Peru. 1990; 10(3): 96-101.
37. Ruiz R, Jaimes A, Montejo G, Hinostroza-Sjogren M. Marcadores serológicos de hepatitis viral en la región amazónica del Perú estudio de una población representativa. Diagnóstico (Perú). 1989; 24(1/2): 5-9.
38. Vildózola H, Bazul V, Cambillo E, Torres J, Flores ME, Ramos E. Prevalencia de la infección y factores de riesgo para hepatitis B en dos grupos de gestantes adolescentes en relación al número de parejas sexuales. Rev Gastroenterol Peru. 2006; 26(3): 242-58.
39. Chang J, Zavaleta A, Phillips I. Seroepidemiología de hepatitis B en cuatro comunidades de la selva central del Perú. Rev Med Exp. 1997; 14(1): 34-39.
40. Cabezas C, Suarez M, Romero G, Carrillo C, García MP, Reátegui J, et al. Hiperendemicidad de hepatitis viral B y delta en pueblos indígenas de la Amazonía peruana. Rev Peru Med Exp Salud Publica. 2006; 23(2): 114-22.
41. Colichón A. Distribución seroepidemiológica de la hepatitis B y hepatitis delta en diferentes comunidades indígenas de la selva peruana. [Tesis doctoral] Lima: Facultad de Medicina, Universidad Peruana Cayetano Heredia; 1989.
42. Cabezas C, Anaya E, Bartalesi F, Sánchez J. Transmisión horizontal de hepatitis viral B en población desplazada de un área hiperendémica a sus contactos en un área de baja endemicidad del Perú. Rev Gastroenterol Perú. 1997; 17(2): 128-34.
43. Cabezas C, Ramos F, Sánchez J. Elevada prevalencia de infección por virus de la hepatitis B y delta en población infantil de Huanta-Ayacucho. IX Triennial International Symposium on viral hepatitis and liver disease. 1996 April 21-25. Rome, Italy.
44. Segovia G, Galván K, Garcia V, Huamaní L, Gotuzzo E. Prevalencia de marcadores sexológicos de hepattiis B y delta y transmisión intrafamiliar en el Valle del Río Pampas, Perú. Rev Peru Med Exp Salud Publica. 2002; 19(2): 57-62.
45. H idalgo H, Reategui G, Rada A. Prevalencia de hepatitis viral A y B y factores de riesgo asociados a su infección en población escolar de un distrito de Huánuco, Perú. Rev Peru Med Exp Salud Publica. 2002; 19(1): 5-9.
46. Cabezas C, Gotuzzo E, Escamilla J, Phillips I. Prevalencia de marcadores serológicos de hepatitis viral A, B y delta en escolares aparentemente sanos de Huanta (Perú). Rev Gastroenterol Peru. 1994; 14(2):123-34.
47. Madelengoitia J, Ishida N, Umenay T, Miyamoto T, Mejia J, Flores W, et al. The prevalence of hepatitis B antigen among hepatitis patients and residents of Peru. Bull Pan Am Health Organ. 1975; 9(2): 142-47.
48. Alter HJ, Holland PV, Purcell RH, Lander JJ, Feinstone SM, Morrow AG, et al. Posttransfusion hepatitis after exclusion of commercial and hepatitis B antigen-positive donors. Ann Intern Med. 1972; 77(5): 691-99.
49. Lok ASF, Lai CL, Wu PC. Prevalence of isolated antibody to hepatitis B core antigen in an area endemic for hepatitis B virus infection: implication in hepatitis B vaccination programs. Hepatology. 1988; 8(4): 766-70.
50. McMahon BJ, Parkinson AJ, Helminiak C, Wainwright RB, Bulkow L, Kellerman-Douglas A, et al. Response to hepatitis B vaccine of persons positive for antibody to hepatitis B core antigen. Gastroenterology. 1992; 103(2): 590-94.
51. Preiksaitis JK, Rivet C. A history of the evolution of hepatitis C testing of blood donors: implications for the Canadian blood supply system. Transfusion. 1995; 35(4): 348-52.
52. Chung HT, Lee STK, Lok AS. Prevention of posttransfusion hepatitis B and C by screening for antibody to hepatitis C virus and antibody to HBcAg. Hepatology. 1993; 18(5): 1045-49.
53. Fuentes Rivera J, Roca V O, Maldonado F, Guillen M. Seroprevalencia de enfermedades hemotransmisibles en donantes de sangre. Rev Peru Enf Infec Trop. 2002; 2: 12- 20.
54. Neaigus A, Gyarmanthy VA, Millar M, Frajzyngier V, Zhao M, Friedman SR, et al. Injecting and sexual risk correlates of HBV and HVC seroprevalence among new drug injectors. Drug Alcohol Depend. 2007; 89(2-3): 234- 43.
55. Alter MJ, Hadler SC, Margolis HS, Alexander WJ; Hu PY, Judson FN, et al. The changing epidemiology of hepatitis B in the United States. Need for alternative vaccination strategies. JAMA. 1990; 263(9):1218-22.
56. Figueroa R, Rolando N, Zumaeta E, Soriano C, Padron A. Marcadores serológicos de hepatitis viral en personal hospitalario de alto riesgo. Rev Gastroenterol Peru. 1984;
57. Colichón A, Slava M, Cantella R, Campomanes E. Estudio de marcadores de hepatitis B en meretrices registradas en el Hospital Regional base docente en Trujillo (Perú). Diagnóstico (Perú). 1986; 17(3): 60-63.
58. Vildósola H, Colichón A, Bardales F, Serván JC. Prevalencia de marcadores serológicos de hepatitis B en personal de salud y administrativo de un hospital general de la selva del Perú. Rev Gastroenterol Peru. 1989; 9(2): 77-82.
59. Paucar J, Solano R, Crespo N, Saavedra R, Leon C, Morales N. Estudio de marcadores serológicos de hepatitis B en personal hospitalario. Rev Serv Sanid Fuerzas Polic. 1989; 50(1): 10-17.
60. Valladares GB, Galarza L, Espinoza J, Nieri A, Makino R, Berrocal A, et al. Determinación de marcadores serológicos del virus de la hepatitis B en áreas de alto riesgo del Hospital Central Fuerzas Aéreas del Perú. Rev Gastroenterol Peru. 1989; 9(1): 13-16.
61. Deville J, Llanos A, Campos M, Phillips I, Gotuzzo E, Kilpatrick M. Factores de riesgo para infección por virus de hepatitis B en personal hospitalario. Rev Gastroenterol Peru. 1989; 9(1): 24-28.
62. Farfán G, Vidal J, Phillips IA, Llerena S. Marcadores serológicos de hepatitis viral B en pacientes drogadictos del hospital Hermilio Valdizán, Lima, Perú. Psicoactiva. 1989; 3(1): 61-74.
63. Colichón A, Cantella R, Romero J, Slava ME. Prevalencia de hepatitis viral B en un grupo de meretrices residentes en Chimbote (Perú). Rev Gastroenterol Peru. 1990; 10(1): 21- 26.
64. H yams KC, Phillips IA, Tejada A, Li O, Hermoza P, Lopez F, et al. Hepatitis B in a highly active prostitute population: evidence for a low risk of chronic antigenemia. J Infect Dis. 1990; 162(2): 295-98.
65. B ussalleu A, Cieza J, Colichón A, Berrios J. Prevalencia de hepatitis viral tipo B en pacientes y personal de tres unidades de hemodiálisis en Lima. Rev Med Hered. 1991; 2(4): 160-67.
66. Mejía P. Exposición ocupacional al virus de la hepatitis B del personal hospitalario del Centro Médico Naval Cirujano Mayor Santiago Távara. [Tesis de bachiller] Lima: Facultad de Medicina, Universidad Peruana Cayetano Heredia; 1992.
67. Muñoz D, Trujillo L, Gotuzzo E, Nizama M, Watts D. Prácticas sexuales de riesgo y seroprevalencia de infección por VIH-1, HTLV-1, sífilis y hepatitis B en varones drogadictos no endovenosos de Lima. Rev Med Hered. 1997; 8(3): 92-103.
68. Loza C, Depaz M, Suarez M, Loza R, Valenzuela R, Valenzuela J, et al. Frecuencia de marcadores serológicos de hepatitis viral B y C en pacientes que ingresan por primera vez al programa de hemodiálisis en el Hospital Cayetano Heredia. Rev Gastroenterol Peru. 2005; 25(4): 320-27.
69. Laguna-Torres VA, Pérez-Bao J, Chauca G, Sovero M, Blichtein D, Chunga A, et al. Epidemiology of transfusiontransmitted infections among multi-transfused patients in seven hospitals in Peru. J Clin Virol. 2005; 34(Suppl 2): s61-68.
70. Agurto H, Lama J, Suarez L, Montano S, Chauca G, Sanchez JL, et al. Epidemiología y factores de riesgo asociado para HBsAg entre hombres que tienen sexo con hombres en el Perú. En: X Congreso Peruano de Enfermedades Infecciosas y Tropicales. Lima: Sociedad Peruana de Enfermedades Infecciosas y Tropicales; 2007.
71. Centers for Disease Control and Prevention. Prevention of perinatal hepatitis B through enhanced case management- -Connecticut, 1994–95, and the United States, 1994. MMWR Morb Mortal Wkly Re. 1996; 45(27): 584-87.
72. Wong VC, Ip HM, Reesink HW, Lelie PN, Reerink-Brongers EE, Yeung CY, et al. Prevention of the HBsAg carrier state in newborn infants of mothers who are chronic carriers of HBsAg and HBeAg by administration of hepatitis-B vaccine and hepatitis-B immunoglobulin. Double-blind randomised placebo-controlled study. Lancet. 1984; 1: 921-26.
73. Lees SD, Lo KJ, Tsai YT, Wu JC, Wu TC, Yang ZL, et al. Role of caesarean section in prevention of mother-infant transmission of hepatitis B virus. Lancet. 1988; 2: 833-34.
74. B easley RP, Stevens CE, Shiao IS, Meng HC. Evidence against breast-feeding as a mechanism for vertical transmission of hepatitis B. Lancet. 1975; 2: 740-41.
75. Chang MH, Chen CJ, Lai MS, Hsu HM, Wu TC, Kong MS, et al. Universal hepatitis B vaccination in Taiwan and the incidence of hepatocellular carcinoma in children. Taiwan Childhood Hepatoma Study Group. N Engl J Med. 1997; 336(26): 1855-59.
76. Cabezas C, Romero Y, Parihuaman R, Suarez M. Bajo riesgo de transmisión vertical del virus de la hepatitis B en un área hiperendémica del Perú. Bol Soc Peru Enf Inf Trop. 1997; 6: 5.
77. Vásquez S, Cabezas C, García B, Torres R, Larrabure G, Suarez M, et al. Prevalencia de portadores de HBsAg y anti-HBs en gestantes residentes en áreas de diferente endemicidad de HVB en departamentos del Centro-Sur del Perú. Rev Gastroenterol Peru. 1999; 19(2): 23-27.
78. Gerberding JL. The infected health care provider. N Eng J Med. 1996; 334: 594-95.
79. Gerberding JL. Incidence and prevalence of human immunodeficiency virus, hepatitis B virus, hepatitis C virus, and citomegalovirus among health care personnel at risk for blood exposure: Final report from a longitudinal study. J Infect Dis. 1994; 170(6): 1410-17.
80. Mast EE, Alter MJ. Prevention of hepatitis B virus infection among health care workers. En: Ellis RW, ed. Hepatitis B vaccines in clinical practice. New York: Marcel Dekker; 1993. p. 295-307.
81. Grady GF, Kane MA. Hepatitis B infections accounts for multi-million dollar loss. Hosp Infect Control. 1981; 8(5): 60- 62.
82. Gibas A, Blewett DR, Schoenfeld DA, Dienstag JL. Prevalence and incidence of viral hepatitis in health workers in the prehepatitis vaccination era. Am J Epidemiol. 1992; 136(5): 603-10.
83. Snydman DR, Muñoz A, Werner BG, Polk BF, Craven DE, Platt R, et al. A multivariate analysis of risk factors for hepatitis B virus infection among hospital employees screened for vaccination. Am J Epidemiol. 1984; 120(5): 684-93.
84. Romero G. Prevalencia de marcadores serológicos de HBV en trabajadores de salud y profesores de Huanta (Perú). [Tesis para optar el grado de Biólogo]. Ayacucho: Universidad Nacional San Cristóbal de Huamanga; 1997.
85. Diaz LA, Afanador LP. Riesgo de infección por hepatitis B entre estudiantes de medicina peruanos luego de exposición a sangre y fluidos corporales. Rev Gastroenterol Peru. 2003; 23(2): 107-10.
86. H oft RH, Pflugfelder SC, Forster RK, Ullman S, Polack FM, Schiff ER. Clinical evidence for hepatitis B transmission resulting from corneal transplantation. Cornea. 1997; 16(2): 132-37.
87. Turner DP, Zuckerman M, Alexander GJ, Waite J, Wreghitt T. Risk of inappropriate exclusion of organ donors by introduction of hepatitis B core antibody testing. Transplantation 1997; 63(5): 775-77.
88. Caldwell SH. Hard times and imperfect organs. Liver Transplant Surg. 1997; 3(2):181-84.
89. Wachs ME, Amend WJ, Ascher NL, Bretan PN, Emond J, Lake JR, et al. The risk of transmission of hepatitis B from HBsAg(-), HBcAb(+), HBIgM(-) organ donors. Transplantation. 1995; 59(2): 230-34.
90. Davis LG, Weber DJ, Lemon SM. Horizontal transmission of hepatitis B virus. Lancet. 1989; 1(8643): 889-93.
91. Karayiannis P, Novick DM, Lok AS, Fowler MJ, Monjardino J, Thomas HC. Hepatitis B virus DNA in saliva, urine, and seminal fluid of carriers of hepatitis B e antigen. Br Med J. 1985; 290: 1853-55.
92. Scott RM, Snitban R, Bancroft WH, Alter HJ, Tingpalapong M. Experimental transmission of hepatitis B virus by semen and saliva. J Infect Dis. 1980; 142(1): 67-71.
93. B ancroft WH, Snitbhan R, Scott RM, Tingpalapong M, Watson WT, Tanticharoenyos P, et al. Transmission of hepatitis B virus to gibbons by exposure to human saliva containing hepatitis B surface antigen. J Infect Dis. 1977; 135(1): 79-85.
94. Cabezas C. Miranda JJ, Romero G, Suarez M, Samlvides F, Echevarria J, et al. Factores de riesgo asociados a la transmisión de hepatitis B en población militar destacada al departamento de Amazonas, Perú. Rev Peru Med Exp Salud Publica. 2007; 24(4): 370-77.
95. Cohen J, Mandolesi JF, Laszlo M, Illanes L. Triatoma infestans como vector del virus de la hepatitis B. Acta Gastroenterol Latinoam. 191; 11(1): 215-23.
96. Chen CC, Shou L, Hwang LL, Tang P, Tu WC, Lo HS. Persistence of hepatitis B viral antigens in Culex quinquefasciatus. Southeast Asian J Trop Med Public Health. 1987; 18(1): 44-51.
97. B low JA, Turrell MJ, Silverman AL, Walker ED. Stercorarial shedding and transtadial transmission of hepatitis B virus by common bed bugs. (Hemiptera: Cimicidae). J Med Entomol. 2001; 38(5): 694-700.
98. Silverman AL, Qu LH, Blow J, Zitron IM, Gordon SC, Walker ED. Assessment of hepatitis B virus DNA and hepatitis C virus RNA in the common bedbug (Cimex lectularius L.) and kissing bug (Rodnius prolixus). Am J Gastroenterol. 2001; 96(7): 2194-98.
99. B low JA, Turrel MJ, Walker ED, Silverman AL. Postbloodmeal diuretic shedding of hepatitis B virus by mosquitoes (Diptera: Culicidae). J Med Entomol. 2002; 39(4): 605-12.
100. Casey JL, Niro GA, Engle RE, Vega A, Gómez H, McCarthy M, et al. Hepatitis B virus (HBV)/hepatitis D virus (HDV) coinfection in outbreaks of acute hepatitis in the Peruvian Amazon basin: the roles of HDV genotype III and HBV genotype F. J Infect Dis. 1996; 174(5):920-26.
101. Pearce N, Milne A, Moyes C. Hepatitis B virus: the importance of age at infection. N Z Med J. 1988; 101(858): 788-90.
102. McMahon BJ, Alward WL, Hall DB, Heyward WL, Bender TR, Francis DP, et al. Acute hepatitis B virus infection: relation of age to the clinical expression of disease and subsequent development of the carrier state. J Infect Dis. 1985; 151(4): 599-603.
103. H oofnagle JH, Dusheiko GM, Seeff LB, JonesEA, Waggoner JG, Bales ZB. Seroconversion from hepatitis B e antigen to antibody in chronic type B hepatitis. Ann Intern Med. 1981; 94(6): 744-48.
104. Realdi G, Alberti A, Rugge M, Bortolotti F, Rigoli AM, Tremolada F, et al. Seroconversion from hepatitis B e antigen to anti-HBe in chronic hepatitis B virus infection. Gastroenterology. 1980; 79(2): 195-99.
105. Lok ASF, Lai CL. A longitudinal follow-up of asymptomatic hepatitis B surface antigenpositive Chinese children. Hepatology. 1988; 8(5):1130-33.
106. Smedile A, Farci P, Verme G, Caredda F, Cargnel A, Caporaso N, et al. Influence of delta infection on severity of hepatitis B. Lancet. 1982; 2: 945-47.
107. Lettau LA, McCarthy JG, Smith MH, Hadler SC, Morse LJ, Ukena, et al. Outbreak of severe hepatitis due to delta and hepatitis B viruses in parenteral drug abusers and their contacts. N Engl J Med. 1987; 317(20):1256-62.
108. Pastore G, Monno L, Santantonio T, Angarno G, Milella M, Giannelli A, Fiore JR, et al. Hepatitis B virus clearance from serum and the liver after acute hepatitis delta virus superinfection in chronic HBsAg carriers. J Med Virol. 1990; 31(4): 284-90.
109. Lok AS, Lindsay I, Scheuer J, Thomas HC. Clinical and histological features of delta infection in chronic hepatitis B virus carriers. J Clin Patho.l 1985; 38(5): 530-33.
110. Fattovich G, Boscaro S, Noventa F, Pornaro E, Stenico D, Alberti A, et al. Influence of hepatitis delta virus infection on progression to cirrhosis in chronic hepatitis type B. J Infect Dis. 1987; 155(5): 931-35.
111. Murray CJ, Lopez AD. Mortality by cause for eight regions of the world: global burden of disease study. Lancet. 1997; 349: 1269-76.
112. Parkin DM, Bray F, Ferlay J, Pisani P. Global cancer statistics, 2002. CA Cancer J Clin. 2005; 55(2):74-108.
113. Pisani P, Parkin DM, Bray F, Ferlay J. Estimates of the worldwide mortality from 25 major cancers in 1990. Int J Cancer. 1999; 83(1): 18-29.
114. Rustgi VK. Epidemiology of hepatocellular carcinoma. Gastroenterol Clin North Am. 1987; 16(4): 545-51.
115. B easley RP. Hepatitis B virus. The major etiology of hepatocellular carcinoma. Cancer. 1988; 61(10): 1942-56.
116. Arce R; León J, Cuellar L. Antígeno de superficie del virus de la hepatitis B causantes del hepatocarcinoma. Rev Gastroenterol Peru 1986; 6(1): 35-45.
117. García F, Antunez de Manolo E, Morales M. Determinación del antígeno de superficie del virus de la hepatitis B por inmunoperoxidasa en un grupo de biopsias de cirrosis hepáticas. Rev Gastroenterol Peru. 2000; 20(2): 134-39.
118. B ueno H, Indacochea S, Oberst R, Chauca G. Rol de los virus de hepatitis B y delta en la etiología del hepatocarcinoma y otras hepatopatías crónicas. Rev Gastroenterol Peru. 1994; 14(2): 135-39.
119. Ruiz E, Almonte M, Pizarro R, Celis J, Montalbeti J, Urbano R. Infección con virus de la hepatitis B y hepatitis C como factores de riesgo para hepatocarcinoma en el Perú: estudio casos y controles. Rev Gastroenterol Peru. 1998; 18(3): 199-212.
120. Donayre M, Bussalleau A, Berrios J, Cok J. Carcinoma primario de hígado en el Hospital Nacional Cayetano Heredia (Enero 1969-Abril 1997): Hallazgos clínicos y de laboratorio. Rev Gastroenterol Peru. 1999; 19(1):15-25.
121. B arham WB, Figueroa R, Phillips IA, Hyams KC. Chronic liver disease in Peru: role of viral hepatitis. J Med Virol. 1994; 42(2): 129-32.
122. Zhao S, Xu Z, Lu Y. A mathematical model of hepatitis B virus transmission and its application for vaccination strategy in China. Int J Epidemiol. 2000; 29(4): 744-52.
123. Zhiqiang G, Zhaohui D, Qinhuan W, Dexian C, Yunyun F, Hongtao L, et al. Cost of chronic hepatitis B infection in China. J Clin Gastroenterol. 2004; 38 (10 Suppl) S175-78.
124. Walker D, Mosqueira NR, Penny ME, Lanata CF, Clark AD, Sanderson CF, et al. Variation in the costs of delivering routine immunization services in Peru. Bull World Health Organ. 2004; 82(9): 676-82.
125. Cabezas C, Echevarria C, Gómez G, Gotuzzo E. Programa piloto de inmunizacion contra hepatitis viral B, integrado al Programa Ampliado de Inmunización (PAI) en Abancay (Perú). Rev Gastroenterol Peru. 1995; 15(3): 215-22.
126. Cabezas C, Ramos F, Vega M, Suárez M, Romero G, Carrillo C, et al. Impacto del programa de vacunación contra hepatitis B integrado al PAI en Huanta Perú 1994- 1997. Rev Gastroenterol Peru. 2000; 20(3): 201- 12.
127. Perú, Ministerio de Salud. Control de la hepatitis viral B en el Perú: conclusiones y recomendaciones de la Comisión Encargada por RM: 633-95- SA/DM. Lima: MINSA; 1995.
128. Vildozola H. Vacunación contra hepatitis B: veinte años después. Rev Gastroenterol Peru. 2007; 27(1): 57-66.
129. Vildósola H. Impacto de la vacunación contra la hepatitis B, sobre la tasa de hepatitis aguda, portadores crónicos y hepatocarcinoma. Rev Gastroenterol Peru. 2000; 20(4)
Correspondencia. Dr. César Cabezas Sánchez. Instituto Nacional de Salud. Lima, Perú.
Dirección: Cápac Yupanqui 1400, Lima 11.
Teléfono: (511) 4719920
Correo electrónico: ccabezas@ins.gob.pe