Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Medicina Experimental y Salud Publica
versión impresa ISSN 1726-4634
Rev. perú. med. exp. salud publica v.25 n.3 Lima jul./set. 2008
Actividad antimicótica in vitro y metabolitos del aceite esencial de las hojas de Minthostachys Mollis (muña)
In vitro antifungal activity and metabolites of the essential oil of minthostachys mollis (muña) leaves
Carlos Cano1,a, Pablo Bonilla1,a, Mirtha Roque2,b, Julio Ruiz2,b
1 Instituto de Ciencias Farmacéuticas y Recursos Naturales Juan de Dios Guevara, Facultad de Farmacia y Bioquímica, Universidad Nacional Mayor de San Marcos. Lima, Perú.
RESUMEN
Objetivos. Demostrar la actividad antimicótica in vitro y la elucidación de algunos de los metabolitos del aceite esencial de hojas de Minthostachys mollis (muña) proveniente del distrito de Huacrapuquio (2700 msnm), Junín. Materiales y métodos. El aceite esencial se obtuvo por el método de destilación por arrastre de vapor de agua. Este fue sometido a análisis físico-químico y determinación de la composición química mediante cromatografía de gases. Mediante el método de agar en difusión se evaluó la inhibición del crecimiento fúngico de Candida albicans y también por el método de dilución en tubo para Trichophytun tonsurans, Trichophytun mentagrophytes, Microsporun canis. Resultados. Se encontraron los siguientes monoterpenos: pulegona, mentona, limoneno y mirceno. El aceite esencial de muña inhibió completamente el desarrollo de T. tonsurasn, T. mentagrophytes y M. canis con ambos métodos de evaluación y dosis, para C. albicans se logró un halo de inhibición de 30 mm para el aceite esencial al 100% y de 35 mm al 50%. Conclusiones. Se demostró la actividad antimicótica del aceite esencial de muña, probablemente por la acción de los monoterpenos encontrados.
Palabras clave. Fitoterapia; Aceites volátiles; Dermatofitos; Monoterpenos (fuente: DeCS BIREME).
ABSTRACT
Objectives. Demonstrate the antifungal activity in vitro and elucidation of some metabolites of the essential oil of Minthostachys mollis (muña) leaves from the Huacrapuquio district (2700 m), Junín (Central Peruvian Andes). Material and methods. The essential oil was obtained by the distillation method by drag of water vapor. This was performed to physical-chemical analysis and identification of the chemical composition by gas chromatography. By agar diffusion method was evaluated inhibition of fungal growth of Candida albicans and by tube dilution method to Trichophytun tonsurans Trichophytun mentagrophytes and Microsporun canis. Results. The following monoterpenes were found: pulegone, menthone, limoneno and myrcene. The muña essential oil completely inhibited T. tonsurasn, T. mentagrophytes and M. canis with both evaluation methods and doses, to C. albicans was a inhibition zone diameters of 30 mm for the essential oil to 100 % and 35 mm to 50%. Conclusions. We showed the antifungal activity of muña essential oil, probably by the action of the monoterpenes found.
Key words: Phytotherapy; Oils; volatile; Dermatophytes; Monoterpenes (source: MesH NLM).
INTRODUCCIÓN
El Perú presenta una riqueza y megadiversidad de plantas medicinales nativas, que es uno de los pilares de la etnofarmacología y la medicina tradicional, desde la época del Incanato hasta la actualidad. Siendo estas utilizadas en forma empírica por sus bondades terapéuticas en el cuidado y restauración de la salud (1).
Dentro de este contexto, los aceites esenciales (AE) son productos naturales de gran valor e importancia económica (2). La bioactividad de los AE se investiga a partir de los efectos farmacológicos que son producidos por sus metabolitos, los cuales son obtenidos por diferentes técnicas fisicoquímicas a partir de las hojas (3).
Son pocas las plantas peruanas que han validado su uso tradicional, una de estas es la Minthostachys mollis, conocida popularmente como muña, la cual es usada para el tratamiento de dolencias de vias respiratorias y digestivas (4). La muña habita en los diferentes pisos ecológicos de nuestra serranía, crece entre 2500 y 3500 msnm, donde existe en abundancia. Es una planta hemicriptófila que durante el invierno –frío y seco– desaparecen sus hojas para brotar nuevamente con las primeras lluvias de la primavera (5).
Diversos estudios han mostrado su efecto antibacteriano (5-7) e insecticida (8), otros han explorado que metabolitos están presentes en su aceite esencial (9-11). Sin embargo, poco se ha explorado sobre su efecto antimicótico, lo cual fue objeto de nuestro estudio.
MATERIALES Y MÉTODOS
RECOLECCIÓN DE LA MUESTRA
La planta fue recolectada entre septiembre y octubre del 2005 (período de floración) en el distrito de Huacrapuquio (2700 msnm), ubicado a 10 km al sur de la provincia de Tarma, departamento de Junín; fueron cortadas con una hoz a unos 10 cm por encima de la superficie del suelo de las laderas de los cerros y zonas pedregosas. Luego se separaron las hojas y fueron estabilizadas por 24 horas. La muestra fue reconocida como Minthostachys mollis (Kunt/rises) según el sistema de clasificación de Engler & Prantil modificado por Melchor por el Museo de Historia Natural de la Universidad Nacional Mayor de San Marcos (UNMSM) en Lima, Perú.
EXTRACCIÓN DEL ACEITE ESENCIAL
La extracción del aceite esencial de muña se realizó con el método de arrastre con vapor de agua (3,5) en el Laboratorio de Química Orgánica de la Facultad de Química de la Universidad Nacional de Ingeniería (Lima, Perú) en noviembre de 2005, obteniéndose 21 mL de aceite esencial después de procesar 10 kg de muña.
Para ello se colocó 1,5 kg de muña en cada canastilla de una autoclave, asegurando que no esté en contacto directo con el agua; luego, se calentó hasta el desprendimiento de vapor de agua conteniendo el aceite esencial a través de los refrigerantes de vidrio, siendo recolectados en una pera de decantación; se dejó en reposo hasta observar la separación del agua y del aceite, procediéndose luego a su decantación. El aceite obtenido fue sometido a desecación con sulfato de sodio anhidro; luego fue filtrado con ayuda de una bomba de vacío, finalmente el aceite se depositó en frasco oscuro cerrado herméticamente que fue almacenado en refrigeración hasta su uso.
ANÁLISIS CROMATOGRÁFICO DE GASES
El aceite esencial obtenido fue analizado en marzo de 2006 en el Laboratorio de Investigación y Química Aplicada de la Facultad de Ingeniería Química de la Universidad Nacional de Ingeniería, por cromatografía de gases, basado en el tiempo de retención de algunos de los componentes, luego mediante estándares conocidos se determinó la composición cuali-cuanti centesimal de cuatro monoterpenos (limoneno, mentona, pulegona y mentol) del aceite esencial de la muña.
DETERMINACIÓN IN VITRO DE LA ACTIVIDAD ANTIFÚNGICA DEL ACEITE ESENCIAL DE Minthostachys mollis
Se usó cepas de Microsporum canis, Trichophyton mentagrophytes, Trichophyton tonsurans obtenidas de muestras clínicas y proporcionadas por el Departamento de Micología del Instituto de Medicina Tropical Daniel A. Carrión de la UNMSM; así como la cepa Candida albicans ATCC 32148 proporcionada por el Instituto de Microbiología Simón Pérez Alva de la Facultad de Farmacia y Bioquímica de la UNMSM.
Agar en difusión (6). Con este método se ensayaron las cuatro cepas fúngicas. Se usó 20 ML de agar dextrosa Sabouraud fundido a 45 ºC que fueron asépticamente mezclados con 1 mL de la suspensión fúngica (1 x 104 UFC/mL) en placas petri de 100 mm x 15 mm. Luego se hizo pozos de 11 mm de diámetro donde se inoculó 0,1 mL del aceite esencial de muña (al 50 ó 100% según correspondía). Se dejó reposar por 30 minutos a temperatura ambiente y se incubó a 28 ºC de 14 a 21 días según el hongo en evaluación, luego se realizó la lectura, registrando el diámetro de los halos de inhibición. Las pruebas se realizaron por triplicado y con un grupo control (alcohol).
Dilución en tubo (12,13). Con este método se ensayaron las cepas de M. canis, T. mentagrophytes y T. tonsurans. Se usó el agar selectivo para dermatofitos (DTM) según la fórmula de Taplin. Se prepararon las suspensiones de los dermatofitos a partir de la mezcla resultante de conidias y fragmentos hifales de cultivos obtenidos en cultivos previos, que fueron mezclados con 10 mL de agua destilada, se les separó de las partículas pesadas por sedimentación y fueron homogeneizadas con un mezclador de vértice. Su densidad fue ajustada con un espectrofotómetro en una longitud de onda de 530 nm para obtener inóculos estandartizados (0,6 a 3 x 106 UFC/mL). Las diluciones se prepararon usando 5 y 50 μL del aceite esencial de muña diluido en 10 mL del agar DTM fundido e inoculado con el dermatofito de prueba. La lectura de la prueba fue medida según la presencia o ausencia del crecimiento de los hongos. Las pruebas se realizaron por triplicado y con un grupo control (alcohol).
RESULTADOS
CARACTERÍSTICAS Y METABOLITOS DEL ACEITE ESENCIAL DE MUÑA
El rendimiento del proceso de extracción del aceite esencial de muña por el método de arrastre con vapor de agua, fue de 0,19% p/p. Las características organolépticas y propiedades fisicoquímicas se detallan en la tabla 1. Por el análisis de cromatografía de gases se encontró en mayor proporción pulegona, luego mentona y limoneno, sin encontrarse mentol (Tabla 2).
ACTIVIDAD ANTIMICÓTICA
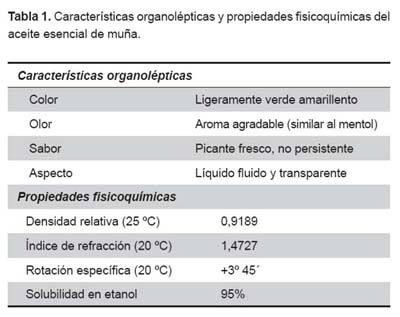
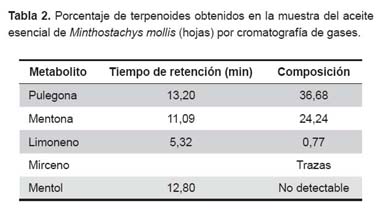
C. albicans. Se observó un halo inhibitorio de 30 mm con el aceite esencial de muña al 100% y de 35 mm al 50%. No se observó halo en las placas control.
T. tonsurans, M canis y T. mentagrophytes. No se observó crecimiento fúngico en todo el diámetro de las placas con aceite esencial de muña al 50 y 100% para todos los dermatofitos ensayados con la prueba de difusión de agar. Las placas controles no presentaron halo inhibitorio. Para la prueba de dilución en tubo no se evidenció crecimiento en ambas dosis (5 y 50 μL) para todos los dermatofitos (Figura 1).
DISCUSIÓN
Por los resultados de la densidad y el índice de refracción del aceite esencial de muña podría preverse que esté conformado por sustancias oxigenadas aromáticas o alicíclicas (9,13), resultados que fueron corroborados por la cromatografía de gases identificando principalmente tres monoterpenos: pulegona, mentona y limoneno que han sido previamente identificados en otros estudios (10,11).
El aceite esencial de muña presentó efectos antimicóticos frente a cepas de Candida albicans a las concentraciones de 50 y 100% y frente a los dermatofitos: (Microsporum canis, Trichophyton mentagrophytes y Trichophyton tonsurans) son sensibles también en los volúmenes ensayados de 5 y 50 μL.
Se reconoce que los AE dependen de sus propiedades lipofílicas o hidrofílicas. Los terpenoides pueden servir como un ejemplo de agentes liposolubles, los cuales afectan la actividad de las enzimas catalizadoras a nivel de membrana, por ej. ciertos componentes del AE pueden actuar como desacopladores, los cuales interfieren en la translocación de protones sobre la membrana y subsecuentemente interrumpir por la fosforilación del ADP (14).
En la acción antimicótica de los metabolitos secundarios, interviene el carácter lipofílico e hidrofílico de sus grupos funcionales y a la polaridad que poseen, para poder tener propiedades antisépticas, antimicrobianas y antimicóticas, siendo esta actividad biológica de mayor a menor en fenoles, aldehídos, cetonas, alcoholes y éteres. Los esfuerzos para encontrar una correlación entre la composición y bioactividad de los aceites esenciales no han sido totalmente dilucidadas. Se presume que la actividad biológica de estos AE no esta determinada por la cantidad de monoterpenos, sino más bien por su tasa de proporcionalidad (14,15).
Se han reportado que algunos aceites esenciales pueden ser más efectivos que los agentes sintéticos (antimicóticos) (15,16), aspecto que podría ser motivo de una futura investigación, comparando el AE de muña frente a antimicóticos comerciales incluyendo un mayor número de repeticiones por ensayo.
La naturaleza es, y seguirá siendo la fuente de una amplia variedad de moléculas bioactivas que podrían ser utilizadas como base para el diseño y la formulación de nuevas generaciones de medicamentos con el fin de solucionar diversos problemas de salud. El objetivo de esta búsqueda debe ser el descubrimiento de fármacos con mayor espectro, menos efectos adversos y menor costo que los existentes.
Las dermatomicosis son un problema frecuente en la población (17,18), por lo que el AE de muña podría ser una alternativa terapeútica; sin embargo, aún se requieren estudios que puedan evaluar formulados en forma de crema a diferentes concentraciones de AE (25% - 50%) y en animales de experimentación (19,20), para luego poder validar su posible uso en humanos (21).
REFERENCIAS BIBLIOGRÀFICAS
1. Salaverry O. La complejidad de lo simple: plantas medicinales y sociedad moderna. Rev Peru Med Exp Salud Publica. 2005; 22(4): 245-46.
2. Roersch C. The marketing of medicinal, aromatic plants and essential oils in the Dominican Republic. Acta Hort (ISHS). 1999; 503: 197-219,
3. Lahlou M. Methods to study the phytochemistry and bioactivity of essential oils. Phytother Res. 2004; 18(6): 435-48.
4. H ammond GB, Fernández ID, Villegas LF, Vaisberg AJ. A survey of traditional medicinal plants from the Callejón de Huaylas, Department of Ancash, Perú. J Ethnopharmacol. 1998; 61(1): 17- 30.
5. Inga BA, Guerra MB. Efecto del aceite esencial de Minthostachys mollis (muña) contra algunas bacterias y hongos de interés en la salud [Tesis de Licenciatura]. Lima: Facultad de Farmacia y Bioquímica, Universidad Nacional Mayor de San Marcos; 2000.
6. Rojas R, Bustamante B, Bauer J, Fernández I, Albán J, Lock O. Antimicrobial activity of selected Peruvian medicinal plants. J Ethnopharmacol. 2003; 88(2-3): 199-204.
7. G uiza Pérez GP, Rincón Prieto LM. Estudio del efecto antimicrobiano del aceite esencial de Minthostachys mollis combinado con inactivación térmica, sobre cepas de Listeria monocytogenes y Bacillus cereus [Tesis de bachiller]. Bogotá: Pontificia Universidad Javeriana; 2007. 298-301. Actividad antimicótica de la muña
8. Banchio E, Zygadlo J, Valladares GR. Quantitative variations in the essential oil of Minthostachys mollis (Kunth.) Griseb. in response to insects with different feeding habits. J Agric Food Chem. 2005; 53(17): 6903-6.
9. Fuertes CM, Munguía Y. Estudio comparativo del aceite esencial de Minthostachys mollis (Kunth) Griseb Muña de tres regiones peruanas por cromatografía de gases y espectrometría de masas. Ciencia e Investigación (Lima). 2001; 4(1): 23-39.
10. Malagon O, Vila R, Iglesias J, Zaragoza T, Cañigueral S. Composition of the essential oils of four medicinal plants from Ecuador. Flavour Fragr J. 2003; 18(6): 527-31.
11. Alkire BH, Tucker AO, Maciarello MJ. Tipo, Minthostachys mollis (lamiaceae): an Ecuadorian mint. Econ Bot. 1994; 48(1): 60-64.
12. Fenner R, Sortino M, Rates SM, DallAgnol R, Ferraz A, Bernardi AP, et al. Antifungal activity of some Brazilian Hypericum species. Phytomedicine. 2005; 12(3): 236-40.
13. Fernández-Torres B, Cabañes FJ, Carrillo-Muñoz A, Esteban A, Inza I, Abarca L, et al. Collaborative evaluation of optimal antifungal susceptibility testing conditions for dermatophytes. J Clin Microbiol. 2002; 40(11): 3999-4003.
14. Kalemba D, Kunicka A. Antibacterial and antifungal properties of essential oils. Curr Med Chem. 2003; 10(10): 813-29.
15. Mesa Arango AC, Bueno Sánchez JG, Betancur Galvis LA. Productos naturales con actividad antimicótica. Rev Esp Quimioterap. 2004; 17(4): 325-31.
16. Ali-Shtayeh MS, Abu Ghdeib SI. Antifungal activity of plant extracts against dermatophytes. Mycoses. 1999; 42(11-12): 665-72.
17. Bejar V, Quiñónez A, Costilla R. Prevalencia de infección por dermatofitos y cándida en región podal sana, Lima, Perú. Rev Peru Epidemiol. 1996; 9(2): 24-28.
18. Fuentes-Rivera D. Epidemiología y diagnóstico clínico etiológico de onicomicosis en un centro médico universitario (junio 97 – mayo 99). Dermatol Peru. 2000; 10(1): 21-33.
19. Rodríguez Pargas A, León Padilla MC, Hernández Rodríguez A, Junco Barranco J. Actividad antifúngica in vitro de una crema de Plantago major L. Rev Cubana Plant Med. 1996; 1(3): 9-12.
20. G uerra Ordóñez M, Rodríguez Jorge M, García Simón G. Llerena Rangel C. Actividad antimicrobiana del aceite esencial y crema de Cymbopogon citratus (DC). Stapf. Rev Cubana Plant Med. 2004; 9(2): 44-47.
21. [Not author listed]. Guía para realizar un protocolo de ensayo clínico con productos herbarios. Rev Cubana Plant Med. 1998; 3(2): 83-88.
Correspondencia:
Carlos A. Cano Pérez
Dirección: Av. Aurelio García y García 1206, Urb. Los Cipreses, Lima 1.
Teléfono: (511) 564-3235.
Correo electrónico: alfcanpe@hotmail.com
Recibido: 13-08-07
Aprobado: 15-02-08