Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Medicina Experimental y Salud Publica
versión impresa ISSN 1726-4634
Rev. perú. med. exp. salud publica v.25 n.3 Lima jul./set. 2008
Evaluación de dos ensayos de elisa IgM en la investigación de un brote de Leptospirosis
Evaluation of two elisa IgM assays in Leptospirosis outbreak research
Manuel Céspedes1,a, Lourdes Balda1,b, Martha Glenny1,a
1 Laboratorio de Leptospirosis, Centro Nacional en Salud Pública, Instituto Nacional de Salud. Lima, Perú
a Biólogo, b Técnica de laboratorio
RESUMEN
Se evaluó dos pruebas rápidas para el diagnóstico serológico de leptospirosis aguda, la prueba de ELISA IgM pool (Instituto Nacional de Salud, Lima) comparada con un ELISA IgM comercial (PANBIO) tomando como gold standar la prueba de microaglutinación (MAT). Se examinó 24 pacientes admitidos en un hospital para la investigación de un brote de leptospirosis. Se tomó dos muestras de suero, la primera cuando fueron hospitalizados y la segunda cuando fueron a la consulta o dados de alta del hospital. Se diagnóstico leptospirosis en 19 de 24 pacientes por MAT. La prueba de ELISA IgM-pool tuvo una mejor sensibilidad para muestras agudas que el ELISA IgM comercial (73,7% vs 31,6%), valores predictivos positivos (93,3 vs 85,7%) y negativos (44,4 vs 23,5%) e igual especificidad (80%). En la evolución de sueros convalecientes tuvieron el mismo rendimiento, sensibilidad de 100% y especificidad de 80%. La prueba rápida ELISA IgM-pool es altamente sensible y específica, no requirere de equipo especializado y se encuentra disponible para el uso en cualquier laboratorio.
Palabras clave: Leptospirosis; Brotes de enfermedades; Prueba ELISA; Pruebas diagnósticas (fuente: DeCS BIREME).
ABSTRACT
Was assessed two rapid tests for serodiagnosis of acute leptospirosis, the ELISA IgM pool (Instituto Nacional de Salud, Lima), compared with a commercial ELISA IgM (PANBIO) against the gold standard microagglutination test (MAT). We examined 24 patients admitted to a hospital for investigation of a leptospirosis outbreak. It took two samples of serum, the first when they were hospitalized and the second when the consultation or discharged from the hospital. Leptospirosis were diagnosed in 19 of 24 patients by MAT. ELISA IgM pool was show a better sensitivity for acute samples that commercial IgM ELISA (73.7% vs 31.6%), positive (93.3 vs 85.7%) and negative (44.4 vs 23.5%) predictive values and same specificity (80%). In the evolution of convalescent sera had the same performance, sensitivity of 100% and specificity of 80%. The rapid test of ELISA IgM pool is highly sensitive and specific, Not requiring specialized equipment and are available for use in any laboratory.
Key words: Leptospirosis; Disease outbreaks; Enzyme-linked immunosorbent assay; Diagnosis test (source: MeSH NLM).
INTRODUCCIÓN
La leptospirosis es una zoonosis causada por una espiroqueta patógena del género Leptospira. Tradicionalmente se ha considerado como una enfermedad ocupacional de personas que se exponen a aguas contaminadas con orina de animales infectados; en la actualidad ha sido reconocida como una causa frecuente de síndromes febriles en áreas tropicales y subtropicales (1,2).
La leptospirosis ha tomado importancia en la salud pública humana debido al incremento de brotes asociados con actividades recreacionales y ocupacionales (3,4) y también a las epidemias de síndrome pulmonar hemorrágico (5). Sin embargo, en los últimos brotes hubo confusión debido a que la presentación clínica asociada con leptospirosis y fiebre del dengue fueron muy similares (6), estas confusiones pueden repercutir en el tratamiento de los pacientes.
En Latinoamérica y el Caribe, los brotes de leptospirosis han estado asociados con las épocas de lluvias y en zonas donde la infraestructura de saneamiento es deficiente, además se ha observado que la mortalidad puede alcanzar hasta 15 % (1,2).
En muchas regiones del mundo y el Perú, los métodos de diagnóstico para esta enfermedad no son muy difundidos debido a múltiples problemas y limitaciones (2,7). El cultivo que se usa tiene una baja sensibilidad debido a las exigencias nutricionales y al crecimiento tardío de la bacteria, que incluso puede tardar meses. Asimismo, la prueba de referencia serológica aglutinación microscópica (MAT) es dificultosa y riesgosa para el operador; por ello, solamente se realiza en laboratorios referenciales nacionales (2,7,8).
Se han descrito muchos métodos comerciales de diagnóstico para la detección de anticuerpos, tales como ELISA y dipstick, los cuales en su mayoría usan serovares no patógenos como antígeno, limitando su sensibilidad y especificidad respecto al MAT (9-14). Además, los costos son relativamente altos, de ahí sus limitaciones para la distribución masiva.
Por ello, es urgente la implementación de metodologías de diagnóstico rápido para auxiliar al clínico y también para realizar investigaciones rápidas de casos sospechosos que nos permitan detectar los brotes de leptospirosis y se realicen las actividades de control y prevención. Se ha desarrollado un ELISA IgM que usa un pool de seis antígenos de leptospiras patógenas, como una alternativa rápida para el diagnostico de una infección aguda por leptospiras (8).
En este estudio se evaluó dos métodos de diagnóstico, ELISA IgM-pool (Instituto Nacional de Salud, Lima, Perú) y ELISA IgM (PANBIO LPM-220) a la vez se hizo una comparación entre ellas y el MAT, en un brote de leptospirosis en militares (15).
EL ESTUDIO
Se incluyó a todos los pacientes que fueron hospitalizados en el Hospital Militar (Lima, Perú) en el mes de mayo de 1999 durante un brote de síndrome febril (15), procedentes de Pichanaki, provincia Chanchamayo, departamento de Junín; quienes clínica y epidemiológicamente eran sospechosos para leptospirosis. El criterio de sospecha de leptospirosis usado fue el recomendada por la Organización Mundial de la salud: febril agudo con cefalea, mialgia y postración asociada con cualquiera de los siguientes síntomas: sufusión conjuntival, irritación meníngea, anuria/oliguria o proteinuria, ictericia, hemorragias, insuficiencia cardiaca y erupción cutánea (16).
De cada paciente se tomó dos muestras pareadas de sangre, la primera muestra fue tomada el primer día de admisión en el hospital y la segunda muestra (convaleciente) después de los 20 días de la primera, cuando fueron a la consulta o en la visita que realizó el personal del hospital. Las muestras de suero obtenidas fueron transportadas al Laboratorio de Leptospirosis del Instituto Nacional de Salud en cadena de frío (4-8 °C) y se mantuvieron en una congeladora a -20 °C hasta su procesamiento.
DIAGNÓSTICO DE LEPTOSPIROSIS
Se evaluó dos pruebas de ELISA, se usó la prueba de microaglutinación como gold standar.
ELISA IgM-pool. Los anticuerpos de tipo IgM fueron detectados usando un método cuantitativo de ELISA descrito por Céspedes (8).
ELISA IgM-PANBIO. Se realizó de acuerdo con las especificaciones descritas en el inserto del kit ELISA (LPM-220).
Prueba de microaglutinación (MAT). Las muestras pareadas de suero fueron examinadas por el MAT, usando una batería de 25 serovares para establecer la seroconversión o incremento del título de anticuerpos (9). Los antígenos usados incluyeron serovares de referencia de los siguientes serogrupos (serovares y parientes): Australis (Australis, Bratislava), Autumnalis (Autumnalis), Ballum (Ballum, Arborea), Bataviae (Bataviae), Canicola (Canicola), Celledoni (Celledoni), Cynopteri (Cynopteri), Djasiman (Djasiman), Grippotyphosa (Grippotyphosa), Hebdomadis (Borincana) Icterohaemorrhagiae (Icterohaemorrhagiae, Mankarso, Copenhageni), Mini (Georgia), Javanica (Javanica), Pomona (Pomona), Pyrogenes (Pyrogenes, Alexi), Tarassovi (Tarassovi), Sejroe (Wolffi), y L. biflexa Semaranga (Patoc, Andamana). Para confirmar el caso como leptospirosis se debió encontrar un incremento del título de anticuerpos en cuatro veces en ambas muestras paredas de suero.
Análisis de datos. Se usó el programa EPIDAT 2.0 para verificar la concordancia de la prueba y también para calcular la sensibilidad, especificidad, valor predictivo positivo y valor predictivo negativo. En la primera y segunda muestra con respecto al diagnóstico confirmatorio por MAT.
HALLAZGOS
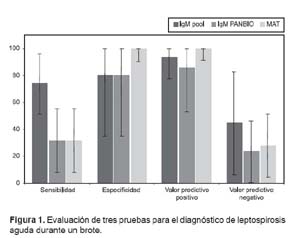
Se incluyó 24 pacientes, la edad promedio fue 22,0 ± 2 años, la totalidad de pacientes realizaba actividades militares como: caminata, natación e inmersión en una charca situada en la hacienda maderera, donde frecuentaban animales domésticos, para beber y bañarse. La curva epidémica y la presentación El gold standar fue la seroconversión en muestra convaleciente por MAT. Las barras expresan el intervalo de confianza al 95%. clínica de este brote se encuentran en el artículo descrito por Russell et al. (15). Los síntomas predominantes fueron fiebre y mialgia (100%), cefalea y escalofríos (94,7%) y otras manifestaciones en menor proporción
Diagnóstico de leptospirosis. De las 24 muestras pareadas, en 19 (79,2%) se observó seroconversión de anticuerpos en cuatro o más veces por MAT. No se logró aislar leptospiras de ninguno de los casos. Los serogrupos a las que se encontró positividad fueron Grippotyphosa, Cynopteri, Georgia, Bataviae y Sejroe en cada uno de ellos con títulos ≥ 1/6 400.
El tiempo transcurrido entre el inicio de los síntomas y la toma de muestras fue de 5,0 ± 4,0 días (rango 1-14 días) para las muestras agudas y de 28,0 ± 5 días (rango 21-39 días) para las muestras convalecientes.
En las muestras agudas, el ELISA pool tuvo una mejor sensibilidad (73,7%; IC95%: 51,3-96,1%) que el ELISA PANBIO (31,6%; IC95%: 8,1-55,1%) y el MAT (31,6%; IC95%: 8,1-55,1%), con resultados similares de especificidad (80%; IC95%: 34,9-100%) y valores predictivos positivos y negativos (Figura 1).
Los sueros positivos en las muestras agudas para el ELISA IgM pool tenían en promedio siete días de enfermedad, a diferencia de los positivos por ELISA IgM PANBIO y MAT que tenían diez días desde el inicio de los síntomas.
En las muestras convalecientes, ambas pruebas tuvieron el mismo rendimiento, sensibilidad de 100% (97,4-100%), especificidad de 80% (34,9-100%), valor predictivo positivo de 95% (83,0-100%) y valor predictivo negativo de 100% (87,5-100%).
DISCUSIÓN
Proporcionar al médico un resultado rápido y oportuno de su sospecha clínica es importante para que realice un tratamiento oportuno y efectivo. Por tanto, un método de diagnóstico rápido e inicial es importante para diferenciar a la leptospirosis de otras enfermedades de presentación clínica similar.
El ELISA IgM pool descrito en este reporte, tiene el mismo rendimiento que el ELISA comercial para las dos muestras; sin embargo, tiene una mejor capacidad de detectar casos agudos (73,7%) de leptospirosis que el ELISA comercial y el MAT (31,6% en ambos casos). Las inmunoglobulinas IgM fueron detectadas por el ELISA IgM a partir de los tres días de iniciado los síntomas, pero con un promedio de siete días, similares reportes se encontraron en estudios previos referidos a estandarizar métodos para esta enfermedad (8-11,17).
Los resultados de este trabajo confirman nuestras sospechas previas en la utilidad del ELISA IgM usando un pool de antígenos, se encontró que este método es más sensible que los ELISA IgM comerciales descritos cuyas sensibilidades varían entre 29-52% en muestras de pacientes con enfermedad aguda (9-11,18).
En la gran mayoría de estos ELISA comerciales, se usan serovares no patógenos, como antígeno de ahí su baja sensibilidad. Comparando con otros métodos comerciales como el dipstick IgM, el ELISA IgM fue más sensible que los otros métodos comerciales (12-14).
En el Perú tenemos reportados más de 55 serovares aislados de personas, animales domésticos y silvestres en los últimos 40 años, de las cuales 19 son serovares nuevos en el mundo (7). La prueba MAT detectó anticuerpos en contra de varios serovares de leptospiras: Grippotyphosa, Cynopteri, Georgia, Bataviae y Sejroe. Los serovares que reaccionaron en el MAT, se aislaron de roedores, marsupiales y animales domésticos en el Perú, por lo que podríamos asumir que la fuente de origen del brote está relacionada con la orina de estos animales.
El diagnóstico clínico temprano de la leptospirosis en áreas tropicales es muy difícil debido a que existen otras enfermedades con sintomatología parecida como malaria, fiebre entérica, dengue, fiebre amarilla, Mayaro, oropuche, encefalitis equina y hepatitis viral, y no podríamos asumir rápidamente a tal agente como causante del brote para tomar las medidas de control e iniciar un tratamiento a las personas sí solo usáramos el MAT (2,6,7).
Debido a la poca cantidad de pacientes evaluados, los intervalos de confianza obtenidos son muy amplios y no permiten encontrar claramente las diferencias de la performance de ambas pruebas diagnósticas; sin embargo, la tendencia observada nos lleva a afirmar que el ELISA IgM pool tiene una mejor sensibilidad que el ELISA PANBIO.
Concluimos que la prueba evaluada fue altamente sensible y específica, no requiriendo equipo especializado, y podría ser realizada en laboratorios periféricos con relativamente poca experiencia en el diagnóstico de leptospirosis. Por tanto, esto repercutiría en beneficio de los pacientes ya que tendría un diagnóstico mucho más rápido, por tanto, un tratamiento adecuado y oportuno.
AGRADECIMIENTOS
Al técnico Benjamín Cárdenas por su apoyo para el procesamiento de las muestras; a Leonid Lecca y Teresa por la revisión del manuscrito, al personal del Hospital Militar de Lima por su apoyo para la ejecución del estudio.
REFERENCIAS BIBLIOGRÁFICAS
1. Bharti AR, Nally JE, Ricaldi JN, Matthias MA, Diaz MM, Lovett MA, et al. Leptospirosis: a zoonotic disease of global importance. Lancet Infect Dis. 2003; 3(12): 757-71.
2. Céspedes M. Leptospirosis: enfermedad zoonótica reemergente. Rev Peru Med Exp Salud Publica. 2005; 22(4): 290-307.
3. Katz AR, Sasaki DM, Mumm AH, Escamilla J, Middleton CR, Romero SE. Leptospirosis on Oahu: an outbreak among military personnel associated with recreational exposure. Mil Med. 1997; 162(2): 101-4.
4. Corwin A, Ryan A, Bloys W, Thomas R, Deniega B, Watts D. A waterborne outbreak of leptospirosis among United States military personnel in Okinawa, Japan. Int J Epidemiol. 1990; 19(3): 743-48.
5. Segura ER, Ganoza CA, Campos K, Ricaldi JN, Torres S, Silva H, et al. Clinical spectrum of pulmonary involvement in leptospirosis in a region of endemicity, with quantification of leptospiral burden. Clin Infect Dis. 2005; 40(3): 343-51.
6. E llis T, Imrie A, Katz AR, Effler PV. Underrecognition of leptospirosis during a dengue fever outbreak in Hawaii, 2001-2002. Vector Borne Zoonotic Dis. 2008; 8(4): 541-47.
7. Céspedes M, Balda L, González D, Tapia R. Situación de la leptospirosis en el Perú, 1994-2004. Rev Peru Med Exp Salud Publica. 2006; 23(1): 56-66.
8. Céspedes M, Glenny M, Felices V, Balda L, Suárez V. Prueba de ELISA indirecta para la detección de anticuerpos IgM para el diagnóstico de la leptospirosis humana. Rev Peru Med Exp Salud Publica. 2002; 19(1): 24-27.
9. Cumberland P, Everard CO, Levett PN. Assessment of the efficacy of an IgM-elisa and microscopic agglutination test (MAT) in the diagnosis of acute leptospirosis. Am J Trop Med Hyg. 1999; 61(5): 731-34.
10. Terpstra W, Ligthart G, Schoone G. ELISA for the detection of specific IgM and IgG in human leptospirosis. J Gen Microbiol. 1985; 131(2): 377-85.
11. W inslow WE, Merry DJ, Pirc ML, Devine PL. Evaluation of a commercial enzyme-linked immunosorbent assay for detection of immunoglobulin M antibody in diagnosis of human leptospiral infection. J Clin Microbiol. 1997; 35(8): 1938-42.
12. Smits HL, Ananyina YV, Chereshsky A, Dancel L, Lai A Fat RF, Chee HD, et al. International multicenter evaluation of the clinical utility of a dipstick assay for detection of Leptospira-specific immunoglobulin M antibodies in human serum specimens. J Clin Microbiol. 1999; 37(9): 2904-9.
13. Smits HL, Hartskeerl RA, Terpstra WJ. International multi-centre evaluation of a dipstick assay for human leptospirosis. Trop Med Int Health. 2000; 5(2): 124-28.
14. Yersin C, Bovet P, Smits HL, Perolat P. Field evaluation of a onestep dipstick assay for the diagnosis of human leptospirosis in the Seychelles. Trop Med Int Health. 1999; 4(1): 38-45.
15. Russell KL, Montiel Gonzalez MA, Watts DM, Lagos-Figueroa RC, Chauca G, Ore M, et al. An outbreak of leptospirosis among Peruvian military recruits. Am J Trop Med Hyg. 2003; 69(1): 53-57.
16. Céspedes M, Ormaeche M, Condori P, Balda L, Glenny M. Prevalencia de leptospirosis y factores de riesgo en personas con antecedentes de fiebre en la Provincia de Manu, Madre de Dios, Perú. Rev Peru Med Exp Salud Publica. 2003; 20(4): 180-85.
17. O oteman MC, Vago Ar, Koury MC. Evaluation of MAT, IgM ELISA and PCR methods for the diagnosis of human leptospirosis. J Microbiol Methods. 2006; 65(2): 247-57.
18. Bajani MD, Ashford DA, Bragg SL, Woods CW, Aye T, Spiegel RA, et al. Evaluation of four commercially available rapid serologic test for diagnosis of leptospirosis. J Clin Microbiol. 2003; 41(2): 803-9.
Correspondencia:
Blgo. Manuel Céspedes Zambrano. Laboratorio de Leptospiras, Centro Nacional de Salud Pública, Instituto Nacional de Salud. Lima, Perú.
Dirección: Av. Defensores del Morro 2268, Chorrillos 9, Perú. Apartado Postal 471.
Teléfono: (511) 251 61 51 Fax: (511) 251 6151
Correo electrónico: mcespedes@ins.gob.pe
Recibido: 10-02-08
Aprobado: 11-04-08