Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Medicina Experimental y Salud Publica
versión impresa ISSN 1726-4634
Rev. perú. med. exp. salud publica v.25 n.4 Lima oct./dic. 2008
Mejora en el diagnóstico y tratamiento oportuno de malaria con el uso de pruebas rápidas por promotores de salud en la Amazonía peruana
Improvements in timely malaria diagnosis and appropriate therapy with the use of rapid tests by health promoters in Peruvian Amazon jungle
Martín Casapía1,a, Luz E. Vásquez2,b, Ángel Rosas2,b, Nelson Pinedo-Ríos1,b, César Cabezas3,4,a, Jaime Chang5,b
1 Dirección Regional de Salud Loreto. Iquitos, Perú.
2 Proyecto VIGIA, Ministerio de Salud del Perú /USAID. Lima, Perú.
3 Instituto Nacional de Salud. Lima, Perú.
4 Facultad de Medicina, Universidad Nacional Mayor de San Marcos. Lima, Perú.
5 Agencia de Desarrollo Internacional de los Estados Unidos de Norteamérica (USAID). Lima, Perú.
a Médico infectólogo; b Médico salubrista.
RESUMEN
Objetivos. Comparar la oportunidad en el diagnóstico y tratamiento apropiado de la malaria antes y después de la incorporación del uso de pruebas rápidas por promotores de salud en comunidades periféricas de Iquitos. Material y métodos. Estudio longitudinal con evaluación pre y postintervención. En ambas evaluaciones se recolectó un número mínimo de 200 pacientes febriles (casos sospechosos de malaria) que habían sido atendidos por el promotor en las seis semanas previas, datos relacionados a la oportunidad en el diagnóstico y tratamiento, y los diagnósticos confirmatorios por gota gruesa. Resultados. Con la intervención hubo una disminución significativa del tiempo transcurrido entre el inicio de síntomas y el inicio del tratamiento de 110 horas (4,6 días) a 46,3 horas (1,9 días) (p<0,001). Dicha variación fue debida mayormente a la reducción del tiempo transcurrido desde la consulta al promotor hasta la obtención del diagnóstico del paciente, de 69 horas (2,9 días) a sólo 20 minutos (p<0,001). Además, hubo un incremento significativo de la proporción de pacientes con malaria que recibieron tratamiento antimalárico oportuno de 15,5 a 54,9% (p<0,001), la proporción de pacientes con malaria que recibieron tratamiento apropiado a la especie del parásito de 26,7% a 83,5% (p<0,001) y la proporción de pacientes con malaria falciparum que recibieron tratamiento apropiado de 5,3 a 73,1%(p<0,001). Conclusiones. A través de la incorporación del uso de pruebas rápidas por promotores de salud en las comunidades seleccionadas, se ha mejorado la oportunidad en el diagnóstico y tratamiento apropiado de la malaria.
Palabras clave: Malaria/diagnóstico; /terapia; Asentamientos rurales; Auxiliares de salud comunitaria; Perú (fuente: DeCS BIREME).
ABSTRACT
Objectives. To compare the achievement of a timely diagnosis and appropriate therapy for malaria before and after the incorporation of rapid tests for diagnosing this disease used by health promoters in peripheral communities in Iquitos. Material and methods. A longitudinal study with pre- and post- intervention assessments was performed. Two hundred febrile patients (suspected malaria cases) seen by health promoters during the last 6 weeks were selected, and data related to a timely malaria diagnosis and therapy, as well as confirmatory diagnoses using thick smears was collected. Results. There was a significant decrease in the time elapsed from symptom onset to therapy initiation with the intervention, from 110 hours (4.6 days) to 46,3 hours (1.9 days) (p<0.001). This variation was mainly due to a reduction of the time since the patient was first seen by a health promoter until the time when a diagnosis was achieved, from 69 hours (2.9 days) to only 20 minutes (p<0.001). There was also a significant increase in the frequency of malaria patients who received timely antimalarial therapy, from 1,5% to 54,9% (p<0.001); the proportion of malaria patients receiving appropriate therapy according to the parasite species increased from 26.7% to 83.5% (p<0.001), and the proportion of P. falciparum malaria patients who received appropriate therapy rose from 5.3% to 73.1% (p<0.001). Conclusions. Now it is possible to achieve a timely diagnosis and appropriate therapy for malaria with the use of rapid tests by health promoters in these selected communities.
Key words: Malaria/diagnosis; /therapy; Rural settlements; Community health aides; Peru (source: MeSH NLM).
INTRODUCCIÓN
La malaria es una enfermedad infecciosa, reemergente en el Perú y en el mundo, que ha aumentado su incidencia en estos últimos 20 años, luego del gran avance en su control, logrado en la década de los setenta (1,2). Esta enfermedad es considerada un problema de salud pública en nuestro país, debido al aumento de su incidencia y extensión geográfica así como su alto costo social y económico (2,3).
El diagnóstico y tratamiento precoz de la malaria es vital para disminuir los casos graves y la mortalidad (4). En el año 2000 un estudio que investigó los factores condicionantes de la malaria grave y complicada por Plasmodium falciparum en el Perú, encontró relación entre el retraso en el tratamiento de la malaria por dos días o más y el riesgo de desarrollar malaria grave (5).
El tratamiento oportuno y apropiado permite disminuir el tiempo de enfermedad, acortando el tiempo de molestias al paciente y su periodo de inactividad, así mismo, contribuye a cortar el ciclo de transmisión de la enfermedad (persona infectada-vectorpersona) (6,7). En 1999, el estudio del impacto económico de la malaria en nuestro país, demostró que el mayor costo por los casos de malaria era asumido por las familias, sobre todo aquellos costos por pérdida de productividad (3). Esto contribuiría a incrementar la pobreza en las zonas más pobres del país, que son justamente los lugares donde la malaria es endémica.
La Organización Mundial de la Salud (OMS) considera como una estrategia central para el control de la malaria, el diagnóstico y tratamiento oportuno de casos (8). En este sentido, el Ministerio de Salud viene realizando importantes esfuerzos para garantizar una atención y tratamiento oportuno de los casos de malaria en todo el Perú. Pese a estos esfuerzos, la oportunidad del diagnóstico, el seguimiento de los casos y el asegurar un tratamiento apropiado aún se constituyen en verdaderos problemas, sobre todo en áreas con alta ruralidad y dispersión poblacional, que afectan la accesibilidad a los servicios (9).
Loreto, departamento de la selva nororiental del país, es considerado como área de alto riesgo para la transmisión de la malaria (10). Sus características geográficas, ecológicas y climatológicas, así como el comportamiento y hábitos de la población, la elevada ruralidad (42% de habitantes viven en centros poblados rurales y comunidades periféricas) y dispersión poblacional, hacen difícil un control de la enfermedad. Por ello, la Dirección de Salud Loreto ha implementando una estrategia de incorporación de la comunidad a las actividades de control de la malaria, a través de promotores de salud (colaboradores voluntarios de la comunidad). Es así que los promotores han sido capacitados en funciones tales como obtención de gota gruesa, administración de tratamiento, seguimiento de los casos y otras actividades de control como promoción, prevención y control vectorial de la malaria.
Si bien esta estrategia venía mejorando la capacidad de diagnóstico y tratamiento de la malaria, aún subsisten dificultades para la oportunidad de estos, en la medida que el diagnóstico se realiza en el establecimiento de salud periférico más cercano a la comunidad que cuenta con condiciones necesarias para realizar un examen microscópico (gota gruesa). Las dificultades consisten en que: a) no todos los establecimientos periféricos tienen las condiciones necesarias para realizar el examen microscópico (que requiere personal técnico entrenado, una adecuada toma y cumplimiento de los procedimientos de la técnica, insumos de laboratorio y microscopios en buen estado); b) el transporte de la gota gruesa al establecimiento de salud (sobre todo en comunidades periféricas) es dificultoso e irregular y; c) la entrega de los resultados de la gota gruesa a la comunidad tiene las mismas dificultades que el transporte hacia el establecimiento (9,11).
Paralelamente, en los últimos 15 años, se viene ensayando el uso de pruebas diagnósticas rápidas (PDR) para malaria con tiras inmunocromatográficas, las cuales son una buena opción frente a la microscopía (12). Estas pruebas han sido ensayadas en el Perú y están basadas en la detección de proteínas ricas en histidina (13-16) o enzimas como la deshidrogenasa láctica (17-20), se ha demostrado su alta sensibilidad, especificidad y simplicidad de uso en lugares con dificultades de acceso al diagnóstico microscópico, tanto por profesionales de la salud como por promotores capacitados.
En este contexto, con la finalidad de mejorar la oportunidad en el diagnóstico y tratamiento apropiado de la malaria, en comunidades ubicadas en la periferia de la ciudad de Iquitos, se realizó una intervención que consistió en fortalecer la capacidad diagnóstica de la malaria a través de la incorporación del uso de pruebas rápidas por los promotores de salud en estas comunidades. Por tanto, el presente trabajo tuvo por objetivo comparar el tiempo en el diagnóstico y tratamiento apropiado de la malaria en las comunidades seleccionadas, antes y después de dotar a promotores de salud con pruebas rápidas para el diagnóstico de la malaria.
MATERIALES Y MÉTODOS
TIPO DE ESTUDIO
Se realizó un estudio longitudinal con evaluación pre y postintervención. La intervención fue realizada entre septiembre de 2001 y mayo de 2003 en 50 comunidades periféricas de la ciudad de Iquitos, ubicadas en la cuenca del río Nanay y en la carretera Iquitos-Nauta. Estas comunidades rurales están bajo la jurisdicción de las microrredes de salud Iquitos Sur, Iquitos Norte y Belén que fueron seleccionadas considerando su alta incidencia de malaria.
La intervención consistió en fortalecer la capacidad diagnóstica de malaria a través de la incorporación del uso de pruebas rápidas (Optimal®) por los promotores de salud en las comunidades seleccionadas. Se distinguieron claramente dos fases de trabajo:
Fase preparatoria. Se realizó entre septiembre de 2001 a julio de 2002, y se desarrolló las siguientes actividades:
Evaluación de la oportunidad al diagnóstico y tratamiento apropiado de la malaria antes de la intervención (11);
Diagnóstico de conocimientos, actitudes y prácticas (CAP) sobre transmisión, síntomas, tratamiento y prevención de la malaria;
Diseño del protocolo de intervención;
Diseño y producción de material de información, educación y comunicación (IEC);
Capacitación inicial a personal de salud y promotores de salud en el uso de pruebas rápidas y consejería en malaria; Dotación a los promotores de pruebas rápidas, medicamentos y material IEC.
Fase de intervención. Entre agosto de 2002 a mayo de 2003 se realizaron las siguientes actividades:
Reforzamiento de la capacitación a personal de salud y promotores en el uso de pruebas rápidas y consejería en malaria;
Actividades para la prevención de la salud y acciones IEC;
Supervisión y vigilancia mensual del trabajo de los promotores;
Evaluación CAP sobre transmisión, síntomas, tratamiento y prevención de la malaria;
Evaluación de la oportunidad al diagnóstico y tratamiento apropiado de la malaria luego de la intervención.
La evaluación de la oportunidad al diagnóstico y tratamiento apropiado de la malaria antes de la intervención fue realizada en septiembre de 2001 y sus resultados han sido publicados previamente (11), para la medición del grupo postintervención se siguió la misma metodología.
POBLACIÓN Y MUESTRA
El universo, en ambas, estuvo conformado por todos los febriles (casos sospechosos de malaria) que acudieron a los promotores en el ámbito del estudio durante las últimas seis semanas, previas a la evaluación en cada comunidad. Fueron excluidos aquellos pacientes febriles que no residían en las comunidades donde fueron atendidos.
Para el cálculo del tamaño muestral se tomó la información del estudio de los factores de riesgo para la gravedad de la malaria en el Perú (5); en el cual se encontró que 85% de los pacientes tenían una demora de más de dos días para iniciar tratamiento. Considerando además una precisión absoluta del 5%, un nivel de confianza de 95%, un poder de 80%, y para el factor de ajuste por muestreo polietápico se calculó una muestra de 200 pacientes febriles.
La selección de la muestra tuvo dos etapas: primero, se seleccionó, de las 50 comunidades elegidas para la intervención, a ocho comunidades con poca accesibilidad al diagnóstico microscópico de malaria que tuvieran el mayor número de febriles reportados durante las últimas seis semanas previas a la evaluación (pre y postintervención); y segundo, la muestra se distribuyó de manera proporcional al número de febriles que tenía cada una de las ocho comunidades seleccionadas.
Como poco accesibles al diagnóstico microscópico fueron calificadas aquellas comunidades en las que el traslado de una persona hasta un establecimiento de salud con capacidad para lectura de gotas gruesas dure un tiempo mayor o igual a 30 minutos con el medio de transporte usual y no se cuente con disponibilidad permanente (al menos cada seis horas) de este medio de transporte (ya sea por vía fluvial o terrestre).
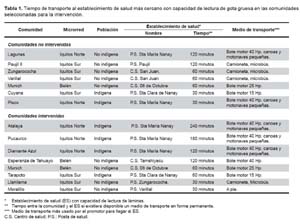
Debido a que se seleccionó a las comunidades que más casos habían reportado en las últimas seis semanas, no fueron las mismas comunidades las que se evaluaron en el pre y postintervención. En la Tabla 1 se presenta las comunidades seleccionadas, además se señala los establecimientos de salud con capacidad para lectura de láminas de gota gruesa más cercanos a estas comunidades y el tiempo que se demora en llegar a ellos.
PROCEDIMIENTOS
En cada una de las comunidades seleccionadas, encuestadores previamente capacitados, ubicaron a todos los pacientes atendidos, basándose en los libros de registro de febriles y registros del promotor. Luego, seleccionaron aleatoriamente al número de febriles requeridos para encuestar, por comunidad, a los cuales visitaron en su domicilio. La encuesta previamente validada, incluyó datos sociodemográficos, datos relacionados con la oportunidad en el diagnóstico y tratamiento (fechas y horas del inicio de síntomas, de la consulta al promotor, de la obtención del resultado de la gota gruesa -antes de la intervención–, de la obtención del resultado de la prueba rápida –después de la intervención–, y del inicio de tratamiento), datos de laboratorio (resultados de la gota gruesa o resultados de la prueba rápida) y datos del tratamiento antimalárico.
Todos los datos obtenidos en la encuesta fueron contrastados con los datos obtenidos de las fichas de registro de los promotores de salud y los cuadernos de control de gotas gruesas de los establecimientos de salud verificándose las fechas de atención y de diagnóstico, así como los resultados de las gotas gruesas de control.
DEFINICIONES
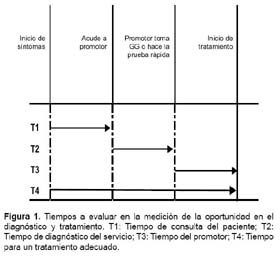
Para la medición de la oportunidad en el diagnóstico y tratamiento apropiado se calcularon los siguientes tiempos en horas (Figura 1):
Tiempo de consulta del paciente (T1). Definido como el tiempo transcurrido entre el inicio de los síntomas y la consulta al promotor; fue obtenido mediante la entrevista al paciente y el registro de atenciones del promotor.
Tiempo de diagnóstico del servicio (T2). Tiempo transcurrido entre la consulta al promotor y la obtención del resultado de la gota gruesa (preintervención) o la prueba rápida (postintervención), fue obtenido de los registros del promotor y del laboratorio.
Tiempo del promotor (T3). Tiempo transcurrido entre la obtención del resultado de la gota gruesa (preintervención) o la prueba rápida (postintervención) y el inicio del tratamiento; fue obtenido de los registros del promotor y del laboratorio.
Tiempo para un tratamiento adecuado (T4). Tiempo transcurrido entre el inicio de los síntomas y el inicio del tratamiento.
Además, se definió como tratamiento apropiado de la malaria al tratamiento recibido por el febril que esté de acuerdo con el diagnóstico de gota gruesa leída en el Laboratorio Referencial de Loreto y la Política Nacional de Medicamentos para el control de la Malaria en el Perú (21).
La información de los pacientes en las evaluaciones pre y postintervención, se codificó y organizó en una base de datos usando el software Excel (en dos digitaciones independientes); para su procesamiento y análisis se usó el paquete estadístico SPSS v.12.0. Los resultados se expresaron en frecuencias relativas y absolutas. Se usó la prueba de Chi-cuadrado para la comparación de las proporciones de la oportunidad en el diagnóstico y tratamiento adecuado, y la prueba de U de Mann Whitnney para la comparación de los tiempos calculados; considerándose un p<0,05 como estadísticamente significativo.
RESULTADOS
El tiempo que toma transportarse desde las comunidades elegidas a los establecimientos de salud con capacidad para la lectura de láminas de gota gruesa fluctúa entre 30 y 240 minutos (Tabla 1).
En la evaluación preintervención se encuestó a 200 pacientes febriles: 107 (53,5%) mujeres y 93 (46.5%) varones; con una edad media de 23,6 años. En la evaluación postintervención se encuestó a 205 febriles: 100 (48,8%) mujeres y 105 (51,2%) varones; con una edad media de 20,0 años.
Según los resultados del diagnóstico por gota gruesa (diagnóstico confirmatorio), en la evaluación preintervención, 129 (64,5%) pacientes febriles tuvieron gota gruesa negativa, y 71 (35,5%) tuvieron diagnóstico confirmatorio de malaria: 50 (25,0%) malaria vivax, 19 (9,5%) malaria falciparum y 2 (1,0%) malaria mixta. En la evaluación postintervención, 114 (55,6%) tuvieron gota gruesa negativa, 65 (31,7%) malaria vivax y 26 (12,7%) malaria falciparum.
La comparación de los resultados en horas de la medición de la oportunidad en el diagnóstico y tratamiento antes y después de la intervención se presenta en la Tabla 2. No hubo diferencias en la mediana del tiempo transcurrido entre el inicio de síntomas y la consulta al promotor (T1) pre y postintervención (p>0,05).
Sin embargo, sí se observó una disminución significativa de la mediana del tiempo transcurrido desde la consulta al promotor hasta la obtención del diagnóstico del paciente (T2), de 69 horas (2,9 días) antes de la intervención a sólo 20 minutos después de la intervención (p<0,001).
Esta variación contribuyó en mayor medida a la disminución de la mediana del tiempo transcurrido entre el inicio de síntomas y el inicio del tratamiento (T4) de 110 horas (4,6 días) a 46,3 horas (1,9 días), luego de la intervención (p<0,001). Con la disminución de este último tiempo, la proporción de pacientes con malaria que recibió un tratamiento oportuno (tratamiento recibido antes de las 48 horas de inicio de síntomas) se incrementó de 15% al inicio de la intervención a 54,9% luego de la intervención.
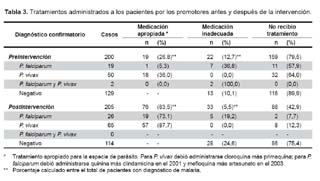
La Tabla 3 presenta el tratamiento aplicado a los pacientes, por los promotores antes de la intervención (septiembre de 2001). En total, 41 (20,5%) pacientes recibieron tratamiento sin confirmación diagnóstica; de los cuales 18 (9,0%) tuvieron finalmente diagnóstico por gota gruesa de malaria vivax, 8 (4,0%) de malaria falciparum, 2 (1,0%) de malaria mixta y 13 (6,5%) reportados como negativos.
Luego de la incorporación del uso de pruebas rápidas, sólo un paciente (0,5%) fue tratado sin habérsele hecho la prueba rápida previamente. El manejo instalado en los pacientes febriles tuvo una concordancia con el diagnóstico por gota gruesa de 79,0% (162/205). De los 91 pacientes con diagnóstico de malaria por gota gruesa, la mayoría (83,5%) recibieron un tratamiento apropiado a la especie de parásito, 5 (5,5%) recibieron un tratamiento antimalárico inapropiado, y 10 (11,0%) no recibieron tratamiento alguno. De los 26 casos confirmados con malaria falciparum, 19 (73,1%) recibieron un tratamiento apropiado con mefloquina/artesunato, 4 (15,4%) recibieron tratamiento con sólo una droga (quinina sola o mefloquina sola), 1 (3,8%) con cloroquina/primaquina y 2 (7,7%) no recibieron tratamiento alguno.
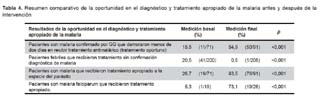
En la Tabla 4 se muestra que después de la intervención hubo un incremento significativo de la proporción de pacientes con malaria que recibieron tratamiento antimalárico oportuno (p<0,001), de la proporción de pacientes con malaria que recibieron tratamiento apropiado a la especie del parásito (p<0,001) y de la proporción de pacientes con malaria falciparum que recibieron tratamiento apropiado (p<0,001).
DISCUSIÓN
En general, aunque se mencionan los tiempos aproximados para el transporte desde las comunidades seleccionadas a los establecimientos de salud con capacidad de lectura de gotas gruesas, éstos son sólo teóricos, ya que dependen básicamente de la disponibilidad del medio de transporte (microbús o bote a motor), el cual es poco frecuente sobre todo para aquellas comunidades que usan los ríos como vías de transporte.
La proporción de casos confirmados de malaria y la proporción de casos de malaria falciparum entre los pacientes febriles encuestados en ambas evaluaciones, no varió significativamente, pese a que la recolección de los datos fue realizada en diferentes comunidades, meses y años. Con relación a este hallazgo, debemos señalar que una serie de factores deben ser tomados en cuenta al analizar la proporción de casos de malaria en el grupo de pacientes febriles. Entre ellos, tenemos los factores de riesgo conocidos para la enfermedad (22,23) como la época del año y las condiciones climatológicas de la zona, la eficiencia del vector para la transmisión, los movimientos migratorios, las actividades en el campo, las prácticas de la población y las medidas de control y prevención adoptadas en la zona. Además, debe considerarse la existencia de otras enfermedades febriles en la zona.
Así, el estudio de vigilancia de pacientes febriles con gota gruesa negativa realizado en zonas endémicas de malaria (costa norte y selva) del país, identificó que 16,2% de los casos correspondieron a enfermedades virales y bacterianas como dengue, encefalitis equina venezolana, Oropuche, leptospirosis, tifus, entre otros (24).
La incorporación del uso de pruebas rápidas para el diagnóstico de la malaria por promotores de salud redujo la mediana de los tiempos comprendidos entre el inicio de síntomas y el inicio de tratamiento (T4) en pacientes con malaria de 110 horas (4,6 días) antes de la intervención a 46,3 horas (1,9 días) después de la intervención, incrementando así la proporción de pacientes con malaria que recibieron tratamientos oportunos de 15,5% a 54,9%. Cualquier factor que contribuya a prolongar el proceso patológico de la malaria, sin administrar tratamiento, incrementa la parasitemia y por tanto el efecto tóxico del parásito; por lo que cuanto más demore el diagnóstico y el tratamiento, la probabilidad de que la infección (sobre todo por P. falciparum) evolucione a grave, es mayor (5,21); en ese sentido, el uso de pruebas rápidas es recomendable para dar un tratamiento oportuno, según los resultados obtenidos, en zonas donde no es posible realizar un examen microscópico (9).
Si bien, con la intervención se logró la reducción del tiempo transcurrido entre el inicio de los síntomas y el inicio de tratamiento antimalárico (T4), el análisis de las subdivisiones de éste no demostró una disminución del tiempo transcurrido entre el inicio de los síntomas y la consulta al promotor (T1), convirtiéndose dentro de la evaluación postintervención en el tiempo que más contribuyó en la demora del tratamiento antimalárico. Por tanto, las actividades para la prevención de la salud y acciones IEC con la población por un corto periodo en la intervención no habrían sido suficientes para modificar aquellos factores que influyen en la búsqueda tardía de atención; siendo la percepción errada sobre las formas de transmisión, prevención y control de la malaria una de las más importantes entre estos factores (25).
Otros factores involucrados en la búsqueda no oportuna de atención por el promotor tendrían relación con los patrones culturales locales (preferencia por la atención por familiares o curanderos) y la falta de confianza en el promotor y en los servicios de salud de primer nivel. Todos estos factores necesitan ser evaluados, y con los resultados debe diseñarse las estrategias adecuadas de información, comunicación y educación que lleven a modificar la conducta de la población y enfermos de malaria frente al manejo de su enfermedad (26). Asimismo, es necesario evaluar la implementación de un sistema de vigilancia comunitaria en el cual los promotores y la comunidad asuman una función más activa en la captación de los pacientes.
En la evaluación preintervención (11) se señalo al tiempo del promotor (T2) como la parte del proceso más importante, contribuyendo en mayor medida a la demora en el inicio de tratamiento, ya que implicaba el transporte de la muestra al centro de salud con microscopista y el tiempo que se demoraban en el centro en emitir el resultado, aspectos que son omitidos con el uso de las pruebas rápidas para el inicio del tratamiento.
El cálculo del tiempo transcurrido entre la obtención del resultado de la gota gruesa por parte del promotor y el inicio del tratamiento (T3), contribuyó poco al retraso en el tratamiento de los pacientes en ambas evaluaciones. En la evaluación postintervención se observa una ligera disminución de este tiempo, debida básicamente a una mayor disponibilidad de medicamentos antimaláricos en las comunidades, la cual debía ser asegurada por la intervención.
Un diagnóstico exacto de la malaria es esencial para asegurar que los pacientes que la padecen reciban un tratamiento apropiado a la especie del parásito y que las drogas antimaláricas no sean empleadas en pacientes con otras enfermedades. Ante la ausencia de confirmación laboratorial, decidir si se debe dar tratamiento antimalárico y qué tratamiento debe darse en un área endémica con presencia de malaria vivax y falciparum como las comunidades estudiadas, es sumamente difícil para el prestador de salud. En este contexto, la Doctrina, Normas y Procedimientos para el control de la Malaria en el Perú propuso para pacientes febriles en 1994, iniciar el tratamiento para malaria falciparum aun sin esperar la confirmación del diagnóstico por laboratorio (limitado acceso al diagnóstico microscópico), en aquellas situaciones y localidades donde se tenga la certeza sobre la existencia de un foco de malaria por P. falciparum (27). Sin embargo, esta norma no ha sido totalmente revisada ante el contexto del cambio de los esquemas de tratamiento.
En las comunidades evaluadas antes de la intervención, una demora mayor de dos días para obtener el resultado de la gota gruesa no puede ser interpretada como un verdadero acceso al diagnóstico microscópico, por lo que se debió contemplar iniciar el tratamiento antimalárico aún sin confirmación diagnóstica. Sin embargo, sólo 20,5% de los pacientes febriles encuestados tuvieron tratamiento sin confirmación diagnóstica (11). Si bien las razones de este bajo porcentaje necesitan ser exploradas, debe considerarse la no disponibilidad de tratamientos por los promotores, así como las instrucciones poco claras (para el manejo del paciente sintomático), dadas a éstos por parte de los servicios de salud.
Por otro lado, un tratamiento sin confirmación diagnóstica llevaría a gastos innecesarios en medicamentos antimaláricos, los cuales pueden ser excesivos teniendo en cuenta los nuevos esquemas de tratamiento implementados (costo aproximado de tratamiento para malaria falciparum con mefloquina/artesunato de 20 dólares en el 2003). Adicionalmente, el administrar un tratamiento sin confirmación diagnóstica, incrementaría el número de tratamientos inapropiados, contribuyendo a la resistencia a drogas antimaláricas que viene apareciendo en los últimos años.
La incorporación del uso de pruebas rápidas por parte de los promotores de salud no sólo disminuyó la proporción de tratamientos de malaria sin confirmación diagnóstica a 0,5% en las comunidades estudiadas; sino además, logró incrementar más de tres veces (de 26,7% a 83,5%) la proporción de pacientes con malaria con tratamientos apropiados según la especie del parásito y más de 13 veces (de 5,3% a 73,1%) la proporción de pacientes con malaria falciparum con tratamientos apropiados. Sin embargo, si la disponibilidad de los medicamentos en las comunidades hubiera sido permanente, el incremento de las proporciones de tratamientos apropiados pudo ser mayor.
Para la interpretación correcta de los resultados, debemos señalar las siguientes limitaciones. En primer lugar, la implementación posterior de establecimientos de salud con equipos necesarios para el diagnóstico microscópico de la malaria en las comunidades incluidas en la evaluación pre intervención, no permitió incluir las mismas comunidades en la evaluación postintervención.
Segundo, los resultados obtenidos sobre la oportunidad en el diagnóstico y tratamiento de la malaria son válidos para comunidades con condiciones similares a las estudiadas en ambas evaluaciones; es decir con similar acceso a establecimientos de salud con capacidad para lectura de gota gruesa, similar participación de los promotores en actividades de diagnóstico y tratamiento de la malaria y similares conocimientos, actitudes y prácticas de la población frente a la malaria.
La tercera limitación, estaría en relación con los meses y años de recolección de información con las diferencias correspondientes en el reporte de casos de malaria falciparum y vivax. Sin embargo, la proporción de casos confirmados de malaria y la proporción de casos de malaria falciparum del total de pacientes febriles encuestados entre ambas evaluaciones no varío significativamente.
Por último, pese al cruce de datos entre los datos proporcionados por los pacientes febriles y otras fuentes de información como los cuadernos de registros de los promotores y de los laboratorios de los centros de salud; existe la posibilidad de sesgo de memoria, ya que tanto los pacientes febriles y el promotor pueden no recordar con detalle fechas y datos sobre su enfermedad ocurrida en las seis semanas previas.
Aun considerando estas limitaciones, las diferencias en los resultados entre ambas evaluaciones son muy grandes, y confirman la mejora de la oportunidad en el diagnóstico y el tratamiento apropiado, a través de la incorporación del uso de pruebas rápidas Optimal® para el diagnóstico de la malaria y la administración de tratamientos antimaláricos por los promotores de salud en las mismas comunidades. La capacidad de los promotores de salud para realizar la prueba no constituye un problema. La sola condición de saber leer y escribir, sumado a un entrenamiento breve y simple en la aplicación e interpretación del procedimiento con una supervisión permanente del desempeño de los promotores por los servicios de salud correspondientes, garantizaría seguir contando con un diagnóstico oportuno y apropiado para la malaria en las comunidades intervenidas.
Además, los resultados iniciales de la evaluación económica de esta incorporación del uso de pruebas rápidas por promotores de salud en las comunidades intervenidas, califican a la intervención como una intervención costo-efectiva (28), resultando en un ahorro para el Estado y la sociedad. En este contexto, se recomienda extender el uso de pruebas rápidas por los promotores de salud a otras comunidades con limitado acceso al diagnóstico microscópico, e implementar la vigilancia comunitaria de la malaria, orientada a apoyar la reducción del tiempo entre el inicio de síntomas y la búsqueda de atención al promotor.
REFERENCIAS BIBLIOGRÁFICAS
1. Sachs J, Malaney 1. P. The economic and social burden of malaria. Nature. 2002; 415:680-85.
2. Neyra D, Cabezas C, Ruebush TK. El proceso de adecuación y cambio en la política del tratamiento de la malaria por Plasmodium falciparum en el Perú, 1990-2001. Rev Peru Med Exp Salud Publica. 2003; 20(3): 162-71.
3. Balcazar RA, Francke P, Quimper M, Portocarrero A, Paulini J, Barrios C. Impacto económico de la malaria en el Perú. Lima: Ministerio de Salud, Proyecto VIGIA; 2000.
4. Nafo Traore F. Rolling back malaria: opportunities and challenges. Trans R Soc Trop Med Hyg. 2005; 99(6): 403-6.
5. Perú, Ministerio de Salud, Proyecto Vigía. Factores de riesgo de la malaria grave en el Perú. Lima: MINSA; 2001.
6. Hetzel MW, Iteba N, Makemba A, Mshana C, Lengeler C, Obrist B, et al. Understanding and improving access to prompt and effective malaria treatment and care in rural Tanzania: the ACCESS Programme. Malar J. 2007; 6:83.
7. Butcher GA. Antimalarial drugs and the mosquito transmission of Plasmodium. Int J Parasitol. 1997; 27(9): 975-87.
8. World Health Organization. A global strategy for malaria control. Geneva: WHO; 1993.
9. Cabezas C. Pruebas rápidas para el diagnóstico de la malaria: una necesidad en áreas rurales con limitado acceso al diagnóstico microscópico. Rev Peru Med Exp Salud Publica. 2006; 23(2): 79-80.
10. Roshanravan B, Kari E, Gilman RH, Cabrera L, Lee E, Metcalfe J, et al. Endemic malaria in the Peruvian Amazon region of Iquitos. Am J Trop Med Hyg. 2003; 69(1): 45-52.
11. Durand S, Ramal C, Huilca M, Cabezas C. Oportunidad en el diagnóstico y tratamiento de la malaria en comunidades periurbanas de la Amazonía peruana. Rev Peru Med Exp Salud Publica. 2005; 22(1): 47-53.
12. Moody A. Rapid diagnostic test for malaria parasites. Clin Microbiol Rev. 2002; 15(1): 66-78.
13. Forney JR, Maguill AJ, Wongsrichanalai C, Sirichaisinthop J, Bautista CT, Heppner DG, et al. Malaria rapid diagnostic devices: performance characteristics of the ParaSight F device determined in a multisite field study. J Clin Microbiol. 2001; 39(8): 2884-90.
14. Forney JR, Wongsrichanalai C, Magill AJ, Craig LG, Sirichaisinthop J, Bautista CT, et al. Devices for rapid diagnosis of malaria: evaluation of prototype assays that detect Plasmodium falciparum histidine-rich protein 2 and a Plasmodium vivax-specific antigen.J Clin Microbiol. 2003; 41(6): 2358-66.
15. Llanos-Zavalaga F, Villacorta J, Reyes R, Lecca L, Mendoza D, Mayca J, et al. Evaluación de la prueba ICT malaria P.f./P.v. (AMRAD ®) para la detección de P.falciparum y P.vivax en una zona endémica de la Amazonía peruana. Rev Peru Med Exp Salud Publica. 2002; 19(1): 39-42.
16. Arróspide N, Marquiño W, Gutiérrez S. Evaluación de una prueba inmunocromatográfica ICT P.f/P.v para el diagnóstico de malaria por Plasmodium falciparum y Plasmodium vivax en establecimientos de la macroregión norte del Perú. Rev Peru Med Exp Salud Publica. 2004; 21(3): 134-38.
17. Cabezas C, Arróspide N, Marquiño W, Gutierrez S, Álvarez E, Chuquipiondo J, et al. Evaluación del uso de una prueba rápida inmunocromatográfica en promotores de salud para el diagnóstico de la malaria en áreas rurales de la Amazonía peruana. Rev Peru Med Exp Salud Publica. 2004; 21(1): 4-11.
18. Arrospide N, Flores R, Ruiz J. Evaluación de una prueba rápida para el diagnóstico de malaria en áreas endémicas del Perú. Rev Peru Med Exp Salud Publica. 2006; 23(2): 81-86.
19. Soto Tarazona A, Solari Zerpa L, Mendoza Requena D, Llanos- Cuentas A, Magill A. Evaluation of the rapid diagnostic test OptiMAL for diagnosis of malaria due to Plasmodium vivax. Braz J Infect Dis. 2004; 8(2): 151-55.
20. Arrospide N, Puray M, Guzmán E, Verano M, Medina S, Mendizábal L, et al. Uso de pruebas rápidas inmunocromatográficas para la detección de Plasmodium falciparum en donantes de sangre en Perú. Rev Peru Med Exp Salud Publica. 2004; 21(2): 76-81.
21. Perú, Ministerio de Salud. Política nacional de medicamentos para el control de la malaria en el Perú. Lima: MINSA; 1999.
22. Guthmann J, Hall A, Jaffar S, Palacios A, Llanos-Cuentas A. Environmental risk factors for clinical malaria: a case-control study in the Grau region of Peru. Trop Med Int Health Hyg. 2001; 95(6): 577-83.
23. Guthmann J, Llanos-Cuentas A, Palacios A, Hall A. Environmental factors as determinants of malaria risk. A descriptive study in the northern coast of Peru. Trop Med Int Health Hyg. 2002; 7(6): 518-25.
24. [Not authors listed]. Perfil etiológico del síndrome febril en áreas de alto riesgo de transmisión de enfermedades infecciosas de alto impacto en salud pública en el Perú, 2000-2001. Rev Peru Med Exp Salud Publica. 2005; 22(3): 165-74.
25. Heggenhougen HK, Hackethal V, Vivek P, Spielman A. The behavioural and social aspects of malaria and its control. An introduction and annotated bibliography. Geneva: WHO; 2003.
26. Nawaz H, Rahman MA, Graham D, Katz DL, Jekel JF. Health risk behaviors and health perceptions in the Peruvian Amazon. Am J Trop Med Hyg. 2001; 65(3): 252-56.
27. Perú, Ministerio de Salud. Doctrinas, normas y procedimientos para el control de la malaria en el Perú. Lima: MINSA; 1994.
28. Rosas AM. Análisis costo-efectividad de la incorporación del uso de pruebas rápidas Optimal® por promotores de salud para el diagnóstico de la malaria en comunidades periféricas de la ciudad de Iquitos [tesis de maestría]. Lima: Universidad Peruana Cayetano Heredia; 2006.
______________
Correspondencia:
Dra. Luz Esther Vásquez Vásquez
Dirección: Calle Pablo Bermúdez N.º 150 – 10mo piso. Telefono: (511) 330-3643
Correo: lvasquez23@telefonica.net.pe
Recibido: 04-06-08
Aprobado: 15-10-08