Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Medicina Experimental y Salud Publica
versión impresa ISSN 1726-4634
Rev. perú. med. exp. salud publica vol.31 no.2 Lima abr. 2014
Original Breve
Especificidad de la prueba intradérmica de Montenegro en pacientes infectados por Trypanosoma cruzi procedentes de diferentes regiones del Perú
Specificity of the intradermal Montenegro test in patients infected by Trypanosoma cruzi from different regions of Peru
Gloria Minaya-Gómez1,a, Silver Vargas-Apaza1,b, Yolanda Monteza-Zuloeta2,c, Enrique Purisaca-Morante3,c , Freddy Delgado-Diaz4,d.
1 Centro Nacional de Salud Pública, Instituto Nacional de Salud. Lima, Perú.
2 Dirección Regional de Salud de San Martin. San Martín, Perú.
3 Dirección Regional de Salud de Amazonas. Amazonas, Perú.
4 Dirección Regional de Salud de Arequipa. Arequipa, Perú.
a Bióloga, magíster en medicina tropical y salud internacional; b biólogo, magíster en biotecnología; c biólogo; d médico cirujano.
* Una versión preliminar fue publicada en la Serie Informes Técnicos N.º 35, 2005. Bajo el título: “Evaluación de la especificidad de la leishmanina (prueba intradérmica de Montenegro) en pacientes con la enfermedad de Chagas”.
RESUMEN
Con el objetivo de evaluar la especificidad de la leishmanina en pacientes con enfermedad de Chagas, sin antecedente clínico de leishmaniosis, actual o antigua. Una muestra de 102 personas infectadas por Trypanosoma cruzi (14 casos agudos con diagnóstico parasitológico y 88 casos crónicos a través de la demostración de anticuerpos IgG por ELISA e inmunofluorescencia indirecta (IFI) fueron evaluados con leishmanina, antígeno soluble que contenia Leishmania (Viannia) peruviana a la concentración de 25-30 ug/mL. Solo cinco personas presentaron reacción de hipersensibilidad cutánea a la aplicación del antígeno a las 48-72 h. La leishmanina evaluada fue negativa en 97 personas infectadas con T. cruzi, con lo cual se alcanzó una especificidad del 95,1%. En conclusión, la prueba intradérmica de Montenegro es una herramienta diagnóstica simple y eficaz, que además podría ser utilizada para discriminar infecciones por Leishmania o T. cruzi, en áreas geográficas del Perú donde ambos parásitos están presentes.
Palabras clave: Enfermedad de Chagas; Leishmaniosis; Diagnóstico; Hipersensibilidad retardada (fuente: BIREME).
ABSTRACT
In order to assess the specificity of the leishmanin skin test in Chagas disease patients without clinical history of leishmaniasis, present or former. A sample of 102 persons infected with Trypanosoma cruzi (14 acute cases with parasitological diagnosis and 88 chronic cases) through the demonstration of IgG antibodies by ELISA and indirect immunofluorescence (IIF) were evaluated with leishmanin soluble antigen which contained Leishmania (Viannia) peruviana concentration of 25-30 ug/mL. Only five people showed cutaneous hypersensitivity reaction to the application of the antigen between hours 48 and 72. The Leishmanin skin test evaluated was negative in 97 people infected with T. cruzi, thus specificity of 95.1% was achieved. In conclusion, the intradermal Montenegro test is a simple and effective diagnostic tool that also could be used to discriminate infections by Leishmania or T. cruzi, in Peruvian geographic areas where both parasites are present.
Key words: Chagas disease; Leishmaniosis; Diagnosis; Hypersensitivity, delayed (source: MeSH NLM).
INTRODUCCIÓN
Leishmania spp. y Trypanosoma cruzi, son protozoarios de la familia Trypanosomatidae, causantes de leishmaniosis y enfermedad de Chagas respectivamente, las que son consideradas enfermedades tropicales desatendidas (1), ampliamente distribuidas en la región amazónica del Perú donde coexisten (2). Para la evaluación serológica de la infección por estos agentes, se emplean antígenos de parásitos enteros, como la prueba de inmunofluorescencia indirecta (IFI) o proteínas solubles totales (ELISA); sin embargo, al pertenecer a la misma familia, es común la reactividad cruzada (3), lo que dificulta el diagnóstico serológico confiable.
Los estudios que han evaluado tanto la prueba de IFI como ELISA para el diagnóstico diferencial entre leishmaniosis y enfermedad de Chagas sugieren bajos índices de reacción cruzada al emplear nuevos métodos diagnósticos, con antígenos recombinantes o de tercera generación, con reacciones cruzadas entre 0 a 3% (4). Sin embargo, estos exámenes tienen un costo elevado y no están disponibles en el primer nivel de atención.
En Perú se emplea, además de las pruebas serológicas, la reacción intradérmica de Montenegro con leishmanina, que evalúa la reacción de hipersensibilidad cutánea retardada a antígenos de promastigotes de Leishmania (Viannia) peruviana, con altos índices de positividad en personas con diversas formas clínicas de leishmaniosis, resultando ser una prueba muy sensible (5), en particular para enfermedad activa (6). Dado que su especificidad era cuestionada, una evaluación preliminar en una muestra pequeña de siete personas con enfermedad de Chagas mostró una especificidad del 100% (7).
El presente estudio tuvo como objetivo determinar la especificidad de la leishmanina en pacientes afectados con enfermedad de Chagas. Ello permitira evaluar la utilidad de una prueba diagnóstica simple y de uso mayoritario, con potencial valor en el diagnóstico diferencial entre infecciones por Leishmania y T. cruzi, contribuyendo a establecer de manera eficaz la naturaleza de la enfermedad, principalmente en áreas geográficas donde ambos parásitos confluyen.
EL ESTUDIO
Se realizó un estudio observacional descriptivo que incluyó el enrolamiento de pacientes con enfermedad de Chagas entre julio de 2003 a diciembre de 2004, en los departamentos de Amazonas, Cajamarca, San Martín, Moquegua, Tacna y Arequipa. En Amazonas fueron las localidades de Cajaruro y El Ron en la provincia de Bagua; en Cajamarca, el distrito de Cutervo; Saposoa y Lamas en San Martin; Tiabaya en Arequipa y Tarata en Tacna. Las áreas de estudio se eligieron por ser endémicas para la enfermedad de Chagas (2).
Se priorizó la búsqueda de pacientes con la enfermedad confirmada por demostración del parásito y cuyas viviendas fueran accesibles. La muestra estuvo constituida por todos los pacientes con enfermedad de Chagas, confirmado por demostración del parásito o serología positiva (concordancia de las pruebas de IFI y ELISA). Para ello, se coordinó y mantuvo comunicación permanente con el personal de laboratorio de las regiones o subregiones de salud en las que se llevó a cabo el estudio. Se excluyeron a niños menores de tres años y gestantes, así como a pacientes chagásicos con antecedentes de lesiones leishmaniásicas activas o cicatriciales, que fueron demostradas al examen clínico. Debido a que la enfermedad de Chagas es usualmente asintomática, el número de pacientes diagnosticados en estado agudo es escaso; por ello, se estimó por conveniente recolectar una muestra de cien casos para evaluar la especificidad de la prueba.
Los datos y antecedentes clínico-epidemiológicos de cada paciente fueron registrados en una ficha diseñada para este fin que, además, incluía información sobre antecedentes de residencia o viaje a zonas endémicas de leishmaniosis; además, se preguntó sobre antecedentes de lesiones de origen leishmaniásico. Para la evaluación, a todos los pacientes se les aplicó, vía intraepidérmica, 0,1 mL de leishmanina, en el tercio anterior de la cara ventral del antebrazo. La lectura de la reacción de hipersensibilidad se efectuó, según patrón establecido, entre las 48 y 72 h posteriores a la aplicación del antígeno. La prueba se consideró positiva si el diámetro promedio de induración de la pápula fue ³ a 6 mm en el sitio de inoculación.
La leishmanina evaluada, fue preparada en el Laboratorio de Leishmaniosis del Instituto Nacional de Salud (INS), siguiendo la metodología de Reed et al. (8), utilizando formas promastigotes de la cepa L. (V.) peruviana MH0M/PE/84/LC26 identificada por análisis de zimodemas e hibridación del kDNA, procedente del Instituto de Medicina Tropical “Alexander von Humboldt” de la Universidad Peruana Cayetano Heredia.
En los pacientes con resultado de leishmanina positivo, se realizó el descarte de lesiones leishmaniásicas mediante observación clínica; de estos pacientes, se solicitó muestra de sangre para el estudio serológico, y en tres de ellos se corroboró la infección por detección de anticuerpos IgG anti-T. cruzi mediante las pruebas de ELISA (Chagatest ELISA recombinante v.3.0, Wiener lab.) e IFI.
A todos los participantes se les informó la finalidad del estudio y se solicitó el consentimiento por escrito; los menores de edad fueron autorizados por sus padres.
HALLAZGOS
De los 102 pacientes con resultados de lectura de la prueba intradérmica, catorce fueron casos agudos y tuvieron diagnóstico parasitológico confirmatorio (gota gruesa, cultivo, PCR o xenodiagnóstico), diez de ellos con presencia de signo de Romaña; en los 88 restantes, en fase crónica de la enfermedad, se demostró la presencia de anticuerpos IgG anti-Trypanosoma cruzi, mediante las pruebas de ELISA e IFI. Del total, 41 (40,1%) fueron varones, con una edad promedio de 28,8 ± 23,7 años, 40 de ellos se encontraban recibiendo tratamiento para la enfermedad de Chagas.
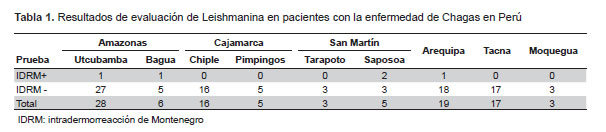
De los cinco pacientes con reacción positiva a la leishmanina, dos provinieron de Amazonas y dos de San Martín, departamentos pertenecientes a la región nororiental del Marañon, áreas geográficas donde cocirculan ambos agentes, siendo 4/63 (6,3%) reactores a la prueba; cuatro de ellos recibieron tratamiento para la enfermedad de Chagas, ninguno tuvo signo de Romaña. De los pacientes con lecturas negativas, 40 tuvieron tratamiento para la enfermedad de Chagas: cuatro de ellos se encontraban en curso de tratamiento durante la evaluación y ocho habían finalizado tratamiento en los últimos dos meses (Tabla 1).
La lectura de la prueba intradérmica a las 48-72 h, reveló que en 5 de 102 personas (4,9%) infectadas con T. cruzi, se evidenció reacción de hipersensibilidad cutánea a la aplicación del antígeno, mientras que en 97 de 102 personas (95,1%) la prueba intradérmica resultó negativa.
DISCUSIÓN
Los resultados obtenidos muestran una alta especificidad de la leishmanina preparada con L. (V.) peruviana en pacientes con enfermedad de Chagas. Estos resultados son similares a los previamente reportados en muestras pequeñas (5,7), por Reed et al.(8), como resultado de la aplicación de leishmanina, en menos del 5% de pacientes chagásicos, cuando se utilizó extracto soluble de L. donovani donovani a la dosis de 25 ug proteínas/mL, como antígeno. Así como con otras publicaciones que han empleado otras especies de Leishmania y procedimientos de diagnóstico de certeza, tales como el PCR (9).
De los casos positivos a la leishmanina, tres de ellos provenían de zonas endémicas de leishmaniosis, lo que podría sugerir que estarían infectados con parásitos de Leishmania spp y que aún no desarrollaban la enfermedad. Por otro lado, al ser la leishmanina un antígeno extracto proteíco soluble, es de esperar que compartan epítopes en común, ya que, como se conoce, Leishmania y Trypanosoma, son trypanosomatídeos estrechamente relacionados. Además, es posible que estos pacientes hayan sido evaluados previamente con la leishmanina dado que provienen de zonas endémicas para Leishmania, y ello podría haber inducido su respuesta cutánea, tal como lo sugieren los estudios que evaluaron aplicaciones secuenciales de la leishmanina (10,11).
Al hacer un análisis diferenciado de la reactividad a la leishmanina, en relación a la procedencia geográfica de infección, se encontró que para los pacientes chagásicos procedentes de la región nororiental del Marañón, donde cocirculan parásitos de Leishmania spp y T. cruzi, la especificidad fue de 93,7%. En áreas endémicas para la enfermedad de Chagas, 38/39 tuvo reacción a la leishmanina, dando una especificidad de 97,4%; el caso reactivo correspondió a un varón de 18 años, diagnosticado en la Universidad San Agustín de Arequipa, con antecedente de viaje a un área endémica de leishmaniosis en el Cusco, donde pernoctó en el campo.
La reactividad cruzada entre estos parásitos está ampliamente estudiada, las primeras descripciones se hicieron en 1980, cuando Fuller et al. (12) reportaron que antígenos hechos con cultivos de T. cruzi pueden dar reacciones positivas en casos activos de leishmaniosis cutánea en las Américas, pero en magnitud menor a los producidos por antígenos de Leishmania. En el Perú, Cornejo y Lumbreras reportaron reacción a la leishmanina a las 48 h en 3 de 9 personas con enfermedad de Chagas comprobada por xenodiagnóstico, durante la ejecución de una encuesta epidemiológica sobre la enfermedad de Chagas efectuada en el valle de Majes del departamento de Arequipa (13). Según los autores, ninguna de estas personas tuvo antecedentes de leishmaniosis tegumentaria.
La diferencia con los resultados que reportamos, podría obedecer a la naturaleza de la leishmanina empleada, que en nuestro caso fue un extracto proteico soluble preparado con L. (V.) peruviana, evaluada en un estudio previo como alternativa a la L. braziliensis (5), empleada por Cornejo y Lumbreras. Al respecto, otras especies de Leishmania no han resultado ser igual de efectivas en la prueba de leishmanina, por ejemplo, en Brasil se evaluó L. (L.) amazonensis con solo una sensibilidad del 52% en pacientes con diagnóstico parasitológico de leishmaniosis (14). Recientemente, Rojas et al. (15), evaluaron la leishmanina en residentes sanos de una localidad endémica de la enfermedad de Chagas, en Cochabamba, Bolivia, sin encontrar reactividad, aun en aquellos que tuvieron serología positiva anti-T. cruzi.
Las condiciones propias del trabajo de campo limitaron realizar una revisión clínica exhaustiva de los pacientes que resultaron positivos a la leishmanina, que permitiera, a su vez, detectar antecedentes de lesiones por leishmaniosis, lo que se considera una limitación del estudio pues podría haber influenciado en el porcentaje de especificidad que se reporta.
En conclusión, la prueba intradérmica de Montenegro, utilizando leishmanina elaborada con Leishmania (Viannia) peruviana, a la concentración de 25-30 ug/mL, resultó negativa en 97 de 102 pacientes infectados con T. cruzi, evidenciando una especificidad de 95,1%; solo en 5 de 102 pacientes presentó reacción a la leishmanina. La prueba intradérmica con aplicación de la leishmanina es una herramienta diagnóstica simple y eficaz, utilizada ampliamente para la confirmación de infecciones por Leishmania, que además podría ser utilizada para discriminar infecciones por Leishmania o T. cruzi, en áreas donde ambos parásitos están presentes.
Contribuciones de autoría: GMG tuvo la idea y concepción del estudio, redactó e hizo la revisión crítica del manuscrito; GMG y SVA participaron en la recolección, análisis e interpretación de los datos; YMZ, EPM y FDD contribuyeron con el marco muestral y búsqueda de pacientes; SVA participó también en la revisión crítica del manuscrito.
Fuentes de financiamiento: el estudio fue financiado por el Instituto Nacional de Salud del Perú.
Conflictos de interés: los autores declaran no tener conflictos de interés.
Referencias Bibliográficas
1. World Health Organization. WHO exhorts dracunculiasis-endemic countries to achieve interruption of transmission by 2015 [Internet]. Ginebra: WHO; c2014 [citado el 19 de marzo de 2013]. Disponible en: http://www.who.int/neglected_diseases/en/
2. Cabrera CR. Enfermedad de Chagas o Trypanosomiasis americana CIE - 10: B57 . En: Protocolos de vigilancia epidemiológica. Parte I. 2a ed. Lima: Oficina General de Epidemiología, Ministerio de Salud; 2006. p. 87-114. [ Links ]
3. Carmelo E, Martínez E, González AC, Piñero JE , Patarroyo ME , Del Castillo A , et al. Antigenicity of Leishmania braziliensis histone H1 during cutaneous leishmaniasis: localization of antigenic determinants . Clin Diagn Lab Immunol. 2002 Jul;9(4):808-811. [ Links ]
4. Caballero ZC, Sousa OE, Marques WP, Saez-Alquezar A, Umezawa ES. Evaluation of serological tests to identify Trypanosoma cruzi infection in humans and determine cross-reactivity with Trypanosoma rangeli and Leishmania spp . Clin Vaccine Immunol. 2007 Aug;14(8):1045-9. [ Links ]
5. Minaya G, Torres Y, Farfán M, Mendizabal L, Colchado M, Arroyo E. Evaluación de la intradermorreacción con antígenos de Leishmania (Viannia) peruviana y Leishmania (Viannia) braziliensis en áreas endémicas de leishmaniasis en el Perú . Rev Peru Med Exp Salud Publica. 1999;16(1-2):5-14. [ Links ]
6. Guarín N, Palma GI, Pirmez C, Valderrama L, Tovar R, Saravia NG. Comparative immunohistological analysis of the Montenegro skin test reaction in asymptomatic infection and in acute and chronic cutaneous leishmaniasis . Biomedica. 2006 Oct;26 Suppl 1:38-48. [ Links ]
7. Minaya G, Arroyo E, Vargas J, Gonzáles A. La prueba intradérmica de Montenegro (IDR) en pacientes con enfermedad de Chagas: observación preliminar . Rev Peru Med Exp Salud Publica. 2002;19(3):146-8. [ Links ]
8. Reed SG, Badaró R, Masur H, Carvalho EM , Lorenco R , Lisboa A , et al. Selection of a skin test antigen for American visceral leishmaniasis . Am J Trop Med Hyg. 1986 Jan;35(1):79-85. [ Links ]
9. Faber WR, Oskam L, van Gool T, Kroon NC , Knegt-Junk KJ , Hofwegen H , et al. Value of diagnostic techniques for cutaneous leishmaniasis . J Am Acad Dermatol. 2003 Jul;49(1):70-4. [ Links ]
10. Borges VC, Ruiz MC, Gomes PM, Colombo AR, Silva Lde A, Romero HD, et al. Intradermorreação de Montenegro após sucessivas repetições do teste em Porteirinha, MG . Rev Soc Bras Med Trop. 2003 Mar-Apr;36(2):249-51. [ Links ]
11. Freire F, da Silva I, Araújo MI, Almeida RP, Bacellar O, Carvalho EM. Avaliação do poder sensibilizante da reação de Montenegro . Rev Soc Bras Med Trop. 2001 Nov-Dec;34(6):537-42. [ Links ]
12. Fuller G, Lemma A, Haile T. A comparison of skin test responses using antigen from Leishmania donovani and a lizard trypanosome . Trans R Soc Trop Med Hyg. 1980;74(2):205-8. [ Links ]
13. Cornejo D, Lumbreras C. Encuesta Epidemiológica sobre Enfermedad de Chagas en el Valle de Majes. Presentación de diez nuevios casos, 1951. Arch Per Patolog Clin. 1952;5:13-39. [ Links ]
14. Silveira FT, Lainson R, Shaw JJ, De Souza AA, Ishikawa EA, Braga RR. Cutaneous leishmaniasis due to Leishmania (Leishmania) amazonensis in Amazonian Brazil, and the significance of a negative Montenegro skin-test in human infections . Trans R Soc Trop Med Hyg. 1991 Nov-Dec;85(6):735-8. [ Links ]
15. Rojas E, Guzmán-Rivero J, Verduguez-Orellana A, Montaño N. Utilidad de la prueba de Montenegro (IDRM) como herramienta para la vigilancia epidemiológica de Leishmaniasis cutánea en áreas de Bolivia donde coexiste la infección por Leishmania spp y T. Cruzi . Gac Med Bol. 2012;35(2):55-8. [ Links ]
Correspondencia: Gloria Minaya
Dirección: Laboratorio de Leishmaniasis, Instituto Nacional de Salud, Lima - Perú.
Teléfono: 748-1111 Anexo 2167
Correo electrónico: gminaya@ins.gob.pe
Recibido:
26-09-13Aprobado: 12-02-14