Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Peruana de Medicina Experimental y Salud Publica
Print version ISSN 1726-4634
Rev. perú. med. exp. salud publica vol.32 no.3 Lima July/set. 2015
Artículo de Revisión
Revisión sistemática sobre la efectividad de intervenciones basadas en la comunidad en la disminución de la mortalidad neonatal
Systematic review of the efectiveness of community-based interventions to decrease neonatal mortality
Adrián V. Hernández1,a, Vinay Pasupuleti2,b, Vicente Benites-Zapata3,c, Enrique Velásquez-Hurtado4,d, Jessica Loyola-Romaní4,e, Yuleika Rodríguez-Calviño4,c, Henry Cabrera-Arredondo4,f, Marco Gonzales-Noriega4,g, Walter Vigo-Valdez4,h
1 Escuelas de Posgrado y Medicina, Universidad Peruana de Ciencias Aplicadas. Lima, Perú.
2 Department of Medicine, Case Western Reserve University, Cleveland. Ohio, EE. UU.
3 Facultad de Medicina, Universidad Particular San Martin de Porres. Lima, Perú.
4 Programa de Apoyo a la Reforma del Sector Salud (PARSALUD II). Lima, Perú.
a Médico cirujano, magíster en Epidemiología Clínica, doctor en Epidemiología Clínica; b médico cirujano, magíster en Salud Pública, doctor en Salud Pública; c médico cirujano; d médico cirujano, magíster en Salud Pública; e bibliotecóloga, magíster en Gestión de la Información y del Conocimiento; f médico cirujano, magíster en Salud Pública; g estadístico, magíster en Epidemiologia Clínica; h médico cirujano, magíster en Gerencia de Proyectos y Programas Sociales
RESUMEN
Se evalúa la eficacia/efectividad de las intervenciones basadas en la comunidad, destinadas a disminuir la mortalidad neonatal. Se realizó una revisión sistemática de ensayos controlados aleatorizados, ensayos aleatorizados de comunidad y estudios de cohortes de intervenciones dirigidas a la mujer gestante, al neonato (hasta 28 días de nacido) o a ambos. Se evaluaron 34 estudios (n=844,989): 20 en mujeres gestantes (n=406,172); 6 en neonatos (n=24,994), y 8 en ambos grupos (n=413,823). El riesgo de sesgo fue generalmente bajo. Hubo heterogeneidad entre los tipos de intervenciones. Las intervenciones educación materna en salud y cuidado en casa de madres y neonatos estuvieron asociadas con disminución de mortalidad neonatal en la mitad de los seis estudios de cada grupo. La suplementación materna con multimicronutrientes, el cuidado de madre canguro y la suplementación materna prenatal con vitamina A no disminuyeron la mortalidad neonatal. Pocas intervenciones comunitarias heterogéneas han demostrado disminuir la mortalidad neonatal.
Palabras clave: Revisión; Efectividad; Estudios de intervención; Mortalidad infantil (fuente: DeCS BIREME).
ABSTRACT
We evaluated the efficacy/effectiveness of community-based interventions to decrease neonatal mortality. A systematic review of randomized controlled trials, cluster randomized trials and cohort studies of interventions on pregnant women, neonates (up to 28 days after birth) or both was made. Thirty four studies were evaluated (n=844,989): 20 in pregnant women (n=406,172), 6 in neonates (n=24,994), and 8 in both (n=413,823). Risk of bias was generally low. There was heterogeneity among interventions. Interventions such as maternal health education and maternal and neonatal home care were associated to a decrease in neonatal mortality in half of the 6 studies of each group. Supplementation with multiple micronutrients, kangaroo mother care, and maternal supplementation with vitamin A did not decrease neonatal mortality. A few heterogeneous community-based interventions demonstrated a decrease in neonatal mortality.
Key words: Review; Effectiveness, Intervention studies; Infant mortality (source: MeSH NLM).
INTRODUCCIÓN
La mortalidad neonatal puede ser temprana cuando se presenta en los primeros siete días de vida, o tardía si la muerte ocurre entre los siete y los 28 días de vida. La mayor cantidad de muertes neonatales se da durante los siete primeros días de vida; principalmente debido a una cobertura inadecuada de atención por parte de los servicios de cuidado prenatal y de atención del parto (1-2), además de una inadecuada capacidad resolutiva de los servicios de salud en la atención del recién nacido y sus complicaciones. La infección neonatal y las complicaciones asociadas al parto prematuro y bajo peso al nacer son las morbilidades más frecuentemente asociadas con mortalidad durante los primeros 28 días de vida (3). En países de bajos y medianos ingresos, la desnutrición y la baja educación de la madre, los niveles elevados de ruralidad y la poca e inadecuada oferta de los servicios de salud son factores asociados con mayor mortalidad neonatal (2-3).
Se realizó un estudio con casi 8000 embarazos en seis países en desarrollo que incluía al Perú, la mortalidad neonatal temprana fue de 9 por mil nacidos vivos (1); esta cifra es el triple de lo reportado para países desarrollados (2). El estudio también reporta que las principales causas de muerte en el periodo perinatal fueron la enfermedad hipertensiva del embarazo y el parto prematuro. En ese estudio las complicaciones derivadas del nacimiento prematuro fueron responsables del 62% de las muertes neonatales en la primera semana de vida. El parto prematuro y el bajo peso al nacer son la cuarta causa de carga de enfermedad en el Perú y la sepsis neonatal se encuentra dentro de las primeras 40 causas de carga de enfermedad en el Perú (4).
En los países poco desarrollados, y sobre todo en sus comunidades rurales, la incidencia de parto domiciliario es elevada. Casi las dos terceras partes de las gestantes en África tienen parto domiciliario. A pesar de la mejora de los sistemas de salud y de la implementación de diversas políticas sanitarias la mortalidad neonatal persiste elevada en estos países (3).
En países de bajos y medianos ingresos el control prenatal y el parto tienen bajas coberturas en las comunidades rurales. Factores relacionados con el acceso geográfico, económico y cultural pueden mermar la posibilidad que una gestante acuda a un establecimiento de salud (5). Existen muchos otros factores que se suman y hacen que la mortalidad neonatal persista elevada en lugares donde existe inequidad a pesar de la mejora en tecnologías sanitarias (6).
Las intervenciones basadas en la comunidad son aquellas intervenciones que se dirigen a un grupo de personas o una comunidad, pero no a un solo individuo; excluye intervenciones implementadas en ámbitos clínicos y las dirigidas a poblaciones tan grandes como países o estados; se dan dentro del marco de un programa de salud pública (7); en otras palabras, la intervención se circunscribe al ámbito de la comunidad y es proporcionada como una política sanitaria (8). Es por ello, que la finalidad de las intervenciones basadas en la comunidad es disminuir el impacto de los problemas de salud pública. No obstante, hay que determinar cuál de estas intervenciones basadas en la comunidad son las más costo-efectivas (9).
La mortalidad neonatal es considerada un problema de salud pública. Se han llevado a cabo muchas intervenciones basadas, mayormente, en comunidades rurales localizadas en países con bajos y medianos ingresos, con el fin de disminuir la mortalidad neonatal (10). Las intervenciones basadas en la comunidad para disminuir la mortalidad neonatal pueden ser aplicadas en el periodo prenatal (antes del parto), en el intraparto o posnatal (10). Estas intervenciones basadas en la comunidad van dirigidas hacia el cambio de conducta de las gestantes respecto al cuidado prenatal y hacia una atención adecuada del binomio madre-recién nacido en el domicilio (11). Por otro lado, hay también intervenciones basadas en la comunidad que buscan la capacitación del personal de salud y de agentes comunitarios y parteras tradicionales (12).
Entre las principales intervenciones dirigidas a la madre se encuentran las intervenciones educativas para mejorar en las madres el cuidado prenatal (13), generación de hábitos de vida saludable (14), suplementación con multimicronutrientes, vitaminas y proteínas durante el embarazo (15), quimioprofilaxis antimalárica y uso de mosquiteros impregnados con insecticida en zonas endémicas de malaria (16), y aplicación, a la madre, de vacunas contra el neumococo y el tétanos (17).
Las intervenciones dirigidas al neonato incluyen la atención adecuada al recién nacido (18,19), la correcta asepsia del cordón umbilical (20), la prevención de la hipotermia -incluyendo el uso de madre canguro- y la hipoglicemia (21,22), la lactancia materna y las visitas domiciliarias durante el periodo posnatal (23). Las intervenciones pueden ser administradas por agentes comunitarios y parteras tradicionales capacitados en temas de promoción de la salud, educación prenatal y suplementación de multimicronutrientes, así como en la atención del recién nacido durante el parto y también para realizar el cuidado posnatal (24-26). Las intervenciones basadas en la comunidad para disminuir la mortalidad lograrían mostrar resultados costo-efectivos aumentando el número de atenciones de control prenatal y parto; sin embargo, el cambio podría durar poco tiempo sino se sostienen estas intervenciones a lo largo de los años (27).
El gobierno cumple un rol central a través del Ministerio de Salud (MINSA) para fortalecer los establecimientos de salud a los cuales accede la mayor parte de la población; además, debe asegurar la generación de políticas públicas para garantizar la oferta adecuada de los servicios de salud (28). Es muy importante que el Gobierno adopte políticas públicas para disminuir la mortalidad neonatal. Las políticas públicas deben ser costo-efectivas y deben ser basadas en la mejor evidencia disponible (29). Conocer la eficacia y la efectividad de las intervenciones destinadas a disminuir la mortalidad neonatal permitirá diseñar estrategias y políticas públicas orientadas de acuerdo a la evidencia disponible, a los recursos que posee el gobierno y acorde al contexto donde se pretende ejecutar la intervención.
En esta revisión sistemática se evalúa la eficacia y efectividad de las intervenciones basadas en la comunidad, destinadas a disminuir la mortalidad neonatal al evaluar ensayos controlados aleatorizados y estudios observacionales. Así, se busca establecer recomendaciones para mejorar la eficacia de las intervenciones basadas en la comunidad ya existentes e implementar aquellas no provistas por el MINSA, y que disminuyan significativamente la mortalidad neonatal.
MÉTODOS
CRITERIOS DE SELECCIÓN
Tipos de estudio:
· Ensayos controlados aleatorizados.
· Ensayos aleatorizados comunitarios o ensayos de campo.
· Estudios de cohorte prospectivos y retrospectivos.
Tipos de participantes:
· Gestantes mayores de 18 años de edad.
· Recién nacidos hasta los 28 días de vida.
· Gestantes sin historia previa de enfermedades metabólicas e inmunosupresión.
· Recién nacidos sin historia previa de enfermedades congénitas.
Tipos de intervenciones:
Las intervenciones estudiadas fueron predefinidas, utilizando como principal insumo una lista elaborada en base a la publicación de Bhutta et al. (10). Tres autores (AVH, EVH, JLR) evaluaron todas las intervenciones para restringir la lista a aquellas dirigidas a la comunidad y no a los servicios de salud. Se identificaron artículos de estudios que realicen sobre la población descrita una o más de las siguientes intervenciones definidas a priori:
INTERVENCIONES A LA MADRE
· Escolaridad/Educación de la salud materna.
· Paquetes de cuidado prenatal.
· Suplementación proteica.
· Suplementación proteico-energética balanceada.
· Suplementación con hierro.
· Suplementación con folato.
· Suplementación con yodo.
· Suplementación prenatal con vitamina A.
· Suplementación con zinc.
· Suplementación con multimicronutrientes.
· Quimioprofilaxis para malaria.
· Protección contra malaria con el uso de mosquiteros impregnados con insecticida.
· Inmunización con toxoide tetánico y parto limpio.
· Inmunización neumocócica materna.
· Promoción del cese del tabaquismo durante el embarazo.
· Promoción del cese de la ingesta de alcohol durante el embarazo.
· Paquetes de cuidado materno.
· Adherencia a los servicios de salud durante el embarazo.
· Parto en un centro de salud u hospital.
INTERVENCIONES AL NEONATO
· Antisepsia del cordón umbilical.
· Manejo y prevención de la hipotermia.
· Manejo y prevención de la hipoglicemia.
· Lactancia materna.
· Prevención y tratamiento de oftalmia neonatorum.
· Cuidado madre canguro.
· Entrenamiento en atención del parto tradicional y entrenamiento de trabajadores de salud comunitarios.
Desenlace primario: mortalidad neonatal
MÉTODOS DE BÚSQUEDA PARA LA IDENTIFICACIÓN DE ESTUDIOS
Se realizaron búsquedas en MEDLINE, EMBASE, SCOPUS, Web of Science, LILACS, La Biblioteca Cochrane, y el registro de ensayos clínicos del gobierno de EE. UU. (www.clinicaltrials.gov). Se elaboró un modelo de búsqueda para MEDLINE usando términos controlados MeSH (Medical Subject Headings) y términos libres para los demás buscadores. No hubo restricción por el idioma del artículo, y las búsquedas se hicieron desde el año de creación del buscador. Adicionalmente, se buscaron manualmente las referencias de estudios seleccionados.
Se realizó las búsquedas electrónicas por cada uno de las intervenciones predefinidas entre el 25 y 31 de mayo de 2014. Las estrategias de búsqueda detalladas se encuentran en el Anexo 1. Dado que se detectaron palabras clave relevantes adicionales durante cualquiera de las búsquedas electrónicas o búsquedas manuales, se modificaron las estrategias de búsqueda electrónicas para incorporar estos nuevos términos y se documentaron los cambios.
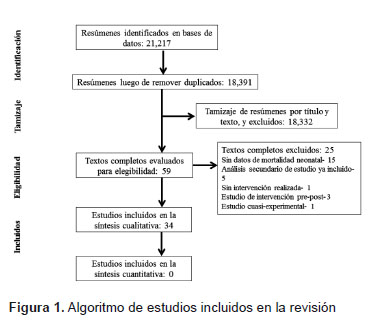
Dos autores (VBZ, VP) revisaron independientemente el resumen, título o ambos de cada uno de los resúmenes obtenidos en todas las estrategias de búsqueda. Todos los estudios potencialmente relevantes fueron buscados en texto completo. Cualquier discrepancia fue resuelta a través de consenso o discusión con un tercer revisor (AVH). Presentamos una figura del proceso de selección de estudios de acuerdo a las guías PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses) (30).
EXTRACCIÓN Y ANÁLISIS DE LOS DATOS
Para los estudios que cumplen con los criterios de inclusión, dos autores (VBZ, VP) extrajeron independientemente características de los participantes, de las intervenciones y de los desenlaces usando formatos de extracción de datos estándares previamente desarrollados. Cualquier desacuerdo fue resuelto por discusión, o si era requerido por un tercer autor (AVH). Debido a que se contó con la información relevante en todos los casos, no fue necesario contactar a los autores de estudios escogidos para preguntar acerca de información no publicada y relevante para el estudio.
En caso de publicaciones duplicadas, documentos acompañantes o reportes múltiples de un estudio primario, se maximizó la extracción al evaluar todo lo disponible y usar la información más completa de todos los artículos disponibles de cada estudio. Se empleó el periodo de seguimiento más largo asociado con los desenlaces primarios o secundarios.
Dos autores (VBZ, VP) evaluaron independientemente el riesgo de sesgo de cada estudio incluido. Cualquier desacuerdo fue resuelto por consenso o por consulta con un tercer autor (AVH). El riesgo de sesgo de los ensayos controlados aleatorizados fue identificado con el instrumento de evaluación de riesgo de sesgo de la Colaboración Cochrane (31,32). Se estimaron los siguientes criterios en la evaluación de riesgo de sesgo de ensayos aleatorizados:
· Generación de la secuencia de aleatorización (sesgo de selección).
· Ocultamiento de la asignación (sesgo de selección).
· Cegamiento (sesgo de detección y de performance), cegamiento de participantes y personal evaluados separadamente del cegamiento de la evaluación de los desenlaces.
· Datos de desenlaces incompletos (sesgo de desgaste).
· Reporte selectivo (sesgo de reporte).
· Otros sesgos.
En caso de los ensayos aleatorizados comunitarios, otros sesgos corresponden a: sesgo de reclutamiento, desigualdad de características de grupos o individuos al inicio del ensayo, desenlaces faltantes de grupos o individuos, y métodos estadísticos inadecuados (31).
Dentro de cada ensayo aleatorizado cada criterio fue descrito como "bajo riesgo", "alto riesgo" o "riesgo no claro" de sesgo tal como está detallado en el Manual Cochrane para Revisiones Sistemáticas de Intervenciones (31).
La evaluación del riesgo de sesgo de estudios de cohorte fue hecha con la parte correspondiente de escala Newcastle-Ottawa o NOS (33). La evaluación de la escala NOS se hace por cada estudio de cohortes y evaluando con estrellas (de una a cuatro) cada uno de los tres criterios (selección, comparabilidad, desenlaces).
ANÁLISIS ESTADÍSTICO
Se expresaron lo efectos de las intervenciones en desenlaces continuos como diferencias de medias (MD) y en desenlaces dicotómicos como odds ratios (OR) o riesgos relativos (RR) con sus intervalos de confianza al 95% (IC 95%). Si los efectos de las intervenciones en desenlaces dicotómicos de algunos estudios son provistos como Hazard Ratios (HR), entonces se procedió a usar la metodología de Chinn et al. para convertirlos a OR (34). Se describen los análisis usados en los estudios: análisis por intención a tratar (ITT o intention-to-treat en Inglés) o por protocolo (PP).
Debido a que encontramos heterogeneidad clínica, metodológica o estadística sustancial, no se reportan en este estudio estimados de efectos agrupados en metaanálisis. Las fuentes de heterogeneidad fueron los tipos específicos de intervenciones, los tiempos de seguimiento, y tipos de diseño de estudios. Tampoco fue posible explorar subgrupos.
RESULTADOS
DESCRIPCIÓN DE LOS ESTUDIOS
Luego de quitar duplicados, identificamos 18 391 resúmenes de estudios únicos en los buscadores utilizados (Figura 1). Los resúmenes fueron tamizados para inclusión en el estudio y excluimos 18 332; las principales causas de exclusión fueron diseños de estudio diferentes a los referidos en 3.1.1 y la existencia de desenlaces diferentes a mortalidad neonatal. Los textos completos de 59 estudios fueron evaluados en detalle y, finalmente, se incluyeron 34 estudios (n=844,989) (18,21,23,24,26,35-63).
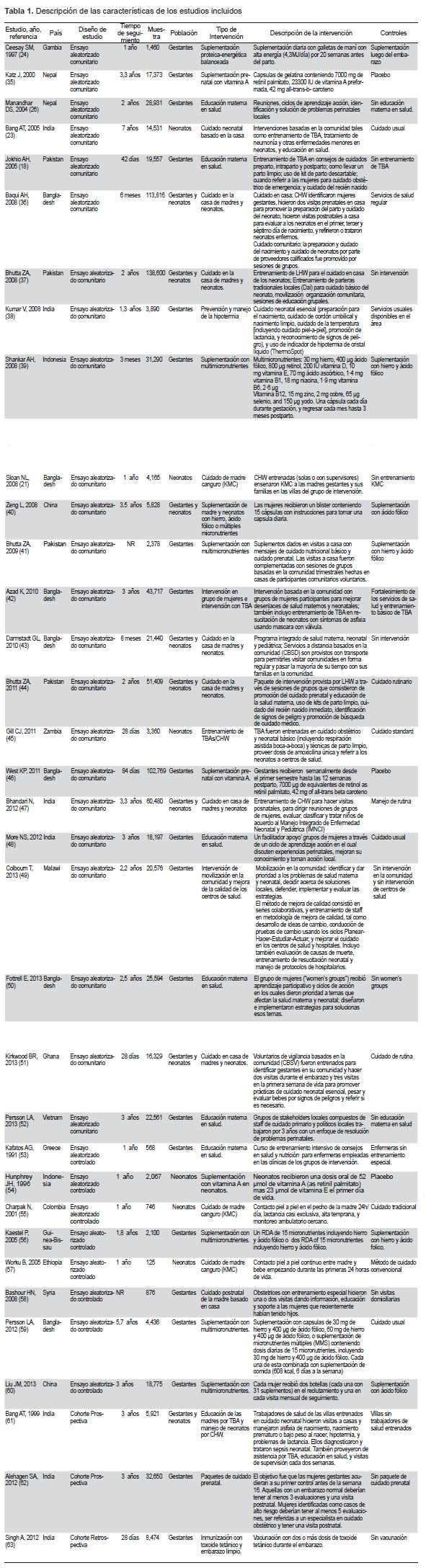
Veinte estudios fueron en mujeres embarazadas (n=406,172), 6 en neonatos (n=24,994), y 8 incluyeron ambos grupos (n=413,823) (Tabla 1). Los estudios fueron realizados en países de ingresos bajos y medianos, con excepción de un ensayo controlado aleatorizado, realizado en Grecia. Veintitrés estudios fueron ensayos aleatorizados de la comunidad, 8 ensayos controlados aleatorizados, y 3 estudios de cohortes. El riesgo de sesgo fue generalmente bajo, especialmente para los ensayos aleatorizados. Los estudios fueron, además, heterogéneos respecto a tamaños de muestra (de 125 a 138,600) y tiempos de seguimiento (de 7 días a 7 años). El grado de acuerdo intercodificadores fue alto (estadístico kappa 0,86).
RIESGO DE SESGO DE LOS ESTUDIOS INCLUIDOS
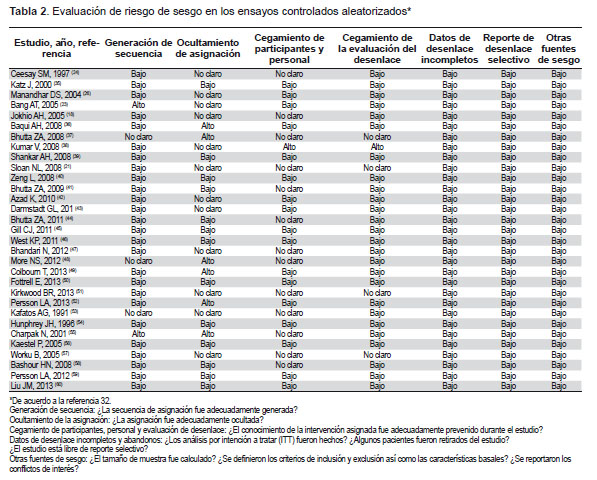
El riesgo de sesgo fue bajo en los 31 ensayos comunitarios y ensayos controlados aleatorizados (Tabla 2). El riesgo de sesgo fue bajo en los 3 estudios de cohortes, marcando 4 estrellas en todos los ítems de selección y desenlace de la escala NOS. La comparabilidad de los grupos en las tres cohortes fue moderada.
EFECTO DE LAS INTERVENCIONES ESPECÍFICAS
Cinco intervenciones basadas en la comunidad tuvieron al menos dos estudios.
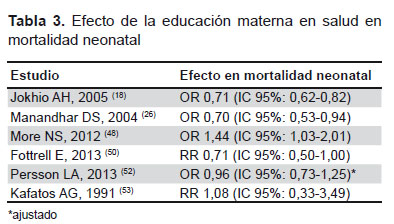
Seis estudios evaluaron diferentes intervenciones de educación materna en salud (18,26,48,50,52,53) (Tabla 3). Tres estudios mostraron reducción del riesgo de mortalidad neonatal (18,26,50); un estudio mostró aumento del riesgo de mortalidad neonatal (48), y dos estudios no mostraron ninguna asociación con mortalidad neonatal (52,53).
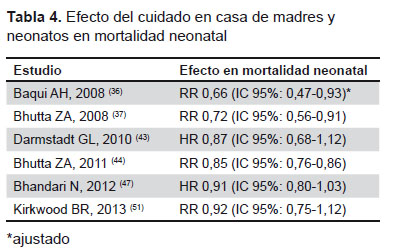
Seis estudios evaluaron diferentes intervenciones de cuidado en casa de madres y neonatos (36,37,43,44,47,51) (Tabla 4). Tres estudios estuvieron asociados con reducción de la mortalidad neonatal (36,37,44), mientras que los otros tres no encontraron reducción de la mortalidad neonatal (43,47,51).
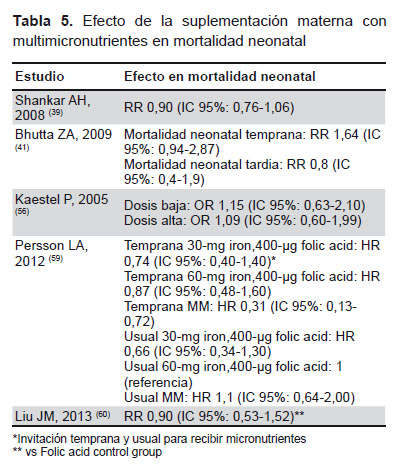
Cinco estudios evaluaron la suplementación con multimicronutrientes durante el embarazo (39,41,56,59,60) (Tabla 5). Solo una intervención muy específica de uso de multimicronutrientes en la etapa temprana del embarazo disminuyó el riesgo de mortalidad neonatal (59). Otros brazos de este estudio y los otros cuatro estudios no demostraron disminución del riesgo de mortalidad neonatal.
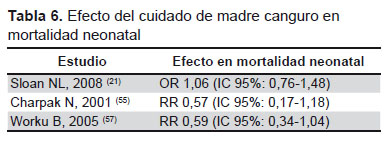
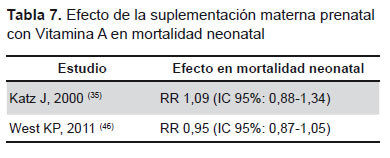
Tres estudios evaluaron el cuidado de madre canguro en neonatos (21,55,57) (Tabla 6). Ninguno de los estudios mostró asociación con disminución de mortalidad neonatal. Finalmente, dos estudios evaluaron la suplementación materna prenatal con vitamina A (35,46) (Tabla 7). Ninguno de estos estudios mostró asociación con la disminución de la mortalidad neonatal.
Las siguientes cinco intervenciones de estudio único no estuvieron asociadas con la disminución de la mortalidad neonatal: La suplementación proteico energética balanceada (24) (OR 0,64, IC 95%: 0,38-1,07), la suplementación materna y neonatal con multimicronutrientes (40) (RR 0,61, IC 95%: 0,34-1,10), la intervención en grupos de mujeres e intervención con parteras tradicionales (42) (RR 0,93, IC 95%: 0,80-1,09), la intervención de movilización en la comunidad y mejora de la calidad de centros de salud (49) (OR 0,78, IC 95%: 0,60-1,01), y el cuidado posnatal de la madre basado en casa (58) (RR 1,54, IC 95%: 0,26-9,91).
Otras cinco intervenciones evaluadas en estudios únicos sí demostraron asociación con la disminución de la mortalidad neonatal: el cuidado neonatal basado en casa (23) (RR 0,51, IC 95%: 0,44-0,60), la prevención y manejo de la hipotermia (38) (RR 0,48, IC 95%: 0,35-0,66), el entrenamiento de parteras tradicionales y trabajadores de salud comunitarios (45) (OR 0,55, IC 95%: 0,33-0,90), la suplementación de vitamina A en neonatos (54) (HR 0,36, IC 95%: 0,16-0,87), e Inmunización con dos o más dosis de toxoide tetánico a las embarazadas (63) (OR 0,45, IC 95%: 0,31-0,66). Finalmente, un estudio que evaluó paquetes de cuidado prenatal estuvo asociado con el aumento de la mortalidad neonatal (62) (RR 1,55, IC 95%: 1,40-1,72).
Tres estudios incluyeron la promoción de lactancia materna casi exclusiva dentro de intervenciones complejas destinadas a reducir mortalidad neonatal (38,55,61). Esto no permitió evaluar el efecto aislado de lactancia materna.
DISCUSIÓN
En la presente revisión sistemática se encontró que las intervenciones basadas en la comunidad para reducir la mortalidad neonatal son heterogéneas entre sí. Además, existe heterogeneidad sustancial de diseño entre los estudios aleatorizados y observacionales que evaluaron estas intervenciones; el riesgo de sesgo fue generalmente bajo. La mitad de los estudios que evaluaron intervenciones para mejorar la educación materna en salud y el cuidado en casa de madres y neonatos demostraron mejor eficacia/efectividad que sus controles. Las intervenciones comunitarias que evaluaron la suplementación de multimicronutrientes y vitaminas y el cuidado madre canguro no demostraron ser eficaces/efectivas. Otros tipos de intervenciones evaluadas en estudios únicos no demostraron ser mejores que sus controles en la mayoría de los casos.
Un artículo muy reciente de Wang et al. (64) del Global Burden of Disease Study 2013 mostró que en Perú la mortalidad neonatal temprana (8 por 1000 nacidos vivos) y neonatal tardía (2,7 por 1000 nacidos vivos) aún se mantienen en niveles elevados. Sin embargo, los riesgos del 2013 son menores que los observados en 2006 (1), estando por encima de lo reportado en países como Argentina, Chile, Uruguay, Colombia, Ecuador y Venezuela, siendo comparables con los de Paraguay, Brasil, Nicaragua, Honduras y muchos del Caribe. Junto a estos países, Perú también comparte la característica que aproximadamente el 50% de las muertes en niños <5 años se deben a mortalidad neonatal (64). De acuerdo con los porcentajes de cambio de riesgo de 1990 a 2013, Perú es uno de los países en vías de desarrollo que probablemente alcanzarán la meta de desarrollo del milenio 4 (en Inglés: The Millenium Development Goal 4) de reducir la mortalidad de niños <5 años en dos tercios de 1990 a 2015.
La exhaustiva revisión de Bhutta et al. (10) en estudios hechos en países en vías de desarrollo identificó varias intervenciones basadas en la comunidad dirigidas a gestantes, neonatos o a ambos para reducir desenlaces neonatales y perinatales, incluyendo mortalidad neonatal. En este estudio se usó estas intervenciones y se escogió luego de una discusión entre los autores a las intervenciones dirigidas a la comunidad y no a los servicios de salud. Así, se pudo manejar un número menor de intervenciones y buscar nuevas publicaciones de intervenciones ya evaluadas el 2004 por Bhutta et al (10) y en estudios con tamaños de muestra mayores.
Solamente la mitad de las intervenciones complejas agrupadas en educación materna en salud y cuidado en casa de la madre y neonato fueron eficaces (Tablas 1, 3 y 4). Jokhio et al (18), Manandhar et al. (26), y Fottrell et al. (50) encontraron además una reducción significativa en la mortalidad materna con la intervención de educación materna en salud. Estas tres intervenciones estuvieron dirigidas, fundamentalmente, a educar a las madres para enfrentar problemas perinatales y neonatales; estas actividades incluyeron consejos de cuidados preparto, intraparto y posparto; cómo llevar un parto limpio; uso de kit descartable de parto; cuándo referir a las mujeres para cuidado obstétrico de emergencia; cuidado del recién nacido; ciclos de aprendizaje acción, identificación y solución de problemas perinatales locales, y aprendizaje participativo. Las intervenciones que no encontraron eficacia de intervenciones educativas maternas de Persson et al (52) and Kafatos et al (53) fueron intervenciones educativas menos complejas y menos intensas; estas intervenciones incluyeron reuniones de grupos de interés locales (equipo de cuidado primario y políticos locales), trabajaron por 3 años con un enfoque de resolución de problemas perinatales; además, un curso de entrenamiento intensivo de consejos en salud y nutrición para enfermeras empleadas en las clínicas de los grupos de intervención materna. More et al (48) incluso, encontró aumento de mortalidad neonatal con una intervención educativa en ciclos de aprendizaje-acción revisando experiencias maternas previas y aprendiendo de ellas.
Los efectos de las intervenciones dirigidas al cuidado en casa de las madres y neonatos tuvieron una tendencia beneficiosa hacia una reducción de la mortalidad neonatal, aunque solo tres fueron significativas (36,37,44). Estas intervenciones incluyeron la identificación, por parte de agentes comunitarios de salud, de mujeres embarazadas, realización de dos visitas prenatales en casa para promover la preparación del parto y el cuidado del neonato, y de visitas posnatales a casa para evaluar a los neonatos en el primer, tercer y séptimo día de nacimiento, para la referencia o tratamiento de neonatos enfermos, el entrenamiento de parteras tradicionales locales para cuidado básico del neonato, la movilización organización comunitaria, y las sesiones de educación grupales. Dos de las otras tres intervenciones no significativas (47, 51) incluyeron entrenamiento de trabajadores de salud comunitarios para hacer visitas posnatales, para dirigir reuniones de grupos de mujeres, para evaluar, clasificar y tratar niños de acuerdo al manejo integrado de enfermedad neonatal y pediátrica, y el entrenamiento de voluntarios de vigilancia basados en la comunidad para identificar embarazadas en su comunidad y hacer dos visitas durante el embarazo y tres visitas en la primera semana de vida para promover prácticas de cuidado neonatal esencial, pesar y evaluar bebes por signos de peligro y referirlos si fuera necesario. El estudio no significativo de Darmstadt et al (43) incluyó una intervención menos elaborada que consistía fundamentalmente en visitas de madres y neonatos a sus comunidades para pasar más tiempo con sus familiares.
La falta de eficacia de la intervención con multimicronutrientes en mortalidad neonatal se ha observado en revisiones Cochrane donde la intervención con vitamina A se daba al neonato (65-68) o a la gestante (69). El cuidado de madre canguro (en Inglés: Kangaroo Mother Care o KMC) ha demostrado eficacia en disminuir la mortalidad neonatal en aquellos pretérmino (70) o con bajo peso al nacer, usualmente <2 000 g (71). En este estudio no se incluyó a estos grupos de neonatos en alto riesgo, y el KMC no fue eficaz en neonatos a término.
En países en vías de desarrollo es importante contextualizar las intervenciones basadas en la comunidad para disminuir la mortalidad neonatal. Se requiere un programa integrado de intervenciones en varios niveles, no solamente aquellas relacionadas con la salud. Estas intervenciones adicionales incluyen disminución de la pobreza, mejora en la educación de las mujeres, mejora en el estatus social de las mujeres, especialmente de su poder de decisión (72). Adicionalmente, las familias grandes y los intervalos cortos entre embarazos determinan desenlaces perinatales desfavorables (73).
Este estudio tiene algunas limitaciones. Primero, las intervenciones fueron muy diferentes entre ellas, incluso entre aquellas que pertenecen al mismo grupo. Por este motivo, no procedimos a hacer metaanálisis formal. Segundo, no se evaluó la costo-efectividad de las intervenciones basadas en la comunidad. Sin embargo, las evaluaciones de costo–efectividad son escasas y deberían ser incorporadas en las investigaciones de salud neonatal para guiar la selección de intervenciones y estimular la inversión en salud neonatal (10). Tercero, no se consideraron otros desenlaces tales como muerte perinatal, muerte posneonatal (29 a 364 días), muerte en la niñez (1-4 años) y muerte por debajo de los 5 años. Estos desenlaces son motivo de evaluación de intervenciones en forma global (64) y deberían ser objeto de investigaciones futuras. Finalmente, no se enfocó en poblaciones en mayor riesgo de muerte tales como neonatos prematuros o neonatos con bajo peso o muy bajo peso al nacer. En ellos, algunas intervenciones tales como el cuidado de madre canguro, han demostrado ser muy eficaces (70-71), hallazgo que no se observó en los estudios de neonatos a término.
En conclusión, las intervenciones basadas en la comunidad destinadas a disminuir la mortalidad neonatal son heterogéneas. Las intervenciones agrupadas en educación materna en salud y en cuidado en casa de madres y neonatos demostraron disminución de la mortalidad neonatal en, aproximadamente, la mitad de los estudios. Otras intervenciones con más de un estudio no han demostrado disminuir la mortalidad neonatal. Las intervenciones con un estudio único disponible tuvieron resultados mixtos.
Las intervenciones específicas, complejas agrupadas en educación materna en salud y en cuidado en casa de madres y neonatos, y que demostraron disminución de la mortalidad neonatal, podrían ser implementadas en la estrategia del MINSA-Perú para mejorar las intervenciones ya existentes. Debido a que las intervenciones en la comunidad para reducir mortalidad neonatal son muy heterogéneas entre sí, no se pudo realizarles el metaanálisis de eficacia. Se necesita elaborar intervenciones multimodales que incluyan todas aquellas que hayan demostrado eficacia/efectividad en ensayos controlados aleatorizados. Estas intervenciones deben evaluarse formalmente en poblaciones más grandes y en el Perú.
Fuentes de financiamiento: Programa de Apoyo a la Reforma del Sector Salud-PARSALUD II, Lima, Perú
Conflicto de interés: los autores declaran que no tienen conflictos de interés.
Contribuciones de autoría: AVH participó en el diseño del artículo, recolección de datos, análisis e interpretación de resultados, redacción del artículo, revisión crítica del estudio, y aprobación de su versión final. VP y VBZ participaron en la recolección de datos, redacción del artículo, revisión crítica del artículo y aprobación de su versión final. EVH y JLR participaron en la concepción y diseño del artículo, redacción del artículo, revisión crítica del artículo y aprobación de su versión final. YRC, HCA, MGN, y WVV participaron en la revisión crítica del artículo y la aprobación de su versión final.
Referencias Bibliográficas
1. Ngoc NT, Merialdi M, Abdel-Aleem H, Carroli G, Purwar M, Zavaleta N, et al. Causes of stillbirths and early neonatal deaths: data from 7993 pregnancies in six developing countries . Bull World Health Organ. 2006;84(9):699-705. [ Links ]
2. Oestergaard MZ, Inoue M, Yoshida S, Mahanani WR, Gore FM, Cousens S, et al. Neonatal mortality levels for 193 countries in 2009 with trends since 1990: a systematic analysis of progress, projections, and priorities . PLoS Med. 2011;8(8): e1001080. doi: 10.1371/journal.pmed.1001080. [ Links ]
3. Rajaratnam JK, Marcus JR, Flaxman AD, Wang H, Levin-Rector A, Dwyer L, et al. Neonatal, postneonatal, childhood, and under-5 mortality for 187 countries, 1970–2010: a systematic analysis of progress towards Millennium Development Goal 4 . Lancet. 2010 Jun 5;375(9730):1988-2008. doi: 10.1016/S0140-6736(10)60703-9. [ Links ]
4. Velásquez A. La carga de enfermedad y lesiones en el Perú y las prioridades del plan esencial de aseguramiento universal . Rev Peru Med Exp Salud Publica. 2009;26(2):222-31. [ Links ]
5. Lawn JE, Cousens S, Zupan J; Lancet Neonatal Survival Steering Team. 4 million neonatal deaths: when? Where? Why? . Lancet. 2005;365(9462):891-900. [ Links ]
6. Pattinson R, Kerber K, Waiswa P, Day LT, Mussell F, Asiruddin SK, et al. Perinatal mortality audit: counting, accountability, and overcoming challenges in scaling up in low-and middle-income countries . Int J Gynaecol Obstet. 2009;107 Suppl 1:S113-21, S121-2. doi: 10.1016/j.ijgo.2009.07.011. [ Links ]
7. Bruce ML, Smith W, Miranda J, Hoagwood K, Wells KB; NIMH Affective Disorders Workgroup. Community-based interventions . Ment Health Serv Res. 2002;4(4):205-14. [ Links ]
8. McLeroy KR, Norton BL, Kegler MC, Burdine JN, Sumaya CV. Community-based interventions . Am J Public Health. 2003;93(4):529-33. [ Links ]
9. Morales Asencio JM, Jiménez EG, Santos FJM, Herrera JCM. Salud Pública basada en la evidencia. Recursos sobre la efectividad de intervenciones en la comunidad . Rev Esp Salud Pública. 2008;82(1):5-20. [ Links ]
10. Bhutta ZA, Darmstadt GL, Hasan BS, Haws RA. Community-based interventions for improving perinatal and neonatal health outcomes in developing countries: a review of the evidence . Pediatrics. 2005;115(2 Suppl):519-617. [ Links ]
11. Neonatal Mortality Formative Research Working Group. Developing community-based intervention strategies to save newborn lives: lessons learned from formative research in five countries . J Perinatol. 2008;28 Suppl 2:S2-8. doi: 10.1038/jp.2008.166. [ Links ]
12. Jones G, Steketee RW, Black RE, Bhutta ZA, Morris SS; Bellagio Child Survival Study Group. How many child deaths can we prevent this year? . Lancet. 2003;362(9377):65-71. [ Links ]
13. Fariña D, Rodríguez S, Vaihinger M, Salva V, Porto R, Ganduglia M, et al. Mortalidad Neonatal: Análisis Causa Raíz. Estudio Prospectivo de los Factores Vinculados a la Muerte de Recién Nacidos Internados en Maternidades Seleccionadas del Sector Público de La República Argentina . Revista Hosp Materno Infant Ramón Sardá. 2012;31(3):117-24. [ Links ]
14. Moss W, Darmstadt GL, Marsh DR, Black RE, Santosham M. Research priorities for the reduction of perinatal and neonatal morbidity and mortality in developing country communities . J Perinatol. 2002;22(6):684-95. [ Links ]
15. Bhutta ZA, Ahmed T, Black RE, Cousens S, Dewey K, Giugliani E, et al. What works? Interventions for maternal and child undernutrition and survival . Lancet. 2008;371(9610):417-40. doi: 10.1016/S0140-6736(07)61693-6. [ Links ]
16. Spencer HC, Kaseje DC, Mosley WH, Sempebwa EK, Huong AY, Roberts JM. Impact on mortality and fertility of a community-based malaria control programme in Saradidi, Kenya . Ann Trop Med Parasitol. 1987;81 Suppl 1:36-45. [ Links ]
17. Boerma JT, Stroh G. Using survey data to assess neonatal tetanus mortality levels and trends in developing countries . Demography. 1993;30(3):459-75. [ Links ]
18. Jokhio AH, Winter HR, Cheng KK. An intervention involving traditional birth attendants and perinatal and maternal mortality in Pakistan . N Engl J Med. 2005;352(20):2091-9. [ Links ]
19. World Health Organization. Pregnancy, childbirth, postpartum, and newborn care: a guide for essential practice [Internet]. Ginebra: WHO; 2003 [citado el 20 de agosto de 2014 ]. Disponible en: http://www.who.int/maternal_child_adolescent/documents/924159084x/en/ [ Links ]
20. Rahman S. The effect of traditional birth attendants and tetanus toxoid in reduction of neo-natal mortality . J Trop Pediatr. 1982;28(4):163-5. [ Links ]
21. Sloan NL, Ahmed S, Mitra SN, Choudhury N, Chowdhury M, Rob U, et al. Community-based kangaroo mother care to prevent neonatal and infant mortality: a randomized, controlled cluster trial . Pediatrics. 2008;121(5):e1047-59. doi: 10.1542/peds.2007-0076. [ Links ]
22. Edmond KM, Zandoh C, Quigley MA, Amenga-Etego S, Owusu-Agyei S, Kirkwood BR. Delayed breastfeeding initiation increases risk of neonatal mortality . Pediatrics. 2006;117(3):e380-6. [ Links ]
23. Bang AT, Reddy HM, Deshmukh MD, Baitule SB, Bang RA. Neonatal and infant mortality in the ten years (1993 to 2003) of the Gadchiroli field trial: effect of home-based neonatal care . J Perinatol. 2005;25 Suppl 1:S92-107. [ Links ]
24. Ceesay SM, Prentice AM, Cole TJ, Foord F, Poskitt EM, Weaver LT, et al. Effects on birth weight and perinatal mortality of maternal dietary supplements in rural Gambia: 5 year randomised controlled trial . BMJ. 1997;315(7111):786-90. [ Links ]
25. Darmstadt GL, Bhutta ZA, Cousens S, Adam T, Walker N, de Bernis L, et al. Evidence-based, cost-effective interventions: how many newborn babies can we save? . Lancet. 2005;365(9463):977-88. [ Links ]
26. Manandhar DS, Osrin D, Shrestha BP, Mesko N, Morrison J, Tumbahangphe KM, et al. Effect of a participatory intervention with women’s groups on birth outcomes in Nepal: cluster-randomised controlled trial . Lancet. 2004;364(9438):970-9.
27. Adam T, Lim SS, Mehta S, Bhutta ZA, Fogstad H, Mathai M, et al. Cost effectiveness analysis of strategies for maternal and neonatal health in developing countries . BMJ. 2005;331(7525):1107. [ Links ]
28. Ippolito PM. How government policies shape the food and nutrition information environment . Food Policy. 1999;24(2–3):295-306. [ Links ]
29. Brownson RC, Fielding JE, Maylahn CM. Evidence-based public health: a fundamental concept for public health practice . Annu Rev Public Health. 2009;30:175-201. doi: 10.1146/annurev.publhealth.031308.100134. [ Links ]
30. Liberati A, Altman DG, Tetzlaff J, Mulrow C, Gøtzsche PC, Loannidis JP, et al. The PRISMA statement for reporting systematic reviews and meta-analyses of studies that evaluate health care interventions: explanation and elaboration . PLoS Medicine. 2009;6(7):e1000100.
31. Higgins JPT, Green S, editores. Cochrane handbook for systematic reviews of interventions. version 5.1. 0 [updated March 2011] . Cochrane Collab. 2011. [ Links ]
32. Higgins JP, Altman DG, Gøtzsche PC, Jüni P, Moher D, Oxman AD, et al. The Cochrane Collaboration’s tool for assessing risk of bias in randomised trials . BMJ. 2011;343:d5928. doi: 10.1136/bmj.d5928.
33. Stang A. Critical evaluation of the Newcastle-Ottawa scale for the assessment of the quality of nonrandomized studies in meta-analyses . Eur J Epidemiol. 2010;25(9):603-5. doi: 10.1007/s10654-010-9491-z. [ Links ]
34. Chinn S. A simple method for converting an odds ratio to effect size for use in meta-analysis . Stat Med. 2000;19(22):3127-31. [ Links ]
35. Katz J, West KP Jr, Khatry SK, Pradhan EK, LeClerq SC, Christian P, et al. Maternal low-dose vitamin A or beta-carotene supplementation has no effect on fetal loss and early infant mortality: a randomized cluster trial in Nepal . Am J Clin Nutr. 2000;71(6): 1570-6. [ Links ]
36. Bhaqui AH, El-Arifeen S, Darmstadt GL, Ahmed S, Williams EK, Seraji HR, et al. Effect of community-based newborn-care intervention package implemented through two service-delivery strategies in Sylhet district, Bangladesh: a cluster-randomised controlled trial . Lancet 2008;371:1936-44. doi: 10.1016/S0140-6736(08)60835-1. [ Links ]
37. Bhutta ZA, Memon ZA, Soofi S, Salat MS, Cousens S, Martines J. Implementing community-based perinatal care: results from a pilot study in rural Pakistan . Bull World Health Organ. 2008;86(6):452-9. [ Links ]
38. Kumar V, Mohanty S, Kumar A, Misra RP, Santosham M, Awasthi S, et al. Effect of community-based behaviour change management on neonatal mortality in Shivgarh, Uttar Pradesh, India: a cluster-randomised controlled trial . Lancet 2008;372(9644):1151-62. doi: 10.1016/S0140-6736(08)61483-X. [ Links ]
39. Supplementation with Multiple Micronutrients Intervention Trial (SUMMIT) Study Group, Shankar AH, Jahari AB, Sebayang SK, Aditiawarman, Apriatni M, et al. Effect of maternal multiple micronutrient supplementation on fetal loss and infant death in Indonesia: a double-blind cluster-randomised trial . Lancet 2008;371(9608):215-27. doi: 10.1016/S0140-6736(08)60133-6. [ Links ]
40. Zeng L, Dibley MJ, Cheng Y, Dang S, Chang S, Kong L, et al. Impact of micronutrient supplementation during pregnancy on birth weight, duration of gestation, and perinatal mortality in rural western China: double blind cluster randomised controlled trial . BMJ 2008;337:a2001. doi: 10.1136/bmj.a2001. [ Links ]
41. Bhutta ZA, Rizvi A, Raza F, Hotwani S, Zaidi S, Moazzam Hossain S, et al. A comparative evaluation of multiple micronutrient and iron-folic acid supplementation during pregnancy in Pakistan: Impact on pregnancy outcomes . Food Nutr Bull. 2009;30(4 Suppl): S496-505. [ Links ]
42. Azad K, Barnett S, Banerjee B, Shaha S, Khan K, Rego AR, et al. Effect of scaling up women’s groups on birth outcomes in three rural districts in Bangladesh: a cluster-randomised controlled trial . Lancet 2010;375(9721):1193-202.
43. Darmstadt GL, Choi Y, Arifeen SE, Bari S, Rahman SM, Mannan I, et al. Evaluation of a Cluster-Randomized Controlled Trial of a Package of Community-Based Maternal and Newborn Interventions in Mirzapur, Bangladesh . PLoS One. 2010;5(3):e9696. doi:10.1371/journal.pone.0009696 [ Links ]
44. Bhutta ZA, Soofi S, Cousens S, Mohammad S, Memon ZA, Ali I, et al. Improvement of perinatal and newborn care in rural Pakistan through community-based strategies: a cluster-randomised eff ectiveness trial . Lancet. 2011;377(9763):403-12. [ Links ]
45. Gill CJ, Phiri-Mazzala G, Guerina NG, Kasimba J, Mulenga C, MacLeod WB, et al. Effect of training traditional birth attendants on neonatal mortality (Lufwanyama Neonatal Survival Project): randomised controlled study . BMJ. 2011;342:d346. [ Links ]
46. West KP Jr, Christian P, Labrique AB, Rashid M, Shamim AA, Klemm RD, et al. Effects of vitamin A or beta carotene supplementation on pregnancy-related mortality and infant mortality in rural Bangladesh: a cluster randomized trial . JAMA. 2011; 305(19):1986-95. doi: 10.1001/jama.2011.656. [ Links ]
47. Bhandari N, Mazumder S, Taneja S, Sommerfelt H, Strand TA; IMNCI Evaluation Study Group. Effect of implementation of Integrated Management of Neonatal and Childhood Illness (IMNCI) programme on neonatal and infant mortality: cluster randomised controlled trial . BMJ. 2012;344:e1634. doi: 10.1136/bmj.e1634. [ Links ]
48. More NS, Bapat U, Das S, Alcock G, Patil S, Porel M, et al. Community Mobilization in Mumbai Slums to Improve Perinatal Care and Outcomes: A Cluster Randomized Controlled Trial . PLoS Med. 2012;9(7):e1001257. doi:10.1371/journal.pmed.1001257 [ Links ]
49. Colbourn T, Nambiar B, Bondo A, Makwenda C, Tsetekani E, Makonda-Ridley A, et al. Effects of quality improvement in health facilities and community mobilization through women’s groups on maternal, neonatal and perinatal mortality in three districts of Malawi: MaiKhanda, a cluster randomized controlled effectiveness trial . Int Health. 2013;5(3):180-95. doi: 10.1093/inthealth/iht011.
50. Fottrell E, Azad K, Kuddus A, Younes L, Shaha S, Nahar T, et al. The effect of increased coverage of participatory women’s groups on neonatal mortality in Bangladesh: A cluster randomized trial . JAMA Pediatr. 2013;167(9):816-25. doi: 10.1001/jamapediatrics.2013.2534.
51. Kirkwood BR, Manu A, ten Asbroek AH, Soremekun S, Weobong B, Gyan T, et al. Effect of the Newhints home-visits intervention on neonatal mortality rate and care practices in Ghana: a cluster randomised controlled trial . Lancet. 2013;381(9884):2184-92. doi: 10.1016/S0140-6736(13)60095-1. [ Links ]
52. Persson LÅ, Nga NT, Målqvist M, Thi Phuong Hoa D, Eriksson L, Wallin L, et al. Effect of facilitation of local maternal-and-newborn stakeholder groups on neonatal mortality: cluster randomized controlled trial . PLoS Med. 2013;10(5):e1001445. doi: 10.1371/journal.pmed.1001445. [ Links ]
53. Kafatos AG, Tsitoura S, Pantelakis SN, Doxiadis SA. Maternal and infant health education in a rural Greek community . Hygie. 1991; 10(1):32-7. [ Links ]
54. Hunphrey JH, Agoestina T, Wu L, Usman A, Nurachim M, Suberdja D, et al. Impact of neonatal vitamin A supplementation on infant morbidity and mortality . J Pediatr. 1996;128(4):489-96. [ Links ]
55. Charpak N, Ruiz-Pelaez JG, Figueroa de C Z, Charpak Y. A randomized, controlled trial of kangaroo mother care: results of follow-up at 1 year of corrected age . Pediatrics. 2001;108(5):1072-9. [ Links ]
56. Kaestel P, Michaelsen KF, Aaby P, Friis H. Effects of prenatal multimicronutrient supplements on birth weight and perinatal mortality: a randomised, controlled trial in Guinea-Bissau . Eur J Clin Nutr. 2005;59(9):1081–9. [ Links ]
57. Worku B, Kassie A. Kangaroo mother care: a randomized controlled trial on effectiveness of early kangaroo mother care for the low birthweight infants in Addis Ababa, Ethiopia . J Trop Pediatr. 2005;51(2):93-7. [ Links ]
58. Bashour HN, Kharouf MH, AbdulSalam AA, El Asmar K, Tabbaa MA, Cheikha SA. Effect of postnatal home visits on maternal/infant outcomes in Syria: a randomized controlled trial . Public Health Nurs. 2008;25(2):115-25. doi: 10.1111/j.1525-1446.2008.00688.x. [ Links ]
59. Persson LÅ, Arifeen S, Ekström EC, Rasmussen KM, Frongillo EA, Yunus M, et al. Effects of prenatal micronutrient and early food supplementation on maternal hemoglobin, birth weight, and infant mortality among children in Bangladesh: the MINIMat randomized trial . JAMA. 2012;307(19):2050-9. doi: 10.1001/jama.2012.4061. [ Links ]
60. Liu JM, Mei Z, Ye R, Serdula MK, Ren A, Cogswell ME. Micronutrient supplementation and pregnancy outcomes: double-blind randomized controlled trial in China . JAMA Intern Med. 2013;173(4):276-82. doi: 10.1001/jamainternmed.2013.1632. [ Links ]
61. Bang AT, Bang RA, Baitule SB, Reddy MH, Deshmukh MD. Effect of home-based neonatal care and management of sepsis on neonatal mortality: field trial in rural India . Lancet. 1999;354(9194):1955–61. [ Links ]
62. Alehagen SA, Finnström O, Hermansson GV, Somasundaram KV, Bangal VB, Patil A, et al. Nurse-based antenatal and child health care in rural India, implementation and effects - an Indian-Swedish collaboration . Rural Remote Health. 2012;12:2140. [ Links ]
63. Singh A, Pallikadavath S, Ogollah R, Stones W. Maternal tetanus toxoid vaccination and neonatal mortality in rural north India . PLoS One. 2012;7(11):e48891. doi: 10.1371/journal.pone.0048891. [ Links ]
64. Wang H, Liddell CA, Coates MM, Mooney MD, Levitz CE, Schumacher AE, et al. Global, regional, and national levels of neonatal, infant, and under-5 mortality during 1990–2013: a systematic analysis for the Global Burden of Disease Study 2013 . Lancet. 2014;384(9947):957-79. doi: 10.1016/S0140-6736(14)60497-9.
65. Darlow BA, Graham PJ. Vitamin A supplementation for preventing morbidity and mortality in very low birthweight infants . Cochrane Database Syst Rev. 2002;(4):CD000501. [ Links ]
66. Darlow BA, Graham PJ. Vitamin A supplementation to prevent mortality and short- and long-term morbidity in very low birthweight infants . Cochrane Database Syst Rev. 2011;(10):CD000501. doi: 10.1002/14651858.CD000501.pub3. [ Links ]
67. Gogia S, Sachdev HS. Vitamin A supplementation for the prevention of morbidity and mortality in infants six months of age or less . Cochrane Database Syst Rev. 2011;(10):CD007480. doi: 10.1002/14651858.CD007480.pub2. [ Links ]
68. Haider BA, Bhutta ZA. Neonatal vitamin A supplementation for the prevention of mortality and morbidity in term neonates in developing countries . Cochrane Database Syst Rev. 2011;(10):CD006980. doi: 10.1002/14651858.CD006980.pub2. [ Links ]
69. van den Broek N, Dou L, Othman M, Neilson JP, Gates S, Gülmezoglu AM. Vitamin A supplementation during pregnancy for maternal and newborn outcomes . Cochrane Database Syst Rev. 2010;(11):CD008666. doi: 10.1002/14651858.CD008666.pub2. [ Links ]
70. Lawn JE, Mwansa-Kambafwile J, Barros FC, Horta BL, Cousens S. ‘Kangaroo mother care’ to prevent neonatal deaths due to preterm birth complications . Int J Epidemiol. 2010.
71. Conde-Agudelo A, Díaz-Rossello JL. Kangaroo mother care to reduce morbidity and mortality in low birthweight infants . Cochrane Database Syst Rev. 2014;4:CD002771. doi: 10.1002/14651858.CD002771.pub3. [ Links ]
72. Stenberg K, Axelson H, Sheehan P, Anderson I, Gülmezoglu AM, Temmerman M, et al. Advancing social and economic development by investing in women’s and children’s health: a new Global Investment Framework . Lancet. 2014;383(9925):1333-54. doi: 10.1016/S0140-6736(13)62231-X.
73. Zhu BP, Rolfs RT, Nangle BE, Horan JM. Effect of the interval between pregnancies on perinatal outcomes . N Engl J Med. 1999;340(8):589-94. [ Links ]
Correspondencia: Jessica Loyola-Romaní.
Dirección: Av. Javier Prado Oeste 2108, San Isidro, Lima 27, Perú.
Teléfono: (+511) 6118181
Correo electrónico: jloyolar@parsalud.gob.pe
Recibido: 22-09-15
Aprobado: 17-06-15
Anexo 1, Estrategias de búsqueda
Pubmed
(Newborn OR neonate OR neonatal) AND (mortality OR death) AND (maternal schooling OR maternal education OR health education OR antenatal care OR maternal care OR protein supplementation OR balanced protein-energy supplementation OR iron supplementation OR folate supplementation OR iodine supplementation OR vitamin A supplementation OR zinc supplementation OR multiple micronutrient supplementation OR malaria prophylaxis OR malaria protection OR tetanus immunization OR pneumococcal immunization OR kangaroo mother care OR smoking cessation OR umbilical cord antisepsis OR breastfeeding OR hypothermia prevention OR hypoglycemia prevention OR ophthalmia neonatorum prevention OR adherence to attendance OR skilled delivery attendant OR traditional delivery attendant OR improved sanitation facilities OR postpartum home visits OR health systems strengthening OR quality of services for newborns OR community health nurses management OR community-based Health Planning and Services OR surfactant therapy OR emergency obstetrics and newborn care OR nurse education OR Maternal-and-Newborn Stakeholder Groups) AND (Randomized Controlled Trial OR Cluster randomized trial OR Field Trial OR Community-based study OR Community study OR Cohort study)
Web of science
TOPIC: (newborn OR neonate OR neonatal) AND TOPIC: (mortality OR death) AND TOPIC: (maternal schooling OR maternal education OR health education OR antenatal care OR maternal care OR protein supplementation OR balanced protein-energy supplementation OR iron supplementation OR folate supplementation OR iodine supplementation OR vitamin A supplementation OR zinc supplementation OR multiple micronutrient supplementation OR malaria prophylaxis OR malaria protection OR tetanus immunization OR pneumococcal immunization OR kangaroo mother care OR smoking cessation OR umbilical cord antisepsis OR breastfeeding OR hypothermia prevention OR hypoglycemia prevention OR ophthalmia neonatorum prevention OR adherence to attendance OR skilled delivery attendant OR traditional delivery attendant OR improved sanitation facilities OR postpartum home visits OR health systems strengthening OR quality of services for newborns OR community health nurses management OR community-based Health Planning and Services OR surfactant therapy OR emergency obstetrics and newborn care OR nurse education OR Maternal-and-Newborn Stakeholder Groups) AND TOPIC:(Randomized Controlled Trial OR Cluster randomized trial OR Field Trial OR Community-based study OR Community study OR Cohort study)
Timespan: All years. Indexes: SCI-EXPANDED.
Cochrane Collaboration
‘newborn OR neonate OR neonatal in Title, Abstract, Keywords and mortality OR death and maternal schooling OR maternal education OR health education OR antenatal care OR maternal care OR protein supplementation OR balanced protein-energy supplementation OR iron supplementation OR folate supplementation OR iodine supplementation OR vitamin A supplementation OR zinc supplementation OR multiple micronutrient supplementation OR malaria prophylaxis OR malaria protection OR tetanus immunization OR pneumococcal immunization OR kangaroo mother care OR smoking cessation OR umbilical cord antisepsis OR breastfeeding OR hypothermia prevention OR hypoglycemia prevention OR ophthalmia neonatorum prevention OR adherence to attendance OR skilled delivery attendant OR traditional delivery attendant OR improved sanitation facilities OR postpartum home visits OR health systems strengthening OR quality of services for newborns OR community health nurses management OR community-based Health Planning and Services OR surfactant therapy OR emergency obstetrics and newborn care OR nurse education OR Maternal-and-Newborn Stakeholder Groups and Randomized Controlled Trial OR Cluster randomized trial OR Field Trial OR Community-based study OR Community study OR Cohort study in Trials’
Scopus
("newborn" OR "neonate" OR "neonatal") AND ("mortality" OR "death") AND ("maternal schooling" OR "maternal education" OR "health education" OR "antenatal care " OR "maternal care" OR "protein supplementation" OR "balanced protein-energy supplementation" OR "iron supplementation" OR "folate supplementation" OR "iodine supplementation" OR "vitamin A supplementation" OR "zinc supplementation" OR "multiple micronutrient supplementation" OR "malaria prophylaxis" OR "malaria protection" OR "tetanus immunization" OR "pneumococcal immunization" OR "kangaroo mother care" OR "smoking cessation" OR "umbilical cord antisepsis" OR "breastfeeding" OR "hypothermia prevention" OR "hypoglycemia prevention" OR "ophthalmia neonatorum prevention" OR "adherence to attendance" OR "skilled delivery attendant" OR "traditional delivery attendant" OR "improved sanitation facilities" OR "postpartum home visits" OR "health systems strengthening" OR "quality of services for newborns" OR "community health nurses management" OR "community-based Health Planning and Services" OR "surfactant therapy" OR "emergency obstetrics and newborn care" OR "nurse education" OR "Maternal-and-Newborn Stakeholder Groups") AND ("Randomized Controlled Trial" OR "Cluster randomized trial" OR "Field Trial" OR "Community-based study" OR "Community study" OR "Cohort study")
EMBASE
(‘newborn’/exp OR newborn OR neonatalnewborn OR ‘neonate’/exp OR neonate OR neonatal) AND (‘mortality’/exp OR mortality OR ‘death’/exp OR death) AND (maternal AND (‘schooling’/exp OR schooling) OR ‘health’/exp OR health AND (‘education’/exp OR education) OR antenatal AND care OR ‘maternal care’/exp OR ‘maternal care’ OR ‘protein’/exp OR protein AND (‘supplementation’/exp OR supplementation) OR balanced AND ‘protein energy’ AND (‘supplementation’/exp OR supplementation) OR ‘iron’/exp OR iron AND (‘supplementation’/exp OR supplementation) OR ‘folate’/exp OR folate AND (‘supplementation’/exp OR supplementation) OR ‘vitamin’/exp OR vitamin AND a AND (‘supplementation’/exp OR supplementation) OR ‘zinc’/exp OR zinc AND (‘supplementation’/exp OR supplementation) OR multiple AND (‘micronutrient’/exp OR micronutrient) AND (‘supplementation’/exp OR supplementation) OR ‘malaria’/exp OR malaria AND (‘prophylaxis’/exp OR prophylaxis) OR ‘malaria’/exp OR malaria AND (‘protection’/exp OR protection) OR ‘tetanus’/exp OR tetanus AND (‘immunization’/exp OR immunization) OR pneumococcal AND (‘immunization’/exp OR immunization) OR ‘kangaroo’/exp OR kangaroo AND (‘mother’/exp OR mother) AND care OR ‘smoking’/exp OR smoking AND maternal AND (‘education’/exp OR education) AND cessation OR ‘umbilical’/exp OR umbilical AND cord AND (‘antisepsis’/exp OR antisepsis) OR breastfeeding OR ‘hypothermia’/exp OR hypothermia AND (‘prevention’/exp OR prevention) OR ‘hypoglycemia’/exp OR hypoglycemia AND (‘prevention’/exp OR prevention) OR ophthalmia AND neonatorum AND (‘prevention’/exp OR prevention) OR adherence AND to AND attendance OR skilled AND (‘delivery’/exp OR delivery) AND attendant OR traditional AND (‘delivery’/exp OR delivery) AND attendant OR improved AND (‘sanitation’/exp OR sanitation) AND facilities OR postpartum AND (‘home’/exp OR home) AND visits OR ‘health’/exp OR health AND systems AND strengthening OR quality AND of AND services AND for AND newborns OR ‘community’/exp OR community AND (‘health’/exp OR health) AND (‘nurses’/exp OR nurses) AND (‘management’/exp OR management) OR ‘community based’ AND (‘health’/exp OR health) AND (‘planning’/exp OR planning) AND services OR ‘surfactant’/exp OR surfactant AND (‘therapy’/exp OR therapy) OR ‘emergency’/exp OR emergency AND (‘obstetrics’/exp OR obstetrics) AND (‘newborn’/exp OR newborn) AND care OR ‘nurse’/exp OR nurse AND (‘education’/exp OR education) OR ‘maternal and newborn’ AND stakeholder AND groups) AND (randomized AND controlled AND trial OR cluster AND randomized AND trial OR field AND trial OR ‘community based’ AND (‘study’/exp OR study) OR’community’/exp OR community AND (‘study’/exp OR study) OR cohort AND (‘study’/exp OR study)