Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Peruana de Medicina Experimental y Salud Publica
Print version ISSN 1726-4634
Rev. perú. med. exp. salud publica vol.34 no.3 Lima July/Sep. 2017
http://dx.doi.org/10.17843/rpmesp.2017.343.2741
CARTAS AL EDITOR
Análisis de micromatrices cromosómicas en niños peruanos con retraso del desarrollo psicomotor o discapacidad intelectual
Chromosomal microarray analysis in peruvian children with delayed psychomotor development or intellectual disability
Hugo H. Abarca-Barriga1,2,a,b, Miguel A. Chávez Pastor1,3,c, Milana Trubnykova1,a, Flor Vásquez1,d, Julio A. Poterico3,4,e
1 Servicio de Genética y Errores Innatos del Metabolismo, Instituto Nacional de Salud del Niño, Sede Breña. Lima, Perú.
2 Programa de Postgrado, Universidad Científica del Sur. Lima, Perú.
3 Facultad de Medicina "Alberto Hurtado", Universidad Peruana Cayetano Heredia. Lima, Perú.
4 Instituto Nacional de Enfermedades Neoplásicas. Lima, Perú.
a Médico genetista; b magíster en Genética Humana; c médico pediatra, endocrinólogo y genetista; d biólogo molecular; e médico residente de Genética Médica
Sr. Editor. La discapacidad intelectual (DI) se define como la limitación en dos áreas: la inteligencia o capacidad mental y el comportamiento adaptativo en cualquiera de sus tres dominios: conceptual, social y práctico (1). El retraso del desarrollo psicomotor (RDPM) representa la adquisición anormal de habilidades psicomotrices, ya sea porque el niño pequeño no alcanzó alguno de los hitos del desarrollo, los alcanzó después del tiempo esperado o de una manera incompleta. Se podría plantear que el RDPM genera una sospecha de DI, por ello, es importante identificar su etiología y mantener un monitoreo continuo (2,3).
La prevalencia de DI se estima entre 1 a 3% en la población mundial, con mayor afección en los países en desarrollo, cuyas tasas podrían subestimarse por la demora en el diagnóstico, falta de acceso a servicios y tecnologías diagnósticas, ausencia de programas con enfoque dirigido hacia este tipo de pacientes, entre otros (2). De acuerdo con la Primera Encuesta Nacional Especializada sobre Discapacidad 2012, se estima que el 1,7% de la población peruana presenta algún grado de limitación del intelecto; así, aproximadamente 506 358 peruanos tendrían alguna limitación en las funciones mentales cognitivas (4). Sin embargo, el diagnóstico de discapacidad intelectual involucra más que lo reportado por la encuesta nacional mencionada.
Debido a que el diagnóstico preciso de este tipo de pacientes constituye un reto, la implementación de tecnologías modernas contribuye con una mayor precisión y manejo.
El Colegio Americano de Genética Médica (ACMG) recomienda desde el 2010 que el análisis de micromatrices cromosómicas (con las siglas CMA, del inglés chromosomal microarray analysis) se establezca como el test de primera línea para el diagnóstico de pacientes con múltiples anomalías congénitas, discapacidad intelectual o retraso del desarrollo sindrómico o no sindrómico; así como el trastorno del espectro autista (3). Esta institución sugiere el análisis con plataformas capaces de detectar microdeleciones o microduplicaciones de al menos 400 kb (1kb: mil pares de bases de nucleótidos). Las ganancias o pérdidas submicroscópicas son llamadas también variantes del número de copias (con las siglas CNV, del inglés copy number variation).
Presentamos resultados preliminares del estudio retroprospectivo: "Microdeleciones y Microduplicaciones en Cromosomas de Niños con Discapacidad Mental, Retraso Del Desarrollo Psicomotor, Problemas de Conducta, Trastornos de Lenguaje y Dismorfias atendidos en Instituto Nacional de Salud Del Niño (INSN), 2016-2017".
En el 2016, durante los meses de enero a septiembre, se evaluaron a 225 pacientes con RDPM y DI, derivados desde otros servicios u otras instituciones al consultorio de genética de INSN. Se recopiló la información mediante la revisión de las historias clínicas, revisión del sistema virtual de imágenes del INSN; y las descripciones morfológicas (e.g. rasgos faciales, medidas antropométricas) mediante un instrumento virtual diseñado por los genetistas del servicio. Para este último proceso, fue necesario volver a contactar a los pacientes en algunas oportunidades.
Se incluyeron a todos los pacientes atendidos en la consulta de genética sin patrón de enfermedad monogénica o multifactorial reconocible, con ADN extraído de buena calidad y con firma de consentimiento informado por los padres o apoderados. Por criterio de los médicos genetistas, se solicitaron las pruebas genéticas y moleculares a los pacientes con RDPM o DI.
Algunos de los pacientes tuvieron análisis de cariotipo en primera instancia, mientras que otros tuvieron CMA como primera elección de prueba diagnóstica. Se realizó el estudio de cariotipo mediante una técnica convencional estandarizada, catalogándose como resultado normal cuando no se apreciaban alteraciones cromosómicas visibles en el estudio por microscopio. Los análisis CMA se realizaron en muestras de ADN de buena calidad, utilizando la plataforma de GeneChip CytoScan 750K Array (Affymetrix, USA). Los resultados de CMA se compararon con los hallazgos de las bases internacionales de referencia (i.e. DECIPHER, The UCSC Genome Browser), para catalogar los CNV como: variantes patogénicas, probablemente patogénicas, de significado incierto, probablemente benignas y benignas. Se consideró CMA anormal a las variantes patogénicas o probablemente patogénicas. Este proyecto cuenta con aprobación por el comité de ética del INSN.
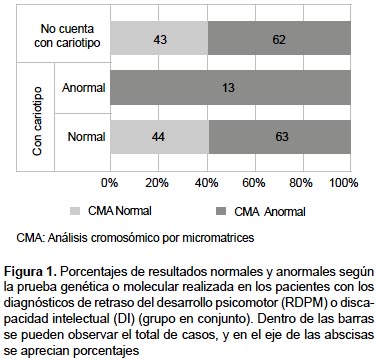
La mediana de la edad de los niños evaluados fue de 46 meses (RIQ: 23-96), con 56,4% de los pacientes del sexo masculino. Todos los participantes (n=225) contaron con CMA realizado, con un resultado de CMA alterado en el 61,3% (138/225) del total de pacientes. Un grupo de 120 pacientes contaron con análisis de cariotipo y CMA, cuya orden de prescripción fue determinada a priori por los genetistas en consulta. Observamos que 58,9% (63/107) de los pacientes que habían obtenido resultado normal en el cariotipo convencional, obtuvieron un reporte de CMA alterado (Figura 1). De aquellos sin cariotipo prescrito, 62 tuvieron un resultado de CMA anormal y 43 normal. Por otra parte, se resalta una concordancia del 100% de los resultados anormales entre las pruebas de cariotipo y CMA. Demostrándose así la utilidad clínica en el diagnóstico de nuestros pacientes, donde más de la mitad hubiera quedado sin diagnóstico preciso si nos limitábamos al uso del cariotipo convencional.
Además, tenemos conocimiento que nuestro estudio representa el primero en una institución médica de referencia nacional, con la cohorte más grande de niños peruanos; y el segundo utilizando CMA para el diagnóstico de pacientes con retraso psicomotor o trastornos del comportamiento. Butler et al. reportaron que dos tercios (10/15) de los lactantes peruanos (14-37 meses de edad) que evaluaron con CMA, portaban CNV relacionados plausiblemente con RDPM o trastorno del comportamiento (5); mientras que en nuestro estudio encontramos que 61,3% (138/225) de los pacientes pediátricos tenían algún CNV patogénico o probablemente patogénico.
El Servicio de Genética y Errores Innatos del Metabolismo del Instituto Nacional de Salud del Niño (INSN), constituye un ente referente de la atención de pacientes pediátricos e implementó, como pionero en el país, la prueba diagnóstica genómica del CMA. Gracias a esta tecnología hemos podido orientar y hasta reorientar diagnósticos, pronósticos, propuestas de manejo y asesorías genéticas. Nuestros hallazgos y la recomendación de agencias internacionales como ACMG, así como estudios de costo-efectividad que evalúan esta tecnología en la práctica clínica diaria (3), sustentan la necesidad y utilidad de continuar con esta prueba personalizada en el Perú.
Contribución de los autores: HHAB, MACP, MT, FVy JAP han participado en la concepción y diseño del estudio. FV realizó los estudios moleculares. HHAB, MT, MACP realizaron la interpretación clínica de los estudios moleculares. HHAB y JAP redactaron la primera versión del manuscrito. JAP realizó los análisis e interpretación de datos de este manuscrito. Todos los autores realizaron la redacción y aprobaron final de este documento.
Conflictos de interés: los autores declaramos no tener conflictos de interés.
Fuentes de financiamiento: el estudio fue autofinanciado.
REFERENCIAS BIBLIOGRÁFICAS
1. American Association of Intellectual and Developmental Disabilities (AAIDD) [Internet]. Definition of Intellectual Disability. Washington, DC: AAIDD; 2017. (Citado el 9 de febrero de 2017). Disponible en: http://aaidd.org/intellectual-disability/definition. [ Links ]
2. Maulik PK, Mascarenhas MN, Mathers CD, Dua T, Saxena S. Prevalence of intellectual disability: a meta-analysis of population based studies. Res Dev Disabil. 2011;32(2): 419-36. doi: 10.1016/j.ridd.2010.12.018. [ Links ]
3. Manning M, Hudgins L, Professional Practice and Guidelines Committee. Array-based technology and recommendations for utilization in medical genetics practice for detection of chromosomal abnormalities. Genet Med. 2010;12(11): 742–45. doi: 10.1097/GIM.0b013e3181f8baad. [ Links ]
4. Instituto Nacional de Estadística e Informática. Encuesta Nacional Especializada de Discapacidad [Internet]; 2012. Disponible en: https://www.inei.gob.pe/media/MenuRecursivo/publicaciones_digitales/Est/Lib1171/ENEDIS2012-COMPLETO.pdf. [ Links ]
5. Butler MG, Usrey K, Roberts JL, Schroeder SR, Manzardo AM. Clinical Presentation and Microarray Analysis of Peruvian Children with Atypical Development and/or Aberrant Behavior. Genet Res Int. 2014; 2014:408516. doi: 10.1155/2014/408516. [ Links ]
Correspondencia: Julio A. Poterico
Dirección: Calle Jorge Buckley 185, Miraflores. Lima, Perú
Teléfono de contacto: (+51) 995912622
Correo electrónico: julio.poterico@upch.pe
Recibido: 15/03/2017
Aprobado: 06/09/2017
En línea: 11/09/2017














