INTRODUCCIÓN
En el Perú, en los últimos años, se ha incrementado el número de pacientes con enfermedades crónicas no transmisibles, como las cardiovasculares y respiratorias, el cáncer y la diabetes mellitus tipo 2, relacionadas con una alimentación inadecuada. En investigaciones con animales de experimentación se ha evidenciado que una dieta rica en fructosa provoca inflamación crónica, lo que puede conducir a la obesidad, resistencia a la insulina y al síndrome metabólico. Esta situación, con el tiempo, puede generar diabetes mellitus tipo 2 1 , 2.
Las enfermedades crónicas no transmisibles están asociadas a situaciones de estrés oxidativo, así como al consumo de fructosa. El estrés oxidativo es el desequilibrio entre la producción de especies reactivas de oxígeno (ROS, por sus siglas en inglés) y el mecanismo de defensa, lo que condiciona la patogénesis de diversas enfermedades 2.
La L-carnitina (L-3-hidroxi-4-N-N-N-trimetilaminobutirato) facilita el ingreso de ácidos grasos de cadena larga a la mitocondria, para la oxidación y producción de adenosín trifosfato (ATP) en diferentes tejidos 3. La L-carnitina (LC) es un nutriente esencial; el 75% se obtiene de la dieta y el 25% se sintetiza endógenamente ( 3 , 4. Diversos estudios han demostrado el efecto antioxidante de la LC en diferentes enfermedades, ya sea como un scavenger (secuestrador) o mediante el incremento de la actividad de las enzimas antioxidantes 3 , 5 , 6.
Existen pocos estudios sobre el efecto de la LC sobre el estrés oxidativo en modelos experimentales con dieta rica en fructosa. El objetivo de esta investigación es evaluar el efecto de la LC sobre el estrés oxidativo asociado al consumo excesivo de fructosa en un modelo experimental con ratas de la cepa Holtzman.
MENSAJES CLAVE
Motivación para realizar el estudio: La L-carnitina (LC) producida en tejidos ejerce funciones en el metabolismo lipídico. Su función antioxidante en un modelo de estrés oxidativo inducido por fructosa no ha sido totalmente evaluada. Este azúcar es altamente consumido sobre todo en los alimentos procesados.
Principales hallazgos: La administración de LC a ratas Holtzman disminuyó la lipoperoxidación hepática e incrementó la producción de insulina. Administrada en el modelo de estrés oxidativo incrementó la actividad de la enzima superóxido dismutasa mitocondrial (SOD Mn) y mejoró marcadamente la HOMA-IR.
Implicancias: La LC muestra protección en sistemas antioxidantes bajo este modelo. Además, este estudio realizado en un laboratorio nacional contribuye con nueva evidencia.
MATERIALES Y MÉTODOS
Población y muestra
El estudio experimental se realizó con cuatro grupos, dos de los cuales recibieron alimentación con y sin LC y agua a libre demanda, y dos grupos recibieron alimentación con y sin LC y fructosa al 40% a libre demanda.
Animales y dieta
Se emplearon 24 ratas Holtzman machos de dos meses de edad con un peso aproximado de 217 ± 40 g, adquiridas en el Instituto Nacional de Salud (Lima, Perú). Se las colocaron en jaulas de policarbonato con tapas de metal inoxidable durante todo el estudio. Se mantuvieron por siete días en aclimatación con alimento a base de un concentrado comercial obtenido de la Universidad Nacional Agraria La Molina y con agua de grifería a libre demanda. El experimento se realizó en el bioterio de la Facultad de Medicina de la Universidad Nacional Mayor de San Marcos, a temperatura ambiental entre 23 y 26 °C, y humedad relativa de 60 a 70% con 12 horas de luz/oscuridad. La LC (500 mg/kg por 24 h) se administró por vía oral con cánula orogástrica.
Se formaron cuatro grupos, cada uno con seis ratas asignadas aleatoriamente mediante el programa OpenEpi. Se conservaron las mismas condiciones de la aclimatación.
El grupo control (C) recibió alimento y agua de grifería a libre demanda durante todo el experimento; el grupo control + L-carnitina (C+LC) recibió alimento y agua de grifería a libre demanda durante todo el experimento y L-carnitina a 500 mg/kg/24 h a partir del día 28; el grupo fructosa (F) recibió alimento y fructosa (40%) a libre demanda durante todo el experimento; y el grupo fructosa + L-carnitina (F+LC) recibió alimento y fructosa (40%) a libre demanda durante todo el experimento y administración de L-carnitina 500 mg/kg/24 h a partir del día 28.
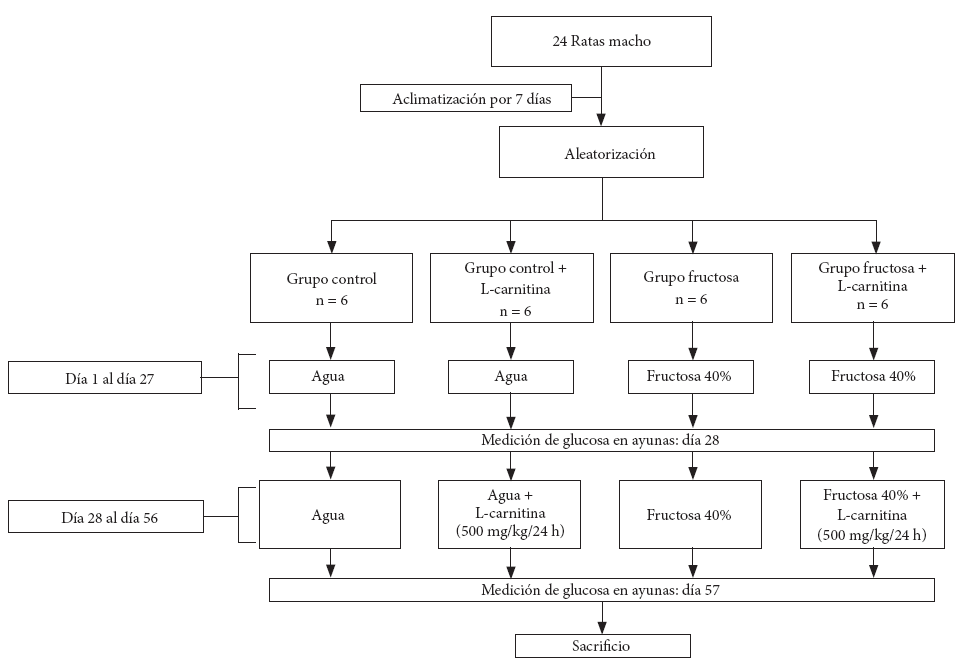
Los días 27 y 56 del experimento, todas las ratas estuvieron en ayunas para la medición de la glicemia. Asimismo, el día 57 las ratas fueron eutanasiadas por decapitación, previa sedación rápida y profunda con éter. Se siguió el flujograma según la figura 1.
Preparación de la fructosa y L-carnitina
Las soluciones se prepararon diariamente. Se usó D-fructosa >99% (Omnichem S.A.C, procedente de Wuxi, China). El agua potable de grifería con fructosa al 40% se basó en la formula peso/volumen. También, se preparó la LC al 10% (Omnichem S.A.C, Ningbo, China).
Preparación de los homogeneizados
El hígado se lavó por perfusión con KCl 0,154 M. Los homogeneizados se prepararon al 10% en buffer fosfato salino (PBS, por sus siglas en inglés) empleando un homogeneizador de vidrio tipo Potter-Elvehjem. Se realizaron tres centrifugaciones a 4 °C (centrífuga refrigerada modelo MPW380R, MPW Med instruments); de la primera, a 700 g por cinco minutos, se descartó el precipitado; la segunda, con el sobrenadante, se llevó a 9500 g durante 15 minutos, este sobrenadante correspondía a la fracción posmitocondrial, y el precipitado a la fracción mitocondrial. Se lavó dos veces el precipitado con el buffer PBS a la misma velocidad y tiempo de la obtención de las mitocondrias. Luego fue resuspendido con 2 mL del mismo buffer. De la misma manera, se preparó el homogeneizado pancreático; solo se hizo una centrifugación a 700 g durante cinco minutos y se obtuvo el sobrenadante denominado homogeneizado de páncreas.
Medición de la carnitina libre, glucosa, insulina y HOMA-IR
La muestra de sangre se obtuvo de la vena de la cola. La glicemia se determinó con un glucómetro basado en el método conductimétrico (Accu-chek Instant) el día 28 y el día 57. La medición de insulina en plasma y en el homogeneizado pancreático se realizó con el kit de ELISA el día 57 (Sigma-Aldrich, Estados Unidos). La resistencia a la insulina se evaluó con el modelo de homeostasis de resistencia a la insulina HOMA-IR= [glucosa (mg/dL) × insulina (mUI/mL)] /405. La medición de la LC-libre en el homogeneizado hepático se realizó con el kit de ELISA (Sigma-Aldrich, Estados Unidos).
Actividad de la superóxido dismutasa
Se midió en tejido hepático, según Marklund y Marklund 7. La inhibición de la autooxidación del pirogalol en medio alcalino fue la misma para la actividad de la superóxido dismutasa (SOD) en la fracción mitocondrial (SOD-Mn) y para la fracción posmitocondrial (SOD-Cu/Zn). La cinética se siguió durante tres minutos a 420 nm en un espectrofotómetro (Thermo Fisher Scientific, modelo G10S UV-Vis). Para reportar la actividad enzimática se tomó como definición de la unidad de la SOD: 1U SOD=Δ de absorbancia 0,02/2 × min (±10%).
Medición de la lipoperoxidación
En el homogeneizado hepático, previa precipitación con ácido tricloroacético al 20%, se midió la reacción entre el ácido tiobarbitúrico y los productos de la descomposición de especies lipoperoxidadas, como el malondialdehído (MDA) formando un complejo coloreado que se leyó a 535 nm. El coeficiente de extinción molar (ε) fue de 1,56 × 105 M-1 cm-1 ( 8.
Medición de proteínas totales
Las proteínas totales se cuantificaron mediante el método de Biuret 9. Se leyó a los cinco minutos a 540 nm. Se usó como estándar una solución de albúmina al 2%. La determinación se realizó en las fracciones mitocondrial y posmitocondrial obtenido del homogeneizado de hígado 8.
Análisis estadístico
Para evaluar la normalidad se aplicó la prueba de Shapiro Wilk y para la homogeneidad de varianzas se usó la prueba de Bartlett. Se utilizó la prueba paramétrica de análisis de varianza (ANOVA) y la de Scheffé como prueba post hoc para las comparaciones múltiples. Se asumió significancia estadística cuando en valor fue de p < 0,05. Se usó el programa estadístico Stata versión 13.
Aspectos éticos
Para el cuidado de los animales se siguieron los principios de las normas éticas para animales de laboratorio, según la Guía de Manejo y Cuidado de Animales de Laboratorio del Ministerio de Salud-Instituto Nacional de Salud. La eutanasia elegida está considerada en la Ley 30407, Ley de Protección y Bienestar Animal.
RESULTADOS
Los resultados de la glicemia en ayunas y los valores de la HOMA-IR no mostraron variaciones significativas. Sin embargo, en los valores de la HOMA-IR, el consumo de fructosa produjo un aumento de 28,3% frente al grupo C. En el grupo F+LC disminuyó en 25,8% frente al grupo F (Tabla 1).
Tabla 1 Parámetros plasmáticos y hepáticos.
| Parámetro | Control (C) | Control + L-carnitina (C+ LC) | Fructosa (F) | Fructosa + L-carnitina (F + LC) | Valor de p a |
|---|---|---|---|---|---|
| Parámetros plasmáticos | |||||
| Glucosa en ayunas - día 28 (mg/dL) | 85,1 ± 8,6 | 82,5 ± 3,9 | 85,5 ± 6,3 | 81,8 ± 16,4 | 0,912 |
| Glucosa en ayunas - día 57 (mg/dL) | 76,5 ± 12,9 | 85,3 ± 5,2 | 78,8 ± 10,6 | 77,6 ± 4,33 | 0,689 |
| HOMA-IR | 2,4 ± 0,4 | 2,8 ± 0,6 | 3,1 ± 0,1 | 2,3 ± 0,30 | 0,131 |
| Parámetros hepáticos | |||||
| Nivel de la L-carnitina libre (nmol/g de tejido) | 553,9 ± 96,8 | 659,3 ± 42,3 | 602,8 ± 48,1 | 673,9 ± 64,6 b | 0,037 |
| Proteínas totales mitocondriales (mg/dL) | 50,5 ± 11,1 | 76,3 ± 14,7 b | 62,0 ± 12,6 | 65,7 ± 10,2 | 0,018 |
| Proteínas totales posmitocondriales (mg/dL) | 27,8 ± 6,7 | 41,1 ± 5,8 b | 32,2 ± 1,4 | 36,5 ± 6,9 | 0,008 |
Valores expresados en media ± desviación estándar
a Prueba de ANOVA, b estadísticamente significativo en comparación con el grupo control
En el hígado, la LC libre, proteínas totales mitocondriales y posmitocondriales mostraron diferencia grupal significativa. Siendo la única diferencia significativa en evaluación por pares, la que se encontró en la LC libre, con un incremento de 21,5% en el grupo F+LC comparado con el grupo C (Tabla 1).
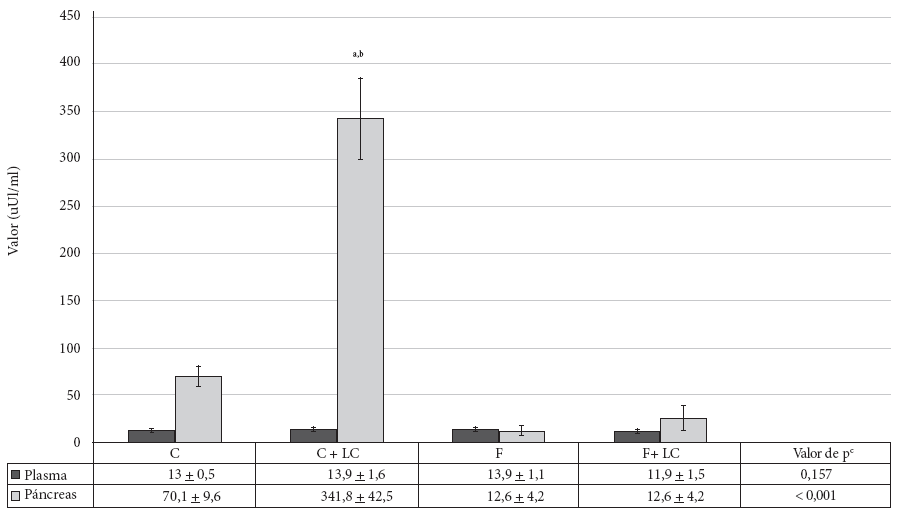
La administración de LC estimuló la producción de la insulina en el tejido pancreático, el incremento de los niveles de insulina en el grupo C+LC fue altamente significativo (p < 0,001) en comparación con el grupo C, llevando un aumento en 387% (341,8 ± 42,5 vs. 70,1 ± 9,6 µUI/mL). El consumo de fructosa produjo una disminución significativa (p < 0,01) de la insulina pancreática (12,6 ± 4,2 µUI/mL). La administración de LC con consumo de fructosa al 40% produjo una recuperación del 100% (25,8 ± 12,7 vs. 12,6 ± 4,2 µUI/mL) pero este valor no se iguala al grupo C (Figura 2).
En la evaluación macroscópica, se observó que la fructosa aumentó la grasa abdominal en el grupo F y grupo F+LC. La masa grasa incrementada incluyó el mesenterio y el retroperitoneo comparado con el grupo C y el grupo C+LC.
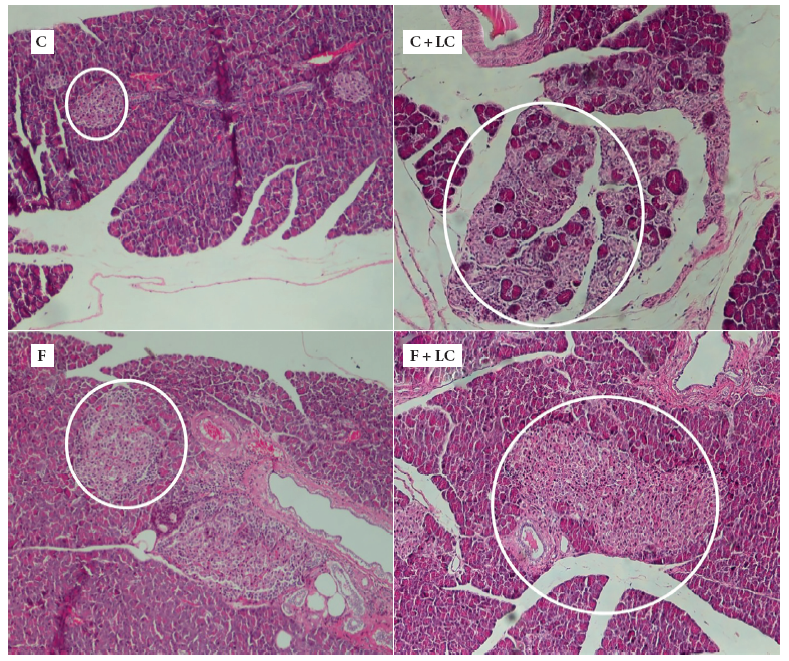
En la evaluación histológica del tejido pancreático, se observó que la presencia de LC (grupo C+LC) incrementó el número y el tamaño de los islotes de Langerhans, incluso el número fue mayor que los ácinos pancreáticos, comparado con los otros grupos. En el grupo F y en el grupo F+LC, se incrementaron el tamaño de los islotes de Langerhans en algunas regiones cerca de los vasos sanguíneos en comparación con el grupo C (Figura 3).
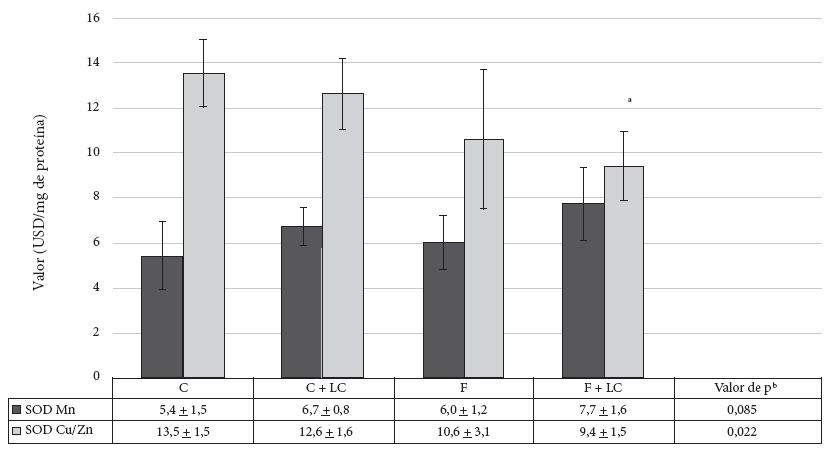
En la evaluación del efecto antioxidante, se observó disminución significativa en 30,5% de la actividad de la SOD Cu/Zn en el grupo F+LC comparado con el grupo C (9,4 ± 1,5 vs. 13,5 ± 1,5 USOD/mg de proteína, p < 0,05) (Figura 4). Sin embargo, fue notorio el cambio compensatorio de las actividades en ambas fracciones, mientras se produce la disminución de la actividad a nivel posmitocondrial se observa un incremento en la actividad mitocondrial.
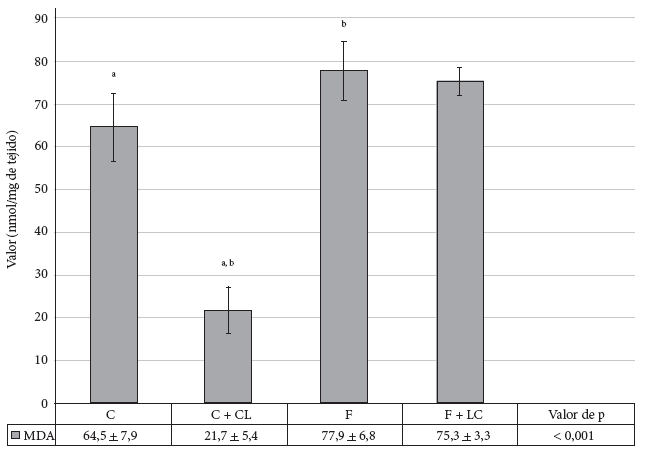
La administración de LC produjo una disminución significativa en los niveles de MDA (p < 0,01) comparado con el grupo C. El consumo de la fructosa al 40% (grupo F) produjo un incremento significativo de 21% (p=0,03) comparado con el grupo C. La administración de LC con consumo de fructosa no muestra una disminución significativa (Figura 5).
DISCUSIÓN
En el presente estudio, podemos observar que la administración de LC cumple un papel antioxidante, en relación con el consumo excesivo de fructosa en ratas de la cepa Holtzman.
En la actualidad, la fructosa es un azúcar que se añade a los alimentos procesados y el consumo de esta se ha incrementado en diversas sociedades. La ingesta excesiva de fructosa se relaciona con resistencia a la insulina, obesidad, dislipidemia y síndrome metabólico 1 , 2 , 10 , 11. La L-carnitina es un aminoácido endógeno asociado con el metabolismo lipídico; también se ha reportado con actividad antioxidante.
El modelo de estrés oxidativo inducido por fructosa se utiliza por los cambios metabólicos que produce a nivel tisular y a nivel sérico. La fructosa es capaz de generar ROS tanto in vivo como in vitro, como lo hace la glucosa (1,2,10,). En este estudio, la fructosa al 40% en la bebida a libre demanda no modificó los niveles de glucosa plasmática en ayunas durante ocho semanas. Resultado similar fue reportado por Andrade et al. 11 en un tratamiento con fructosa al 10% a libre demanda durante 18 semanas. Sin embargo, Mamikutty et al. 1 demostraron el incremento de glicemia usando fructosa al 20% y al 25% en ratas Wistar durante ocho semanas. Asimismo, Bulboacă et al. 2 informaron el incremento de glicemia administrando fructosa al 10% en ratas Wistar durante 12 semanas. Es importante mencionar que existen diferencias genéticas que expresan variaciones metabólicas según la cepa de la rata 12.
Sobre el proceso de absorción de la fructosa, existe una diferencia sustancial con la glucosa. La fructosa se absorbe mediante el transportador GLUT 5, independientemente de la absorción de la glucosa. Luego de diversos procesos, puede ingresar a la glucólisis, evitando los puntos de regulación de la hexoquinasa y fosfofructoquinasa-1 10. El ingreso a la glucólisis aporta metabolitos para la lipogénesis e inhibe el proceso de beta-oxidación. En nuestro estudio, se observó macroscópicamente un aumento de grasa visceral en el grupo F y el grupo F+LC y esto podría ser explicado por este proceso. Por otro lado, la fructosa no constituye un sensor importante a nivel pancreático, pues las células beta-pancreáticas no tienen transportadores GLUT 5 ( 1 , 10, por lo que el metabolismo de la fructosa es independiente de la insulina y no incrementaría la glicemia 10, lo cual explicaría los resultados, en cuanto a la conservación de esta. Asimismo, se relaciona con la conservación de la insulina plasmática, expresada como HOMA-IR, donde no se observaron diferencias significativas en los grupos. Aunque la HOMA-IR, como parámetro de resistencia a la insulina, mostró un incremento de 28,3% entre el grupo F comparado con el grupo C; este moderado incremento sugeriría el uso de fructosa en un tiempo mayor podría generar resistencia a la insulina, como se ha descrito en otras investigaciones ( 1 , 2 , 10 , 13. Además, se mostró una disminución de 25,8% en el grupo F+LC comparado con el grupo F. Por ejemplo, Ringseir et al. ( 14 revisaron seis estudios en ratas en los que la LC disminuyó la glicemia y la HOMA-IR.
En el páncreas, el consumo de fructosa produjo una marcada disminución del nivel de insulina. Este resultado en el grupo F puede relacionarse con el incremento del número y tamaño de los adipocitos, lo cual provoca la liberación de MCP-1, que lleva al reclutamiento de macrófagos-M1 con liberación de citoquinas como TNF-α, IL1 e IL6, generando un estado de inflamación crónica ( 15. Asimismo, el TNF-α se une a su receptor muerte, activando la vía extrínseca y posteriormente la vía intrínseca de la apoptosis y produciendo la muerte de las células beta-pancreáticas 16. Además, Maiztegui et al. 17 ) demostraron la disminución del número de células beta-pancreáticas debido al incremento de apoptosis; en su estudio usaron fructosa al 10% a libre demanda durante tres semanas. Contrariamente, se observa en la histología un aumento del tamaño de los islotes de Langerhans en el grupo F, lo que podría deberse a que las otras células de los islotes (células alfa, delta, F y G) se encontrarían estimuladas como efecto compensatorio.
Frente a este modelo de estrés inducido por fructosa al 40%, consumida a libre demanda, la administración de LC (grupo F+LC) indujo una recuperación del 100% de la insulina tisular frente al consumo de F (grupo F), este resultado, aunque no significativo es importante porque es evidencia del rol de LC en el tejido pancreático. En cambio, el grupo C+LC tuvo un comportamiento diferente, pues se observó incremento en 387% en el nivel de insulina, además hay mayor número y tamaño de los islotes de Langerhans (incluso por regiones hubo más islotes) que los ácinos pancreáticos comparado con el grupo C.
Diversos estudios demuestran que la administración de LC inhibe la apoptosis. Bonomini et al. 18 ) revisaron diferentes estudios y sugirieron la posible acción de inhibir a la caspasa 3. Un resultado similar fue reportado por Agarwal et al. 6 ) después analizar varias investigaciones, donde la LC inhibe la caspasa 3, 7 y 8, además de regular las proteínas supresoras de tumores, lo que favorece la supervivencia del ovocito. Asimismo, Cao et al. 3 ) reportaron en su estudio in vitro que el uso de LC favorece la disminución de la relación Bax/Bcl-2 y la producción de ROS. En términos metabólicos, según el estudio de Jiang et al.19, la presencia de LC favorece la expresión de CPT1 mediada por el PPARγ, lo que incrementa el proceso de beta-oxidación. Los resultados de nuestro estudio nos llevan a creer que la LC podría inhibir la apoptosis de las células beta-pancreáticas, por lo que el nivel de insulina pancreática aumentó significativamente en el grupo C+LC, mientras que en el grupo fructosa+LC no sería tan elevado, debido al daño previo que sufrió por la fructosa. Por lo tanto, la administración de LC (grupo C+LC) demostró la capacidad de estimular significativamente (p < 0,01) la producción de insulina a nivel tisular (Figura 2) sin afectar los niveles plasmáticos de la hormona.
En el hígado, los niveles de LC libre aumentaron significativamente en 21,5% cuando esta se administró como tratamiento al grupo F frente al grupo C. Además, se observó que en la administración de LC no se evidenció un incremento significativo con sus pares, esto podría deberse a que la LC puede actuar como scavenger. Según Gülçin 20 la LC in vitro actúa como scavenger del anión superóxido y del peróxido de hidrógeno, además favorece la quelación del ion ferroso, debido a su grupo carbonilo, que puede estabilizar los radicales libres en el carbono alfa mediante conjugación. También puede plantearse que en situaciones fisiológicas los niveles de la LC libre son estables, pero su participación en situaciones fisiopatológicas cambia, como en el consumo de fructosa a través de diversos mecanismos, como el reportado por Chang et al. 4 ) , quienes refieren que el incremento de ROS podría disminuir la expresión y función de OCTN-2 (transportador de carnitina en la membrana plasmática de los tejidos).
En diferentes estudios, el consumo de fructosa por largo tiempo incrementó la producción de ROS 2 , 21. Si la fructosa continúa hacia la glucólisis y el ciclo de Krebs, se produce NADH y FADH2, estos en la mitocondria van a la cadena transportadora de electrones, donde hay gran producción de anión superóxido. Si se forman ácidos grasos, estos pueden ser metabolizados por el proceso de beta-oxidación, con generación de ROS, además se produce acetil-CoA, a partir del cual se puede formar más NADH y FADH2 22 ) . En este sentido, Furukawa et al. 16 reportaron que en los adipocitos de las personas obesas había mayor actividad de NAPDH-oxidasa y disminución en la expresión de enzimas antioxidantes, lo cual genera fácilmente estrés oxidativo.
Por otro lado, la mayor producción de ROS compromete los mecanismos de defensa antioxidante; a nivel enzimático, la primera que actúa ante la reducción univalente del oxígeno es la SOD. Como se mencionó, la LC ejerce su papel principal en las mitocondrias, así que, puede explicarse el aumento en 25% de la actividad de la enzima mitocondrial sobre el grupo C que se apoya además en los niveles de LC (grupo C+CL) ligeramente incrementada. Asimismo, se muestra un comportamiento acoplado entre las isoenzimas citosólica y mitocondrial. Mientras que la actividad de la SOD Cu/Zn expresa una disminución del 30,5%, la SOD Mn exhibe un incremento del 42% en el grupo F+LC en comparación con el grupo C. Según Suzuki et al. 23, el exceso de ROS puede llevar a la inhibición de la enzima SOD Cu/Zn y al aumento de SOD Mn, lo que probablemente es una respuesta adaptativa a la producción de ROS. Se debe tener en cuenta que probablemente la SOD Mn es la más importante para la supervivencia en un ambiente oxidativo 24.
En este ambiente oxidativo, derivado de la actividad mitocondrial, la administración de LC favorece la producción de gran cantidad de acetil-CoA, lo cual genera grupos acetilos para procesos de acetilación de proteínas o histonas, y produce cambios postraduccionales o epigenéticos ( 25. En su investigación, Kerner et al. 26 observaron que el tratamiento con acetil-LC incrementó la acetilación de SOD Mn. Puede asumirse que la acetilación podría favorecer una mayor actividad de esta enzima. Por otro lado, se observó el incremento significativo de niveles de proteínas totales mitocondriales y posmitocondriales en el grupo C+LC, lo mismo se observó en el grupo F, aunque no fue significativo. Estos resultados permiten presumir que la LC no solo actuaría como regulador de la actividad, sino también a nivel de la síntesis proteica, entre ellos, las enzimas antioxidantes.
La evaluación de la lipoperoxidación refleja el daño sufrido por reacciones peroxidativas de los ácidos grasos poliinsaturados (PUFA) en la membrana, esta determinación de MDA se considera un marcador de estrés oxidativo. Las propiedades antioxidantes de LC que se presentaron en el hígado, también fueron observados en el MDA, lo cual produjo una disminución altamente significativa (p < 0,01) en ausencia de factores de estrés oxidativo, como la fructosa, lo que corrobora el papel de scavenger discutido anteriormente 3 , 4 , 6 , 20. Si bien el consumo a libre demanda de fructosa al 40% produjo un aumento de lipoperoxidación en un 21%, la administración de LC no pudo revertir ese incremento. El consumo de fructosa generó una gran cantidad de ROS, por lo que probablemente un mayor tiempo de tratamiento podría disminuir el estrés oxidativo, expresado como MDA, como se demuestra en diversos estudios 5 , 27 , 28. Los mecanismos que podrían intervenir para disminuir la lipoperoxidación serían a través del incremento de la expresión de la SOD Mn y SOD Cu/Zn mediado por el incremento de la expresión RNAm de PPARα, según lo reportado por Liu et al. 29.
Diversas investigaciones muestran que la expresión de PPAR activa la expresión de genes de SOD Mn y SOD Cu/Zn mediante la vía transcripcional 5 , 29 , 30. Entonces, con base en los resultados del presente estudio y con mayor tiempo de tratamiento de LC podríamos proponer que de esta manera se reducirían los niveles de ROS, lo que evitaría la lipoperoxidación y se eludirían sus efectos perjudiciales a nivel celular.
Como una limitación del presente estudio se debe mencionar la disposición de recursos, puesto que no se pudieron evaluar las concentraciones del MDA y SOD basal, además de requerir un tiempo más prolongado de tratamiento.
En conclusión, en este trabajo se observó que la fructosa no afecta la glicemia, pero favorece la lipogénesis y el ambiente oxidativo; en este escenario, la administración de LC favorece cambios metabólicos que corroboran su función antioxidante.











 texto en
texto en