INTRODUCCIÓN
Los asilos de ancianos son instituciones de cuidado de largo plazo con una alta prevalencia de enfermedades infecciosas 1; la infección del tracto urinario (ITU), cuyo principal agente etiológico es Escherichia coli, es la infección más frecuente en este tipo de instituciones 1. Asimismo, entre el 20 a 40% de las bacteriemias en ancianos es ocasionada por bacterias que ascienden por el tracto urinario; E. coli y Proteus mirabilis son los agentes microbianos más comunes 2.
Los residentes de asilos de ancianos presentan una alta probabilidad de colonización y de infecciones por E. coli multidrogorresistentes ( 3. Además, la alta recurrencia de ITU y el tratamiento inapropiado de bacteriurias asintomáticas incrementa el uso de antibióticos, lo que conlleva a la selección de este tipo de bacterias 1, con un aumento de la tasa de mortalidad de los residentes 2.
Los antibióticos del grupo ß-lactámico representan aproximadamente el 50% de los antibióticos prescritos en el mundo 4; sin embargo, su eficiencia terapéutica ha disminuido debido a la rápida selección de mecanismos de resistencia. Las ß-lactamasas de espectro extendido (BLEE) representan el mecanismo más importante para la resistencia a cefalosporinas de tercera generación en E. coli. La enzima denominada CTX-M es la BLEE de mayor predominancia a nivel global debido a su alta eficiencia de propagación desplazando a ß-lactamasas del tipo SHV y TEM en la epidemiología global ( 4. La CTX-M tiene un linaje heterogéneo que incluye seis grupos (CTX-M-1, CTX-M-2, CTX-M-8, CTX-M-9, CTX-M-25 y KLUC) que difieren entre sí por una cantidad mayor o igual al 10% de residuos aminoacídicos ( 4. En el Perú existe una alta frecuencia de E. coli productoras de BLEE; en el 2011, en un programa de vigilancia multinacional en el que se evaluaron once países de América Latina se reportó que el 54,0% de las E. coli eran productoras de BLEE ( 5.
Por otro lado, aunque la diseminación de BLEE de tipo CTX-M en E. coli uropatógenas (UPEC, por sus siglas en inglés) es un problema global que disminuye las opciones terapéuticas en los pacientes, la severidad de la infección depende de la capacidad patogénica en las UPEC ( 6. Las UPEC poseen factores de adherencia (p.ej. Pap G II) que le permiten iniciar la infección exitosamente y migrar hacia regiones ascendentes del conducto urinario agravando la condición del paciente 6. Asimismo, las UPEC producen sistemas sideróforos (p.ej. ChuA, Aer) y exotoxinas (p.ej. α-Hly, TcpC, Cnf-1) que, en conjunto, constituyen un sistema proteico que les permiten eludir y/o afectar al sistema inmune en detrimento de la salud del paciente ( 6. En bacteriemias cuyo punto de origen es una ITU las UPEC requieren de la expresión de proteínas que le permiten adaptarse a las condiciones ambientales del tejido sanguíneo (p.ej. nanA) ( 7.
A nuestro conocimiento, no se han publicado en Perú estudios relacionados que hayan descrito la frecuencia de las UPEC productoras de BLEE de tipo CTX-M en asilos de ancianos. La población de estos asilos es susceptible a ITU y a tener complicaciones sistémicas; por ello, el objetivo del estudio fue determinar la frecuencia de genes de virulencia y la presencia del gen bla CTX-M en UPEC aisladas en residentes de asilos de ancianos ubicados en Lima Metropolitana.
MENSAJES CLAVE
Motivación para realizar el estudio: los asilos de ancianos, por la alta prevalencia de infecciones urinarias debido a Escherichia coli multidrogo resistente y el alto riesgo de generar urosepsis, merecen una especial atención epidemiológica.
Principales hallazgos: el 57,1% de las E. coli productoras de BLEE fueron portadores del gen bla CTX-M; de los cuales el 70% pertenecieron al gen bla CTX-M-grupo 2. Además, se obtuvo una frecuencia del 46% y 37% de hly-alfa y cnf-1, respectivamente; y, finalmente, una frecuencia del 46% y 91% del gen pap G II y nanA, respectivamente.
Implicancias: este es el primer reporte de genes resistentes asociados con BLEE en E. coli uropatógenas identificado en asilos de ancianos en el Perú; lo que tiene gran relevancia por constituir una amenaza para la salud de los adultos mayores.
EL ESTUDIO
Diseño de estudio y población
Estudio descriptivo observacional realizado en el 2018, en donde se recolectaron de forma aleatoria 35 aislamientos no repetidos de E. coli productoras de BLEE obtenidas de muestras de orina de adultos mayores residentes de seis asilos de ancianos privados de Lima Metropolitana en Perú.
Estudio microbiológico
La identificación bacteriana se realizó por pruebas bioquímicas convencionales (triple sugar iron agar, lysine iron agar, agar citrato, agar movilidad-indol-orinitina y rojo de metilo/Voges-Proskauer) y confirmadas molecularmente, por reacción en cadena de la polimerasa (PCR, por sus siglas en inglés), a través de la amplificación del gen uspA.
Pruebas de susceptibilidad
Las E. coli productoras de BLEE fueron confirmadas por el método de disco difusión especificado en el documento M02-13 del Clinical & Laboratory Standards Institute (CLSI) 8; además, se determinó la susceptibilidad antimicrobiana por el método de disco difusión de acuerdo con los lineamientos del CLSI ( 8, empleando como control de calidad a la E. coli ATCC 25922. Se incluyeron los discos de antibióticos con los siguientes antibióticos: piperacilina/tazobactam 100/10 µg (PTZ); amoxicilina/ácido clavulánico 20/10 µg (AMC); cefotaxima 30 µg (CTX); ceftazidima 30 µg (CAZ); cefepime 30 µg (FEP); cefoxitina 30 µg (FOX); aztreonam 30 µg (AZM); meropenem 10 µg (MEM); imipenem 10 µg (IMP); amikacina 30 µg (AK); gentamicina 10 µg (GM); ciprofloxacina 5 µg (CIP); nitrofurantoina 300 µg (NIT) y trimetoprim/sulfametoxazol 1,25/23,75 µg (SXT).
Detección de genes de virulencia y resistencia
El ADN bacteriano se extrajo usando DNA Purification kit GeneJetGenomic (ThermoScientific), siguiendo las recomendaciones del fabricante. Se determinó la presencia de ocho genes de virulencia: aer, hly, cnf-1, chuA, TcpC, nanA, pap GII, iucC ( 9 , 10 ) y tres genes de resistencia asociados a BLEE: bla CTX-M, bla SHV y bla TEM ( 11. Además, se realizó la detección de diferentes grupos de aislados portadores de bla CTX-M (1, 2, 8 y 9) ( 12. Las condiciones de la PCR fueron llevadas a cabo en un volumen final de 30 μl que contenía 1X del MaximoTaq DNA (GeneON) así como 0,5 uM de cada uno de los cebadores y 1,5 mM de MgCl2. El volumen de ADN incorporado fue de 2,0 μL. El termociclador Labnet, Multigene optimax se programó con los siguientes parámetros: denaturación inicial a 94 °C por tres minutos; denaturación a 94 °C por 30 s; extensión a 72 °C por 30 s; en 30 ciclos de reacción y extensión final a 72 °C durante tres minutos, mediante el termociclador Labnet, Multigene optimax. En la Tabla 1 se muestra la secuencia de cebadores utilizados, el tamaño de los productos de amplificación, la temperatura de hibridación y la referencia del estudio. Los fragmentos de ADN amplificados fueron separados mediante electroforesis en gel de agarosa al 1% durante 50 min a 110 voltios. Finalmente, se usó el buffer de carga Runsafe (GeneON) para su revelado en UV.
Tabla 1 Genes de virulencia y resistencia, características de amplificación.
| Gen | Secuencia de cebadores (5’ - 3’) | Producto (pb) | Temperatura de hibridación (°C) |
|---|---|---|---|
| Genes de virulencia | |||
| α-hemolysin (α-hly) | AACAAGGATAAGCACTGTTCTGGCT | 1177 | 63 |
| ACCATATAAGCGGTCATTCCCGTCA | |||
| chuA | GACGAACCAACGGTCAGGAT | 279 | 55 |
| TGCCGCCAGTACCAAAGACA | |||
| Aerobactin synthesis (aer) | TACCGGATTGTCATATGCAGACCGT | 602 | 63 |
| AATATCTTCCTCCAGTCCGGAGA AG | |||
| Aerobactin synthesis (iucC) | CTCGAATTCACTGGGATTTGGTCAACC | 1701 | 62 |
| CTCTCTAGAATTCCTGAGTTACCAGCC | |||
| Cytotoxic necrotizing factor (cnf1) | AAGATGGAGTTTCCTATGCAGGAG | 498 | 61 |
| CATTCAGAGTCCTGCC CTCATTATT | |||
| P - fimbriae (pap)- alelo II | GGGATGAGCGGGCCTTTGAT | 190 | 65 |
| CGGGCCCCCAAGTAACTCG | |||
| nanA | ACCGGTGAGGGGAAATAAAC | 216 | 59 |
| GGTGAGTACCAGGGCGATTA | |||
| tcpC | GGCAACAATATGTATAATATCCT | 386 | 51 |
| GCCCAGTCTATTTCTGCTAAAGA | |||
| Genes de resistencia | |||
| blaSHV | ATGCGTTATATTCGCCTGTG | 544 | 58 |
| GTTAGCGTTGCCAGTGCTCG | |||
| blaTEM | ATAAAATTCTTGAAGACGAAA | 1080 | 54 |
| GACAGTTACCAATGCTTAATC | |||
| blaCTX-M | TTTGCGATGTGCAGTACCACTAA | 865 | 60 |
| CGATATCGTTGGTGGTGCCAT | |||
| blaCTX-M-grupo 1 | ATGGTTAAAAAATCACTG C | 900 | 55 |
| GGTGACGATTTTAGCCGC | |||
| blaCTX-M-grupo2 | CGTTAACGGCACGATGAC | 404 | 59 |
| CGATATCGTTGGTGGTGCCAT | |||
| blaCTX-M-grupo8 | ACGCTCAACACCGCGATC | 490 | 63,3 |
| CGTGGGTTCTCGGGGATAA | |||
| blaCTX-M-grupo9 | GATTGACCGTATTGGGAGTTT | 831 | 58 |
| CGGCTGGGTAAAATAGGTCA |
Análisis estadístico
El análisis estadístico se realizó mediante el programa SPSS Statistics for Windows, versión 25.0. Armonk, NY: IBM Corp. La descripción de las variables cualitativas se realizó a través de gráficas de frecuencia.
Consideraciones éticas
El presente estudio obtuvo la aprobación del Comité de Ética de la Facultad de Medicina de la Universidad Nacional Mayor de San Marcos. Acta 1812 con código de proyecto 0013.
HALLAZGOS
Susceptibilidad antimicrobiana
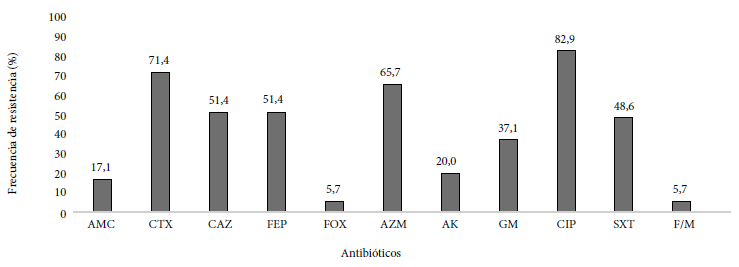
Se analizaron 35 UPEC productoras de BLEE provenientes de asilos de ancianos. La mayoría de los aislamientos fueron resistentes a cefotaxima (25/35), no hubo aislamientos resistentes a carbapenémicos, y solo dos (2/35) aislamientos fueron resistente a cefoxitina. Además de la resistencia a los ß-lactámicos se pudo observar que las cepas de UPEC presentaron amplia resistencia a ciprofloxacina, 82,9% (29/35) de los casos. Asimismo, no se encontraron UPEC resistentes a PTZ, MEM e IMP. En la Figura 1 se detalla las frecuencias de resistencia por antibiótico.
Genotipificación de UPEC productoras de bla CTX-M
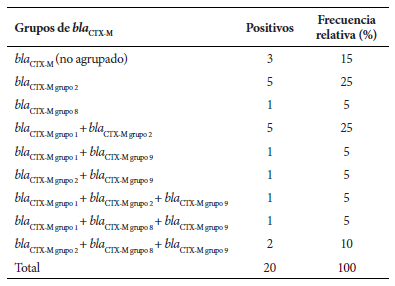
De los 35 aislamientos, 57,1% (20/35) fueron portadores del gen bla CTX-M, de los cuales el 70% (14/20) correspondieron al bla CTX-M-grupo 2, 40% (8/20) al bla CTX-M-grupo 1, 30% (6/20) al bla CTX-M-grupo 9 y 20% (4/20) al bla CTX-M-grupo 8. Por otro lado, el 60% (12/20) de las UPEC portadoras del gen bla CTX-M tuvieron dos o más variantes alélicas del gen bla CTX-M en la misma bacteria. Además, hubo un mayor nivel de confluencia entre los genes pertenecientes al bla CTX-M-grupo 1 y bla CTX-M-grupo 2 (Tabla 2). También se evaluó la presencia de otros genes productores de ß-lactamasas (bla SHV y bla TEM ) en los productores y no productores de bla CTX-M. De un subestrato de las UPEC analizadas el 48,1% (13/27) no resultaron portadoras del gen bla CTX-M, pero sí a los genes bla SHV , y/o bla TEM . Asimismo, el 51,9% (14/27) de las UPEC presentaron al gen bla CTX-M, además de los genes bla SHV , y/o bla TEM . No se analizó las secuencias nucleotídicas de las variantes alélicas que confirmarían su pertenencia al grupo BLEE.
Genotipificación de factores de virulencia en UPEC productoras de BLEE
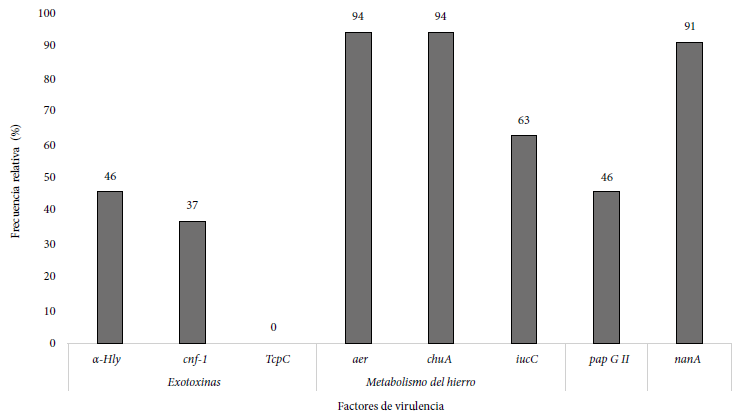
De las 35 UPEC productores de BLEE se analizaron los genes relacionados con exotoxinas, en los cuales se obtuvo una frecuencia del 46% (15/35) y 37% (13/35) de hly-alfa y cnf-1, respectivamente. En los genes asociados al metabolismo del hierro se observó una elevada presencia de los genes aer, 94% (33/35) y chuA, 94% (33/35). Además, se evaluó la presencia de la adhesina pap GII obteniendo una frecuencia del 46% (16/34) y del gen nanA en el 91% (32/35) (Figura 2).
DISCUSIÓN
Los resultados de este estudio estudio muestran que el 57,1% de las Escherichia coli productoras de BLEE presentaron el gen bla CTX-M, siendo el 70% del grupo bla CTX-M-grupo 2. Por otro lado, los genes: hly-alfa y cnf-1, codificantes a exotoxinas, se detectaron con una frecuencia del 46 y 37%, respectivamente.
Los asilos de ancianos son instituciones de larga estancia con una alta prevalencia de ITU ocasionado por bacterias multidrogorresistentes ( 3. En este estudio, el 57,1% de las UPEC fueron portadoras del gen bla CTX-M. Este resultado es similar a los descritos por Galván et al.13 y Arce-Gil et al.11, quienes reportaron una frecuencia del 54,7% y 51,4%. Sin embargo, difieren de los descrito por Ramirez et al.14 ) y Chavez ( 15 ) en diversos hospitales de Lima (70% y 91,7%). Esto último demuestra la gran variabilidad en la presencia de este gen en las instituciones de salud.
En lo referente a los resultados obtenidos sobre los subgrupos de bla CTX-M, fueron bla CTX-M-grupo 2 (14/20) seguido del bla CTX-M-grupo 1 (8/20) los de mayor presencia. Esto difiere de lo reportado por Chavez ( 15, en donde no se detectó al bla CTX-M-grupo 2 y el bla CTX-M-grupo 1 (26/33) fue el de mayor frecuencia, y por Palma et al. ( 16, donde predominó el bla CTX-M-grupo 1 (13/27). Sin embargo, estudios recientes indican que en Sudamérica bla CTX-M-grupo 2 es aún significativo ( 17 y una reciente revisión en Brasil identifica a los bla CTX-M-grupo 2 y bla CTX-M-grupo 1 como las variantes más prevalentes en la región ( 18.
También se evaluó la presencia de los genes bla TEM (54,3%) y bla SHV (51,4%); asimismo, se observó la presencia de los genes bla TEM y bla SHV entre las UPEC portadoras del gen bla CTX-M. Vale la pena resaltar que en el 37% de los aislamientos solo se identificó la presencia del gen bla TEM y/o bla SHV, y que, a pesar de que no se determinó su variante alélica y su dominio al grupo BLEE es un fuerte indicador de su pertenencia. Además, no se detectó la presencia de ninguno de los genes de resistencia evaluados en el 5,7% de los aislamientos, lo cual indica la presencia de otros genes de resistencia tipo BLEE no analizados en este estudio.
Con relación con los factores de virulencia, el gen pap GII estuvo presente en el 47,1% de las UPEC. Este resultado difiere de lo reportado por Paniagua-Contreras et al. 19, en México, con un 21,1% de frecuencia del gen pap G II en UPEC comunitarias. También, se observó una alta frecuencia de genes asociación al transporte de hierro, similar a lo reportado por Dadi et.al 20, con 54,5% respecto al gen iucC.
Con relación a las exotoxinas estudiadas, obtuvimos una frecuencia del 44,2 y 38,2% de hly-alfa y cnf-1, respectivamente, resultados comparables al reportado por Dadi et al. 20 ) con un 50,4 y 29% de hly-alfa y cnf-1, respectivamente. Por otro lado, en este estudio no encontramos UPEC portadoras del gen tcpC, a diferencia de otros trabajos en los que se han reportado prevalencias de hasta el 25% 10.
También encontramos una frecuencia del 88,2% para el gen nanA, el cual es importante en la producción energética. Se ha propuesto que la presencia del gen nanA genera una alta competitividad en las UPEC para generar bacteriemias, aunque su rol en la patogénesis de la ITU es menos importante ( 6, los resultados indican la existencia de un alto riesgo en los residentes con bacteriemias de desarrollar sepsis.
Este estudio presenta algunas limitaciones. Si bien se realizó en varios asilos de ancianos, no se obtuvo información clínica de los pacientes, además de presentar un número limitado de muestras. Por otra parte, no se analizaron más genes de virulencia y resistencia (otros tipos de BLEE) relevantes en la epidemiología de las UPEC.
En conclusión, este es el primer reporte de UPEC productoras de BLEE en asilos de ancianos en Perú; donde podemos observar el predominio del gen bla CTX-M, de los cuales el 70% pertenecen al bla CTX-M-grupo 2. También, se puede indicar que las UPEC productoras de BLEE en los asilos de ancianos presentan una elevada frecuencia de exotoxinas y del gen nanA, lo que les confiere una ventaja para diseminarse hacia el torrente sanguíneo. Esperamos que estos hallazgos permitan fortalecer la vigilancia epidemiológica de bacterias multirresistentes y prevenir su diseminación.











 text in
text in