Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Horizonte Médico (Lima)
versión impresa ISSN 1727-558X
Horiz. Med. vol.15 no.1 Lima ene./mar. 2015
ORIGINAL BREVE
Evaluación de la técnica 2,2-Difenil-1-Picrilhidrazilo (DPPH) para determinar capacidad antioxidante
Assessment of 2,2-diphenyl-1-picrilhidrazilo (DPPH) Technique to determine antioxidant capacity
Emilio Guija-Poma1, Miguel Ángel Inocente-Camones2, John Ponce-Pardo2, Edwin Zarzosa-Norabuena3
1 Doctor en farmacia y Bioquímica. Instituto de Investigación. Centro de Investigación de Bioquímica y Nutrición, FMH. USMP. Lima, Perú.
2 Químico Farmacéutico. Instituto de Investigación. Centro de Investigación de Bioquímica y Nutrición, FMH. USMP. Lima, Perú.
3 Magister en Bioquímica y Nutrición. Instituto de Investigación. Centro de Investigación de Bioquímica y Nutrición, FMH. USMP. Lima, Perú.
RESUMEN
Este estudio evalúa la actividad antioxidante usando el método del radical libre 2,2-difenil-1-picrilhidracilo (DPPH). Este método se utiliza para determinar la capacidad antioxidante de alimentos y compuestos sintéticos; para este fin se ha hecho uso de este radical libre en concentraciones comprendidas entre 0,037 y 0,200 mM, así mismo, para llevar a cabo esta evaluación se utilizó los estándares de catequina y epicatequina en un rango de concentración que estuvo entre 6,67 x 10-3 y 2,2 x 10-2 mM. Los valores de IC50 para ambos estándares fueron dependientes de la concentración de DPPH, habiéndose observado que el valor anterior aumenta al incrementar la concentración de DPPH. El resultado obtenido en este estudio indica la importancia de la concentración del DPPH para evaluar la capacidad antioxidante.
Palabras clave: Antioxidante, DPPH, catequina, epicatequina, radical libre. (Fuente: DeCS BIREME).
ABSTRACT
We assessed the technique using free radical 2,2-diphenyl-1-picrilhidrazil (DPPH) used to determine the antioxidant capacity of foods and synthetic compounds; for that purpose this free radical has been used in concentrations between 0.037 and 0.2 mM, likewise, to perform this evaluation the catechin and epicatechin standards have been used in a concentration range of 6.67 x 10(-3) and 2.2 x 10(-2) mM. CI(50) values for both standards were dependent on the concentration of DPPH, having observed that the above value increases with increasing concentration of DPPH, for which reason it is suggested that all research use a single concentration of DPPH in the reaction medium.
Key words: Antioxidant, DPPH, catechin, epicatechin, free radical. (Source: MeSH NLM).
INTRODUCCIÓN
Los radicales libres son moléculas o fragmentos de moléculas caracterizadas por tener uno o más electrones desapareados en su orbital externo, condición que los torna altamente reactivos (1). En el ser humano se generan radicales libres en la cadena respiratoria mitocondrial, cuando reacciona el peróxido de hidrógeno con el ion ferroso, por acción catalítica de la ciclooxigenasa, la reacción de vitamina C con el ion ferroso, por acción de la NADPH reductasa, etc.
En los seres vivientes existen sistemas de defensa antioxidante que tienen la propiedad de impedir la acción nociva de los radicales libres, habiéndose identificado compuestos con propiedades antioxidantes de naturaleza enzimática como la catalasa, superóxido dismutasa, glutatión peroxidasa, etc., así como, sustancias no enzimáticas: ascorbato, ferritina, ceruloplasmina, polifenoles, antocianinas.
Cuando la defensa antioxidante es insuficiente para proteger al organismo del efecto dañino de los radicales libres puede conducirlo al estrés oxidativo, condición que está estrechamente vinculado a una gran diversidad de patologías como la psoriasis, cáncer, diabetes mellitus, aterosclerosis, cataratas, hipertensión arterial. (2-5)
Existe un gran número de estudios epidemiológicos que vinculan la ingesta de una dieta rica en frutas y verduras con un disminuido riesgo de padecer enfermedades cardiovasculares, cáncer, aterosclerosis, artritis, etc., y ello debido a que dichos alimentos tienen un elevado contenido de polifenoles, flavonoides, antocianinas, vitamina C, vitamina E, B-caroteno, licopeno (6-8).
Se han descrito diversas técnicas para evaluar la capacidad antioxidante de alimentos y plantas medicinales (9,10), pero aquella que ha recibido una preferencial atención es la técnica que utiliza el radical libre 2,2-difenil-1-picrilhidrazilo conocido por las siglas DPPH (11,12).
Este radical libre es susceptible de reaccionar con compuestos antioxidantes a través de un proceso caracterizado por la cesión de un átomo de hidrógeno proporcionado por el agente antioxidante.
Los estudios cinéticos muestran que este proceso ocurre a través de una reacción de pseudo primer orden la que puede seguirse midiendo la disminución de la absorbancia en función del tiempo (13).
Esta medición permite observar una primera fase muy rápida, seguida ulteriormente por una reacción lenta, lo que podría ocurrir debido a un proceso de dimerización de los productos de la reacción o a reacciones de los productos de ésta.
La reacción antes descrita, entre el DPPH y un antioxidante, podemos representarla de la siguiente manera:
[DPPH*] + [AOH] → [DPPH-H] + [AO*]
Por cuyo motivo, las condiciones de ensayo en que se mide la capacidad antioxidante puede describirse por la siguiente ecuación:
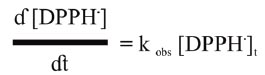
La determinación de la concentración de compuestos antioxidantes utilizando la técnica del DPPH ha sido descrita hace más de cincuenta años (14), pero hemos observado que los autores no utilizan la misma concentración del DPPH en los medios de reacción y ello no permite realizar una evaluación precisa, considerando especialmente que los resultados experimentales se expresan como el valor IC50, es decir, la concentración de la muestra problema que produce una inhibición del 50% del radical libre DPPH (15-17).
En tal sentido, podemos considerar que el valor IC50 es dependiente de la concentración del DPPH, así como, de la naturaleza del compuesto antioxidante.
El objetivo del presente trabajo reside en mostrar que la concentración del DPPH en el medio de reacción influye en la evaluación de la capacidad antioxidante.
METODOLOGÍA
El medio de reacción estuvo constituido por concentraciones finales de DPPH comprendidas 0.035 y 0.20 mM disuelto en metanol grado HPLC, mientras que las concentraciones de los estándares catequina y epicatequina se utilizaron en concentraciones comprendidas entre 6.67 x 10-3 y 2.2 x 10-2 mM, disueltas en metanol grado HPLC. La reacción se desarrolló a temperatura ambiente (22º C) durante 30 minutos en la oscuridad, a cuyo término se procedió a leer la densidad óptica en un espectrofotómetro marca Shimadzu modelo UV-250. Paralelamente se incubó un tubo blanco que solamente contenía metanol. Todos los reactivos utilizados fueron de grado para análisis.
HALLAZGOS
Para la evaluación del valor IC50 de la catequina se utilizaron tres concentraciones de DPPH, 0.035, 0.070 y 0.125 mM, mientras que la catequina se utilizó en concentraciones comprendidas entre 6.67 x 10-3 y 2.2 x 10-2 mM, habiéndose observado que los valores IC50 fueron 8.5, 10.8 y 20.7 µM respectivamente, conforme se observa en la Tabla 1, en la que es posible apreciar que cuando se incrementa la concentración del DPPH paralelamente aumenta el valor IC50.

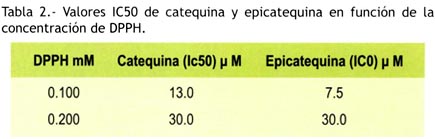
Así mismo, se evaluaron los valores IC50 de catequina y epicatequina utilizando dos concentraciones distintas de DPPH: 0.100 y 0.200 mM; en estas condiciones de ensayo cuando la concentración del DPPH fue 0.100 mM el IC50 de la catequina fue de 13.0 µM mientras que el de la epicatequina fue 7.5 µM; pero, cuando se usó una concentración final de DPPH correspondiente a 0.200 mM, la catequina y epicatequina mostraron prácticamente un mismo valor IC50, como se muestra en la Tabla 2, dicho valor se obtuvo por extrapolación, ya que en las condiciones experimentales se observó que la máxima inhibición alcanzada fue de 33.0 y 31.3 % para la catequina y epicatequina respectivamente, por cuyo motivo, no pudo alcanzarse el 50% de inhibición del DPPH.
DISCUSIÓN
Conforme se ha observado, las concentraciones utilizadas del DPPH para evaluar el valor IC50 de los antioxidantes catequina y epicatequina estuvieron comprendidas en un amplio rango: 0.035 y 0.2 mM, habiéndose obtenido resultados que fueron dependientes de la concentración del radical libre DPPH; el hecho de obtener valores diferentes de IC50 para los antioxidantes antes citados, sugiere que es necesario realizar una revisión de las evaluaciones de la capacidad antioxidante de alimentos con DPPH, publicadas desde hace más de 30 años (8,10,12,16,17).
Hemos observado que cuando se utiliza concentraciones altas de DPPH (0.2 mM) se torna menos sensible la determinación del valor IC50, conforme sucede con las evaluaciones de catequina y epicatequina determinadas con dicha concentración, mientras que cuando se utilizan concentraciones menores de DPPH (0.035 mM) el valor IC50 es el más bajo, y ello naturalmente conduce a una apreciación errada de las propiedades antioxidantes de un alimento o planta medicinal, ya que para efectos de comparación aquella muestra que tiene el menor valor IC50 es la que posee una mejor actividad antioxidante.
En diversos trabajos de investigación en los que se realiza un análisis cinético del comportamiento del radical libre DPPH, se observa que cuando se evalúa la capacidad antioxidante de epicatequina con una concentración de DPPH 0.097 mM se obtiene un valor IC50 de 19.5 µM (18), en cambio, cuando esta evaluación se realiza con una concentración 0.063 mM se obtiene un valor de 4.5 µM (19), así mismo, la evaluación del IC50 de catequina utilizando una concentración 0.063 mM de DPPH muestra un valor de 6.0 µM (19), mientras que el valor que hemos obtenido en nuestro laboratorio usando una concentración de DPPH 0.070 mM, es de 10.8 µM.
Conforme se ha mostrado anteriormente, existe una amplia variedad de concentraciones de DPPH que se utiliza para la determinación de la capacidad antioxidante de compuestos naturales y sintéticos, por cuyo motivo, consideramos que sería conveniente adoptar una definida concentración del DPPH para todas las determinaciones analíticas la que podría ser 0.1 mM, ya que a concentraciones mayores disminuye la sensibilidad de esta técnica para evaluar la capacidad antioxidante de una muestra.
REFERENCIAS BIBLIOGRÁFICAS
1. Cascales M. Bioquímica y Fisiopatología del estrés oxidativo. Fundación José Casares Gil.- España. 1997.
2. Lee J, Koo N, Min DB. Reactive oxygen species, aging, and antioxidative nutraceuticals. Comp Rev Food Sci Saf 2004;3:21-33.
3. Keher JP, Smith CV. Free radicals in Biology: Sources, reactivities, and roles in the etiology of human diseases. En: Frei B editor. Natural antioxidants in human health and disease. New York: Academic Press, 25-62.
4. Halliwell B, Gutteridge JMC. Free radicals in biology and medicine. 4º ed. Oxford, UK: Clarendon Press, 2007.
5. Pham-Huy LA, He H, Pham-Huy C. Free radicals, antioxidants in disease and Health. Int. J Biomed Sci. 2008;4(2):89-96.
6. Riccioni G, Bucciarelli T, Mancini B, Di Ilio C, Capra V, D'Orazio N. The role of antioxidant vitamin supplementation in the prevention of cardiovascular diseases. Expert Opin Investig Drugs. 2007;16(1):25- 32.
7. Iqbal R, Anand S, Ounpuu S, Islam S, Zhang X, Rangarajan S y col. Dietary patterns and the risk of acute myocardial infarction in 52 countries: results of the INTERHEART study. Circulation 2008;118(19):1929-1937.
8. Paredes-López O, Cervantes-Caja ML, Vigna-Pérez M, Hernández- Pérez T. Berries improving human health and healthy aging, and promoting quality life-A review. Plant Foods Human Nutr. 2010;65(3):299-308.
9. Halvorsen BL, Blomhoff R. Validation of a quantitative for the total content of lipophilic and hydrophilic antioxidants in foods. Food Chem. 2011;127:761-768.
10. Ozgen M, Reese RN, Tulio AZ, Scheerens JC, Miller AR. Modified 2,2-azino-bis-3-ethylbenzothiazoline-6-sulfonic acid (ABTS) method to measures antioxidant capacity of selected small fruits and comparison to ferric reducing antioxidant power (FRAP) and 2,2'-diphenyl-1-picrylhydrazyl (DPPH) methods. J Agric Food Chem. 2006;54:1151-1157.
11. Villaño D, Fernández-Pachón MS, Moyá ML, Troncoso AM, García- Parrilla MC. Radical Scavenging ability of polyphenolic compounds towards DPPH free radical. Talanta 2007:230-235.
12. Goupy P, Dufour C, Loonis M, Dangles O. Quantitative kinetic analysis of hydrogen transfer reactions from dietary polyphenols to the DPPH radical. J Agric Food Chem 2003;51:615-622.
13. Brand-Williams W, Cuvelier ME, Berset C. Use of a free radical method to evaluate antioxidant activity. LWT Food Sci Technol. 1995;28(1):25-30.
14. Blois MS. Antioxidant determination by use of a stable free radical. Nature. 1958;181:1199-1200.
15. Nenadis N, Lazaridou O, Tsimidou M. Use of reference compounds in antioxidant activity assessment. J Agric Food Chem. 2007;55:5452- 5460.
16. Suja KP, Jayalekshmy A, Arumughan C. Free radical scavenging behavior and antioxidant compounds of sesame (Sesamum indicum L.) in DPPH system. J Agric Food Chem. 2004;52:912-915.
17. Chaouche TM, Haddouchi F, Ksouri R, Medini F, El-Haci IA, Boucherit Z y col. Antioxidant activity profi by spectrophotometric methods of phenolic extract of Prasium majus L. Free Rad Antiox. 2013;3:43-46.
18. Xie J, Schaich KM. Re-evaluation of the 2,2-diphenyl-1-picrylhydrazyl free radical (DPPH) assay for antioxidant activity.
Fuentes de financiamiento
El estudio ha sido financiado por el Instituto de investigación, Centro de Investigación de Bioquímica y Nutrición de la Facultad de Medicina Humana de la Universidad de San Martín de Porres.
Conflictos de interés
Los autores declaran no tener conflictos de interés.
Correspondencia:
Emilio Guija-Poma
Dirección: Av. Alameda Del Corregidor 1531, Urb. Los Sirius, La Molina, Lima 12.
Teléfono: +(51 1) 3650483 - 3650485
Correo electrónico: eguijap@usmp.pe














