INTRODUCCIÓN
La actual pandemia por la enfermedad relacionada al coronavirus 2019 (COVID-19 por su sigla del inglés coronavirus disease 19) es la tercera epidemia adquirida por el hombre a partir de coronavirus animales en, aproximadamente, dos décadas. Las tres infecciones masivas han sido ocasionadas por los virus SARS-CoV (Severe acute respiratory síndrome- related coronavirus) en el 2003, MERS-CoV (Middle East respiratory síndrome-related coronavirus) en el 2012 y por el reciente SARS-CoV-21. Según la Organización Mundial de la Salud (OMS), este nuevo agente etiológico, al día de hoy, 24 de marzo del 2020, ha infectado a 372 755 personas y ha causado 16 231 fallecimientos, la mayoría de ellos en China (81 747 casos y 3283 muertes), Italia (63 927 casos con 6077 muertes), Estados Unidos (42 164 casos y 471 muertes), España (33 089 casos y 2182 muertes), Alemania (29 212 casos y 126 muertes) e Irán (23 049 casos con 1812 muertes) 2. Según la OMS, para la misma fecha, el Perú, con 395 casos y dos fallecidos, se coloca por detrás de Brasil (1546 casos con 14 muertes), Ecuador (790 y 15 muertes) y Chile (746 casos con 1 muerte) 2. Esta incidencia es incompatible con los valores reportados por el Ministerio de Salud del Perú que informa sobre 480 casos positivos con nueve muertes a nivel nacional. En este contexto, afortunadamente, no existe evidencia científica que indique una mayor sensibilidad al SARS-CoV-2 por parte de mujeres embarazadas y niños 3, 4. Sin embargo, recientemente, se mencionó la probable infección horizontal de un neonato en China 5 y otro en Londres.
El objetivo del presente artículo es otorgar perspectivas actuales sobre este virus, ya que la aparición de nueva información es constante y es necesario comprenderla y difundirla.
ORIGEN Y DISEMINACIÓN
Los coronavirus pertenecen a la familia Coronaviridae, subfamilia Coronavirinae. Son virus encapsulados con un diámetro entre 60-140 nm, tienen un ARN no segmentado, positivo y largo (27,9 kb y 30,1 kb). Se clasifican en 4 géneros que son Alfacoronavirus, Betacoronavirus, Deltacoronavirus y Gamacoronavirus; solo algunas especies pertenecientes a los dos primeros han sido descritos como agentes etiológicos de enfermedades respiratorias en humanos (adultos y niños).
La morfología observada del SARS-CoV-2 concuerda con la de los demás coronavirus 6. Está formado por peplómeros con espigas virales que están relacionadas con su tropismo. Adicionalmente, los coronavirus presentan las proteínas de la cápsula, membrana y nucleocápside que constituyen sus estructuras básicas, como se observa en la Figura 1. Recientes estudios muestran que el SARS-CoV-2 tiene lugares optimizados para su ligación a los receptores de la enzima convertidora de angiotensina 2 (ACE2) humana, así como espigas virales modificadas en el sector S, específicamente, entre las subunidades S1 y S2, que podría ser cribado por la enzima furina y aumentar así el potencial infectivo del virus 7-10 .
Este es el séptimo coronavirus capaz de infectar a los humanos. Estos virus afectan al tracto respiratorio superior e inferior de niños y adultos donde ocasionan cuadros clínicos que pueden ser leves (HKU1, NL63, OC43 y 229E) o muy severos (SARS-CoV, MERS-CoV y SARS-CoV-2) 11-14. Estos últimos tres tienen como hospederos naturales a los murciélagos (SARS-CoV y SARS-CoV-2) y camélidos (MERS-CoV) 12-14.
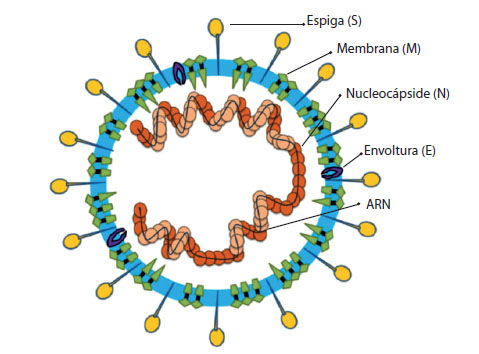
Figura 1 Partícula de coronavirus. El virión tiene un nucleocápside compuesta de ARN genómico y la proteína de la nucleocápside (N) fosforilada que está dentro de las bicapas de fosfolípidos y cubierta por un recortador de glucoproteína como una espiga (S). La proteína de membrana (M) y la proteína de envoltura (E) se encuentran entre las proteínas S en la envoltura del virus. Modificado de Li et al
Los primeros cuadros de síndrome respiratorio agudo grave (SARS, por su sigla en inglés) producidos por SARS-CoV-2 fueron reportados a mediados de diciembre. A fines de diciembre, China informó a la OMS sobre el brote de casos de neumonía severa en Wuhan, China. El 7 de enero, el SARS-CoV-2 es aislado por primera vez, e identificado como el responsable del cuadro descrito; además, el mercado pesquero de Wuhan fue reconocido como el lugar de la transmisión zoonótica. El primer óbito a consecuencia de esta nueva pandemia ocurrió el 20 de enero 16. A partir de esa fecha, debido a la celebración del Año Nuevo chino (25 de enero) y a la evasión de la cuarentena dictada a la ciudad de Wuhan (23 de enero), el virus se diseminó por varias provincias de China y otros países 17. Estudios realizados en la población infectada determinaron que el virus se propaga de persona a persona, principalmente 18, 19. En este contexto, en Alemania fue identificado el primer paciente asintomático con capacidad de contagiar aun durante el periodo de incubación 20. Esta última forma, según últimos reportes, explicaría la prevalencia y el potencial pandémico de la enfermedad, ya que plantea que el 86 % de los casos no se encuentran diagnosticados y el 79 % de los casos diagnosticados provienen de la interacción con personas no diagnosticadas 21. Zou et al.(22) describieron que personas sintomáticas poseen mayor carga viral, especialmente, en los hisopados nasales después de presentar los síntomas, y que la carga viral presente en personas asintomáticas es la misma. Resultados parecidos fueron descritos por Pan et al. que observaron mayores cargas virales en esputos.
Aunque en las muestras de excremento de pacientes infectados aparecen pequeñas cantidades del SARS-CoV-223-25, la principal forma de diseminación de este virus, al igual que otros coronavirus, es por el contacto con las gotitas de saliva o mucosidad provenientes de personas infectadas. Recientemente, se ha evaluado la posible viabilidad del virus en aerosoles por tres horas; en plásticos y acero inoxidable por setenta y dos horas; en cobre, por cuatro horas, y en cartón por veinticuatro horas 26.
EPIDEMIOLOGÍA Y PATOGÉNESIS
Estudios epidemiológicos realizados en Wuhan al inicio de la actual pandemia indicaron que el 56 % de los infectados son hombres y que las franjas etarias más afectadas son las siguientes: de 45 a 64 años (42 %), los mayores de 65 años (38 %), de 15 a 44 (20 %) y, en menor porcentaje, el grupo entre 0 y 14 años (0,9 %) 18, 27. Los estudios en Jinan y Rizhao indicaron que las mujeres infectadas representan el 52,2 % 28. Por otro lado, recientes informes realizados en personas infectadas en EE. UU. han mostrado que la letalidad de la enfermedad es mayor en personas de más de 85 años y que el 20 % de los casos que necesitan hospitalización corresponde a personas entre 20 a 44 años 29.
PERFIL CLÍNICO
El perfil clínico de la COVID-19 es variado, los casos leves y asintomáticos son los más frecuentes. En mayor grado se pueden encontrar infiltraciones pulmonares, y en los casos más severos se observa disnea a los cinco días. Los síntomas más frecuentes en el momento del internamiento son dolor de cabeza, faringalgia, neumonía, fiebre (88,7-91 %), tos seca (67,8 %), fatiga (51 %), náuseas y vómitos (5 %) y diarrea (3,8 %). Tales síntomas pueden incluir, posteriormente, linfocitopenia (83,2 %), trombocitopenia (36,2 %), leucopenia (33,7 %), aumento de la proteína C reactiva (PCR) y aceleraciones respiratorias repentinas originadas por la neumonía intersticial 18, 27. A nivel local, la autoridad sanitaria ha señalado como principales síntomas la tos seca, fiebre y dificultad respiratoria.
En los casos más severos, la disnea (30 %) puede causar daño alveolar, insuficiencia renal y finalmente, la muerte 14. El tiempo de incubación del virus es 5,2 días en promedio, y su pico epidémico ocurre a los 7,4 días 18. La recuperación se da después de 13 días, pero se puede prolongar hasta 17 en pacientes con síntomas respiratorios 30. Sin embargo, la letalidad de la enfermedad tiene una relación directa con la edad del infectado y con la presencia de comorbilidades como hipertensión (presente en el 17 %), diabetes (8 %), enfermedades cardiacas (5 %), especialmente las que se tratan con drogas promotoras de ACE2, y enfermedades respiratorias (2 %) 28, 31,32,33 o tuberculosis 34.
Estudios comparativos de los síntomas en niños y adultos describieron que los primeros usualmente presentan síntomas leves (fiebre y tos seca) y, a diferencia de los adultos, tienen un aumento en la concentración de LDH, disminución del número de neutrófilos, IL-6 y CPR, y rara vez presentan flema 35 .
Una investigación reciente ha vinculado la gravedad de COVID-19 con malestares digestivos como anorexia (83,8 %), diarrea (29,3 %), vómitos (0,8 %) y dolores abdominales (0,4 %); además se describió una relación directa entre el grado de estos malestares con el tiempo de infección por COVID-19 y el pronóstico clínico 36. Por otro lado, una reciente búsqueda ha determinado que no existe relación entre el hábito de fumar y la severidad de la enfermedad 37.
DIAGNÓSTICO
Los casos sospechosos son los que presentan fiebre persistente, dolor de garganta y tos, sobre todo en personas que han viajado a países con transmisión local persistente o que han estado en contacto con alguna persona con SARS-CoV-2 confirmado. Estos síntomas pueden estar acompañados por infiltrados bilaterales, opacidad "de vidrio esmerilado" y subsegmentos consolidados, aunque estos elementos pueden no ser visibles al inicio de la infección.
Estas pruebas son usualmente utilizadas para confirmar diagnósticos moleculares negativos en pacientes sospechosos con COVID-19 38, 39. En el Perú, estos exámenes diagnósticos son hechos exclusivamente por el Instituto Nacional de Salud (INS) .
Los ensayos moleculares son realizados cinco o seis días después de la aparición de los síntomas, por lo que pueden ayudar a determinar el tiempo de infección, ya que la evaluación a los pocos días muestra falsos negativos 23, 40. Estos ensayos evalúan hisopados nasales y nasofaríngeos, principalmente, mediante la reacción en cadena de la polimerasa a tiempo real (RT-PCR). Los resultados obtenidos en los hisopados nasofaríngeos son menos fluctuantes lo que, a su vez, permitirá reducir el tiempo de cuarentena 30.
Los análisis complementarios para confirmar la enfermedad de forma no específica son el conteo de linfocitos (<1000), plaquetas, proteína C reactiva, sedimentación eritrocítica y LDH. Estos datos inmunológicos, como fue descrito para SARS y MERS, son importantes para prever la severidad de los cuadros clínicos 41. Recientemente, se han desarrollado diversas pruebas rápidas basadas en la afinidad anticuerpo-antígeno que podrán agilizar la confirmación de personas infectadas con el SARS-CoV-2, aunque sean asintomáticas 42.
TRATAMIENTO
En la actualidad, no existe un tratamiento definitivo para las infecciones con SARS-CoV-2; sin embargo, el tratamiento de los casos sospechosos y confirmados necesita ser realizado en lugares aislados y seguros 39 .
En el Perú, de manera general, los casos con síntomas leves a moderados, que no ponen en riesgo la vida de la persona, son tratados en los domicilios de los pacientes con la recomendación de mantener un aislamiento del resto de familiares. A estos pacientes se les recomienda descanso e hidratación 39 .
En los casos graves, el tratamiento deberá proveer cantidades de oxígeno suficientes mediante catéteres nasales, máscaras de oxígeno, terapias nasales con alta fluidez de oxígeno, ventilación no invasiva o, en casos más graves, mecanismos de ventilación mecánica. El flujo de oxígeno deberá ser inicialmente de 5 L/min, el cual deberá aumentar hasta conseguir una saturación de oxígeno capilar periférica (SpO2) ≥ 90 % en adultos, ≥ 92-95 % en embarazadas, ≥ 94 % en niños con disnea obstructiva, apnea, síndromes de respiración aguda, cianosis central, choque, coma o convulsiones, y de ≥ 90 % en niños sanos. En los casos más severos, en pacientes que presentan hipercapnia, inestabilidad hemodinámica, falla multiorgánica, se deberá recurrir a la respiración mecánica asistida con volumen (4-8 mL/kg) y presión de succión (<20 cmH O) 39 .
Finalmente, no existen evidencias científicas que avalen medicamentos contra el SARS-CoV-2; sin embargo, recientes investigaciones que han utilizado la combinación de lopinavir y ritonavir al inicio de la infección han reducido la mortalidad, pero con gran cantidad de eventos adversos 43. Otros estudios que han empleado hidroxicloroquina 44, 45 y azitromicina han demostrado la remisión la enfermedad 46, 47. Estos trabajos se han incluido en la reciente revisión Clinical trials of drug repositioning for COVID-19 treatment48.
PREVENCIÓN
En este momento, en que no existen vacunas ni tratamientos disponibles contra el COVID-19, la prevención es la mejor herramienta que tiene la humanidad.
La prevención deberá estar enfocada, primeramente, en resguardar la salud de los profesionales sanitarios ya que, como se observó en las pandemias de SARS y MERS, ellos, además de ser indispensables para la recuperación de los pacientes sintomáticos o asintomáticos, se podrían convertir en vectores de la enfermedad.
El empleo de las mascarillas por parte de toda la población es aún discutible, sin embargo, su uso en compañía de buenas prácticas de higiene, como el lavado de manos cada 15-20 minutos y la higienización con alcohol y/o lejía, ha demostrado reducir la transmisión de los virus respiratorios 49 .
No obstante, el uso de las mascarillas sí es muy recomendable para quienes están en interacción constante con otras personas o enfermos, sobre todo los pacientes con síntomas respiratorios ya que, como se ha explicado, tienen una mayor carga viral en los esputos y las secreciones nasales y debe evitarse la diseminación de estos 30, con igual cuidado se debe manipular el material fecal de las personas infectadas. Las mascarillas N95 deberán ser utilizadas solo por profesionales de la salud. Finalmente, los pacientes sospechosos con diagnostico confirmado o que tuvieron la enfermedad y que aún poseen carga viral deberán mantenerse en aislamiento social hasta que se confirme que ya no son más agentes diseminadores.
PERSPECTIVAS
Frente a la actual pandemia, una de las principales preocupaciones de los gobiernos es evitar el aumento indiscriminado de personas infectadas por el SARS-CoV-2 en el corto plazo. Frente a esto, son diversas las respuestas gubernamentales que se basan en lo siguiente:
Identificar y acompañar a las personas potencialmente infectadas, las cuales serán determinadas por sus historiales de viaje y la interacción con otras personas infectadas.
Proveer el equipamiento adecuado a los profesionales de la salud para poder cumplir su función de una forma eficiente y segura.
Informar a la población sobre las características de esta nueva pandemia, para no caer en la desinformación o la histeria colectiva.
Aconsejar o implantar el aislamiento social.
Definir las fortalezas del sistema de salud para así determinar la capacidad de combate a la epidemia.
Asegurar la correcta distribución de alimentos, medicinas y servicios básicos a la población.
Las personas infectadas deberán ser aisladas y cada caso deberá ser tratado de forma única. Así mismo, el entorno social de dichas personas deberá ser aislado y evaluado.
Es importante el intercambio de información entre gobiernos para poder erradicar conjuntamente la epidemia.
CONCLUSIONES
La nueva pandemia traerá desafíos económicos, políticos, médicos y sociales a todos los países del mundo, pero no es la primera ni la última vez que la humanidad combatirá una pandemia. Sin embargo, la falta de vacunas y medicamentos hace evidente que, científicamente, aún existen muchos microorganismos olvidados y que la investigación en busca de nuevos fármacos debe ser constante















