Introducción
El síndrome de bajo gasto cardíaco (SBGC), una manifestación clínica de gasto cardíaco insuficiente y perfusión tisular periférica, fue propuesto por primera vez por Rao et al. 1. Estudios previos han demostrado que la mortalidad por todas las causas en el SBGC varía de 14,8 a 62,5 % a corto plazo (1 mes después del inicio) y de 21,4 a 36,6 % a largo plazo (2 meses a 1 año después del inicio) 2. El SBGC después de la cirugía cardíaca no solo conduce a la mal perfusión tisular, sino también a la disfunción orgánica múltiple del cerebro, los pulmones, el hígado, los riñones y el tracto gastrointestinal, lo que aumenta la utilización de los recursos de atención médica y los costos asociados 3. Más importante aún, el SBGC puede provocar la reducción reversible del gasto cardíaco (CO) después de la cirugía cardíaca. El reconocimiento temprano y el tratamiento adecuado del SBGC pueden evitar su progresión a shock cardiogénico refractario y mejorar los resultados clínicos, por lo que su detección temprana es de gran importancia 4.
Según estudios de Norteamérica (EE. UU. y Canadá), existió una reducción de la actividad quirúrgica de un 45 % global entre marzo y abril de 2020 frente a la realizada en el 2019. Existió un incremento de hasta el 7 % en cirugía coronaria, probablemente a expensas de la cirugía urgente, con descensos importantes en la cirugía valvular de hasta el 7,5 % 5.
En el año 2020 (6), en España, la cirugía de sustitución valvular y coronaria muestra una mortalidad del 13,61 %. La cirugía polivalvular y coronaria también presenta cifras similares (12,07 %), teniendo relación con las complicaciones intray posoperatorias, entre ellas el bajo gasto cardiaco.
Según Vera-Rivero et al. 7, Cuba es uno de los pocos países en vías de desarrollo capaz de realizar la colaboración en el campo de la cirugía cardiovascular, y con la creación de los cardiocentros en diferentes regiones del país se pone en marcha el desarrollo de la especialidad.
Datos estadísticos 8 muestran que en el periodo 2019-2020 hubo un total de 3004 pacientes que tuvieron tratamiento quirúrgico por alguna patología cardiovascular.
Bertini et al. 9 refieren que la morbimortalidad perioperatoria continúa siendo una de las principales limitaciones de la cirugía cardíaca con circulación extracorpórea, a pesar de verse reducida de forma progresiva en las últimas décadas.
Dada la situación antes descrita, se planteó realizar esta investigación con la finalidad de determinar los posibles elementos predictores clínicos y ecocardiográficos asociados a la aparición del síndrome de bajo gasto cardíaco y cómo pueden influir en su evolución.
Materiales y métodos
Diseño y población de estudio
Se realizó un estudio analítico de casos y controles en pacientes que presentaron síndrome de bajo gasto cardíaco en el periodo posoperatorio, luego de recibir intervención quirúrgica cardiovascular y circulación extracorpórea en el Servicio de Cardiología y Cirugía Cardiovascular del Hospital Provincial Docente Saturnino Lora de Santiago de Cuba, en el período comprendido entre enero 2019 y diciembre 2021.
A tal efecto, se conformaron los dos grupos de estudio, cuyos integrantes fueron seleccionados de la siguiente manera:
Shoonen et al. 10 definieron como caso a aquel paciente con oliguria (diuresis inferiores a 0,5 ml/kg/h), saturación venosa central <60 % (con saturación arterial normal) y/o lactato >3 mmol/l, sin hipovolemia relativa. Para conseguir una situación hemodinámica adecuada, se mantuvieron los inotropos en los pacientes que provinieron del quirófano.
Ambos grupos de estudio (casos y controles) formaron parte de la misma población de pacientes operados de cirugía cardiovascular (360 pacientes), solo diferenciados por el hecho de presentar o no SBGC postoperatorio al momento del ingreso. El grupo de casos quedó conformado por todos los pacientes con SBGC (56 pacientes) y el de control, por quienes no presentaron SBGC, seleccionados del número de casos mediante un muestreo aleatorio simple 1:1 (56 pacientes).
Se excluyeron del estudio aquellos controles en los que, durante la revisión de la historia clínica, se evidenció la falta de información suficiente para cumplir los objetivos de la investigación, tanto en los grupos como en los controles.
Variables y mediciones
Variable dependiente: síndrome de bajo gasto cardíaco (SBGC) posoperatorio.
Variables independientes: factores clínicos, hemodinámicos
y ecocardiográficos.
Para dar cumplimiento a los objetivos de la investigación se definieron y operacionalizaron las siguientes variables:
1. Edad: mayor de 65 años, menor de 65 años.
2. Sexo: masculino, femenino.
3. Comorbilidades de interés en la investigación: enfermedad pulmonar obstructiva crónica (EPOC), diabetes mellitus (DM), cardiopatía isquémica, fibrilación auricular (según constancia en la historia clínica de que el paciente tuviese este antecedente).
4. Variables ecocardiográficas.
Las ecocardiografías se realizaron con un equipo de ecocardiograma Philips iE33, 48 horas antes de la operación en los pacientes programados para cirugía electiva, y el día de la intervención en los que requirieron ser operados de urgencia.
II. Excursión sistólica del plano anular tricuspídeo (TAPSE): permite la evaluación de la función sistólica del ventrículo derecho; valores superiores a 17 mm son considerados normales.
FEVD ≥ 17 mm (función sistólica del ventrículo derecho conservada)
FEVD < 17 mm (función sistólica del ventrículo derecho deprimida)
III. Presión sistólica de arteria pulmonar (PSAP): al calcular el gradiente de presión sistólica entre la aurícula derecha y el ventrículo a partir de la velocidad pico del flujo regurgitante transtricuspídeo estima la PSAP sistólica. Valores inferiores a 30 mmHg son considerados normales.
PSAP Sí (cuando el valor fue mayor de 30 mmHg)
PSAP No (cuando el valor fue menor de 30 mmHg)
Análisis estadístico
La información sobre las variables de interés epidemiológicas, clínicas y ecocardiográficas se obtuvo de las historias clínicas y se introdujo en una planilla de recolección diseñada para ese fin, lo que garantizó su preservación en caso de daño irreversible del soporte digital, pues los datos fueron compilados en una hoja de cálculo de Microsoft Excel.
La hoja de cálculo de Microsoft Excel que contiene la información primaria, tanto de los casos como de los controles, fue importada con el paquete estadístico SPSS versión 22, con el cual se realizó todo el procesamiento estadístico. Para las variables cualitativas se calcularon como medidas de resumen el número y el porcentaje; para las cuantitativas se realizó el test de Kolmogorov-Smilrov para establecer la normalidad de la variable.
Se aplicó la prueba de ji al cuadrado. Todos los análisis estadísticos se hicieron a dos colas (bilateral) y se consideraron estadísticamente significativos los valores de p < 0,05. Para establecer la fuerza de la asociación se calculó la razón de disparidad (OR) con intervalo de confianza del 95 %, así como el riesgo atribuible porcentual poblacional (RAPP) y el riesgo atribuible porcentual en expuestos (RAPE).
Las tablas se analizaron y discutieron mediante los métodos científicos inductivo y deductivo. Los resultados se compararon con estudios similares, lo que permitió arribar a conclusiones y emitir recomendaciones.
Consideraciones éticas
Los autores declaran su compromiso de confidencialidad y protección de la información recogida durante la investigación. También se solicitó la autorización a la dirección del centro y la aprobación del Comité de Ética de la Investigación y del Consejo Científico para su ejecución.
Resultados
En la Tabla 1 se observa predominio de pacientes menores de 65 años (51,81 %) y una mayor cantidad de pacientes en el grupo de casos (60,71 %), mostrando un valor de p = 0,008, lo que corresponde a una alta asociación significativa. Por otra parte, se mostró la presencia de fibrilación auricular en 96 (85,68 %) pacientes, teniendo un número menor en ambos grupos de estudio, aunque se evidenció una altísima asociación estadística (p = 0,007); en cuanto a parámetros ecocardiográficos, se observó amplio predominio de pacientes con FEVI > 50 % (91,10 % [p = 0,047]), teniendo un número mayor en ambos grupos de pacientes. Respecto a la función sistólica del ventrículo derecho, se evidenció un número mayor de pacientes con FEVD > 17 mm (88,40 % [p = 0,008]), mostrándose en ambas variables significación estadística; otras variables como sexo, diabetes mellitus, EPOC, cardiopatía isquémica y PSAP no mostraron significación estadística (Tabla 1).
Tabla 1 Análisis multivariado según grupo de estudio
| Variables clínicas y ecocardiográficas | Grupo de estudio | |||||||
|---|---|---|---|---|---|---|---|---|
| Casos | Control | Total | ||||||
| No | % | No | % | No | % | p | ||
| Edad | <65 años | 22 | 39,29 | 36 | 64,24 | 58 | 51,81 | 0,008 |
| >65 años | 34 | 60,71 | 20 | 35,76 | 54 | 48,19 | ||
| Sexo | Mujer | 31 | 55,45 | 25 | 44,53 | 56 | 50,15 | 0,257 |
| Hombre | 25 | 44,55 | 31 | 55,47 | 56 | 49,85 | ||
| Diabetes mellitus | No | 44 | 78,61 | 39 | 69,62 | 83 | 74,10 | 0,281 |
| Sí | 12 | 21,39 | 17 | 30,38 | 29 | 25,90 | ||
| EPOC | No | 40 | 71,28 | 45 | 80,23 | 85 | 75,88 | 0,269 |
| Sí | 16 | 28,72 | 11 | 19,77 | 27 | 24,12 | ||
| Fibrilación auricular | No | 43 | 76,83 | 53 | 94,62 | 96 | 85,68 | 0,007 |
| Sí | 13 | 23,17 | 3 | 5,38 | 16 | 14,31 | ||
| Cardiopatía isquémica | No | 40 | 71,42 | 41 | 73,15 | 81 | 72,27 | 0,833 |
| Sí | 16 | 28,58 | 15 | 26,75 | 31 | 27,72 | ||
| FEVI | <50 % | 8 | 14,32 | 2 | 3,65 | 10 | 8,90 | 0,047 |
| >50 % | 48 | 85,68 | 54 | 96,35 | 102 | 91,10 | ||
| FEVD | <17 mm | 11 | 19,60 | 2 | 3,55 | 13 | 11,60 | 0,008 |
| >17 mm | 45 | 80,40 | 54 | 96,45 | 99 | 88,40 | ||
| PSAP | No | 39 | 69,61 | 42 | 75,25 | 81 | 72,30 | 0,526 |
| Sí | 17 | 30,39 | 14 | 25,75 | 31 | 27,70 |
Fuente: historias clínicas; chi cuadrado: p ≤ 0,05; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: función sistólica del ventrículo izquierdo; FEVD: función sistólica del ventrículo derecho; PSAP: presión sistólica de arteria pulmonar.
La intervención de emergencia es uno de los parámetros que se evalúa en la presente investigación; en la Tabla 3 se muestra amplio dominio de pacientes (45,24 % [p ≤ 0,05; OR: 2,14]) con cirugías de emergencia, mostrando tener significación estadística; aunque se mostró como un factor de riesgo presentar bajo gasto cardiaco en pacientes con cirugía de emergencia.
Las medidas de impacto, tales como RAPE y RAPP, indican que 33 % de los casos, es decir, pacientes con bajo gasto cardiaco, se debe a cirugía no electiva. De conseguirse la implementación de cirugías electivas adecuadas, estas secuelas se reducirían en un 51,7 % (Tabla 2).
Tabla 2 Relación de pacientes según cirugía de emergencia y grupo de estudio
| Cirugía de emergencia | Grupo de estudio | |||||||
|---|---|---|---|---|---|---|---|---|
| Casos | Control | Total | p | OR | ||||
| No | % | No | % | No | % | |||
| Sí | 34 | 60,71 % | 42 | 37,50 % | 76 | 45,24 % | 0,004 | 2,14 |
| No | 22 | 39,29 % | 70 | 62,50 % | 92 | 54,76 % | ||
| RAPE = 33 %; RAPP = 51,7 % |
Fuente: historias clínicas; chi cuadrado: p ≤ 0,05; OR: odds ratio.
RAPE: riesgo atribuible porcentual en expuestos; RAPP: riesgo atribuible porcentual poblacional.
En cuanto a parámetros como el tiempo de circulación extracorpórea, se mostró datos de 50 pacientes (29,76 % [p = 0,000; OR: 1,54; LI: 0,73; LS: 3,24]), los cuales demuestran que este se comporta como factor predisponente en pacientes cuyo tiempo exceda los 90 minutos; en cuanto al sangramiento periprocedimiento, se mostró una minoría de pacientes (12,50 % [p = 0,013; OR: 3,12; LI: 1,22; LS: 7,93]), con una altísima significación estadística y se comportó como un factor de riesgo el sangramiento mayor de 500 ml para la aparición del síndrome de bajo gasto cardiaco (Tabla 3).
Tabla 3 Análisis multivariado según grupo de estudio
| Variables | Grupo de estudio | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Periprocedimiento | Caso | Control | Total | ||||||||
| No | % | No | % | No | % | p | OR | LI | LS | ||
| Tiempo de CEC | ≥90 minutos | 31 | 55,36 | 19 | 16,96 | 50 | 29,76 | 0,000 | 1,54 | 0,73 | 3,24 |
| <90 minutos | 25 | 44,64 | 93 | 83,04 | 118 | 70,24 | |||||
| Sangramiento perioperatorio | ≥500 ml | 12 | 21,43 | 9 | 8,04 | 21 | 12,50 | 0,013 | 3,12 | 1,22 | 7,93 |
| <500 ml | 44 | 78,57 | 103 | 91,96 | 147 | 87,50 |
Fuente: historias clínicas; tiempo de CEC: tiempo de circulación extracorpórea; chi cuadrado: p ≤ 0,05; OR: odds ratio; LI: límite inferior; LS: límite superior.
Se realizó una regresión logística para determinar cómo las variables clínicas y ecocardiográficas en estudio afectan la probabilidad de presentar SBGC. Se utilizó un total de 112 casos en el análisis. El modelo explicó el 78,9 % de la aparición de SBGC en pacientes operados. Se mostraron valores de p ≤ 0,05 en variables tales como edad, FEVD, CEC, PSAP, lo cual nos permite concluir que tienen una asociación estadísticamente significativa con las complicaciones. No tuvieron significación estadística variables tales como FEVI y sangramiento perioperatorio (p > 0,05) (Tabla 4).
Tabla 4 Regresión logística según variables de estudio
| Variables | B | Wald | Sig. | Exp(B) | 95% C.I. para EXP(B) | |
|---|---|---|---|---|---|---|
| Inferior | Superior | |||||
| Edad | -2,039 | 23,317 | 0,000 | 0,130 | 0,057 | 0,298 |
| Sangramiento perioperatorio | -1,028 | 3,246 | 0,072 | 0,358 | 0,117 | 1,095 |
| Tiempo de CEC | 1,639 | 12,574 | 0,000 | 5,150 | 2,082 | 12,744 |
| FEVI | -0,826 | 2,021 | 0,155 | 0,438 | 0,140 | 1,368 |
| FEVD | 1,894 | 10,566 | 0,001 | 6,644 | 2,121 | 20,812 |
| PSAP | -1,089 | 4,137 | 0,042 | 0,337 | 0,118 | 0,961 |
| Constante | 0,952 | 0,246 | 0,620 | 2,592 |
Fuente: historias clínicas; chi cuadrado: p ≤ 0,05; FEVI: función sistólica del ventrículo izquierdo; FEVD: función sistólica del ventrículo derecho; PSAP: presión sistólica de arteria pulmonar.
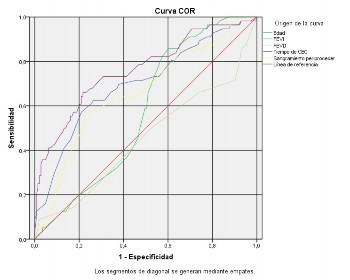
Al analizar el área bajo la curva (Tabla 5) y la curva operativa del receptor (Figura 1), a partir de la sensibilidad y especificidad, se comprobó que el área bajo la curva (AUC) tuvo un rango de 0,452-0,762; de ahí la capacidad de las variables para predecir el riesgo de SBGC, donde sobresalieron edad, FEVI, tiempo de circulación extracorpórea y sangramiento.
Tabla 5 Análisis del área bajo la curva
| Área bajo la curva | 95 % de intervalo de confianza | |||
|---|---|---|---|---|
| Variable(s) | Área | Significación asintótica | Límite inferior | Límite superior |
| Edad | 0,699 | 0,000 | 0,614 | 0,784 |
| FEVI | 0,574 | 0,106 | 0,493 | 0,654 |
| FEVD | 0,452 | 0,293 | 0,358 | 0,546 |
| Tiempo de CEC | 0,762 | 0,000 | 0,683 | 0,840 |
| Sangramiento perioperatorio | 0,660 | 0,000 | 0,574 | 0,746 |
Fuente: historias clínicas; chi cuadrado: p ≤ 0,05; FEVI: función sistólica del ventrículo izquierdo; FEVD: función sistólica del ventrículo derecho; tiempo de CEC: tiempo de circulación extracorpórea.
Discusión
El SBGC es una complicación frecuente y grave en los pacientes sometidos a cirugía cardíaca. Sin embargo, tanto la incidencia como la respuesta al tratamiento y su posterior evolución son ampliamente variables en las diferentes publicaciones hasta el momento.
La edad es un factor de riesgo cardiovascular independiente, por lo tanto, la probabilidad de muerte se incrementa, lo cual se ha validado en diferentes escalas de riesgo. Si bien el riesgo de muerte aumenta exponencialmente, hay estudios que muestran una triplicación de la probabilidad de morir cuando se sobrepasa los 75 años 11.
Lorenzo 12, en un artículo de revisión, refiere que la edad superior a 65 años es uno de los elementos predisponentes de complicaciones y bajo gasto cardiaco en pacientes con cirugía cardiaca.
Pérez Vela et al., en un estudio multicéntrico publicado en 2018, señalaron la edad de 68,3 ± 9,3 años como uno de los factores que más se asociaron con la aparición de bajo gasto postoperatorio, asimismo, el 65,2 % pertenecía al sexo masculino 13. Un estudio realizado por Fernández Mesa et al. 14, que incluyó 156 enfermos que fueron intervenidos quirúrgicamente por enfermedades valvulares cardíacas izquierdas en el año 2018, reportó que 46 de ellos presentaron bajo gasto cardiaco, predominando en este grupo los pacientes mayores de 65 años.
Lo anteriormente planteado por los diferentes autores citados coincide con lo mostrado en el presente estudio.
Zhao et al. 15, en un estudio realizado en el Hospital Popular Provincial de Guangdong, mostraron como resultados el predominio del sexo masculino (69,8 %) en relación con el femenino (30,2 %). El sexo masculino no tuvo mayoría en lo observado en la investigación, lo cual discrepa con lo observado en la literatura y lo mostrado en la presente investigación.
La presencia de comorbilidades, como diabetes mellitus, hipertensión arterial y EPOC, etc., también se asocia a complicaciones, entre ellas, el bajo gasto cardíaco. Según Cubides Núñez, en su estudio, la comorbilidad más frecuente fue la hipertensión arterial, seguida por la EPOC 16.
En el estudio ya citado de Fernández Mesa et al. 14, la EPOC y la fibrilación auricular crónica fueron las comorbilidades más frecuentes en el grupo de pacientes que presentó bajo gasto cardíaco.
Pérez Vela et al. 13 reportan en su estudio que la hipertensión arterial y la dislipidemia estuvieron presentes en los pacientes que desarrollaron SBGC de su serie, con un 70,8 % y 63,5 %, respectivamente.
En una investigación sobre fibrilación auricular en el paciente quirúrgico, realizada por Gómez Núñez et al. 17, se observó que una de las complicaciones más frecuentes fue el bajo gasto cardiaco en un 23 % de pacientes.
Al comparar estas evidencias con la actual investigación, existen puntos de similitud encontrados por la descripción de la fibrilación auricular de los autores antes citados; en la presente investigación, la fibrilación tuvo alta significación estadística, la cual coincide con lo planteado.
La disfunción sistólica preoperatoria del ventrículo izquierdo ha sido considerada un factor determinante para el desarrollo postoperatorio de SBGC, lo cual se muestra en publicaciones realizadas. Sepúlveda et al. 18 reportaron trastornos segmentarios de la contractilidad en 273 pacientes (58,6 %), de los cuales 208 (59,4 %) requirieron soporte inotrópico en el intraoperatorio; además, que de 42 pacientes que tenían fracción de eyección reducida o inferior al 40 %, 35 (83,3 %) presentaron bajo gasto cardíaco. Esto coincide con otro estudio realizado por Li et al. 19, donde muestran como predictor a la fracción de eyección menor de 40 %. Burstein et al. 20 mostraron valores de fracción de eyección aproximadamente a 47,3 %, con derivación estándar ±16,2 %. En nuestro estudio se observó la aparición de bajo gasto cardíaco en pacientes con fracción de eyección >50 %, lo cual muestra lo diverso de dicha entidad.
La evaluación de la función del VD es un aspecto clave en pacientes sometidos a cirugía cardíaca, no solo antes de la intervención, sino también en el período del postoperatorio precoz, lo que se demuestra en estudios como los de Fernández et al. 14, que expresaron que los pacientes que presentaron BGC tenían menor FEVD, así como mayor presión media en la arteria pulmonar y la aurícula derecha y mayor presión sistólica en la arteria pulmonar, todas con diferencias significativas (p < 0,0001). Esto concuerda con lo expresado en la presente investigación.
Fernández Mesa et al. 14, en su análisis multivariable, encontraron que los principales predictores de la aparición del bajo gasto cardíaco fueron el tiempo prolongado de circulación extracorpórea (OR 4,89; p = 0,001) y la edad superior a 65 años, sexo y FEVI ≤ 40 %, lo cual concuerda con la presente investigación.
En otro punto, Gonzalez Kadashinskaia et al. 21 refieren que la circulación extracorpórea fue uno de los procederes más empleados en intervenciones quirúrgicas, con casi un 55 %, lo cual indica el amplio uso de esta técnica. Así mismo, Fernández Mesa et al. 14 señalaron en su estudio que el tiempo prolongado de circulación extracorpórea se asocia a una mayor probabilidad de sufrir esta complicación, lo cual guarda similitud con lo referido en el presente estudio.
En otra publicación de Fernandez Mesa et al. 22, se concluyó que los pacientes con bajo gasto cardíaco tuvieron 3,5 veces más probabilidades de fallecer en el periodo de 5 años a la operación que los que no padecieron esta entidad.
Lorenzo 12, en su artículo de revisión, refiere que un estudio unicéntrico, publicado por Ding W, et al., incluyó 1524 pacientes sometidos a cirugía cardíaca, de los cuales 205 desarrollaron síndrome de bajo gasto cardíaco. Entonces, se concluyó por análisis multivariado que la edad >65 años, la fracción de eyección del ventrículo izquierdo (FEVI) <50 % y la cirugía con circulación extracorpórea fueron factores independientes de bajo gasto cardíaco. Al respecto, Jiménez Hernández et al. 23 plantean similares conclusiones.
Aslan et al. 24 plantean que el tiempo de pinzamiento aórtico y el tiempo total de derivación cardiopulmonar marcadamente prolongado son predictores de la aparición de bajo gasto cardíaco.
Maganti et al. (25 alegan en un estudio que el 7 % de casos presentó bajo gasto cardíaco postoperatorio, asociándose a cirugía de urgencia y fracción de eyección baja.
Kochar et al. 26 señalan, en una investigación de análisis multivariado y multicéntrico, que los factores que más se asociaron con mayor riesgo de bajo gasto cardíaco fueron la fracción de eyección preoperatoria y la edad, razón por la cual estos pacientes tuvieron peores resultados. En el mismo punto, Lui et al. 27 evidenciaron un modelo predictivo basado en variables como la edad y factores preoperatorios como la FEVI baja y tiempo de circulación aórtico.
Elhenawy et al. 28 asociaron la cirugía valvular mitral con una mayor prevalencia de síndrome postoperatorio de bajo gasto cardíaco al intervenir factores tales como la edad, la urgencia de la operación y la función preoperatoria del ventrículo izquierdo; por su parte, Seguel et al. 29 reportaron una baja incidencia del bajo gasto cardiaco.
En otro punto, De Lima et al. 30 plantean en su investigación que las entidades que exacerban las complicaciones en el posoperatorio inmediato de la cirugía cardiaca son el sangramiento perioperatorio y la fibrilación auricular, la primera con una incidencia de hasta un 50 %.
La limitación principal de esta investigación radica esencialmente en no contar con una muestra suficiente para poder establecer el comportamiento de las complicaciones posquirúrgicas. Cabe resaltar que se trata de datos provenientes de un centro especializado en medicina cardiovascular, lo que permite, en todo caso, reflejar sus fortalezas y sus evidentes limitaciones.
En conclusión, los elementos clínicos y ecocardiográficos como la edad, la presencia de fibrilación auricular, la función sistólica del ventrículo izquierdo y la presión sistólica de la arteria pulmonar se asociaron de manera independiente a la aparición de bajo gasto.











 texto en
texto en