Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Revista Peruana de Biología
versión On-line ISSN 1727-9933
Rev. peru biol. v.18 n.3 Lima dic. 2011
TRABAJOS ORIGINALES
Estudio de la actividad fermentativa de Hansenula anomala y producción de compuestos químicos de importancia sensorial
Study of the fermentative activity of Hansenula anomala and production of chemical compounds of sensory importance
Waldir Estela Escalante1,4 ; Mojmír Rychtera1 ; Karel Melzoch1 ; Elena Quillama Polo2 y Beatriz Hatta Sakoda3
1 Department of Fermentation Chemistry and Bioengineering, Faculty of Food and Biochemical Engineering. Institute of Chemical Technology Prague. Technická 5, 166 28. Praha 6, Dejvice. Czech Republic. Email: Waldir.Desiderio.Estela.Escalante@vscht.cz
2 Laboratorio de Microbiología Industrial, Facultad de Ciencias Biologicas, Universidad Nacional Mayor de San Marcos. Apartado postal 110058, Lima 11, Perú. Email: equillamap@unmsm.edu.pe
3 Facultad de Ingeniería de Industrias Alimentarias, Universidad Nacional Agraria La Molina. Av. La Molina s/n, La Molina, Lima, Perú. Email: bhs@lamolina.edu.pe
4 Laboratorio de Biotecnología Agroindustrial, Escuela de Ingeniería Agroindustrial, Universidad Nacional Micaela Bastidas de Apurímac. Av. Arenas 121, Abancay-Apurimac, Perú.
Resumen
Se ha estudiado la actividad fermentativa de Hansenula anomala RIVE 7-1-5 con el objetivo de evaluar la producción de compuestos químicos de importancia sensorial. Los resultados mostraron que fermenta bien monosacáridos y también sucrosa y maltosa. Su actividad fermentativa es inhibida a concentraciones de 100,0mg/L de metabisulfito de sodio en el medio. Además, es capaz de producir 5,81±0,1 % v/v de etanol. La agitación del medio de cultivo incrementa la producción de alcoholes superiores (679,2 mg/L) y etil acetato (206,0±8,0 mg/L), por el contrario disminuye la producción de ácido acético (196,0±7,0 mg/L). La producción de glicerol fue similiar tanto en cultivo estático (sin agitación) como agitado. Durante el cultivo batch en biorreactor a condiciones aireadas la tasa de crecimiento (µ) alcanzó el valor de 0,13 h-1 y se observó la producción de ácido acético hasta 4,2±0,3 g/L. La concentración de oxígeno en el medio afecta su metabolismo, así cantidades insuficientes de oxígeno provocaría un metabolismo respirofermentativo con la producción de etanol, alcoholes superiores, ésteres y ácido acético. El control de la aireación al medio de fermentación es una herramienta útil para controlar el balance entre la actividad respiratoria y fermentativa y así la síntesis de compuestos de importancia sensorial en la producción de bebidas fermentadas no tradicionales.
Palabras clave: Hansenula anomala, fermentación alcohólica, alcoholes superiores, etil acetato, cultivo por lote.
Abstract
The fermentative behaviour of Hansenula anomala RIVE 7-1-5 was studied in order to evaluate the production of chemical compounds of sensory importance. The results demonstrated that the strain ferments very well monosaccharides and also sucrose and maltose. Its fermentative activity was inhibited at concentrations of 100 mg/L of sodium metabisulphite in the medium. Furthermore, it was able to produce 5,81±0,1% (v/v) of ethanol. Agitation of the culture medium increases the production of higher alcohols (679,2 mg/L) and ethyl acetate (206,0±8,0 mg/L), but on the contrary affects the production of acetic acid (196,0±7,0mg/L). Glycerol production was similar in static (without agitation) and shaken cultivation. During batch cultivation carried out in biorreactor under aerated conditions the growth rate (µ) reached value of 0,13 h-1 and, it was also observed production of acetic acid at levels of 4,2±0,3 g/L. The oxygen concentration in the medium affects its metabolism, thus insufficient amounts of oxygen would provoke a respirofermentative metabolism with production of ethanol, higher alcohols, esters and acetic acid. The control of aeration during fermentation is a useful tool to control the balance between the respiratory and fermentative activity and thus; synthesis of compounds of sensory importance in the production of non-traditional fermented beverages.
Keywords: Hansenula anomala, alcoholic fermentation, higher alcohols, ethyl acetate, batch cultivation.
Introducción
Hansenula anomala ó Pichia es una levadura no-Saccharomyces que frecuentemente es referida como contaminante en la producción de bebidas fermentadas ya que produce compuestos químicos en cantidades que afectan la calidad organoléptica (Thomas 1993). Sin embargo, en ciertas bebidas no tradicionales su presencia es beneficioso ya que los metabolitos que produce contribuye al aroma y sabor del producto final (Fleet 1992). Por ejemplo, Hansenula anomala forma parte de la microflora en la fermentación espontánea de un tipo de "vino de arroz" consumido en Vietnam (Dung et al. 2006). Además es también responsable del aroma y sabor característico del "takju", bebida alcohólica consumida en Corea del sur, hecha a base de arroz (Shin & Cho 1970).
Hansenula anomala es una levadura osmotolerante, ha sido aislada de productos con baja actividad de agua como por ejemplo en mermeladas de fruta (Tokuoka et al. 1992) y además de lugares con bajo contenido de oxígeno (Naito 1984). H. anomala frecuentemente forma parte aúnque no es predominante de la microflora de uvas y mostos y, participa en la etapa temprana de la fermentación alcohólica espontánea hasta que el oxígeno se agote y el etanol alcance niveles de 5-6% (a los 3 - 4 días) y consecuentemente mueren (Fleet & Heard 1993; Torija et al. 2001). Subsecuentemente, las cepas resistentes al etanol como Saccharomyces cerevisiae predominan y completan la fermentación (Ribereau-Gayon 1985).
Metabolismo de azúcares en Hansenula anomala.- Los azúcares fermentables son la fuente de energía más importante en el metabolismo de levaduras. Hansenula anomala al igual que las demás levaduras utiliza vías metabólicas comúnes para la degradación de azúcares, llámese glucólisis, ciclo de krebs y vía de la pentosa fosfato. Estos para ser utilizados deben ser transportados hacia el interior de la célula mediante mecanismos de transporte específicos (Kruckeberg 1996, Flores et al. 2000). La velocidad de utilización de azúcares esta influenciada por la concentración y el tipo de azúcar, la concentración de oxígeno disuelto en el medio así como de la temperatura, el pH entre otros factores (van Dijken et al. 1993, Bisson 1993, Goffrini et al. 2002). Hansenula anomala puede crecer a valores bajos de pH, baja actividad de agua, y alta presión osmótica (Fredlund et al. 2002). Además, no requiere adición externa de vitaminas para su crecimiento. Es una levadura Crabtree negativa, oxidativa, debido a que altas concentraciones de glucosa no reprime su respiración a condiciones aerobias (De Deken 1966a,b). Durante su crecimiento totalmente aerobio produce cantidades pequeñas de etanol y glicerol, es decir tiene preferencialmente un metabolismo respiratorio (De Deken 1966b, Fredlund et al. 2004a). A condiciones anaerobias su crecimiento se inhibe (Fredlund et al. 2004b).
A condiciones aerobias la glucosa-6-fosfato se metaboliza mayormente (50%) vía glucólisis y otra parte (30%) vía pentosa fosfato. Así mismo, a estas condiciones la mayor parte del piruvato entra a la mitocondria para su oxidación en el ciclo de Krebs, el cual funciona como un ciclo completo (Fredlund et al. 2004a). La limitación de oxígeno activa las enzimas de la vía fermentativa, como resultado se producen considerables cantidades de etanol y glicerol y, la tasa específica de toma de glucosa incrementa sustancialmente comparado con la tasa de toma de glucosa a condiciones aerobias. A estas condiciones, la oxidación de la glucosa-6-fosfato por la vía pentosa fosfato se reduce a solo 10% y el ciclo de Krebs funciona como una vía ramificada (Fredlund et al. 2004a). El flujo metabólico de Hansenula anomala en estas condiciones es similar al metabolismo fermentativo de Saccharomycescerevisiae (Gombert et al. 2001, Fiaux et al. 2003). Condiciones de limitación de oxígeno causa una mayor producción de etanol y también la acumulación de glicerol dentro de la célula y en el medio externo comparado a condiciones aerobias (Fredlund et al. 2004a y b). La producción de glicerol a condiciones de limitación de oxígeno esta relacionado a la necesidad de reoxidar los equivalentes redox producidos durante la síntesis de aminoácidos (Gancedo & Serrano 1989). Ácido acético también es producido durante su crecimiento respiratorio y respirofermentativo, pero no a condiciones severas de limitación de oxígeno (Fredlund et al. 2004a yb).
En levaduras Crabtree negativas cultivadas a condiciones aerobias, el piruvato se metaboliza preferentemente vía piruvato deshidrogenasa hasta acetil-CoA y luego éste entra al ciclo de Krebs para su oxidación completa (van Dijken et al. 1993, Gancedo & Serrano 1989); esto se debe a que presentan bajos niveles de piruvato descarboxilasa y una alta actividad de enzimas respiratorias como la piruvato deshidrogenasa, acetaldehído deshidrogenasa y acetil-CoA sintetasa (Postma et al. 1989). La ausencia de oxígeno en el medio es crucial y conduce a la cesación del crecimiento (Bulder 1964, van Dijken et al. 1993). La producción de acetato, glicerol y etanol se debería a una baja actividad de las enzimas respiratorias especialmente la piruvato deshidrogenasa, acetaldehído deshidrogenasa y la acetil-CoA sintetasa como resultado de la limitación de oxígeno en el medio (van Dijken et al. 1993), lo que a la vez conduce a una disminución de la tasa de respiración y a la estimulación del metabolismo fermentativo.
La producción de glicerol en medios con alta concentración de azúcar también estaría conectado al mecanismo de adaptación que utiliza la levadura frente al estrés osmótico y así prevenir su deshidratación (Andre et al. 1988). Sin embargo, también ha sido sugerido que la producción de glicerol no siempre es un factor relacionado a la osmorregulación (Tokuoka et al. 1992). Así mismo, la formación de glicerol esta acoplado a la oxidación de NADH a NAD+, lo que causa un desbalance redox en el citosol (NADH:NAD+) el cual es corregido con la producción de ácido acético cuya síntesis reconvierte nuevamente NAD+ a NADH (Blomberg & Alder 1992; Remize et al. 1999). Finalmente, la producción de glicerol también esta ligado a la necesidad de reoxidar el NADH generado durante la glucólisis (Prior y Hohmann 1997).
En la Figura 1 se presenta en forma general el metabolismo respiratorio y respirofermentativo de Hansenula anomala en la degradación de glucosa.
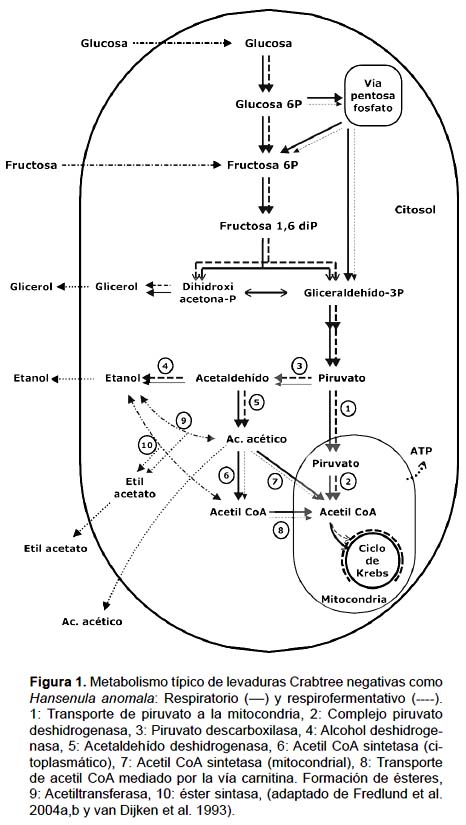
Las levaduras no-Saccharomyces no son muy tolerantes a bajas concentraciones de oxígeno, especialmente comparado con S. cerevisiae (Hansen et al. 2001). A condiciones de limitación de oxígeno se estimularía la fermentación (van Dijken 1993), así entonces el piruvato es convertido a acetaldehído por la piruvato descarboxilasa, y luego es reducido bien a etanol por la alcohol deshidrogenasa (Bisson 1993), u oxidado a ácido acético por la acetaldehído deshidrogenasa NADP-dependiente (Jacobson & Bernofsky 1974). El acetaldehído funciona como receptor terminal de electrones cuya reducción por el NADH genera etanol (Bisson 1993, Boulton et al. 1996). En levaduras Crabtree negativas en presencia de oxígeno, el acetaldehído es preferentemente oxidado a acetato por la aldehído deshidrogenasa y luego convertido en acetil CoA por la acetil-CoA sintetasa (van Urk et al. 1990, Remize et al. 2000). Sin embargo, la acumulación de ácido acético bajo condiciones de limitación de oxígeno resultaría de la insuficiente actividad de la acetil-CoA sintetasa requerida para la oxidación completa del acetato (van Urk et al. 1990).
Efecto del etanol y sulfito en Hansenula anomala.- Hansenula anomala no es una levadura tolerante a altas concentraciones de etanol y ácido acético (Kalathenos et al. 1995, Fredlund et al. 2002). El etanol inhibe la viabilidad de las células, la tasa de crecimiento específico, y la tasa específica de fermentación (Sa-Correia & Van Uden 1983, Pina et al. 2004, Ricci et al. 2004). Se considera que el etanol provoca la disminución del contenido de esteroles en la membrana celular y esto afecta el transporte de azúcares. Así mismo, se cree que el etanol tendría un efecto inhibidor sobre la actividad del sistema hexoquinasa, enzimas responsables de transferir grupos fosfato de una molécula a otra en la glucólisis (Nagodawithana et al. 1977, D'Amore et al. 1990, Ricci et al. 2004).
En general, la tolerancia al etanol depende de la habilidad de la célula de levadura para exportar el etanol producido hacia el exterior, un proceso que depende de la composición y fluidez de la membrana citoplasmática (Nagodawithana & Steinkraus 1976). El dioxido de azufre se ha utilizado desde hace mucho tiempo como agente antimicorbiano durante la elaboración de vinos y otras bebidas fermentadas. Este compuesto inhibe el crecimiento de bacterias y ciertas levaduras, entre ellas las no-Saccharomyces (Beech 1979). La capacidad inhibitoria del SO2 esta influenciada por el pH del medio. El pH determina el equilibrio entre tres compuestos, el SO2, HSO-3, y SO=3. El SO2 es el responsable del efecto tóxico y su concentración en medio acuoso es favorecido a valores bajos de pH ya que provoca el desbalance del equilibrio hacia este compuesto (Jarvis & Lea 2000).
Los sulfitos tienen actividad a nivel del metabolismo energético, afectan la glucólisis, así bajas concentraciones conducen a una rápida reducción del contenido de ATP en la célula a bajos valores de pH. Las enzimas más afectadas serían la gliceraldehído-3-fosfato deshidrogenasa y la alcohol deshidrogenasa (Maier et al. 1985). Así mismo, el sulfito sería responsable de la inhibición de la alcohol deshidrogenasa, enzima responsable de la reducción de acetaldehído a etanol durante la fermentación (Maier et al. 1985).
Producción de compuestos sensoriales por Hansenula anomala.- Hansenula anomala durante su crecimiento aerobio produce una variedad de compuestos volátiles. Esta especie es conocida por producir altas concentraciones de etil acetato y ácido acético (Romano et al. 1992, Grbin 1999, Plata et al. 2003). Los ésteres representan el mayor grupo de componentes aromáticos en bebidas alcohólicas fermentadas (Suomalainen 1981), y son producidos mediante reacción enzimática dentro de la célula. La principal enzima que cataliza la reacción es una acetiltransferasa (Malcorps et al. 1991, Yoshioka & Hashimoto 1984, Mason & Dufour 2000). En S.cerevisiae la síntesis de ésteres de acetato ha sido atribuído a la actividad de al menos tres acetiltransferasas: alcohol acetiltransferasa (AATasa), etanol acetiltransferasa e isomail alcohol acetiltransferasa (Lilly et al. 2000). La alcohol acetiltransferasa cataliza la reacción: acetil CoA + alcohol '! CoA + acetil éster. Actúa sobre un rango de alcoholes alifáticos de cadena corta incluyendo metanol y etanol. La AATasa reacciona con la acetil-CoA y dependiendo del grado de afinidad con una variedad de alcoholes (Fujii et al. 1994). Por ejemplo, etil acetato es principalmente producido a partir de acetil CoA y etanol (Yoshioka & Hashimoto 1981). La AATasa de S. cerevisiae es fuertemente reprimida bajo condiciones aerobias y por la adición de ácidos grasos insaturados en el medio (Malcorps et al. 1991, Fujii et al. 1997). Por otra parte, se ha reportado que la actividad de la éster sintasa (esterasa reversa) en la síntesis de ésteres en S. cerevisiae es limitada. Etil caprilato y etil acetato serían producidos a partir de etanol y los respectivos ácidos grasos (Hilary & Peddie 1990, Plata et al. 1998, Rojas et al. 2002).
La vía de síntesis de ésteres en Hansenula anomala difiere de la vía usada por S. cerevisiae. Así, etil acetato se sintetiza preferentemente a partir de ácido acético y etanol mediante una reacción reversa de esterasa (Yoshioka & Hashimoto 1981, Rojas et al. 2002). Etil acetato se produce durante el crecimiento en glucosa y a diferentes niveles de aireación. El incremento de la oxigenación del medio reduce la producción de etil acetato (Tabachnick & Joslyn 1953, Fredlund et al. 2004a). Sin embargo, Rojas et al. (2001) han reportado menor producción de etil e isoamil acetato a condiciones de limitación de oxígeno comparado a condiciones aerobias. Mucho antes ya se había reportado que la producción de etil acetato requiere la presencia de pequeñas cantidades de oxígeno, y que su sintesís se inhibe a condiciones totalmente anóxicas (Davies et al. 1951, Tabachnick & Joslyn 1953). Los ésteres de acetato se forman en altas concentraciones durante la fermentación temprana (Henschke & Jiranek 1993). Hansenula anomala también produce otros ésteres como etil propanoato y 2-feniletil acetato (Westall 1999). Debido a la solubilidad de los ésteres en lípidos, estos pueden atravezar de manera relativamente fácil la membrana celular. Sin embargo, la tasa de difusión depende de la longitud de la cadena, así por ejemplo el etil acetato se excreta rápida y completamente, mientras que la excreción de los demás ésteres etílicos disminuye dramáticamente a medida que incrementa la longitud de la cadena, desde 100% para etil hexanoato hasta 54 - 68% para etil octanoato y 8 - 17% para etil decanoato (Nykanen & Nykanen 1977). Finalmente, la tasa de formación de ésteres depende de la concentración de sus precursores y de la actividad de las enzimas incolucradas en la síntesis e hidrólisis (Swiegers & Pretorius 2005). De ahí que todos los parámetros que afectan la concentración de los precursores o la actividad de las enzimas involucradas pueden afectar la producción de ésteres. Sin embargo, la producción de ésteres varía también entre cepas de una misma especie de levadura.
Las levaduras no-Sacccharomyces también producen diferentes niveles de alcoholes superiores. Altas concentraciones de estos afectan negativamente la calidad organoléptica por ejemplo en vinos, pero bajas concentraciones más bien confieren complejidad (Romano & Suzzi 1993). Estas levaduras frecuentemente producen bajas concentraciones de alcoholes superiores comparado a S. cerevisiae, pero hay una gran variabilidad entre cepas (Romano et al. 1992, Zironi et al. 1993).
Los alcoholes superiores son formados a partir de ±-cetoácidos, los cuales derivan de la desaminación de los correspondientes aminoácidos (valina, leucina, isoleucina, fenilalanina, etc.) a travez de la vía de Ehrlich ó a partir del metabolismo de la glucosa como precursores en la síntesis de aminoácidos (Ouchi et al. 1980, Mauricio et al. 1997). Concentraciones de alcoholes superiores a 400 mg/L contribuirían negativamente a la calidad organoléptica especialmente en vinos (Rapp & Mandery 1987). A excepción de 2-feniletanol el cual presenta aroma floral (Ribereau-Gayon et al. 2006a), cuyo valor umbral de percepción es 10 mg/L (Rous et al. 1983), los demás alcoholes superiores imparten características sensoriales desagradables (Rapp & Mandery 1987, Ribereau-Gayon et al. 2006a).
El presente estudio descriptivo se realizó con la finalidad de contribuir al entendimiento del comportamiento fermentativo de Hansenula anomala RIVE 7-1-5 y la producción de compuestos químicos de interés organoléptico como potencial para su aprovechamiento en la producción de bebidas fermentadas. Así mismo, se discute la influencia del oxígeno en la actividad metabólica y fermentativa y su repercusión en la síntesis de compuestos químicos de importancia sensorial.
Material y métodos
Microorganismo.- Se utilizó Hansenula anomala RIVE 7-1-5 adquirido de la colección de levaduras del Instituto de Investigación de Viticultura y Enología, Bratislava-República Eslovaca, y fue mantenido en agar extracto de malta a 7 oC con renovación periódica cada 3 meses.
Fermentación de azúcares y tolerancia al metabisulfito de sodio.- En los ensayos de fermentación de azúcares se utilizó caldo tipo Saboraud 2% como medio de cultivo base en el cual se sustituyó sólo la fuente de carbono. La actividad fermentativa se determinó visualmente mediante la producción de gas, para ello se usó la técnica de tubos Durham. Los ensayos se realizaron por triplicado a 28 oC durante 96 horas. En los ensayos de tolerancia al metabisulfito de sodio se utilizó medio sintético de la siguiente composición: glucosa 50,0 g/L; KH2PO4 5,0 g/L; MgSO4.7H2O 0,4 g/L; (NH4)2SO4 2,0 g/L y extracto de levadura 1,0 g/L. La tolerancia al metabisulfito de sodio (Na2S2O5) se determinó mediante la capacidad de fermentar glucosa a diferentes concentraciones de Na2S2O5 en el medio. El Na2S2O5 se adicionó de acuerdo al pH del medio: 100 mg/L al medio de pH 3,3; 150 mg/L al medio de pH 3,65 y 200 mg/L al medio de pH 4,24. En la evaluación de la fermentación se utilizaron tubos Durham y se observó visualmente la producción de CO2 hasta las 72 horas. Todos los ensayos se realizaron a 28 oC y por triplicado.
Producción de etanol.- Para los ensayos de producción de etanol se adquirió jugo de manzana concentrado, esterilizado por ultrafiltración y aroma removido de Severofrukt a.s., Terezin, República Checa. La remoción del aroma se realizó durante el proceso de concentrado en un evaporador provisto de una columna de separación de volátiles. El jugo concentrado así como el aroma obtenido fue entregado por separado al grupo de investigación. El jugo concentrado se reconstituyó con agua desionizada estéril hasta una concentración de azúcares totales de 12,8% w/v y pH 3,8 para utilizarlo como medio de fermentación. Los ensayos se realizaron en frascos Erlenmeyer de 1 L conteniendo 0,5 L de medio de cultivo. Las fermentaciones se llevaron a cabo en cultivo estático y agitado a 16 oC y 28 oC respectivamente. Las fermentaciones en cultivo agitado se realizaron en frascos agitados a 200 min-1 en un agitador orbital. Las fermentaciones en cultivo estático se consideraron terminadas cuando no se observó producción de CO2 y aquellas en cultivo agitado, el tiempo de cultivo fue el equivalente al tiempo utilizado durante la fermentación en cultivo estático.
El inóculo se propagó utilizando medio de cultivo de la misma composición. Los frascos Erlenmeyer se agitaron a 200 min-1, durante 48 horas, la temperatura de cultivo fue 28 oC. Así, el medio de fermentación se inoculó con 14,0 % v/v de inóculo. Finalmente, el contenido de etanol producido se determinó mediante picnometría. Todos los ensayos se realizaron por triplicado.
Síntesis de compuestos de importancia sensorial
Preparación de inóculo y condiciones de fermentación.- Jugo de manzana reconstituido y aroma removido (explicado anteriormente) se ha utilizado como medio de fermentación. Las fermentaciones se realizaron en cultivo agitado y estático en frascos Erlenmeyer de 0,5 L conteniendo 250 mL de medio. En las fermentaciones en cultivo agitado los frascos se agitaron a 200 min-1 durante 8 días y, aquellos en cultivo estático el tiempo de fermentación fue de 15 días. Los experimentos se realizaron a 28 oC.
La propagación del inóculo se llevo a cabo en 100 mL de jugo de manzana estéril a 28 oC durante 24 horas, los frascos se agitaron a 200 min-1 en un agitador orbital. Las células se separaron por centrifugación (3000 min-1 durante 10 minutos) y se lavaron tres veces con solución fisiológica estéril. Los medios de fermentación se inocularon con 1,0±0,1 g de células en peso húmedo.
Cultivo batch en biorreactor.- Como medio de cultivo se utilizó jugo de manzana variedad Rubin con un contenido de azúcares totales de 13% en peso y pH 3,8. Las manzanas fueron adquiridas de la distribuidora de frutas y hortalizas Fruit-CZ, Praga, República Checa. Luego de la extracción, el jugo se vertió en envases estériles de 10 L y se pasteurizó en un termostato a 65 - 70 oC durante 12 horas (incluyendo el tiempo de enfriado) con la finalidad de eliminar la flora microbiana y además todos los compuestos volátiles varietales (El-Nemra et al. 1988, Su & Wiley 1998). Al jugo de manzana se suplementó con KH2PO4 1,2 g/L y (NH4)2SO4 1,2 g/L como fuente de fósforo y amonio para promover el crecimiento de la levadura.
Los cultivos se realizaron en un biorreactor (BIOSTAT-B.Braun International, Alemania) de 2 L conteniendo 1,5 L de medio de cultivo. El biorreactor estuvo conectado a una unidad de regulación y medición micro-DCU-300 y además estuvo equipado con un agitador, medidor de pH, termómetro y un electrodo de medición de oxígeno disuelto. Los parámetros considerados en el cultivo los cuales fueron mantenidos constante a lo largo del proceso fueron: temperatura 18 oC, frecuencia de agitación 300 min-1 y flujo de aire 25 L/h (0,2 moles O2/h). El tiempo de cultivo se dejó hasta el incremento de la concentración de oxígeno disuelto en el medio a su valor inicial.
El inóculo se propagó en 80 mL de medio sintético de la siguiente composición: glucosa 8,0 g/L; peptona 10,0 g/L; KH2PO4 1,2 g/L; (NH4)2SO4 1,2 g/L y extracto de levadura 10,0 g/L, el pH se ajustó a 3,6. La propagación de células se llevo a cabo en un agitador orbital a 150 min-1 durante 48 horas a 28 oC. Las células se separaron por centrifugaron (3000 min-1 durante 10 minutos), se lavaron tres veces con solución fisiológica estéril y, finalmente las células obtenidas se inocularon en el biorreactor.
Métodos analíticos y presentación de resultados
Los compuestos volátiles producidos durante la fermentación (alcoholes superiores y ésteres) se analizaron en un cromatógrafo de gas (Hewlett-Packard 5890II), equipado con una columna HP5 (30m x 0,32mm) y un detector FID.
Las muestras fermentadas por triplicado se centrifugaron y filtraron en una membrana de microfiltración de 0,45 µm de porosidad, luego se extrajeron los compuestos volátiles mediante el método de microextracción con diclorometano (Ortega et al. 2001). Finalmente, 1 µL de cada extracto se inyectó en el cromatógrafo.
El ácido acético, succínico, málico, etanol, glicerol, fructosa y glucosa se analizaron en un HPLC (Pump LCP 4000), equipado con una columna Watrex 250 x 8mm (Ostion LGKS 0800 H+) y un detector RID. En el análisis se utilizó 0,005M de H2SO4 como fase móbil a una tasa de flujo de 1 mL/min. Las muestras fermentadas por triplicado luego de ser filtradas y centrifugadas se diluyeron con agua desmineralizada (1:3) y se inyectaron al equipo.
La biomasa celular se determinó mediante gravimetría. Las células se separaron por centrifugación a 3000 min-1 durante 10 minutos, se lavaron 3 veces con agua destilada luego se secaron a 110 °C durante 2 horas y finalmente se pesaron. Además, se determinaron el coeficiente global de rendimiento de biomasa YX/S y la tasa de crecimiento (µ) respectivamente (van Hoek et al. 1998). Los ensayos y análisis se realizaron por triplicado, los resultados se presentan como los promedios y su desviación estandard.
Resultados y discusión
Fermentabilidad de azúcares y tolerancia al etanol y metabisulfito de sodio.- Las levaduras difieren en su capacidad de fermentar azúcares, esta característica es fundamental para definir su utilidad en procesos fermentativos. Como se muestra en la Tabla 1, Hansenula anomala RIVE 7-1-5 es capaz de fermentar glucosa, fructosa y manosa. Estos azúcares generalmente estan presentes en los jugos de fruta. La fermentación de sucrosa y maltosa es una característica interesante ya que puede fermentar también medios que contengan estos azúcares, por ejemplo mostos a base de cereales.

La capacidad inhibitoria del SO2 esta influenciada por el pH del medio (Jarvis & Lea 2000). Como se observa en la Tabla 1, la actividad fermentativa de Hansenula anomala RIVE 7-1-5 ha sido inhibida totalmente a concentraciones de metabisulfito de sodio (precursor de SO2) incluso hasta 100 mg/L. La utilización de dioxido de azufre (SO2) en el caso de la producción de vinos esta regulado debido a los posibles efectos tóxicos que produce. La OIV (Organización Internacional de la Viña y el Vino) recomienda dosis entre 150-400 mg/L de sulfito, dependiendo del tipo de vino (Ribereau-Gayon et al. 2006b).
Producción de etanol.- Las levaduras oxidativas cultivadas bajo limitación de oxígeno producen etanol debido a la interrupción de su actividad respiratoria. La respiración y la fermentación suceden simultaneamente, la concentración de oxígeno determina el balance entre ambos metabolismos. Sin embargo, en un metabolismo mixto la generación de energía disminuye y como resultado también la tasa de crecimiento, para dar formación a compuestos típicos de la fermentación alcohólica. En la Tabla 2 se muestra las concentraciones de etanol producido por Hansenula anomala RIVE 7-1-5. Se ha observado una mayor producción de etanol en cultivo estático (5.81±0,1% v/v) a 28 oC. La agitación del medio disminuyó la producción de etanol dramáticamente en cultivos a 28 oC y un efecto contrario se observó a 16 oC. Así mismo, la diminución de la temperatura afectó sustancialmente la producción de etanol en cultivo estático, sin embargo esto no sucedió en cultivo agitado donde la producción de etanol incrementó de 2,35±0,1 a 4,69±0,1% v/v. Esta cepa es capaz de producir hasta 5,8±0,1% v/v de etanol que es una cantidad suficiente para producir bebidas con contenido medio de etanol (por ejemplo cidras). Nuestros resultados demuestran que algunas cepas de Hansenula anomala pueden producir concentraciones de etanol por encima de 5% v/v contrariamente a lo encontrado por Kalathenos et al. (1995) y Fredlund et al. (2002). La disminución de producción de etanol en cultivo agitado (al menos a 28 oC) se debería al efecto del oxígeno incorporado al medio durante la agitación. Esto explica que Hansenula anomala RIVE 7-1-5 prefiere oxidar la glucosa en presencia de oxígeno antes que fermentarla. Para casos prácticos la producción de etanol podría ser controlado mediante la tasa de aireación.

La temperatura juega un rol importante en la producción de compuestos secundarios durante la fermentación. En la producción de vinos blancos y cervezas por ejemplo se prefiere temperaturas bajas de fermentación ya que influye positivamente en la síntesis de compuestos químicos de importancia sensorial (Torija et al. 2003). Para casos prácticos la producción de etanol por Hansenula anomala RIVE 7-1-5 podría ser controlado ajustando la temperarura y la aireación del medio de fermentación.
Síntesis de compuestos de importancia sensorial.- La variación de parámetros que dan paso a la fermentación conducen a la producción de etanol y otros compuestos químicos de importancia sensorial. En la Tabla 3 se muestra las concentraciones de los compuestos producidos por Hansenula anomala RIVE 7-1-5 durante cultivo estático y agitado, así mismo se muestra con fines de comparación los principales compuestos encontrados en cidras y jugo de manzana. Un ligero incremento de glicerol se observó en cultivo estático (1,5±0,4 g/L), comparado con el cultivo agitado (1,4±0,15 g/L). La disminución se debería en parte a que el metabolismo aerobio promueve la respiración celular disminuyendo así la producción de glicerol. Sin embargo, su producción también sería una respuesta al estrés osmótico del medio de fermentación debido a la alta concentración de azúcar. Una mayor producción de glicerol sería favorable para el perfil sensorial de la bebida fermentada ya que impartiría un ligero sabor dulce (Nieuwoudt et al. 2002).
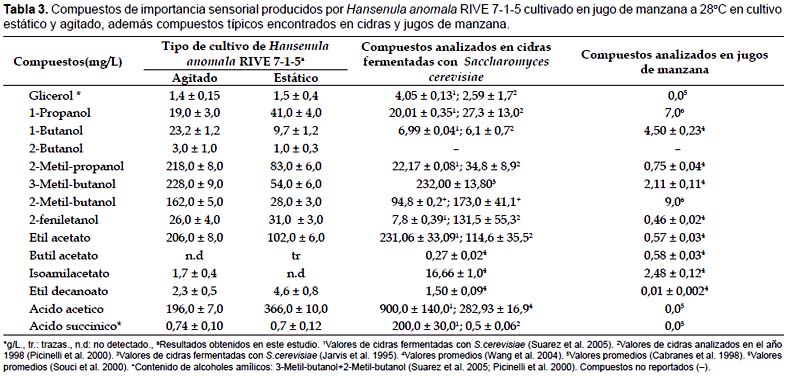
Con respecto a la producción total de alcoholes superiores se observa que en cultivo agitado se produjo mayor cantidad (679,2 mg/L) comparado al cultivo estático (247,7 mg/L); la mayor producción se debería al efecto del oxígeno incorporado al medio durante la agitación. El oxígeno promueve el metabolismo respiratorio y como consecuencia un mayor flujo de glucosa y aminoácidos, cuya degradación produce compuestos intermediarios (cetoácidos) de la síntesis de alcoholes superiores (Ribereau-Gayon et al. 1975; Valero et al. 2002). Otros factores que incrementan la producción de alcoholes superiores incluyen la clarificación del mosto, la madurez de la fruta, la temperatura entre otros (Ough et al. 1966; Blanco et al. 1992; Mangas et al. 1994).
Los ésteres imparten el aroma frutal en las bebidas fermentadas, por esta razon su presencia determina en parte la calidad sensorial. El etil acetado es el éster de mayor importancia por su concentración. Como se muestra en la Tabla 3, la mayor producción de etil acetado por Hansenula anomala RIVE 7-1-5 se observó en cultivo agitado (206,0±8,0 mg/L). La tasa de formación de etil acetato estaría relacionado con la disponibilidad de ácido acético, etanol y, además de la actividad de la ester sintasa necesarios para su formación (Yoshioka & Hashimoto 1981, Rojas et al. 2002). Por otro lado, la concentración de ácido acético en cultivo agitado (196,0±10,0mg/L) resultó ser menor comparado al cultivo estático (366,0±10,0mg/L), lo que indicaría que la tasa de formación de etil acetato en cultivo agitado ha sido suficientemente alta para convertir el ácido acético en etil acetato. El incremento de la síntesis de ácido acético también esta unido a la producción de glicerol (Prior et al. 2000). Nuestros resultados concuerdan con lo reportado por Rojas et al. (2001) quienes reportaron que la aireación promueve una mayor síntesis de etil acetato e isoamil acetato. Sin embargo Fredlund et al. (2004a) reportaron un efecto contrario de la aireación en Hansenula anomala. La mayor formación de etil acetado en cultivo agitado con Hansenula anomala RIVE 7-1-5 involucraría otros factores propios de la cepa. Por otra parte, también se ha observado la producción de isoamil acetato y etil decanoato en concentraciones menores. La producción de estos ésteres es ventajosa si se desea producir bebidas no tradicionales con aromas especiales. En el caso de la fermentación de vinos la presencia de etil acetato en concentraciones menores a 80 mg/L contribuye positivamente al aroma y sabor (Ribereau-Gayon 1978). Altas concentraciones de etil acetato sobre 200 mg/L imparte un sabor a vinagre (Dequin et al. 2003).
Así mismo, se ha observado la formación de ácido succínico tanto en cultivo agitado (0,74±0,10 mg/L) como estático (0,7±0,12 mg/L). Este ácido contribuye a la acidez total de la bebida. En presencia de oxígeno el ácido succínico se produce normalmente como un intermediario del ciclo de Krebs ó bien por la actividad de las enzimas relacionadas al ciclo de Krebs cuya síntesis no sería inducida por el oxígeno (Arikawa et al. 1999).
Los cultivos agitados en frascos Erlenmeyer presentan limitaciones en la transferencia de oxígeno (Gupta & Rao 2003, Tolosa et al. 2002), esto provocaría un metabolismo respirofermentativo mixto en Hansenula anomala RIVE 7-1-5 con la consecuente variabilidad en la producción de productos de la fermentación. Los factores que influyen en la transferencia de oxígeno incluyen la relación volumen del frasco Erlenmeyer/volumen del medio de cultivo, diametro del cuello del frasco e inclusive el tipo y las características del tapón (Nikakhtari & Hill 2006).
Cultivo batch en biorreactor.- La Figura 2 muestra el transcurso del consumo de oxígeno, el crecimiento celular y la variación del pH durante 11 días de cultivo de Hansenula anomala RIVE 7-1-5. El oxígeno es el factor más importante que determina el balance entre la actividad respiratoria y fermentativa en esta levadura. A concentraciones inferiores a la concentración crítica la velocidad de respiración es dependiente de la concentración de oxígeno, por el contrario a concentraciones superiores es independiente (Johnson 1976). En presencia de oxígeno como subtrato, la relación entre la tasa de crecimiento y concentración de oxígeno en el medio sigue la cinética de Michaelis Menten (Johnson 1976). La concentración crítica de oxígeno para levaduras es muy baja, en el orden de 0,12mg/L a 20oC.
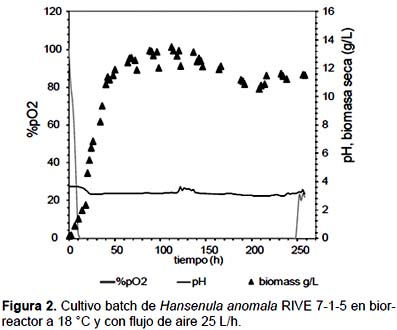
Como se observa en la Figura 2 luego de las 10 horas la concentración de oxígeno disuelto en el medio cayó a cero y así permaneció hasta las 250 horas. Esto significa que el oxígeno transferido al medio ha sido consumido en su totalidad, sin embargo este valor no da información de la tasa de consumo de oxígeno. El oxígeno es poco soluble en agua pura (9,1 mg/L, 20 oC) y a medida que la temperatura y la viscocidad del medio incrementa la solubilidad disminuye. La tranferencia de oxígeno al medio es crucial y depende de muchos factores, entre ellos, el flujo de aire, la velocidad de agitación, la composición química del medio, la geometría del biorreactor, entre otros. El oxígeno consumido es utilizado mayormente en la respiración es decir en la oxidación de la glucosa, pero también en vías no respiratorias como en la síntesis de esteroles y ácidos grasos insaturados que son componentes esenciales de la membrana celular (Rosenfeld & Beauvoit 2003).
El agotamiento rápido del oxígeno indica que esta cepa manifiesta un metabolismo aerobio pero que probablemente experimenta limitación de oxígeno, en este caso se recomienda trabajar a concentraciones de saturación o exceso de oxígeno si se desea suprimir al máximo la actividad fermentativa. En este caso la producción de etanol se acercaría a cero.
Además, se observa un incremento gradual de biomasa celular alcanzando un valor de 11,5 g/L al final del cultivo (Tabla 4). Estequiométricamente este valor es inferior a lo esperado, esto sugiere que la fuente de carbono no solamente habría sido utilizado para el crecimiento, sino en algún otro proceso como en "maintenance" (Beeftink et al. 1990), o en la formación de productos de la fermentación. Sin embargo en los compuestos residuales al final del cultivo no reporta etanol, además bajos niveles de glicerol (0,91±0,05 g/L) y alta concentración de ácido acético (4,2±0,3 g/L). La producción de ácido acético a condiciones aerobias ha sido reportado por Fredlund et al. (2004 a,b), sin embargo concentraciones tan elevadas sería una característica aún no reportada.
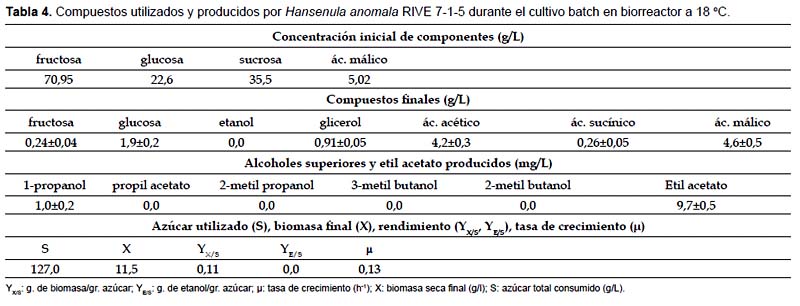
Así mismo, no se ha observado una variación significante del pH (de 3,64 a 3,09) al final del proceso. La variación del pH esta asociado con el proceso de crecimiento celular y la actividad metabólica como la principal causa del intercambio de protones en el medio. También no se ha observado una disminución significante del contenido de ácido málico, lo que significaría que esta cepa utiliza limitadamente este ácido en presencia de oxígeno. Sin embargo, Corte-Real et al. (1990) y Corte-Real y Leao (1990) reportaron la utilización de ácido málico por Hansenula anomala. Desde el punto de vista práctico concentraciones de oxígeno que conducen principalmente al metabolismo respiratorio debe ser evitado.
La ausencia de muchos compuestos de la fermentación como por ejemplo alcoholes superiores y además la baja cantidad de algunos de ellos indicarían que el metabolismo ha sido predominantemente respiratorio (Tabla 4). En todo caso, el etanol probablemente producido durante el cultivo podría haber servido como fuente de carbono al agotarse los azúcares fermentables. Al final del cultivo, el incremento del porcentaje de oxígeno disuelto estaría conectado al agotamiento de la fuente de carbono que limitaría el crecimiento y así el consumo de oxígeno.
Reportes anteriores mostraron la utilización de Hansenula anomala junto a otras levaduras no-Saccharomyces en la producción de vinos de bajo contenido alcohólico (3% v/v) en envases aireados. Sin embargo, la agitación resultó en el incremento de biomasa celular y la disminución de la producción de etanol (Erten & Campbell 2001).
Conclusiones
Hansenula anomala RIVE 7-1-5 tiene una gran capacidad de fermentar azúcares comunmente encontrados en frutas y en mostos preparados a base de cereales, característica que la hace interesante para su aprovechamiento y utilización en fermentación de bebidas. Su sensibilidad al SO2 es importante ya que concentraciones de 100 mg/L sería suficiente para inhibibir su actividad fermentativa en caso que sea necesario. Así mismo, su capacidad de producir etanol hasta 5,81±0,1 % v/v la hace adecuada para producir bebidas con bajo contenido alcohólico. Sin embargo, la producción de etanol puede ser controlada mediante la tasa de agitación y la temperatura. Temperaturas de 16 oC con agitación de 200 min-1 o menos se recomienda.
Por otro parte, la aireación promueve una mayor producción de alcoholes superiores y etil acetato, lo que no sucede con ácido acético. Así mismo, la tasa de agitación puede utilizarse para controlar la tasa de aireación y así balancear la producción de compuestos de importancia sensorial. Con la finalidad de producir bebidas fermentadas no tradicionales se recomienda airear intermitentemente el medio de fermentación para conseguir la mayor producción de compuestos volátiles de interés sensorial.
La demanda por bebidas fermentadas con características sensoriales particulares hace a las levaduras no-Saccharomyces oxidativas aprovechables. El suministro constante y controlado de oxígeno (0,2 moles/h) desvía el metabolismo fermentativo hacia el oxidativo, sin embargo el oxígeno disuelto bajo estas condiciones no provoca un metabolismo enteramente oxidativo. La concentración de oxígeno es el factor clave que determina la formación de compuestos de la fermentación alcohólica al menos en esta cepa de levadura.
Finalmente, bebidas fermentadas no tradicionales con altas concentraciones de compuestos aparentemente indeseables pueden parecer placenteros para algunos y lo opuesto para otros.
Agradecimientos
Los autores agradecen a la colección de levaduras del Instituto de Investigación de Viticultura y Enología, Bratislava, República Eslovaca por proporcionarnos la cepa de levadura estudiada.
Literatura citada
Andre L., A. Nilsson & L. Adler. 1988. The role of glycerol in osmotolerance of the yeast Debaryomyces hansenii. Journal of General Microbiology, 134: 669-677.
Arikawa Y., T. Kuroyanagi, M. Shimosaka, et al. 1999. Effect of gene disruptions of the TCA cycle on production of succinic acid in Saccharomyces cerevisiae. Journal of Bioscience and Bioengineering, 87(1): 28-36.
Beech, F.W., L.F. Burroughs, C.F. Timberlake, et al. 1979. Current progress in the chemical aspects and antimicrobial effects of sulphur dioxide (SO2). Bulletin de L'O.I.V., 52: 1001-1022.
Beeftink H.H., R.T.J.M. van der Heijden & J.J. Heijnen. 1990. Maintenance requirements: Energy supply from simultaneous endogenous respiration and substrate consumption. FEMS Microbiology Letters, 73(3): 203-209.
Bisson L.F. 1993. Yeasts metabolism of sugars. In: G.H Fleet, eds. Wine Microbiology and Biotechnology. Harwood Academic Publishers, Chur, Switzerland., pp. 55-57.
Blanco D., M.J. Moran, M.D, et al. 1992. Biochemical study of the ripening of cider apple varietes. Zeitschrift-fuer-Lebensmittel-Untersuchung und Forschung, 194(1): 33-37.
Blomberg A. & L. Alder. 1992. Physiology of osmotolerance in fungi. Advances in Microbial Physiology, 33: 145-212.
Boulton B., V.L. Singleton, L.F. Bisson, et al. 1996. Yeast and biochemistry of ethanol fermentation. In: B. Boulton, B.L. Singleton, L.F. Bisson and R.E. Kunkee, eds. Principles and Practices of Winemaking. Chapman and Hall Publishers, New York., pp. 139-172.
Bulder C.J.E.A. 1964. Induction of petite mutation and inhibition of synthesis of respiratory enzymes in various yeasts. Antonie van Leeuwenhoek, 30: 1-9.
Cabranes C., J. Moreno & J.J. Mangas. 1998. Cider production with immobilized Leuconostoc oenos. Journal of the Institute of Brewing, 4: 127-130.
Corte-Real M. & C. Leao. 1990. Transport of malic acid and other dicarboxylic acids in the yeast Hansenula anomala. Applied and Environmental Microbiology, 56: 1109-1113.
Corte-Real M., C. Leao & N. Van Uden. 1990. Inverse diauxy in the yeast Hansenula anomala: Mutants derepressed for malic acid utilization in the presence of glucose. Applied and Environmental Microbiology, 56(11): 3402-3404.
Davies R., E.A. Falkiner, J.F. Wilkinson, et al. 1951. Ester formation by yeast. 1. Ethyl acetate formation by Hansenula species. Biochemical Journal, 49: 58-60.
D'Amore T., C.J. Panchal, I. Russell, et al. 1990. Ethanol tolerance in yeasts. Critical Reviews in Biotechnology, 9: 287-304.
De Deken, R.H. 1966a. The Crabtree effect and its relation to the petite mutation. Journal of Genetic Microbiology, 44: 157-165.
De Deken R.H. 1966b. The Crabtree effect: a regulatory system in yeast. Journal of Genetic Microbiology, 44: 149-156.
Dequin S., J.M. Salmon, H.V. Nguyen, et al. 2003. Wine yeasts. In: T. Boekhout and V. Robert, eds. Yeasts in Food-Beneficial and Detrimental Aspects. Behr's Verlag, Hamburg., pp. 389-412.
Dung N.T.P., F.M. Rombouts & M.J.R. Nout. 2006. Functionality of selected strains of moulds and yeasts from Vietnamese rice wine starters. Food Microbiology, 23(4): 331-340.
El-Nemra S.E., I.A. Ismaila & A. Askar. 1988. Aroma changes in mango juice during processing and storage. Food Chemistry, 30(4): 269-275.
Erten H. & I. Campbell. 2001. The production of low-alcohol wines by aerobic yeasts. Journal of the Institute of Brewing, 107: 207-215.
Fiaux J., P. Cakar, M. Sonderegger, et al. 2003. Metabolic-flux profiling of the yeasts Saccharomyces cerevisiae and Pichia stipitis. Eukaryotic Cell, 2: 170-180.
Fleet G.H. 1992. Spoilage yeasts. Critical Reviews in Biotechnology, 12: 1-44.
Fleet G.H. & G.M. Heard. 1993. Yeasts-growth during fermentation. In: G.H. Fleet, eds. Wine Microbiology and Biotechnology. (Harwood Academic Publishers, Switzerland., pp. 27-54.
Flores C.L., C. Rodriguez, T. Petit, et al. 2000. Carbohydrate and energy-yielding metabolism in non-conventional yeasts. FEMS Microbiology Reviews, 24: 507-529.
Fredlund E., U. Druvefors, M.E. Boysen, et al. 2002. Physiological characteristics of the biocontrol yeast Pichia anomala J121. FEMS Yeast Research, 2: 395-402.
Fredlund E., L.M. Blank, U. Sauer, et al. 2004a. Oxygen and glucose dependent regulation of central carbon metabolism in Pichia anomala. Applied and Environmental Microbiology, 70: 5905-5911.
Fredlund E., A. Broberg, M.E. Boysen, et al. 2004b. Metabolite profiles of the biocontrol yeast Pichia anomala J121 grown under oxygen limitation. Applied Microbiology and Biotechnology, 64: 403-409.
Fujii T., N. Nagasawa, A. Iwamatsu, et al. 1994. Molecular cloning, sequence analysis, and expression of the yeast alcohol acetyltransferase gene. Applied and Environmental Microbiology, 60: 2786-2792.
Fujii T., O. Kobayashi, H. Yoshomoto, et al. 1997. Effect of aeration and unsaturated fatty acids on expression of the Saccharomyces cerevisiae alcohol acetyltransferase gene. Applied and Environmental Microbiology, 63(3): 910-915.
Gancedo C. & R. Serrano. 1989. Energy yielding metabolism. In: A.H. Rose and J.S. Harrison, eds. The Yeasts. Academic Press, London., pp. 205-259.
Goffrini P., I. Ferrero & C. Donnini. 2002. Respiration-dependent utilization of sugars in yeasts: A determinant role for sugar transporters. Journal of bacteriology, 184(2): 427-432.
Gombert A.K., M.M. dos Santos, B. Christensen, et al. 2001. Network identification and flux quantification in the central metabolism of Saccharomyces cerevisiae under different conditions of glucose repression. Journal of Bacteriology, 183: 1441-1451.
Grbin P.R. 1999. Are indigenous yeast that important to wine production?. Australian Grapegrow and Winemaker, 427: 42-43.
Gupta A. & G.A. Rao. 2003. Study of oxygen transfer in shake flasks using a non-invasive oxygen sensor. Biotechnology and Bioengineering, 84(3): 351-358.
Hansen E.H., P. Nissen, P. Sommer, et al. 2001. The effect of oxygen on the survival of non-Saccharomyces yeasts during mixed culture fermentations of grape juice with Saccharomyces cerevisiae. Journal of Applied Microbiology, 91: 541-547.
Henschke P.A. & V. Jiranek. 1993. Yeasts-metabolism of nitrogen compounds. In: G.H. Fleet, eds. Wine Microbiology and Biotechnology. Harwood Academic Publishers, Langhorne., pp. 77-164.
Hilary A. & B. Peddie. 1990. Ester formation in brewery fermentations. Journal of Institute of Brewing, 96: 327-331.
Jacobson M.K. & C. Bernofsky. 1974. Mitochondrial acetaldehyde dehydrogenase from Saccharomyces cerevisiae. Biochimica et Biophysica Acta, 350: 277-291.
Jarvis B., M.J. Forster & W.P. Kinsella. 1995. Factors affecting the development of cider flavour. Journal of Applied Bacteriology, 79: 5S-18S.
Jarvis B. & A.G.H. Lea. 2000. Sulphite binding in ciders. International Journal of Food Science and Technology, 35: 113-127.
Johnson M.J. 1976. Aerobic microbial growth at low oxygen concentrations. Journal of Bacteriology, 94(1): 101-108.
Kalathenos P., J.P. Sutherland & T.A. Roberts. 1995. Resistance of some wine spoilage yeasts to combinations of ethanol and acids present in wine. Journal of Applied Bacteriology, 78: 245-250.
Kruckeberg A.L. 1996. The hexose transporter family of Saccharomyces cerevisiae. Archives of Microbiology, 166: 283-292.
Lilly M., M.G. Lambrechts & I.S. Pretorius. 2000. Effect of increased yeast alcohol acetyltransferase activity on flavor profiles of wine and distillates. Applied and Environmental Microbiology, 66: 744-753.
Maier K., H. Hinze & L. Leuschel. 1985. Mechanism of sulfite action on the energy metabolism of Saccaromyces cerevisiae. Biochimica et Biophysica Acta, 848: 120-130.
Malcorps P., J.M. Cheval, S. Jamil, et al. 1991. A new model for the regulation of ester synthesis by alcohol acetyltransferase in Saccharomyces cerevisiae during fermentation. Journal of the American Society of Brewing Chemists, 49: 47-53.
Mangas J.J., C. Cabranes, J. Moreno, et al. 1994. Influence of cider making technology on cider taste. Lebensmittel und Wissenschaft Technologie, 27: 583-586.
Mason A.B. & J.P. Dufour. 2000. Alcohol acetyltransferases and the significance of ester synthesis in yeast. Yeast, 16(4): 1287-1298.
Mauricio J.C., J. Moreno, L. Zea, et al. 1997. The effects of grape must fermentation conditions on volatile alcohols and esters. Journal of the Science of Food and Agriculture, 75: 155-160.
Nagodawithana T.W. & K. Steinkraus. 1976. Influence of the rate ethanol production and accumulation on the viability of Saccharomyces cerevisiae in rapid fermentation. Applied and Environmental Microbiology, 31: 158-162.
Nagodawithana T.W., J.T. Whitt & A.J. Cutaia. 1977. Study of the feedback effect of ethanol on selected enzymes of the glycolytic pathway. Journal of the American Society of Brewing Chemist, 35: 179-193.
Naito S. 1984. Identification of some yeasts isolated from white spotted cake and some examination of tolerance on sugar and salt. Annual Report of the Food Research Institute, Aichi Prefecture (Japan), 76-84.
Nieuwoudt H.H., B.A. Prior, I.S. Pretorius, et al. 2002. Glycerol in South African table wines: an assessment of its relationship to wine quality. South African Journal of Enology and Viticulture, 23: 22-30.
Nikakhtari H. & G. Hill. 2006. Closure effects on oxygen transfer and aerobic growth in shake flasks. Biotechnology and Bioengineering, 95(1): 15-21.
Nykanen L. & I. Nykanen. 1977. Production of esters by different yeast strains in sugar fermentations. Journal of the Institute of Brewing, 83:30-31.
Ortega C., R. Lopez, J. Cacho, et al. 2001. Fast analysis of important wine volatile compounds: Development and validation of a new method based on gas chromatography-flame ionization detection analysis of dichloromethane micro extracts. Journal of Chromatography A, 923: 205-214.
Ouchi K., Y. Yamamoto, M. Takagishi, et al. 1980. Regulation of isoamyl alcohol formation via Ehrlich pathway in Saccharomyces cerevisiae. Journal of Fermentation Technology, 58: 301-309.
Ough C.S., J.F. Guymon & E.A. Crowell. 1966. Formation of higher alcohols during grape juice fermentation at various temperatures. Journal of Food Science, 31: 620-625.
Picinelli A., B. Suarez, J. Moreno, et al. 2000. Chemical characterization of Asturian cider. Journal of Agricultural and Food Chemistry, 48: 3997-4002.
Pina C., J.A. Couto & T. Hogg. 2004. Inferring ethanol tolerance of Saccharomyces and non-Saccharomyces yeasts by progressive inactivation. Biotechnology Letters 26: 1521-1527.
Plata M.C., J.C. Mauricio, C. Millan, et al. 1998. In vitro specific activity of alcohol acetyltransferase and esterase in two flor yeast strains during biological aging of Sherry wines. Journal of Fermentation and Bioengineering, 85: 369-374.
Plata C., C. Millan, J.C. Mauricio. 2003. Formation of ethyl acetate and isoamyl acetate by various species of wine yeasts. Food Microbiology, 20: 217- 224.
Postma E., C. Verduyn, W.A. Scheffers, et al. 1989. Enzymic analysis of the Crabtree effect in glucose-limited chemostat cultures of Saccharomyces cerevisiae. Applied and Environmental Microbiology, 55: 468-477.
Prior B.A. & S. Hohmann. 1997. Glycerol production and osmoregulation. In: F.K. Zimmermann and K.D. Entian, eds. Yeast Sugar Metabolism. Technomic Publishing, Lancaster., pp. 313-337.
Prior B.A., T.H. Toh, N. Jolly, et al. 2000. Impact of yeast breeding for elevated glycerol production on fermentation activity and metabolite formation in Chardonnay. South African Journal of Enology and Viticulture, 21: 92-99.
Rapp A. & H. Mandery. 1987. New progress in wine and wine research. Experientia 42(8): 873-884.
Remize F., J.L. Roustan, J.M. Sablayrolles, et al. 1999. Glycerol overproduction by engineered Saccharomyces cerevisiae wine yeast strains leads to substantial changes in byproduct formation and to a stimulation of fermentation rate in stationary phase. Applied and Environmental Microbiology, 65: 143-149.
Remize F., E. Andrieu & S. Dequin. 2000. Engineering of the pyruvate dehydrogenase bypass in Saccharomyces cerevisiae: Role of the cytosolic Mg2+ and mitochondrial K(+) acetaldehyde dehydrogenases Ald6p and Ald4p in acetate formation during alcoholic fermentation. Applied and Environmental Microbiology, 66: 3151-3159.
Ribereau-Gayon J., E. Peynaud, P. Ribereau-Gayon, et al. 1975. Traite d'oenolgie: Sciences et techniques du vin. Dunod, Paris.
Ribereau-Gayon P. 1978. Wine aroma. In: G. Charalambous and G.E. Inglett, eds. Flavour of Foods and Beverages. Academic Press, NewYork., pp. 362-371.
Ribereau-Gayon P. 1985. New developments in wine microbiology. American Journal of Enology and Viticulture, 36: 1-10.
Ribereau-Gayon P., D. Dubourdieu, B. Doneche, et al. 2006a. Biochemistry of alcoholic fermentation and metabolic pathways of wine yeasts. In: Handbook of Enology. The Microbiology of Wine and Vinifications, (2nd edition) 74-77 (John Wiley and Sons, Ltd. The Atrium, Southern Gate, Chichester, England).
Ribereau-Gayon P., D. Dubourdieu, B. Doneche, et al. 2006b. The use of sulfur dioxide in must and wine treatment. In: Handbook of Enology. The Microbiology of Wine and Vinifications, (2nd edition) 193-197 (John Wiley and Sons, Ltd. The Atrium, Southern Gate, Chichester, England).
Ricci M., S. Martini, C. Bonechi, et al. 2004. Inhibition effects of ethanol on the kinetics of glucose metabolism by S. cerevisiae: NMR and modelling study. Chemical Physics Letter, 387(4-6): 377-382.
Rojas V., J.V. Gil, F. Pinaga, et al. 2001. Studies on acetate ester production by non-Saccharomyces wine yeasts. International Journal of Food Microbiology, 70: 283-289.
Rojas V., J.V. Gil, P. Manzanares, et al. 2002. Measurement of alcohol acetyltransferase and ester hydrolase activities in yeast extracts. Enzyme and Microbial Technology, 30: 224-230.
Romano P., G. Suzzi, G. Comi, et al. 1992. Higher alcohol and acetic acid production by apiculate wine yeasts. Journal of Applied Bacteriology, 73: 126- 130.
Romano P. & G. Suzzi. 1993. Higher alcohol and acetoin production by Zygosaccharomyces wine yeasts. Journal of Applied Bacteriology, 75: 541-545.
Rosenfeld E. & B. Beauvoit. 2003. Role of the non-respiratory pathways in the utilization of molecular oxygen by Saccharomyces cerevisiae. Yeast, 20: 1115-1144.
Rous C.V., R. Snow & R.E. Kunkee. 1983. Reduction of higher alcohols by fermentation with a leucine-auxotrophic mutant of wine yeast. Journal of the Institute of Brewing, 89(4): 274-278.
Sa-Correia I. & N. Van Uden. 1983. Temperature profiles of ethanol tolerance: Effects of ethanol on the minimum and maximum temperature for growth of Saccharomyces cerevisiae and Kluyveromyces fragilis. Biotechnology and Bioengineering 25: 1665-1667.
Shin Y.D. & D.H. Cho. 1970. A study on the microflora changes during takju brewing. Korean Journal of Microbiology, 8: 53-54.
Souci S.W., W. Fachmann & H. Kraut. 2000. Juices from fruits and berries: Food composition and nutrition tables. (6th ed.), Stuttgart: Scientific publishers., pp. 1352.
Suarez Valles B., R. Pando Bedrinana, N. Fernandez Tascon, et al. 2005. Analytical differentiation of cider inoculated with yeast (Saccharomyces cerevisiae) isolated fromAsturian (Spain) apple juice. LWT, 38: 455-461.
Su S.K. & R.C. Wiley. 1998. Changes in apple juice flavor compounds during processing. Journal of Food Science, 63(4): 688-691.
Suomalainen, H. 1981. Yeast esterase and aroma esters in alcoholic beverages. Journal of the Institute of Brewing, 87: 296-300.
Swiegers J.H. & I.S. Pretorius. 2005. Yeast modulation of wine flavour. Advances in Applied Microbiology, 57: 131-175.
Tabachnick J. & M.A. Joslyn. 1953. Formation of esters of yeast. I. The production of ethyl acetate by standing surface cultures of Hansenula anomala. Journal of Bacteriology, 65: 1-9.
Thomas D.S. 1993. Yeasts as spoilage organisms in beverages. In: A.H. Rose and J.S. Harrison, eds. The Yeasts (Vol. 5). Academic Press, New York., pp. 517-561.
Tokuoka K., T. Ishitani & W.C. Chung. 1992. Accumulation of polyols and sugars in some sugar-tolerant yeasts. Journal of General and Applied Microbiology, 38: 35-46.
Tolosa L., Y. Kostov, P. Harms, et al. 2002. Noninvasive measurement of dissolved oxygen in shake flasks. Biotechnology and Bioengineering, 80(5): 594-597.
Torija M.J., N. Rozes, M. Poblet, et al. 2001. Yeast population dynamics in spontaneous fermentations: Comparison between two different wine-producing areas over a period of three years, Antonie van Leeuwenhoek, 79: 345-352.
Torija M.J., G. Beltran, M. Novo, et al. 2003. Effects of fermentation temperature and Saccharomyces species on the cell fatty acid composition and presence of volatile compounds in wine. International Journal of Food Microbiology, 85: 127-136.
Valero E., L. Moyano, M.C. Millan, et al. 2002. Higher alcohols and esters production by Saccharomyces cerevisiae. Influence of the initial oxygenation of the grape must. Food Chemistry, 78: 57-61.
van Dijken J.R., R.A. Weusthuis & J.T. Pronk. 1993. Kinetics of growth and sugar consumption in yeasts. Antonie van Leeuwenhoek, 63: 343-352.
van Hoek P., J.P. van Dijken & J.T. Pronk. 1998. Effect of specific growth rate on fermentative capacity of Baker's yeast. Applied and Environmental Microbiology 64(11): 4226-4233.
van Urk H., W.S.L. Voll, W.A. Scheffers, et al. 1990. Transient-state analysis of metabolic fluxes in Crabtree-positive and Crabtree-negative yeasts. Applied and Environmental Microbiology, 56: 281-287.
Wang L., Y. Xu, G. Zhao, et al. 2004. Rapid analysis of flavor volatiles in apple wine using Headspace Solid-Phase microextraction. Journal of the Institute of Brewing, 110(1): 57-65.
Westall S. 1999. Characteristics of yeast species by their production of volatile metabolites. Journal of Food Mycology, 1: 187-201.
Yoshioka K. & N. Hashimoto. 1981. Ester formation by alcohol acetyltransferase from brewer's yeast. Agricultural and Biological Chemistry, 45: 2183-2190.
Yoshioka K. & N. Hashimoto. 1984. Acetyl-CoA of brewer's yeast and formation of acetate esters. Agricultural and Biological Chemistry, 48: 207-209.
Zironi R., P. Romano, G. Suzzi, et al. 1993. Volatile metabolites produced in wine by mixed and sequential cultures of Hanseniaspora guilliermondii or Kloeckera apiculata and Saccharomyces cerevisiae. Biotechnology Letters, 15: 235-238.
Presentado: 17/05/2011
Aceptado: 20/12/2011
Publicado online: 08/02/2012













