Introducción
En la actualidad muchos ecosistemas dulceacuícolas son susceptibles a padecer invasiones biológicas, debido al incremento desmedido de impactos antrópicos y al cambio climático que pueden llegar a afectar las vías de dispersión y el proceso de invasión en ecosistemas huéspedes (Sutherst et al. 2000). Por tanto, durante los últimos años, la integridad de los sistemas acuáticos se ha visto fuertemente amenazada por la invasión de especies exóticas que alteran la dinámica de poblaciones de especies nativas vulnerables, reprimiéndolas o excluyéndolas directamente mediante la depredación, el pastoreo y la competencia por recursos, o indirectamente cambiando la estructura del hábitat en general (Mack et al. 2000).
En ecosistemas neotropicales, se han reportado especies invasoras de microcrustáceos, como es el caso del cladócero australiano Daphnia lumholtzi (Simões et al. 2009) y del copépodo Mesocyclops ogunnus (Lansac-Tôha et al. 2002) afro-asiático. Dentro de los rotíferos reportados como invasores en el trópico, se encuentran Synchaeta jollyae (Negreiros et al. 2011), originario de Australia, y Kellicottia bostoniensis (Serafim-Junior et al. 2003), esta última perteneciente a la familia Brachionidae y al género Kellicottia (Ahlstrom 1938), que incluye solo dos especies: K. longispina (Kellicott 1879) y K. bostoniensis (Rousselet 1908).
Kellicottia bostoniensis es nativa de Norte América (Edmondson 1959), encontrada por primera vez en un lago ornamental de la ciudad de Boston por Rousselet (1907). Posteriormente, fue reportada en Suecia en 1943 por Carlin (Pejler 1998) y luego en gran parte del continente europeo, como en lagos suecos (Arnemo et al. 1968), Países Bajos (Leentvaar 1961), en Finlandia (Eloranta 1988) y Francia (Balvay 1994).
En 2021, el estudio de Mantovano et al. (2021) reportó 802 registros (celdas) de la especie, de los cuáles 545 (68%) se ubican en la región nativa (Norte América) y 257 (32%) en otras regiones como Europa, África, Asia y Sudamérica, en donde su dispersión inició rápidamente (Mantonavo et al. 2021). Lopes et al. (1997) la reportaron por primera vez habitando un embalse mesotrófico en el estado de Paraná, al sur de Brasil, luego se registró en las regiones Centro-oeste, Sureste y Noreste de Brasil (Bezerra-Neto et al. 2004; Peixoto et al. 2010; Padovesi-Fonseca et al. 2011; Garraffoni & Lourenço 2012; Bomfim et al. 2016, Picapedra et al. 2016; Gomes et al. 2022). De Paggi (2002) la identificó en Argentina y Conde et al. (2002) publicaron el único reporte hallado para Uruguay (Carballo et al. 2022). Se deduce que la inmigración de K. bostoniensis a la región Neotropical, pudo haber estado asociada con el transporte de huevos de resistencia por las aves migratorias (Lopes et al. 1997), por los organismos arrastrados en el agua de lastre de grandes barcos (Reid & Pinto-Coelho 1994), por la introducción junto con peces exóticos utilizados en acuicultura (Peixoto et al. 2010) y por el transporte mediante elementos de pesca deportiva.
Nosotros presentamos el primer registro de Kellicottia bostoniensis para diferentes ecosistemas de Colombia, extendiendo el registro de esta especie hacía el norte de Sudamérica.
Material y métodos
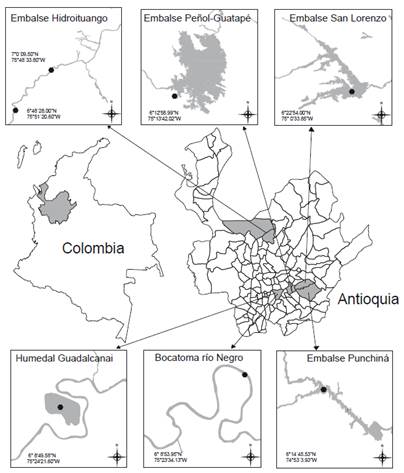
Se realizaron muestreos de plancton en seis ecosistemas acuáticos (un humedal urbano, cuatro embalses y un río) ubicados en la vertiente Caribe, en las cuencas de los ríos Magdalena y Cauca, al noroccidente de Colombia (Fig. 1). Los muestreos fueron realizados en temporadas climáticas diferentes (húmeda, transición y seca) con una temporalidad particular en cada ecosistema. En los ambientes lénticos (registros 1, 3-11) se tomó una muestra integrada de tres profundidades de la zona fótica (zf), subsuperficie, parte central zf y límite inferior zf, y se recolectaron entre 15 y 30 litros de agua por medio de una botella Schindler de 5 litros de capacidad. En el río (registro 2) se tomaron muestras usando un recipiente plástico de 20 L, integrando varias profundidades de acuerdo con la profundidad de la columna de agua hasta completar un volumen total de 60 L. En ambos casos, el volumen fue filtrado en un tamiz certificado con un tamaño de poro de 38 µm y las muestras fueron preservadas con solución Transeau (6 partes de agua destilada, 3 partes de alcohol al 70% y 1 parte de formol al 37%) en proporción 1:1 (Baird et al. 2017). La densidad de K. bostoniensis, se estimó mediante una cámara de Sedgwick-Rafter de 1 mL, en microscopio compuesto bajo un aumento de 100x. Las medidas morfométricas fueron tomadas a 30 individuos seleccionados al azar mediante reglilla ocular micrométrica en un aumento 100x. Kellicottia bostoniensis fue identificada siguiendo las claves taxonómicas de José de Paggi et al. (2020) y Joko (2011).
Resultados y discusión
Kellicottia bostoniensis no había sido reportada anteriormente en el norte de Sudamérica. De acuerdo con el modelo propuesto por Mantovano et al. (2021), los ambientes acuáticos de esta región, como los de Venezuela, Guyana, el norte de Brasil y Colombia no presentarían las condiciones climáticas o limnológicas para la invasión de K. bostoniensis, en particular la altitud y la estacionalidad de la precipitación. Sin embargo, entre 2019 y 2022 K. bostoniensis fue registrada en la zona fótica de diferentes ecosistemas del departamento de Antioquia, occidente de Colombia, como son el humedal urbano Guadalcanai y el río Negro, y los embalses Punchiná, San Lorenzo, El Peñol-Guatapé e Hidroituango (Fig. 1).
Registros donde se reporta K. bostoniensis; se informa localidad, coordenadas, altitud, tipo de muestreador, fecha de colecta, temporada climática, colector, depósito en colección:
Registro 1: Colombia, Antioquia, Rionegro, Humedal Guadalcanai, 6°8’49.58”N 75°24’21.60”W, 2089 m de altitud, recolectado mediante botella Schindler, 03-11-2021, temporada húmeda, K. García, Colección limnología Universidad Católica de Oriente .
Registro 2: Colombia, Antioquia, Rionegro, río Negro, estación Bocatoma, 6°8’53.95”N 75°23’34.13”W, 2125 m, recolectado mediante botella Schindler, 06-06-2022, temporada húmeda, S. Villabona, Colección limnología Universidad Católica de Oriente.
Registro 3: Colombia, Antioquia, San Carlos, embalse Punchiná, Zona de cola, 6°14’45.53”N 74°53’3.93”W, 800 m, recolectado mediante botella Schindler, 31-10-2019, temporada húmeda, Y. López, Colección limnología Universidad Católica de Oriente.
Registro 4. Colombia, Antioquia, San Carlos, embalse Punchiná, Zona de cola, 6°14’45.53”N 74°53’3.93”W, 800 m, recolectado mediante botella Schindler, 19-02-2020, temporada seca, E. Peláez, Colección limnología Universidad Católica de Oriente.
Registro 5: Colombia, Antioquia, San Carlos, embalse Punchiná, Zona de cola, 6°14’45.53”N 74°53’3.93”W, 800 m, recolectado mediante botella Schindler, 26-08-2020, temporada transición lluvias-sequía, E. Peláez, Colección limnología Universidad Católica de Oriente.
Registro 6: Colombia, Antioquia, Alejandría, embalse San Lorenzo, Brazo del río San Lorenzo, 6°22’54.00”N 75°0’33.85”W, 1260 m, recolectado mediante botella Schindler, 24-08-2020, temporada transición lluvias-sequía, E. Peláez, Colección limnología Universidad Católica de Oriente.
Regsitro 7: Colombia, Antioquia, Alejandría, embalse San Lorenzo, 6°22’54.00”N 75°0’33.85”W, 1260 m, recolectado mediante botella Schindler, 21-07-2021, temporada seca, E. Peláez Colección limnología Universidad Católica de Oriente.
Registro 8: Colombia, Antioquia, Alejandría, embalse San Lorenzo, Brazo del río San Lorenzo, 6°22’54.00”N 75°0’33.85”W, 1260 m, recolectado mediante botella Schindler, 01-12-2021, temporada húmeda, E. Peláez, Colección limnología Universidad Católica de Oriente.
Registro 9: Colombia, Antioquia, Peñol, embalse Peñol-Guatapé, 6°12’58.99”N 75°13’42.02”W, 1887 m, recolectado mediante botella Schindler, 07-06-2022, temporada húmeda, S. Villabona, Colección limnología Universidad Católica de Oriente .
Registro 10: Colombia, Antioquia, Sabanalarga, embalse Hidroituango, 6°48’28,00”N 75°51’20.60”W, 400 m, recolectado mediante botella Schindler, 07-11-2021, temporada húmeda, C. Rangel, Colección Limnología Universidad de Antioquia-CLUA.
Registro 11: Colombia, Antioquia, Peque, embalse Hidroituango, 7°0’09.5”N 75°48’33.80”W, 400 m, recolectado mediante botella Schindler, 06-03-2022, temporada seca, K. Huertas, Colección Limnología Universidad de Antioquia-CLUA.
Los especímenes analizados muestran las características típicas de K. bostoniensis, lóriga rígida, cónica, con una compresión dorso-ventral leve, margen anterior con cuatro espinas (dos laterales y dos intermedias), espinas medianas de tamaño diferente o menor, llegando a medir hasta un cuarto del tamaño de la espina de mayor tamaño, espinas laterales finas y relativamente cortas y espina posterior larga y fina (Fig. 2) (Joko 2011). Los especímenes estuvieron dentro de los rangos de medidas para la especie, según lo propuesto por Zhdanova et al. (2019). La longitud total del cuerpo varió entre 330 y 420 µm ( = 370 µm; DE = 32.40 µm, n = 30), la longitud de la espina posterior varió entre 110 y 150 µm ( = 130 µm; DE = 15.81 µm, n = 30), la longitud de la espina anterior varió entre 100 y 140 µm ( = 112 µm DE =17.89 µm, n = 30) y la longitud de la lóriga varió entre 90 y 110 µm ( = 98 µm; DE = 8.37 µm, n = 30).

Figura 2 Kellicottia bostoniensis recolectada en febrero/2020 en el embalse Punchiná, zona riverina, Municipio de San Carlos, Antioquia, en temporada seca. A) Vista general y medidas morfométricas bajo un aumento de 100 x; B) Vista lateral de una hembra portando un huevo; C. Esquema de las medidas tomado y modificado de Zhdanova et al. (2019). LEa = Longitud espina anterior; Lloriga = longitud lóriga; LEP = Longitud espina posterior.
Un espécimen de K. bostoniensis fue registrado a los 2089 m en el humedal Guadalcanai (Registro 1), ubicado en zona urbana del municipio de Rionegro, Oriente antioqueño, en época húmeda. El espejo de agua presentó una alta cobertura de macrófitas acuáticas, baja oxigenación (2.85 mg/L) y una temperatura de 20.70 °C (Quijano-Abril et al. 2022). En ecosistemas lóticos, Gomes et al. (2022) registraron K. bostoniensis en zonas de remanso del río Araguaia, en el estado de Mato Grosso, en Brasil. En este estudio, se halló en zonas de remanso en la cuenca media del río Negro (Registro 2 ), Oriente antioqueño a los 2125 m, durante alta precipitación, con condiciones de alta oxigenación (6.10 - 6.85 mg/L) y temperaturas entre 18.3 y 23.0 °C.
Kellicottia bostoniensis ha sido registrada comúnmente en embalses de otros países de Sudamérica (Mantovano et al. 2021). En Colombia se reporta en este trabajo entre los 400 y 1890 m de altitud (cota) , en los embalses oligo-mesotróficos (Ríos-Pulgarín et al. 2020) Punchiná y San Lorenzo para las tres temporadas (Registros 3 al 8); en el embalse meso-eutrófico (SAG 2021) de El Peñol-Guatapé (en temporada húmeda) (Registro 9), así como para el embalse Hidroituango, en el Cañón del río Cauca, en las temporadas húmeda y seca (Registros 10 y 11). Todos estos embalses presentaron concentraciones de oxígeno entre 5.46 y 8.85 mg/L y temperaturas entre 18.3 a 27.3 °C.
La presencia de K. bostoniensis en diferentes tipos de ecosistemas acuáticos de Colombia se explicaría porque es una especie capaz de adaptarse a una gran variedad de ambientes tropicales, desde sistemas oligotróficos hasta eutróficos (Bezerra-Neto 2001; Landa et al. 2002). Kellicottia bostoniensis ha sido encontrada abundante en sistemas con condiciones anóxicas (< 1 mg/L) y temperaturas superiores a 20 °C (Bezerra-Neto et al. 2004), lo cual demuestra su habilidad para tolerar niveles muy bajos de oxígeno (Stemberger & Gilbert 1987). Es una especie típica de ambientes eutróficos o influenciados por afluentes ricos en materia orgánica (Arnemo et al. 1968; Eloranta 1988; Bezerra-Neto 2001). En general, ha sido encontrada en diferentes ambientes, con frecuencia de ocurrencia y abundancia variada, lo que refleja su potencial invasor (Palazzo 2014).
Es posible que K. bostoniensis continué dispersándose hacia otras cuencas y ecosistemas colombianos, así como hacia otros países de Sudamérica. Investigaciones futuras sobre este rotífero invasor, deben no solo identificar los sistemas que colonizan, sino también identificar las variables que determinan su establecimiento exitoso y su interacción con especies nativas relacionadas filogenéticamente, como se ha hecho en otros países. Finalmente, es importante tener atención especial en el transporte de individuos hacia otros ecosistemas por medio de los aparejos y materiales de muestreo utilizados en las campañas de recolección de muestras de agua y del uso de artes de pesca en actividades como pesca deportiva. La introducción de esta especie puede alterar la estructura de la comunidad zooplanctónica y de las redes tróficas acuáticas, disminuir la producción de biomasa y modificar la concentración de nutrientes en los sistemas donde habita.












 uBio
uBio