Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Acta Médica Peruana
versión On-line ISSN 1728-5917
Acta méd. peruana v.24 n.3 Lima sep./dic. 2007
Artículo original
Inmunopatología de sujetos sanos de un área endémica para pénfigo foliáceo en Perú: Estudio comparativo con familiares
Immunopathologic characterization of healthy subjects in an endemic area for pemphigus foliaceus: Comparative study with relatives.
Willy Ramos1,2, Alex G. Ortega-Loayza1,3, Jorge Hancco1, Ericson Gutiérrez1, Jorge Hurtado1, Gerardo Jiménez4, Gerardo Ronceros1, Isabel Rojas5, Carlos Galarza1,6.
1. Instituto de Investigaciones Clínicas de la Universidad Nacional Mayor de San Marcos. Lima, Perú.
2 Centro de Salud Villa María del Perpetuo Socorro. DISA V Lima Ciudad. Lima, Perú.
3 Departament of Medicine. The University of North Carolina at Chapel Hill. USA.
4 Servicio de Dermatología. Hospital Regional de Pucallpa. Ucayali, Perú
5 Puesto de Salud de Pueblo Libre. DISA, Ucayali. Ucayali, Perú.
6 Servicio de Dermatología. Hospital Nacional Dos de Mayo. Lima, Perú. Profesor de la UNMSM
RESUMEN
Introducción: el pénfigo foliáceo endémico (PFE) ha sido descrito a principios de los años 50 en la selva peruana. En el 2006, Ortega y col. reportaron la presencia de anticuerpos anti-desmogleina 1 en Pueblo Libre, Ucayali. Sin embargo, no existen reportes inmunológicos sobre los familiares de pacientes con PFE en la zona.
Objetivos: comparar las características inmunopatológicas de los sujetos sanos de Pueblo Libre (Campo Verde-Ucayali) endémico para pénfigo foliáceo, con familiares sanos de pacientes con PFE y controles sanos de áreas no endémicas.
Material y métodos: estudio prospectivo y multicéntrico realizado de junio a agosto del 2006 que incluyó a 41 sujetos sanos de la comunidad de Pueblo Libre, 11 familiares de pacientes con PFE y 20 sujetos sanos de áreas no endémicas de la enfermedad de los que se obtuvo muestras de sangre para la realización del estudio inmunopatológico (ELISA para anticuerpos anti desmogleína 1 y anti desmogleína 3) comparándose las características de cada grupo de investigación. Para fijar los valores de corte se realizó la estandarización del ELISA usando el análisis de características operativas del receptor (ROC).
Resultados: en Pueblo Libre se encontró una prevalencia de anticuerpos anti desmogleína 1 de 46,3%. El patrón predominante fue el IgG2 (62,5%) y el IgG1 (56,3%). En el 31,7% se detectó anticuerpos anti-desmogleína 3. Existió alta correlación entre los valores índice de anticuerpos anti desmogleína 1 y anti desmogleína 3 (r=0,76), significativa a un nivel α=0,01. Para los familiares de los pacientes con PFE, el 45,5% fueron positivos para anticuerpos anti-desmogleína 1 con un patrón predominante IgG1 (63,6%) e IgG2 (54,5%). Se detectó anticuerpos anti-desmogleína 1 en el 10 % de sujetos sanos de áreas no endémicas; no se detectó anticuerpos anti desmogleína 3 en este grupo.
Conclusiones: las personas sanas expuestas a factores ambientales de los focos endémicos de PFE y los familiares de pacientes desarrollan anticuerpos no patogénicos anti desmogleína 1 y 3 con características inmunopatológicas similares.
Palabras clave: pénfigo foliáceo endémico, sujetos sanos de áreas endémicas, familiares de pacientes con PFE.
ABSTRACT
Introduction: endemic pemphigus foliaceus (PFE) has been described at the beginning of the 50s in the peruvian forest. In 2006,Ortega & col. reported the presence of desmoglein 1 antibodies in Pueblo Libre, Ucayali. Nevertheless, immune reports does not exist on patients relatives with PFE in the zone.
Objetives: to compare the immunopathologic profiles of healthy subjects from Pueblo Libre (an area in Ucayali, endemic for pemphigus foliaceus), with healthy relatives of patients with endemic pemphigus foliaceus (EPF) and healthy controls from non-endemic areas.
Materials and methods: this is a prospective multicentric study performed from June to August 2006. The sample consisted of 41 healthy subjects from the Pueblo Libre community, 11 relatives of EPF patients and 20 healthy subjects from non-endemic areas. Blood samples were obtained for immunopathologic studies (ELISA technique for antibodies against desmoglein-1 and desmoglein- 3). The immunopathologic profiles of each group were compared. Standardization of ELISA was performed using the analysis of receptor operative characteristics (ROC) to find appropriate cut-off values.
Results: in Pueblo Libre, the prevalence of antibodies against desmoglein-1 was 46,3%. The predominant pattern was 56,3% for IgG1 and 62,5% for IgG2. Antibodies against desmoglein-3 were found in 31,7% of the sample. A high correlation was found between the index values of antibodies against desmoglein-1 and desmoglein-3. (r=0.76); this is statistically significant, with an alpha = 0,001. The frequency of antibodies against desmoglein-1 was 45,5% in the relatives of EPF patients; the predominant pattern was 63,6% for IgG1 and 54,5% for IgG2. Antibodies against desmoglein-1 were detected in two healthy subjects from non-endemic areas; antibodies against desmoglein-3 were not detected.
Conclusion: healthy subjects who are exposed to environmental factors in a focus of endemic pemphigus foliaceus and the relatives of patients with EPF develop non-pathogenic antibodies against desmoglein-1 and -3 with similar immunologic profiles.
Key words: endemic pemphigus foliaceus, EPF, healthy subjects from endemic areas, relatives of EPF patients.
INTRODUCCIÓN
El pénfigo foliáceo endémico (PFE) es una enfermedad ampollar autoinmune endémica en áreas de la amazonía peruana1-4. La enfermedad histológicamente se caracteriza por acantolisis subcorneal e inmunológicamente por la presencia de autoanticuerpos circulantes IgG4 contra la glicoproteína desmosomal del grupo de las caderinas identificada como desmogleína 1 del epitelio escamoso de la piel5-9.
La producción de anticuerpos estaría vinculada a la presencia de antígenos ambientales existentes en los focos endémicos los cuales desencadenarían reacción cruzada con las células de la epidermis5-12. Adicionalmente, se sabe que sujetos sanos expuestos a la ecología de los focos de PFE desarrollan anticuerpos anti-desmogleína 1 como un trastorno inmunológico previo al desarrollo de la enfermedad la cual se desencadenaría en individuos genéticamente predispuestos por la presencia de alelos HLA DRB1*102, 0404 y 1406 5,7,13,14.
El área mejor estudiada en Perú es el departamento de Ucayali en donde Galarza y col3. encontraron un foco de PFE en el distrito de Campo Verde (70° longitud oeste, 10° latitud sur) con una tasa de prevalencia de 4,3 casos por 10 000 habitantes, la aparición de 1-3 casos nuevos por año y un registro de 17 casos desde el año 2001 (Hospital Regional de Pucallpa y Hospital de Apoyo N° 2 de Yarinacocha).
En el distrito de Campo Verde se ubica la comunidad de Pueblo Libre (Localizada a 44 Km. de la ciudad de Pucallpa) en donde Ortega y col reportaron la presencia de anticuerpos anti-desmogleína 1 en 31,7% (13/41) de sujetos sanos15. Los autores en el año 2005 realizamos un censo epidemiológico en Pueblo Libre encontrando que la población total de esta comunidad estaba compuesta por 115 personas.
Si bien es cierto que las características clínicas y epidemiológicas de los pacientes han sido determinadas, se encuentran disponibles pocos datos en sujetos sanos de áreas endémicas de nuestro país y no se tiene datos publicados de la presencia de anticuerpos anti desmogleína 1 y 3 en familiares de pacientes.
El presente estudio tiene por objetivo comparar las características inmunopatológicas de los sujetos sanos de Pueblo Libre (Campo Verde-Ucayali) endémico para pénfigo foliáceo, con familiares sanos de pacientes con pénfigo foliáceo endémico (PFE) y controles sanos de áreas no endémicas mediante la detección con ELISA de anticuerpos IgG anti desmogleína 1 y 3, así como realizar un seguimiento luego de 3 años en los sujetos sanos de Pueblo libre estudiados por Ortega-Loayza.
MATERIAL Y MÉTODOS
Diseño
Estudio prospectivo, comparativo y multicéntrico, realizado de junio a agosto del 2006 en los departamentos de Ucayali y Lima. La muestra estuvo constituida por tres grupos de investigación:
Grupo 1: conformado por 41 sujetos sanos de la comunidad de Pueblo Libre (distrito de Campo Verde, endémico para pénfigo foliáceo) a quienes se les había determinado previamente la presencia de anticuerpos anti desmogleína 1 (2003).
Grupo 2: conformado por 11 familiares sanos de pacientes con pénfigo foliáceo endémico que recibían tratamiento en el Servicio de Dermatología del Hospital Regional de Pucallpa y en el Hospital Nacional Dos de Mayo (Referidos de la ciudad de Pucallpa).
Grupo control: conformado por 20 sujetos sanos (Donantes voluntarios de sangre) de áreas no endémicas de la enfermedad (Ciudades de Pucallpa, Chachapoyas y Lima).
Técnica y método
Inicialmente, los pobladores de Pueblo Libre (Figuras 1 y 2), familiares de pacientes y donantes de sangre de áreas no endémicas fueron evaluados por un especialista en Dermatología para confirmarse la ausencia de enfermedades ampollares. Luego se obtuvo muestras de sangre para la realización del estudio inmunopatológico mediante ELISA para anticuerpos anti-desmogleína 1 (IgG total y subclases)y anti-desmogleína 3 (IgG total) de acuerdo a la técnica descrita por Ishi y Amagai16-17.

Inmunoensayos y recolección de muestras
Las muestras fueron conservadas a – 20° C siendo almacenadas inicialmente en el Instituto de Investigaciones Clínicas de la Universidad Nacional Mayor de San Marcos (Lima, Perú) y luego transportadas según protocolo a los Laboratorios de Investigación Dermatológica de la Universidad de Carolina del Norte de Chapel Hill (U.S.A) donde se realizó su procesamiento y lectura.
Procesamiento de muestras
Para los estudios de ELISA se generó formas recombinantes de DSG 1 y DSG 3 mediante su producción en baculovirus16. Para fijar los valores de corte se realizó la estandarización de la prueba con muestras de sangre de sujetos sanos y pacientes con pénfigo foliáceo endémico de Brasil y Perú usando el análisis de características operativas del receptor (ROC). Los resultados fueron expresados como valores índice de acuerdo a lo reportado por Amagai y col. en el año 199917:
Cálculo del valor índice para ELISA:
Valor = (D.O muestra evaluada) (D.O control negativo) x 1000
índice (D.O control positivo) (D.O control negativo)
D.O = Densidad óptica.
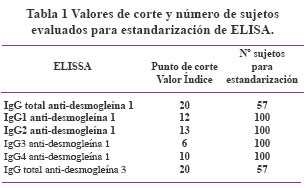
En la Tabla 1 se puede apreciar los valores de corte y número de sujetos evaluados para estandarización de ELISA.
Análisis estadístico
La estadística descriptiva se realizó con el programa SPSS versión 13.0. Se usó inicialmente estadística univariada (Descriptiva), luego estadística inferencial con las pruebas chi cuadrado y análisis de varianza (ANOVA) de una vía. Para correlacionar los valores de anticuerpos anti desmogleína 1 y anti desmogleína 3 (ELISA) se calculó el coeficiente de correlación de Pearson (r).
Aspectos éticos
Con relación a los aspectos éticos, los sujetos aceptaron enrolarse voluntariamente en el estudio y firmaron un consentimiento informado respetándose sus derechos de acuerdo a la Declaración de Helsinki.
RESULTADOS
Análisis en sujetos sanos de Pueblo Libre
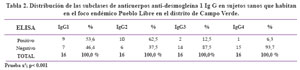
- Anticuerpos IgG (total y subclases) anti-desmogleína 1
En un primer análisis realizado entre febrero y marzo del 2003 se evaluó a 41 sujetos sanos encontrándose que 13 (31,7%) fueron positivos para anticuerpos anti desmogleína 1 mediante ELISA. Luego de 3 años, 6 pacientes que no presentaban anticuerpos han virado a positivos (14,6 %) siendo la prevalencia final de 46,3 % y en 2 sujetos evaluados se encontró un valor índice mayor de 100 (Fuertemente positivo). De los 19 positivos (19/41), se encontraron disponibles para el análisis 16 (Tabla 2). El patrón predominante en las subclases de Inmunoglobulina G fue el IgG2 (62,5 %) y el IgG1 (56,3 %) los cuales son considerados no patogénicos. Un sujeto sano fue positivo para IgG4 y para las otras las subclases de IgG.
- Anticuerpos IgG anti-desmogleína 3
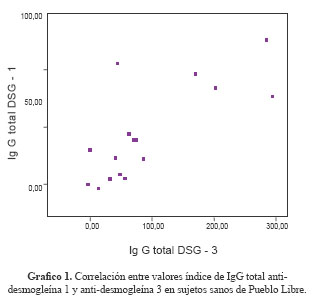
En 13 personas sanas (31,7 %) se detectó anticuerpos anti-desmogleína 3 los cuales se expresaron simultáneamente con los anticuerpos anti-desmogleína 1 en 10 personas (62,5 %); cuatro sujetos sanos (30,8 %) presentaron un valor índice mayor de 100. Existió alta correlación entre los valores índice de IgG total anti-desmogleína 1 y anti-desmogleína 3 (r = 0,76), la cual fue significativa a un nivel α = 0,01. Ver Gráfico 1.
Análisis en sujetos sanos familiares de pacientes con PFE
- Anticuerpos IgG (total y subclases) anti-desmogleína 1
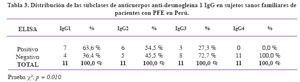
Para los sujetos sanos familiares de los pacientes con PFE (n = 11), 5 fueron positivos para anticuerpos antidesmogleína 1 (45,5 %). Los familiares estuvieron compuestos por 2 grupos: los que vivían en áreas endémicas de PFE (n = 6) y los de áreas no endémicas (n = 5); no existiendo diferencia significativa en los valores índice de anticuerpos entre ambos grupos. Las personas sanas con parentesco de primer grado con los pacientes con PFE fueron los que expresaron con mayor frecuencia anticuerpos anti-desmogleína 1 (60,0%) seguidos por los de segundo grado (40,0 %).
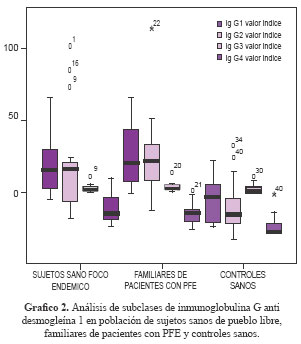
El análisis de las subclases de IgG mostró un patrón predominante IgG1 (63,6 %) e IgG2 (54,5 %); en ningún sujeto sano se expresó IgG4 . Ver Tabla 3 y Gráfico 2.
- Anticuerpos IgG anti-desmogleína 3
En 6 personas sanas (54,5 %) se detectó anticuerpos anti desmogleína 3 que se expresaron simultáneamente con los anticuerpos anti-desmogleína 1 en 4 personas (36.4 %); de los positivos, 4 correspondían a áreas endémicas y 2 a áreas no endémicas. Sólo 1 sujeto presentó un valor índice mayor de 100. Al correlacionarse los valores índice de anticuerpos anti-desmogleína 1 y 3, no se encontró correlación estadísticamente significativa para los familiares de áreas endémicas (r = 0,75; p = 0,145) ni para los de áreas no endémicas (r = - 0,77; p = 0,071).
Análisis en sujetos sanos de áreas no endémicas
Se evaluó a 20 sujetos sanos de áreas no endémicas de Lima, Chachapoyas (Amazonas) y Pucallpa (Ucayali), detectándose anticuerpos anti-desmogleína 1 en 2 de ellos (10,0 %) y anti desmogleína 3 en ninguno de los sujetos. Los valores índice pueden observarse en la Tabla 4 y Gráfico 2.
DISCUSIÓN
El presente estudio muestra que la presencia de anticuerpos anti-desmogleína 1 es un fenómeno frecuente en sujetos sanos de focos de PFE así como en familiares sanos de pacientes. En Pueblo Libre, área endémica de PFE, en el lapso de tres años de seguimiento la prevalencia aumentó de 31,7 % a 46,3 % probablemente por acción de factores ambientales. En ambos grupos se presentó una respuesta no patogénica IgG1 e IgG2, predomi-nantemente IgG2 en sujetos procedentes del área endémica de Pueblo Libre y principalmente de tipo IgG1 en familiares de pacientes. De este modo se demuestra la heterogenicidad de las subclases de inmunoglobulina G anti desmogleína 1 de acuerdo a lo descrito por Warren5,18 en sujetos sanos. El análisis de los familiares de pacientes con PFE mostró que éstos presentaron valores índices mayores que los sujetos sanos de el área endémica, pero la prevalencia de anticuerpos anti desmogleína 1 fue similar en ambos (45,5 % vs 46,3 %).
De manera análoga a lo descrito por Hilario-Vargas para áreas endémicas de Brasil, nosotros encontramos que los sujetos sanos de Pueblo Libre presentaron anticuerpos antidesmogleína 3 con una prevalencia del 31,7 % similar a la reportada en Lima o Verde-Brasil (36,0%)19.
Los argumentos presentados por Hilario-Vargas a favor de un factor desencadenante ambiental de anticuerpos antidesmogleína 3 en los focos de PFE son la prevalencia de anticuerpos anti-desmogleína 3 similar a la de anticuerpos anti-desmogleína 1 y que la proporción de sueros de sujetos normales positivos se incrementa con la proximidad a los focos endémicos19. Adicionalmente, se ha reportado en Brasil una forma endémica de pénfigo vulgar20 y que una fracción de pacientes con pénfigo foliáceo endémico y no endémico expresan simultáneamente anticuerpos anti-desmogleína 1 y 321. Una hipótesis que desestimaría la inducción ambiental de anticuerpos anti-desmogleína 3 sería que debido a la similitud entre ambas caderinas desmosomales (DSG-1 y DSG-3) podría existir reactividad cruzada para los anticuerpos18,22.
Nosotros encontramos que las prevalencias de ambos anticuerpos son similares en el área endémica estudiada y existe fuerte correlación lineal positiva entre sus valores índices (Gráfico 1), relación que podría existir en el caso reactividad cruzada pero que debería repetirse en los familiares de los pacientes. Por otro lado, existe controversia acerca de la prevalencia real de anticuerpos anti-desmogleína 3 en familiares sanos de pacientes con PFE puesto que la mayoría de estos en nuestro estudio procedían de áreas endémicas por lo que son susceptibles de haber recibido influencia ambiental, sin embargo este fenómeno también fue observado en observado en familiares sanos de áreas no endémicas.
A diferencia de los sujetos de Pueblo Libre, los familiares sanos de pacientes (tanto de áreas endémicas como no endémicas) no mostraron correlación significativa entre los valores índice de ambos anticuerpos. Esto es un argumento en contra de la teoría de la reactividad cruzada de anticuerpos puesto que si ésta existiese, deberíamos encontrar correlación para los valores índice de manera similar que para los sujetos sanos de Pueblo Libre lo que estaría a favor del argumento que el desarrollo de anticuerpos anti-desmogleína 3 seguiría un patrón similar al de los anticuerpos anti-desmogleína 1: inducido por factores ambientales.
Se presentaron anticuerpos anti-desmogleína 1 en el 10% de sujetos sanos de áreas urbanas no endémicas para pénfigo foliáceo los cuales procedían de Pucallpa. Esto puede atribuirse a la cercanía de esta ciudad con las áreas endémicas de PFE (44 Km); de este modo, las personas que viven en áreas no endémicas se desplazan a áreas rurales con fines agrícolas o de comercio siendo expuestos por periodos transitorios a los factores ambientales induciendo la producción de anticuerpos, lo cual concuerda con lo descrito por Ortega y col. para personas sanas de Pucallpa en el año 200315.
En conclusión, las personas sanas expuestas a la factores ambientales de los focos endémicos de pénfigo foliáceo y los familiares de pacientes desarrollan anticuerpos no patogénicos anti-desmogleína 1 y 3 con prevalencia y características inmunopatológicas similares siendo la respuesta más intensa en los familiares de pacientes. Esto explica la presencia de casos de pénfigo en sujetos de áreas endémicas que previamente habían desarrollado anticuerpos anti-desmogleína 1 cuando se encontraban sanos así como la presencia de casos familiares de la enfermedad23-30.
AGRADECIMIENTOS:
Al Dr. Luis A. Díaz de la Universidad de Carolina del Norte de Chapel Hill por su apoyo en el procesamiento de muestras para la caracterización inmunopatológica de los sujetos sanos de áreas endémicas de PFE y familiares de pacientes.
REFERENCIAS BIBLIOGRÁFICAS
1. Heimgartner E, de Heimgartner V. Experiencias en enfermedades dermatológicas endémicas en la selva peruana: Leishmaniasis y pénfigo foliáceo endémico. Med Cut ILA 1976; 1: 1-6. [ Links ]
2. Castillo A, Maguiña C. Pénfigo foliáceo variedad Fuego Salvaje en la selva peruana. Bol Soc Per Med Int .1993; 6: 65-7. [ Links ]
3. Galarza C, Ronceros G, Mendoza D, Sánchez G, Vilcarromero M, Ráez E y col. pénfigo foliáceo endémico en el departamento de Ucayali, Perú. Reporte de 16 casos. An Fac Med Lima. 2002; 63: 19-24. [ Links ]
4. De Amat F, Diaz J. Pénfigo foliáceo endémico en las comunidades de Vista Alegre y San Francisco (Ucayali, Perú) Octubre 2000 - septiembre 2001. Tesis Universidad Nacional Mayor de San Marcos 2001.
5. Warren S, Lin MS, Giudice G, Hoffman R, Hans-Filho G, Aoki V, Rivitti E, Santos V, Diaz LA. The pevalence of antibodies against desmoglein 1 in endemic pemphigus foliaceus in Brazil. N Eng J Med .2000; 343 : 23-30. [ Links ]
6. Emery DJ. Diaz LA, Fairley JA, López A, Taylor AF, Giudice GP. Pemphigus foliaceus and penphigus vulgaris autoantibodies react with the extracellular domain of desmoglein 1. J Invest Dermatol 1995: 104:323-328. [ Links ]
7. Moraes ME, Fernandez-Viria, Lazaro A, Diaz LA, Hans- Filho GH, Friedman H, et al. An epitope in the third hypervariable region of the DRB1 gene is envolved in the susceptibility to endemic pemphigus foliaceus (Fogo Selvagem) in three differents brazilian populations. Tissue Antigens. 1997; 49: 35-40. [ Links ]
8. Sampaio SA, Rivitti EA, Aoki V, Diaz LA. Brazilian pemphigus foliaceus, endemic pemphigus foliaceus, or fogo selvagem (Wild Fire). Dermatol Clinics 1994;12: 765-76. [ Links ]
9. Friedman H, Campbell I, Rocha-Alvarez R, Ferrari I, Coimbra CE, Moraes JR, et. al. Endemic pemphigus foliaceus (fogo selvagem) in native americans from Brasil. J Am Acad Dermatol 1996; 107: 68-75. [ Links ]
10. Diaz LA, Sampaio SA, Rivitti EA,Martins CR, Cunha PR , Lombardi C , Almeida FA, Castro RM, Macca
ML, Lavrado C. Endemic pemphigus foliaceus (fogo selvagem). II. Current and historic epidemiologic studies. J Invest Dermatol 1989; 92: 4-12.
11. Eaton DP, Diaz LA, Hans-Filho G, dos Santos VD, Aoki V, Friedman H, et al. Comparison of black fly species (Diptera Simullidae) on an amerindian reservation with a high prevalence of Fogo Selvagem to neighboring disease of free sites in the States of Matto Grosso do Sul, Brazil. The Cooperative Group on Fogo Selvagem Research . J Med Entomol 1998; 35: 120-31. [ Links ]
12. Lombardi C, Borges PC, Chaul A, Sampaio SA, Rivitti EA, Friedman H, et al . Enviromental risk factors in endemic pemphigus foliaceus (fogo selvagem). The Cooperative Group on Fogo Selvagem Research. J Invest Dermatol 1992; 98: 847-50. [ Links ]
13. Kallel Sellami M, Ben Ayed M, Mouquet H et al. Anti-desmoglein 1 Antibodies in Tunisian healthy subjects: arguments for the role of environmental factors in the courrence of Tunisan pemphigus foliaceus. Clin Exp Immunol 2004; 137:195-200. [ Links ]
14. Moraes JR, Moraes ME, Fernadez-Viria M, Diaz LA, Friedman H, Campbell IT, et al. HLA antigens and risk for development of pemphigus foliaceus (fogo selvagem) in endemics areas of Brazil. Inmunogenetics 1991; 33: 388-91. [ Links ]
15. Ortega A, Ramos W, Elgart G, Bouman P, Jiménez G, Ávila J, Rojas I, Vilcarromero M, Hurtado J, Lindo G and Galarza C. Antibodies against desmoglein 1 in healtly subjects in endemic and nonendemic areas of pemphigus foliaceus (fogo selvagem) in Peru. Int J Dermatol 2006; 45: 538 – 42. [ Links ]
16. Ishii K, Amagai M, Hall RP, Hashimoto T, Takayanagi A, Gamou S, Shimizu N and Nishikawa T. Characterization of Autoantibodies in pemphigus using antigen-specific enzyme-linked immunosorbent assay with baculovirus-expressed recombinant desmogleins. J Immunol 1997; 159: 2010-17. [ Links ]
17. Amagai M, Komai A, Hashimoto T, Shirakata Y, Hashimoto K, Yamada T, Kitajima Y, Ohya K, Iwanami H, and Nishikawa T. Usefulness of enzyme-linked immunosorbent assay using recombinant desmogleins 1 and 3 for serodiagnosis of pemphigus. Br J Dermatol 1999; 140: 351-357. [ Links ]
18. Warren SJP, Arteaga LA, Rivitti EA, Aoki V, Hans-Filho G, Qaquish BF, Lin MS, Giudice GJ, Diaz LA. The role of IgG subclass switch in the pathogenesis of fogo selvagem. J Invest Dermatol 2003;120:104-8. [ Links ]
19. Hilario-Vargas J, Dasher DA, Li N, Aoki V, Hans-Filho G, dos Santos V, Qaquish BF, Rivitti E, Diaz LA. Prevalence of anti-desmoglein 3 in endemics regions of fogo Selvagem in Brasil. J Invest Dermatol 2006; 126: 2044 - 48. [ Links ]
20. Rocha-Alvarez R, Campbel IP, Friedman H, Aoki V, Diaz LA. Aspectos nao usuais de penfigo vulgar em areas endemicas de penfigo foliaceo endemico. 50° Congresso da Sociedade Brasileira de Dermatología. Belem, Para, Brazil. 1995.
21. Arteaga LA, Prisayanh PS, Warren S et al. A subset of pemphigus foliaceus patients exhibits pathogenic autoantibodies against desmoglein 1 and desmoglein 3. J Invest Dermatol 2002; 118: 806-11. [ Links ]
22.Amagai M. Non-pathogenic anti-desmoglein 3 IgG autoantibodies in Fogo Selvagem. J Invest Dermatol. 2006; 126:1931-2. [ Links ]
23. Paes-Leme C. Contribucao ao estudo do Tokelau. Doctoral thesis. Rio de Janeiro, Brazil: Facultade de Medicina 1903.
24. Hans-Filho G, dos Santos V, Katayama JH, Aoki V, Rivitti EA, Sampaio SA, Friedman H, Moraes ME, Eaton DP, Lopez AL, Hoffman RG, Fairley JA, Giudice GJ, Diaz LA. An active focus of high prevalence of fogo selvagem on an Amerindian reservation in Brazil. J Invest Dermatol 1996; 107: 68-75. [ Links ]
25. Aoki V, Millikan RC, Rivitti EA, Hans-Filho G, Eaton DP, Warren S, Ning L, Hilario-Vargas J, Hoffman RG, Diaz LA. Environmental Risk Factors in endemic pemphigus foliaceus (fogo selvagem). J Investig Dermatol Symp Proc 2004; 9: 34-40. [ Links ]
26. Hans-Filho G, Aoki V, Rivitti EA, Eaton DP, Lin MS, LA Diaz. Endemic pemphigus foliaceus (fogo selvagem)-1998. Clin Dermatol 1999;17:225–35. [ Links ]
27. Quinteiro AM, Rocha-Alvarez R, Friedman H, Campbel I. The profile of fogo selvagem (endemic pemphigus foliaceus) at the University Hospital of Brasilia–Brazil. Epidemiological and clinical considerations. Int J Dermatol 2005; 44: 293–98. [ Links ]
28. Aoki V, Rivitti EA, Ito LM, Hans-Filho G, LA Diaz. Perfil histórico da imunopatogenia do pênfigo foliáceo endêmico (fogo selvagem). Historical profile of the immunopathogenesis of endemic pemphigus foliaceus (fogo selvagem). An Bras Dermatol 2005; 80: 287-92. [ Links ]
29. Chiossi MP, Roselino AMF. Endemic pemphigus foliaceus (fogo selvagem): a series from the northeastern Region of the state of São Paulo, Brazil, 1973-1998. Rev Inst Med Trop S Paulo 2001; 43: 59-62. [ Links ]
30. Chagas ACF, Ivo ML, Honer MR, Correa R Filho. Situação do pênfigo foliáceo endêmico em Mato Grosso do Sul, Brasil, 1990-1999. Rev Latinoam Enfermagem 2005; 13: 274-6. [ Links ]
MENCIONES
El mencionado estudio fue galardonado con el Premio a la Investigación en Medicina 2006: Abeefe Bristrol Myers squibb
CORRESPONDENCIA
Willy César Ramos Muñoz
willy_investcl@yahoo.es
Recibido: 01/07/07
Aprobado: 31/08/07
Evaluación: Sistema de Arbitraje por pares