Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Acta Médica Peruana
versión On-line ISSN 1728-5917
Acta méd. Peru vol.34 no.4 Lima oct./dic. 2017
ARTÍCULO DE REVISIÓN
Interpretación de las pruebas usadas para diagnosticar la infección por virus de la inmunodeficiencia humana
Interpretation of rapid tests for diagnosing the infection caused by the human immunodeficiency virus
Ricardo Iván Álvarez-Carrasco1a
1 Instituto Nacional Materno Perinatal.
a Médico patólogo clínico
RESUMEN
Desde la aparición de las primeras pruebas de laboratorio que diagnosticaban la infección por el virus de la inmunodeficiencia humana, hace más de treinta años, el avance tecnológico ha permitido contar con una diversidad de pruebas cada vez más sensibles y específicas, cuya adecuada interpretación en la práctica médica diaria es indispensable para el manejo terapéutico de los pacientes. El objetivo de esta revisión es difundir la apropiada comprensión interrelación de los resultados de aquellas pruebas de uso común actualmente.
Palabras clave: Pruebas de competencia de laboratorios; VIH; Diagnóstico (fuente: DeCS BIREME).
ABSTRACT
Since the advent of the first laboratory tests for diagnosing the human immunodeficiency virus infection more than thirty years ago, technological advances have allowed us to have more sensitive and specific tests, and their adequate interpretation in clinical practice is indispensable for proper management of patients. The purpose of this review is to describe the adequate understanding and relationships of the results of all commonly used tests.
Keywords: Laboratory proficiency testing; HIV; Diagnosis (source: MeSH NLM).
INTRODUCCIÓN
En 1981, en los Estados Unidos de América se reportaron los primeros casos de una enfermedad desconocida que producía una intensa inmunodepresión en varones homosexuales, quienes padecían de infecciones oportunistas (neumonía por Neumocystis carinii entre otras) y/o neoplasias malignas poco frecuentes (sarcoma de Kaposi) (1).
En 1983, el doctor Luc Montagnier del Instituto Pasteur de París, reportó el descubrimiento del agente etiológico que llamó virus asociado a linfadenopatía (LAV) (2), denominación que coexistió temporalmente con la propuesta por el médico estadounidense Robert Gallo: HTLV-III. En 1987 un subcomité de la Organización Mundial de la Salud (OMS) propuso el nombre virus de la inmunodeficiencia humana (VIH) (1).
En 1985 se dispuso de la primera prueba diagnóstica por el método de la inmunoabsorción ligado a enzimas (ELISA) (3-6), en 1987 se contó con el Western Blot (WB) (4,7), y en 1989 con la primera prueba para detectar la antigenemia p24 (4). La primera generación de ELISA tenía una especificidad relativamente baja (95-98%) que mejoró progresivamente con la segunda generación en 1987 (3), la 3ra en 1994 (3) y la 4ta en 2000 (5).
En el Perú, el primer caso se presentó en 1983 (7); a fines de 1999 la Organización Panamericana de la Salud (OPS) estimaba que los peruanos viviendo con VIH-SIDA eran 44 200 (8). En 1985 el Navy Medical Research Institute Detachment (NAMRID), un organismo de investigación de la armada norteamericana, introdujo en nuestro país las pruebas diagnósticas, instalando laboratorios en Lima e Iquitos, en los que se efectuaba la prueba de ELISA, y que permitió desarrollar el primer gran estudio de prevalencia del VIH (7,8).
En 1988 la responsabilidad del tamizaje del VIH se transfirió al Ministerio de Salud, que constituyó una red de laboratorios encabezada por el Instituto Nacional de Salud (INS) (7,8); a partir de 1990 se comenzó a difundir el WB y en la segunda mitad de esa década ocurrió lo propio con la inmunofluorescencia indirecta (IFI) (9). Luego se introdujeron otras pruebas que mejoraron la performance diagnóstica, haciendo absolutamente indispensable su conocimiento y adecuada interpretación en la práctica médica diaria.
CLASIFICACIÓN, ALGORITMO E INTERPRETACIÓN DE LAS PRUEBAS DIAGNÓSTICAS
El uso de pruebas de laboratorio es indispensable para el diagnóstico de la infección por VIH, puesto que ninguna manifestación clínica es lo suficientemente específica; sin embargo, estas pruebas no permiten determinar si el individuo se encuentra en el estadio del síndrome de inmunodeficiencia adquirida (SIDA), además tienen limitante de que, al ser estandarizadas in vitro, aunque se ejecuten en condiciones óptimas, se pueden obtener resultados que no se condigan con la realidad.
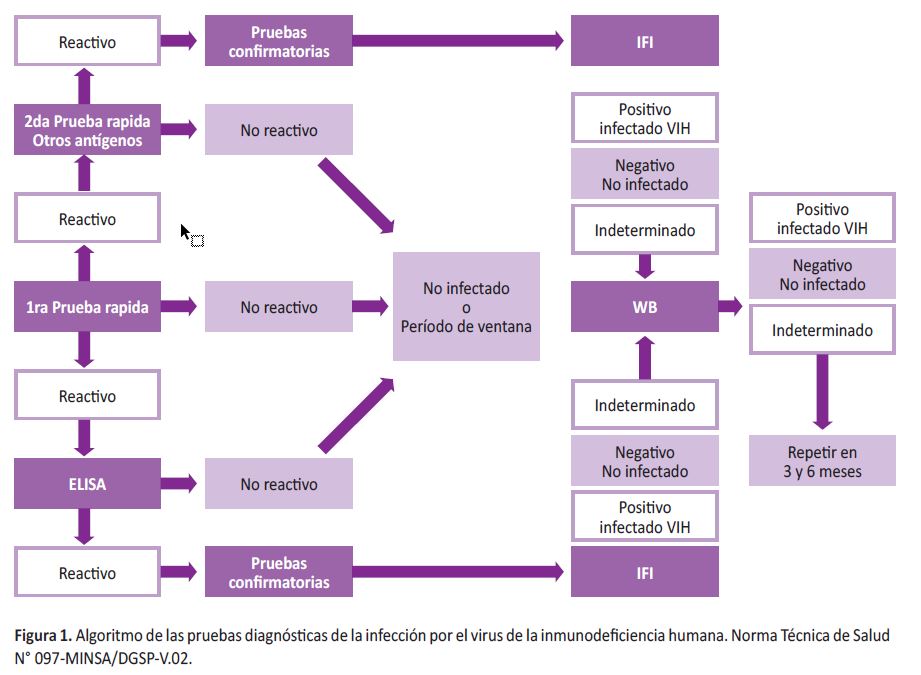
Su adecuada interpretación requiere de un conjunto de conocimientos teóricos y prácticos, que se deben correlacionar con el algoritmo establecido en la Norma Técnica de Salud N° 097-MINSA/DGSP-V.02 (Figura 1) (10).
La infección por VIH ocasiona una respuesta inmunológica luego de un periodo inicial de intensa replicación viral, en el que aparecerán altos niveles de ARN y antígeno p24, que son seguidos por el incremento de los anticuerpos anti-VIH, primero del tipo Ig M y luego del tipo Ig G (11).
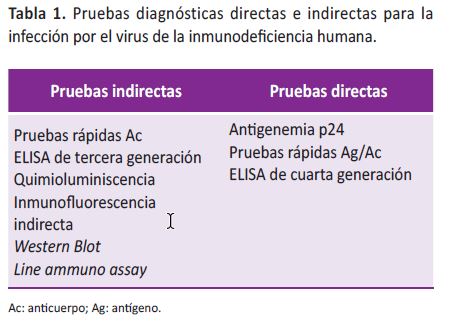
Las pruebas más difundidas hacen diagnósticos indirectos, pues sólo muestran la respuesta inmunitaria del infectado (pruebas rápidas Ac, ELISA de tercera generación, IFI y WB) (11); las que emplean métodos directos muestran la presencia del virus o sus constituyentes (pruebas rápidas Ag/Ac, antigenemia p24 (11) y ELISA de cuarta generación) (10) (Tabla 1).
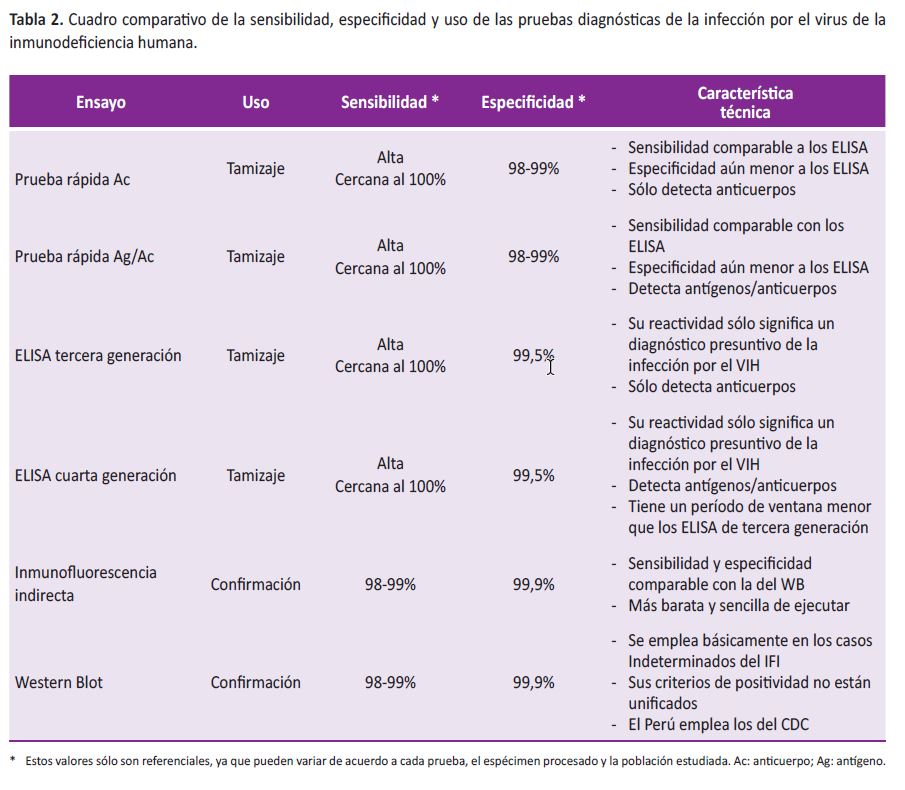
La sensibilidad y la especificidad suelen ser los parámetros más importantes para valorarlas; la sensibilidad es la capacidad del ensayo para detectar correctamente los sueros que contienen anticuerpos contra el VIH, y la especificidad es la capacidad para detectar correctamente los sueros que no contienen anticuerpos contra dicho virus (12-16). Tales características permiten dividirlas en pruebas de tamizaje y confirmación (Tabla 2).
PRUEBAS DE TAMIZAJE
Las de primera línea son las de tamizaje, se caracterizan por tener una buena sensibilidad. Entre ellas tenemos las siguientes:
Pruebas rápidas
A pesar de ser exámenes de diversa metodología y diferente capacidad diagnóstica, tienen ciertas características en común: su tiempo de ejecución es de 20 minutos o menos (17), no necesitan equipamiento (pueden realizarse fuera del laboratorio) y tienen incorporados sistemas de control de calidad interno (18). En general, tienen una sensibilidad comparable con las pruebas de ELISA, pero su especificidad suele ser menor (18,19).
Según la normativa vigente en nuestro país, las pruebas rápidas pueden emplearse para realizar el diagnóstico presuntivo de VIH en dos circunstancias (10):
En el caso que el ensayo resultara reactivo y el establecimiento de salud contara con otra prueba rápida cuyos antígenos para atrapar los anticuerpos fueran diferentes a la primera, entonces se procederá a efectuarla y si el resultado reactivo persistiera, se considerará que el individuo tiene un diagnóstico presuntivo de infección por el VIH.
En el caso que el ensayo resultara reactivo y el establecimiento no contara con otra prueba rápida cuyos antígenos para atrapar los anticuerpos fueron diferentes a la primera, entonces se procederá a efectuar un ELISA de tercera o cuarta generación, y si este resultara reactivo, se considerará que el individuo tiene un diagnóstico presuntivo de infección por el VIH.
En ambas situaciones, la ratificación definitiva del diagnóstico de la infección por el VIH requiere de una prueba confirmatoria (10). Si las pruebas rápidas resultaran no reactivas en cualquiera de las fases mencionadas, se considerará que el individuo no está infectado, salvo que exista la presunción que se encuentra en el periodo de ventana (18).
La inmunocromatografía es el método más utilizado en el país, por lo que ha sido objeto de diversas evaluaciones (20,21), aunque también existen otros métodos como la aglutinación, immunoconcentración y fase sólida. Se los emplea en (22):
- Gestantes en trabajo de parto que desconocen su estado serológico. Su introducción ha sido esencial para establecer las medidas de profilaxis que eviten la trasmisión vertical (23,24). En este grupo, la sensibilidad y especificidad de dichas pruebas se consideran generalmente adecuadas; sin embargo, persiste cierto número de falsos positivos que varía según la prevalencia de la infección por el VIH en cada población y del tipo de muestra utilizada (24). Se recomienda que la gestante expuesta a la infección por VIH se analice cada tres meses hasta el final del embarazo, en previsión de un periodo de ventana prolongado (18).
- Los servicios de urgencia, cuando se desconoce el estado serológico del paciente.
- Los casos de exposición ocupacional o no ocupacional a VIH.
- Los programas de acceso directo de las poblaciones de alto riesgo de infección por VIH.
Actualmente las pruebas rápidas permiten efectuar diagnósticos múltiples y simultáneos con otras infecciones de transmisión sexual (ITS), entre ellas la sífilis y la hepatitis B, e incluso pueden detectar a la vez antígenos/anticuerpos del VIH.
ELISA
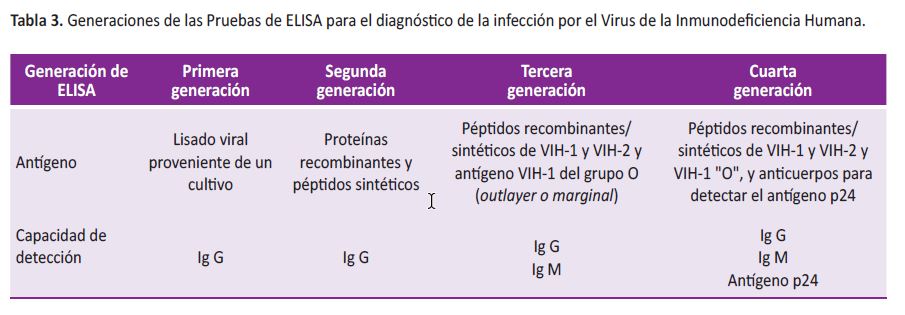
Se caracterizan por una alta sensibilidad, cercana al 100% (16,25), y una buena especificidad (99,5%) que aún es superior a la de las pruebas rápidas e inferior a la de las confirmatorias (9,25). La especificidad depende de la calidad del antígeno que contiene la prueba, que es el componente que define su generación (Tabla 3); hoy sólo son aceptables los ELISA de tercera y cuarta generación.
Otro aspecto a considerar es el mecanismo con el que los ELISA capturan los anticuerpos, que los diferencia en diversos tipos, haciendo posible encontrar pruebas de una misma generación con distintos mecanismos de acción (16). Los principales mecanismos vigentes son: 1) indirecto: tiene alta sensibilidad (26) pero una menor especificidad, lo que puede ocasionar falsos reactivos. 2) competitivo: son altamente específicos (26,27). 3) sándwich: tienen una mejor sensibilidad, sus resultados pueden ser más precoces y son altamente específicos (16) y 4) de captura: tienen buena sensibilidad y una alta especificidad (26).
Según la normativa vigente en nuestro país, los exámenes de ELISA pueden emplearse en el tamizaje de los pacientes, bajo dos modalidades (10):
Cuando una prueba rápida resulta reactiva, una de las alternativas es efectuar un ELISA; si esta última fuera también reactiva, se solicitará otra muestra sanguínea al paciente con la que se realizará una segunda prueba de ELISA, pero esta vez por duplicado. Si una o ambas persistieran reactivas, entonces se considerará que el individuo tiene un diagnóstico presuntivo de infección por el VIH.
El ELISA también puede desarrollarse como prueba de tamizaje inicial, y si resultara reactivo, se procederá de manera análoga a la anterior modalidad y la interpretación será la misma.
En ambos casos la ratificación definitiva del diagnóstico requiere de una prueba confirmatoria (10). Si el ELISA resultara no reactivo, en cualquiera de las fases, se considerará que el individuo no está infectado, salvo que exista la presunción que esté en el periodo de ventana (18).
En algunas marcas comerciales existe el concepto de zona gris, que es una franja de incertidumbre en la que los valores obtenidos no definen si la prueba es reactiva o no reactiva; su interpretación debe estar detallada inequívocamente en el inserto del fabricante. Cuando se presenta esta eventualidad la prueba debe repetirse.
Las pruebas diagnósticas tienen limitantes que se expresan a través de los falsos positivos (falsos reactivos) y negativos (falsos no reactivos):
Falsos negativos: cuando un individuo infectado con VIH tiene pruebas diagnósticas negativas o no reactivas. Esta ocurrencia es cada vez menos frecuente por la alta sensibilidad de las actuales pruebas de tamizaje. Las principales causas pueden ser:
- El periodo de ventana. Periodo de tiempo que transcurre desde que la persona se infecta por VIH hasta el momento en el que el sistema inmunológico produce niveles de anticuerpos detectables mediante las pruebas diagnósticas (6,16,23). Esta respuesta inmune depende de cada individuo, habiéndose descrito una amplia gama de respuestas inmunológicas (22). Durante este período todos los pacientes son altamente infectantes (6).
Cada prueba tiene un periodo de ventana específico. En aquellas pruebas que sólo detectan anticuerpos (por ejemplo, el ELISA de tercera generación) puede ser tan breve como tres a cuatro semanas (2,5); sin embargo, por lo general se acepta que el 97% de los infectados producirá anticuerpos detectables tres meses después de la infección, quedando un pequeño porcentaje de infectados que requerirá de seis meses a más para producir una cantidad de anticuerpos detectable (10,16,26). En aquellas pruebas que detectan simultáneamente antígenos y anticuerpos (por ejemplo, el ELISA de cuarta generación), el tiempo de detección suele ser menor, aunque subsiste la controversia sobre la cuantía de esta reducción (5,6,11,26,28).
- Terapia inmunosupresora (20,29).
- Disfunción de los linfocitos B (20).
- Estadio de SIDA terminal (29).
- Enfermedades crónicas que produzcan el colapsoinmunológico (26).
- Errores de laboratorio (20,29).
Falsos positivos: cuando un individuo que no está infectado por VIH tiene pruebas diagnósticas positivas o reactivas. Son más frecuentes en las pruebas rápidas y sumamente infrecuentes en las confirmatorias. Las causas son variadas, dependen de ciertas condiciones derivadas del paciente y del método diagnostico (calidad de los antígenos y principio técnico):
- Las reacciones cruzadas producto de las interacciones con moléculas presentes en la sangre de las personas estudiadas. Tal como ocurre en la hipergamaglobulinemia, vacunaciones recientes contra la hepatitis B, la rabia o la influenza, y por la presencia de anticuerpos con características similares a los anticuerpos anti-VIH que se producen contra otros agentes infecciosos (por ejemplo, HTLV-I y HTLV-II), enciertas neoplasias hematológicas (plasmocitoma) o en enfermedades autoinmunes (por ejemplo, el lupus eritematoso sistémico (LES)) (29). El embarazo también puede ocasionar reacciones cruzadas, ya que la placenta normal contiene moléculas similares a los antígenos del VIH (2).
- Factores dependientes del laboratorio. Entre ellos la calidad de las muestras sanguíneas (fallos en la extracción o su identificación, contaminación bacteriana e inadecuada conservación), y la especificidad del ensayo utilizado.
Los ELISA no son útiles para identificar la infección de los neonatos o lactantes de madres VIH positivas en los primeros 18 meses de vida porque los anticuerpos maternos atraviesan la placenta y pueden persistir por ese lapso (2,16). Para el diagnóstico precoz de la infección vertical se debe recurrir a la detección de antígenos virales (p24) (6), ADN-VIH o ARN-VIH (2,16). Después de ese lapso, los ELISA recién se podrán emplear en este grupo etario (11).
La terapia antiretroviral profiláctica posterior a la exposición al VIH (por ejemplo, zidovudina) puede disminuir la presencia del antígeno p24 (2) e incluso retardar la seroconversión (16,29).
La OMS recomienda el empleo de dos pruebas de ELISA de diferente mecanismo de acción como estrategia alternativa para corroborar la infección por el VIH, pues si ambas resultaran reactivas, ello sería equivalente a una prueba confirmatoria (11,30).
Para garantizar la fiabilidad de los resultados es obligatorio seguir estrictamente el protocolo de control de calidad interno establecido por cada fabricante, y contar con un laboratorio que efectué el control de calidad externo. No se recomienda mezclar los sueros de varios pacientes (pool) para procesarlos juntos con el propósito de ahorrar reactivo.
Antigenemia p24
Es una prueba altamente especifica (30) pero su sensibilidad no es óptima (6), presentando falsos negativos; limitándose su uso al diagnóstico precoz durante el periodo de ventana, cuando hay signos clínicos de primoinfección o presunción de exposición (18). Por ello se ha preferido incorporarla a los ELISA de cuarta generación.
Puede detectarse de once a trece días después de la infección, su concentración permanece alta y detectable en sangre aproximadamente por un mes y medio después de la infección, pero a medida que aparecen los anticuerpos anti-VIH, su concentración disminuye y aumentan los complejos p24/ anti-p24 (6,31). En la etapa de SIDA, la replicación viral aumenta nuevamente y la p24 alcanza niveles muy altos (31). Los resultados dudosos o débilmente positivos deben confirmarse por medio de la prueba de neutralización (27,32,33).
Quimioluminiscencia
Es un método automatizado basado en el principio de emisión luminosa a través de una reacción enzima-sustrato (34); es más sensible que los ELISA (32), por eso un resultado no reactivo es más confiable, y es muy específico (34). Los resultados reactivos deben corroborarse mediante las pruebas confirmatorias; los débilmente reactivos o dudosos deben repetirse y si persisten así, para efectos prácticos, se considerarán reactivos.
PRUEBAS CONFIRMATORIAS
Cuando los resultados de las pruebas de tamizaje determinan un diagnóstico presuntivo de infección por VIH, se recurrirá a las pruebas confirmatorias que se caracterizan por su alta especificidad (11), superior a todas las de tamizaje. Actualmente se emplean tres:
Inmunofluorescencia indirecta
Tiene una sensibilidad y especificidad similar al WB, incluso su positividad puede ocurrir antes que el WB (35), es mucho más barata (de 10 a 11 veces menor), su tiempo de ejecución es menor y la técnica más simple (9); por ello ha desplazado al WB. constituyendo el 95% de las confirmaciones a nivel nacional. Su positividad constituye diagnóstico definitivo de la infección por el VIH y la negatividad, en general, también es definitiva de no infección, excepto cuando existe evidencia de exposición reciente y reiterada, en tales circunstancias se recomienda repetir el ensayo luego de tres y seis meses respectivamente.
Cuando el resultado de la IFI es indeterminado se deberá recurrir al WB (9), y si persiste por más de seis meses, sería sumamente raro que se trate de una genuina infección por el VIH (16) y se debería considerar un proceso patológico de otra etiología.
Western Blot
Es una prueba altamente especifica (6) pero por su alto costo se emplea básicamente para corroborar los resultados indeterminados de la IFI (9). Sus criterios de interpretación no se han unificado entre la OMS, el Centers for Disease Control and Prevention (CDC) norteamericano y la Cruz Roja norteamericana (3,30). En el Perú se utilizan los valores del CDC, que considera positiva la prueba de WB cuando aparecen la p24 + (gp160, gp120 o gp41) o la p41 + (gp160 o gp120).
El resultado positivo confirma definitivamente la infección por el VIH; el negativo la descarta, excepto cuando existe evidencia de exposición reciente y reiterada a esta infección. En tales circunstancias se debe repetir el ensayo luego de tres y seis meses respectivamente. Cuando el resultado es indeterminado, que ocurre cuando sólo aparecen algunas bandas que no cumplen con los criterios del CDC, se recomienda repetir la prueba después de tres y seis meses, dependiendo de los factores de riesgo identificables en cada caso (2,3,29).
Los resultados indeterminados pueden ocurrir (3,26) en las fases tempranas o estadios avanzados de la infección con deterioro inmunológico grave, en los recién nacidos de madre VIH positiva, en sueros hemolizados y que contienen el factor reumatoide o niveles altos de bilirrubina, en las reacciones cruzadas con otros retrovirus (HTLV-I y HTLV-II), en la hipergammaglobulinemia secundaria a la hiperestimulación antigénica, en multitransfundidos y en las enfermedades autoinmunes (por ejemplo, el LES).
Si después de seis meses el WB persiste indeterminado, al igual que en la IFI, muy rara vez se trataría de una genuina infección por VIH (16), siendo más probable que sea una patología de otra etiología, o en algunos pocos casos, un resultado indeterminado por largo tiempo, sin una explicación especifica.
Una de las limitaciones del WB es el diferente valor predictivo diagnóstico que tiene la presencia de cada una de las bandas, así los anticuerpos contra las proteínas de la envoltura del VIH son mucho más específicos, aunque también se han descrito falsos positivos (30).
Line Immuno Assay (LIA)
Su empleo está menos difundido que la IFI y el WB, su performance es superior a este último e incluso se le considera el estándar de oro (20).
Una vez confirmada la infección por el VIH recién se procederá a efectuar las pruebas pronosticas (recuento de linfocitos CD4 y carga viral) (17), cuya interpretación no está dentro del objetivo de este artículo.
DISCUSIÓN
Desde el descubrimiento del VIH, la tecnología de las pruebas diagnósticas ha evolucionado sustancialmente y en paralelo con los nuevos descubrimientos sobre la patogénesis del VIH/SIDA, ello ha generado el flujo dinámico de estos ensayos, en el que unos han sido dejados de lado, siendo actualmente reemplazados por aquellos que tienen mejor performance.
Las pruebas rápidas no sólo han mejorado su sensibilidad y especificidad, sino que ahora son capaces de hacer diagnósticos simultáneos con otras ITS y detectar antígenos del VIH; eso podría significar, en el futuro relativamente cercano, el definitivo desplazamiento de los ELISA.
Las pruebas rápidas permitieron llevar los exámenes fuera de los establecimientos de salud y beneficiaron particularmente a las gestantes que carecían de un diagnóstico expedito cerca o durante el trabajo de parto. Sin embargo, aún es necesario corroborar el diagnóstico presuntivo con las pruebas de ELISA de tercera y cuarta generación, que para convertirse en un diagnóstico definitivo requiere de las pruebas confirmatorias.
La IFI y el WB son ensayos comparables, pero la primera es la más utilizada en el país por su costo significativamente menor. La IFI positiva confirma plenamente la infección por el VIH, la negativa lo descarta, excepto en los casos señalados, y el resultado indeterminado hace necesario recurrir al WB, hasta seis meses después de la prueba primigenia, ya que este es el lapso máximo que tardaría la gran mayoría de pacientes infectados con el VIH para seroconvertirse.
El WB positivo confirma definitivamente la infección, el resultado negativo lo descarta, excepto en los casos señalados, y el indeterminado requiere repetir el ensayo hasta seis meses después de la prueba primigenia, por la razón expuesta anteriormente. También es admisible el uso del LIA como prueba confirmatoria (10). En la práctica médica los resultados de las pruebas confirmatorias siempre prevalecerán sobre los obtenidos en las de tamizaje.
El algoritmo nacional establecido en la Norma Técnica de Salud N° 097-MINSA/DGSP-V.02 (Figura 1) (10), ha incorporado estos nuevos ensayos y ha detallado los criterios para definir el diagnóstico presuntivo y definitivo de la infección por el VIH.
Fuente de financiamiento: El autor declara no haber recibido ninguna financiación para la realización de este trabajo.
Declaración de conflicto de intereses: El autor declara no tener conflicto de intereses con la publicación de este artículo.
REFERENCIAS BIBLIOGRÁFICAS
1. Najera R, Loma A, Estébanez P, Anabitarte H, Usieto R. SIDA un problema de salud pública. 1ra edición. Madrid: Gráficas Lormo; 1987. [ Links ]
2. Tobón J, Toro A. Estudio del paciente con infección por VIH. Medicina & Laboratorio. 2008;14(1-2):11-42. [ Links ]
3. García F, Álvarez M, Bernal C, Chueca N, Guillot V. Diagnóstico de laboratorio de la infección por el VIH, del tropismo viral y de las resistencias a los antirretrovirales. Enferm Infecc Microbiol Clin. 2011;29(4):297-307. [ Links ]
4. Centers for Disease Control & Association of Public Health Laboratories. 2016 HIV Diagnostics Conference (Internet). Atlanta, Georgia; 2016. (citado el 13 de julio de 2017). Disponible en: http://hivtestingconference.org/wp-content/uploads/2016/03/2016-HIVDX-Program-Book_WEB_FINAL.pdf [ Links ]
5. Cornett J, Kirn T. Laboratory diagnosis of HIV in adults: A review of current methods. Clin Infect Dis. 2013;57(5):712-8. [ Links ]
6. Luft S, Seme K, Poljak M. Laboratory diagnosis of human immunodeficiency virus infection. Acta Dermatovenerol Alp Pannonica Adriat. 2004;13(2):43-9. [ Links ]
7. Cueto M. El rastro del SIDA en el Perú. Hist Cienc Saude-Manguinhos. 2002;9(Supl 1):17-40. [ Links ]
8. Cueto M. Culpa y coraje: historia de las políticas sobre el VIH/Sida en el Perú. Lima: Universidad Peruana Cayetano Heredia; 2001. [ Links ]
9. Valverde A, Romero S, Cabezas C. Inmunofluorescencia Indirecta como prueba alternativa para la confirmación diagnóstica de infección por VIH en el Perú. Rev Peru Med Exp Salud Publica. 1997;14(1):19-21. [ Links ]
10. Norma Técnica de Salud N° 097-MINSA/DGSP-v.01. Norma técnica de salud de atención integral del adulto/a con infección por el Virus de la Inmunodeficiencia Humana (VIH). Lima: Ministerio de Salud; 2014. [ Links ]
11. Ospina S. Diagnóstico de la infección por el virus de la inmnodeficiencia humana. Infect. 2006;10(4):273-8. [ Links ]
12. World Health Organization. HIV assays: operational characteristics (phase I). Report 15. Antigen/Antibody ELISAs. Geneva: World Health Organization; 2004. [ Links ]
13. Pita S, Pértegas S. Pruebas diagnósticas. Cad Aten Primaria. 2003;10:120-4. [ Links ]
14. World Health Organization. HIV assays: operational characteristics (phase I). Report 17. HIV Rapids diagnostic test. Geneva: World Health Organization; 2013. [ Links ]
15. World Health Organization. HIV assays: operational characteristics. Report 16. Rapid assays. Geneva: World Health Organization; 2009. [ Links ]
16. Hoffmann C, Rockstroch J, Kamps B. HIV Medicine 2007. Paris: Flying Publisher; 2007. [ Links ]
17. Métodos para las pruebas del VIH. Actualización técnica. Ginebra: ONUSIDA; 1997. [ Links ]
18. Oliva G, Almazán M, Guillen M. Prueba de detección rápida de la infección por VIH. AATRM. Número 2007/3. Barcelona: Agència d’Avaluació de Tecnologia i Recerca Mèdiques de Cataluña; 2009.
19. Ministerio de Salud Pública del Uruguay. Evaluación del desempeño de tres pruebas rápidas para el diagnóstico de infección por VIH en adultos. Montevideo: Imprenta Rojo; 2014. [ Links ]
20. Sharma A, Marfalia L. Laboratory diagnosis of HIV. Indian J Sex Trasm Dis. 2008;29(1):42-5. [ Links ]
21. Miranda-Ulloa E, Romero-Ruíz S, Briceño-Espinoza R, Santos-Anaya D. Evaluación de tres marcas comerciales de Pruebas Rápidas para la detección del VIH. Rev Peru Med Exp Salud Publica. 2015;32(2):404-5. [ Links ]
22. Snell J, Supran E, Tamashiro H. Sistema internacional de la OMS para evaluar la calidad de las pruebas detectoras de anticuerpos contra el VIH: resultados de la segunda distribución de sueros. Bol Of Sanit Panam. 1994;16(2):124-34. [ Links ]
23. The Well Project. HIV Testing (Internet). The Well Project; 2016. (citado el 13 de julio de 2017). Disponible en: www.thewellproject.org/printpdf/116 [ Links ]
24. Vásquez J. Uso de prueba rápida para la detección de infección por VIH en pediatría. Bol Med Hosp Infant Mex. 2009; 66(4):382-8. [ Links ]
25. Codina C, Martín M, Ibarra O. La infección por el virus de la inmunodeficiencia humana. En: Farmacia Hospitalaria. Tomo II. Madrid: Sociedad Española de Farmacia Hospitalaria; 2002. p. 1493-1516. [ Links ]
26. Mendoza C, Poveda E, Soriano V. Diagnóstico de laboratorio de la infección por VIH-1. En: Gatell JM. Guía práctica del SIDA. Clínica, diagnóstico y tratamiento. 12da ed. Madrid: Tesigraf; 2013. p. 55- 72. [ Links ]
27. Díaz H, Ribas M, Lubian A, Joanes J, Ricardo Fonseca ME. Antigenemia P24: correlación con algunos aspectos clínicos y epidemiológicos en 100 individuos cubanos infectados por VIH-1. Rev Cubana Med Trop. 2001;53(3):137-44. [ Links ]
28. Jané E. Impacto de los tratamientos antirretrovirales en la patología oral de pacientes VIH positivos (Tesis doctoral). Barcelona: Facultad de Odontología, Universidad de Barcelona; 2002. [ Links ]
29. Döpel S, Schubert U, Grunow R, Rönspeck W, Pmili G, Porstmann T. Comparison of four anti-hiv screening assays which belong to different test generations. Eur J Clin Chem Clin Biochem. 1991;29(5):331-7. [ Links ]
30. Centers for Disease Control. Interpretation and use of the Western Blot Assay of serodiagnostics of Human Inmunodeficiency Virus type 1 infections. MMWR. 1989; 38(S-7):1-7. [ Links ]
31. Buttò S, Suligoi B, Fanales-Belasio E, Raimondo M. Laboratory diagnostics for HIV infection. Ann Ist Super Sanità. 2010;46(1):24-33. [ Links ]
32. García C, Martínez I. Ventajas del método de quimioluminiscencia frente al de radioinmunoanálisis (RIA). Visión Científica. 2007;2(1):60-8. [ Links ]
33. Organización Mundial de la Salud (Internet). WHO Prequalification of In Vitro Diagnostics Programme. Public Report. INNOLIA HIV I/ II Score (Internet). Geneva: WHO; 2015 (citado el 13 de julio de 2017). Disponible en: http://www.who.int/diagnostics_laboratory/evaluations/150508_final_report_innolia_hiv_score.pdf [ Links ]
34. Jaramillo Tobón AC. Serología de cuarta generación, biología molecular diagnóstica y el nuevo algoritmo para diagnóstico de infección por VIH. Rev Med FCM-UCSG. 2012;18(1):45-52. [ Links ]
35. Arya S, Lal P, Singh P, Kumar A. Recent advances in diagnosis HIV and future prospects. Indian J of Biotechnol. 2015;15:9-18. [ Links ]
Correspondencia
Ricardo Iván Álvarez Carrasco ralvarezcarrasco@yahoo.com
Recibido: 23/08/2017
Arbitrado por pares
Aprobado: 11/10/2017
Citar como: Álvarez-Carrasco RI. Interpretación de las pruebas usadas para diagnosticar la infección por virus de la inmunodeficiencia humana. Acta Med Peru. 2017;34(4):309-16