INTRODUCCIÓN
El accidente cerebro vascular (ACV) es la lesión neurológica aguda que se caracteriza por la presencia de una disfunción focal del tejido cerebral (desequilibrio entre el aporte y el requerimiento de oxígeno). Es considerada la segunda causa de muerte y discapacidad en el mundo, existen dos tipos: el ACV isquémico (ACVi) y el hemorrágico (ACVh); siendo el ACVi el responsable del 85% de todos los casos de ACV 1. Además, el ACVi es una emergencia médica con una ventana estrecha para el reconocimiento y administración del tratamiento. El daño generado por esta enfermedad se estima a través de la mortalidad, discapacidad e impacto en la población 2,3.
La importancia de un diagnóstico y tratamiento oportuno de la etapa aguda del ataque cerebrovascular isquémico radica en reducir la mortalidad, evitar que el área de isquemia-necrosis aumente, reducir las complicaciones asociadas al ACVi, reducir las secuelas neurológicas y optimizar la rehabilitación 4,5.
Por este motivo, la Dirección de Guías de Práctica Clínica, Farmacovigilancia y Tecnovigilancia del Instituto de Evaluación de Tecnologías en Salud e Investigación (IETSI) del Seguro Social del Perú (EsSalud) priorizó la realización de la presente guía de práctica clínica (GPC) con la finalidad de establecer lineamientos basados en evidencias para el diagnóstico y tratamiento de la etapa aguda del ataque cerebrovascular isquémico, cuyas recomendaciones serán aplicadas por profesionales de la salud en EsSalud. El presente artículo es un resumen de dicha GPC (Tabla 1).
MATERIALES Y MÉTODOS
El procedimiento seguido para la elaboración de la presente GPC está detallado en su versión "in extenso", la cual puede descargarse de la página web del IETSI de EsSalud (http://www.essalud.gob.pe/ietsi/guias_pract_clini.html).
En resumen, se aplicó la siguiente metodología:
Conformación del grupo elaborador de la guía local (GEG): Se conformó un GEG, que incluyó metodólogos y médicos especialistas en neurología.
Formulación de preguntas: En concordancia con los objetivos y alcances de esta GPC, el GEG formuló 8 preguntas clínicas (Tabla 1), cada una de las cuales pudo tener una o más preguntas PICO (Population, Intervention, Comparator, Outcome). A su vez, cada pregunta PICO pudo tener uno o más desenlaces (outcomes) de interés.
Búsqueda y selección de la evidencia: Para cada pregunta PICO, se realizó la búsqueda y selección de la evidencia. Para ello, durante el 2018 se buscaron revisiones sistemáticas (RS) publicadas como artículos científicos (mediante búsquedas sistemáticas en PubMed y Cochrane Controlled Register of Trials) o realizadas como parte de una GPC previa (mediante una búsqueda sistemática de GPC sobre el tema) (Material Suplementario 1). Cuando se encontró RS de calidad aceptable, se escogió una RS para la toma de decisiones, la cual fue actualizada cuando el GEG lo consideró necesario. Cuando no se encontró ninguna RS de calidad aceptable, se realizó una búsqueda de novo de estudios primarios.
Evaluación de la certeza de la evidencia: La certeza de la evidencia para cada desenlace de cada pregunta PICO pudo ser alta, moderada, baja o muy baja (Figura 1). Para evaluar la certeza de la evidencia, se siguió la metodología de Grading of Recommendations Assessment, Development, and Evaluation (GRADE) 6 y se elaboró las tablas de perfiles de evidencias de GRADE (Material Suplementario 2). Finalmente, se le asignó a la pregunta PICO el nivel de certeza más bajo alcanzado por alguno de los desenlaces importantes.
Formulación de las recomendaciones: El GEG revisó la evidencia seleccionada para cada pregunta clínica en reuniones periódicas, y formuló recomendaciones fuertes o condicionales (Figura 1) por consenso o por mayoría simple, usando la metodología GRADE 7. Para ello, se tuvo en consideración: 1) Beneficios y daños de las opciones, 2) Valores y preferencias de los pacientes, 3) Aceptabilidad por parte de los profesionales de salud, 4) Factibilidad de las opciones en los establecimientos de salud de EsSalud, y 5) Uso de recursos. Asimismo, el GEG formuló puntos de buenas prácticas clínicas (BPC) en consenso, para los cuales no se realizó una búsqueda sistemática de la evidencia o no se encontró evidencia suficiente para basar una recomendación.
Revisión por expertos externos: La presente GPC fue revisada en reuniones con médicos especialistas representantes de otras instituciones y tomadores de decisiones. Asimismo, su versión in-extenso fue enviada por vía electrónica a externos para su revisión (mencionados en la sección de agradecimientos). El GEG tuvo en cuenta los resultados de estas revisiones para modificar las recomendaciones finales.
Aprobación de la GPC: La presente GPC fue aprobada para su uso en EsSalud, con Resolución N°128-IETSI-ESSALUD-2019.
Actualización de la GPC: La presente GPC tiene una validez de tres años. Al acercarse al fin de este período, se procederá a realizar una RS de la literatura para su actualización, luego de la cual se decidirá si se actualiza la presente GPC o se procede a realizar una nueva versión.
RECOMENDACIONES
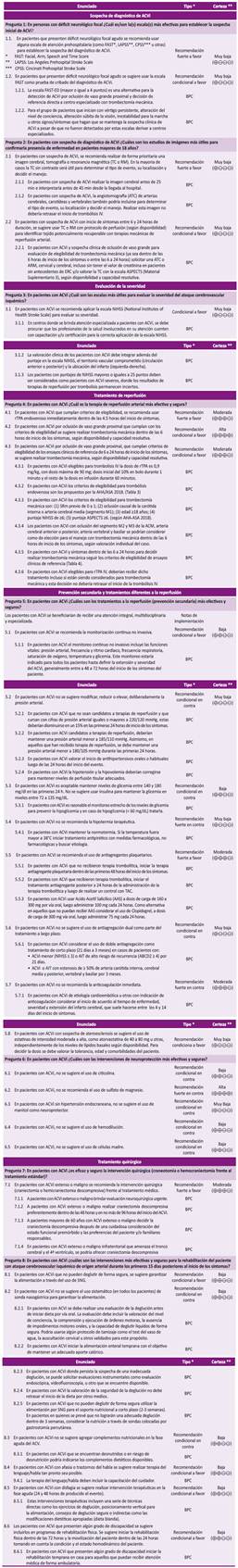
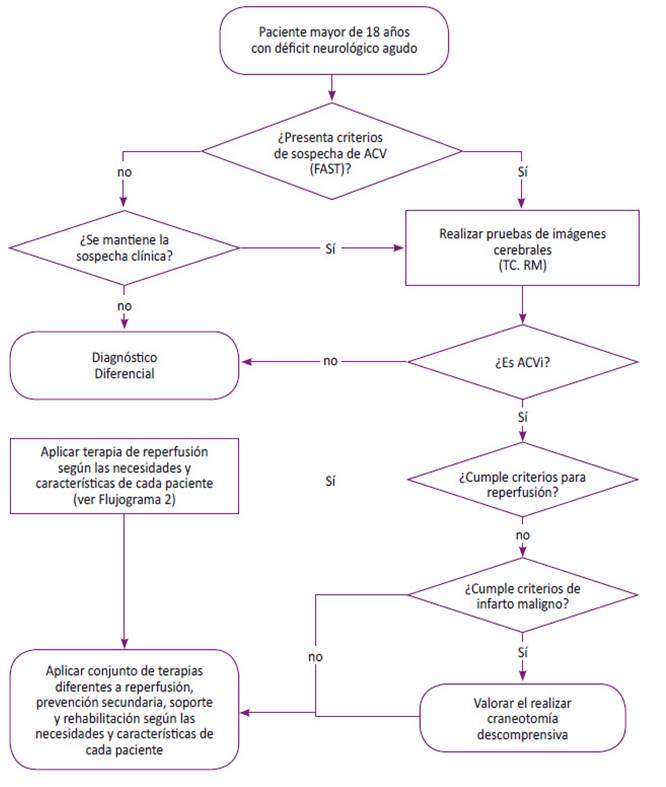
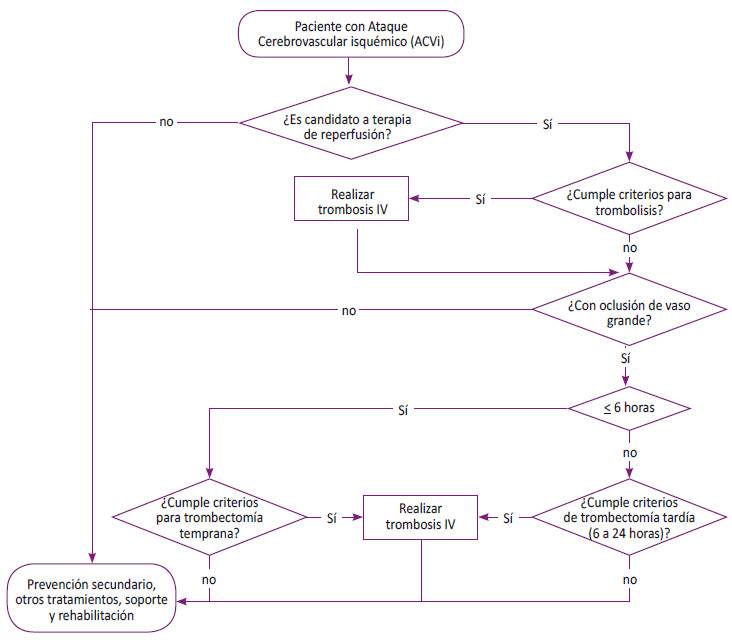
La presente GPC abordó ocho preguntas clínicas con relación a cuatro temas: tamizaje, diagnóstico, tratamiento y soporte y rehabilitación. En base a dichas preguntas, se formularon 28 recomendaciones (8 fuertes y 20 condicionales), 39 puntos de BPC, 1 nota de implementación y 2 flujogramas (Tabla 1, Figuras 2 y 3).
A continuación, se expondrá un resumen del razonamiento seguido para llegar a las recomendaciones y puntos de BPC de cada pregunta clínica.
Pregunta 1: En pacientes con déficit neurológico focal ¿Cuál es/son la(s) escala(s) más efectivas para establecer la sospecha inicial de ACVi?
De la evidencia a la decisión:
Actualmente existen escalas que tratan de identificar oportunamente a un paciente con ACVi, entre ellas destacan: Los ángeles Prehospital Stroke Screen (LAPSS), Cincinnati Prehospital Stroke Scale (CPSS), Face Arm Speech Test (FAST) y Ontario Prehospital Stroke Screening tool (OPSS). Actualmente, no se conoce si alguna de estas herramientas es útil para la precisión diagnóstica oportuna 8,9.
Se seleccionó la RS de Rudd 2015 8, la cual fue actualizada debido a que su búsqueda fue hasta el 2014 y no realizó metaanálisis (MA). Se encontró que la escala LAPSS (n=3264) presentó un AUC de 0,83 (IC95%: 0,79 - 0,86), sensibilidad de 70% (IC95%: 60% - 78%) y especificidad del 89% (IC95%: 77% - 95%). La escala CPSS (n=4482); un AUC de 0,78 (IC95%: 0,74 - 0,82), sensibilidad de 82% (IC95%: 73% - 88%) y especificidad de 58% (IC95%: 45% - 70%). La escala de FAST (n=1841); un AUC de: 0,83 (IC95%: 0,80 - 0,86), sensibilidad de 85% (IC95%: 79% - 89%) y especificidad de 49% (IC95%: 25% - 74%) y la escala OPSS (n=554); una RV+ de 4,23, RV- de 0,139, sensibilidad de 89% (IC95%: 85% - 92%) y una especificidad de 79% (IC95%: 0,63 - 0,90). (Material Suplementario 3).
En base a lo presentado se evidencia que es necesario aplicar una escala para el screening diagnóstico oportuno de ACVi.
El GEG decidió emitir una recomendación fuerte a favor al empleo de una escala para el screening diagnóstico oportuno de ACVi, debido a que presentaron una precisión diagnóstica moderada a buena, alta aceptación de pacientes/médicos y un adecuado uso de los recursos. Además, de todas las escalas evaluadas, el GEG decidió emitir una recomendación condicional a favor al uso de la escala FAST-ED debido a que es más práctica para emplearla (solo emplea evaluación clínica y no requiere de pruebas de laboratorio) y presenta una certeza de la evidencia baja.
Puntos de BPC:
El GEG consideró importante tener una herramienta para la detección prehospitalaria de pacientes con ACVi de vaso grande cuando se dispone de un centro especializados para el manejo de ACVi con trombectomía mecánica y hospital general con trombólisis (escala FAST-ED mayor o igual a 4 puntos) 10. Además, se consideró importante identificar la localización (circulación anterior o posterior), debido que estos afectan a distintas regiones del cerebro. Además, la mayor parte de los ítems están enfocados en la identificación de infartos en la circulación anterior, por esto, se considera importante la evaluación de otros signos y síntomas, que no sean identificados por las escalas, y que son indicios de un cuadro de ACVi.
Pregunta 2: En pacientes con sospecha de diagnóstico de ACVi ¿Cuáles son los estudios de imágenes más útiles para confirmar la presencia de enfermedad en pacientes mayores de 18 años?
De la evidencia a la decisión:
El diagnóstico de la ACVi se realiza mediante la evaluación clínica y que se confirma y localiza con imágenes cerebrales como la tomografía axial computarizada (TC), resonancia magnética cerebral (RM) y la tomografía con perfusión (TCp) 11-13.
Se encontraron 2 RS: Brazzelli 2009 14 y Biesbroek 2013 15, ambas presentaron una adecuada calidad metodológica (AMSTAR-2: 14/16 y 13/16; respectivamente). La RS de Brazzelli 2009 (n=909) encontró que la TC presentó una sensibilidad de 39% (IC95%: 16% - 68%) y una especificidad de 100% (IC95%: 94% - 100%). Por otro lado, la RM presentó una sensibilidad de 99% (IC95%: 23% - 100%) y una especificidad de 92% (IC95%: 83% - 97%). La RS de Biesbroek 2013 (n=1107) encontró que la TCp presentó una sensibilidad de 80% (IC95% 72% - 86%) y especificidad de 95% (IC95%: 86% - 98%) para detectar la zona de penumbra/isquémica.
El GEG decidió emitir una recomendación fuerte a favor al uso de la TC y RM, debido a que presentan una adecuada precisión diagnóstica para la confirmación de ACVi, priorizando entre ellas, el uso de la TC sin contraste por su mayor accesibilidad, buena aceptación de los pacientes/médicos y una certeza de la evidencia baja. Además, el GEG emitió una recomendación condicional a favor al uso de la TCp, debido a su adecuada precisión diagnóstica para la identificación de la zona de penumbra/isquémica; sin embargo, su uso es restringido.
Puntos de BPC:
El GEG sugiere indicar la toma de una imagen cerebral antes de los 25 minutos 16 y que su interpretación se realice antes de los 45 minutos, desde la llegada del paciente al hospital 5. Así también, la empleo de la angiotomografía (ATC) de arterias cerebrales, carotídeas y vertebrales, debido a que el incremento de la sensibilidad diagnóstico conllevaría a una mejor toma de decisiones (trombólisis o trombectomía) de los pacientes con ACVi, sin que esto signifique un mayor uso de tiempo (5 minutos adicionales) o de exposición de la radiación ni a un incremento de costos 17,18. Así mismo, ante la sospecha clínica de ACVi de vaso grande, solicitar una ATC cervical y cerebral, para valorar la elegibilidad de trombectomía mecánica (escala ASPECTS) 19,20 (Tabla 2).
Pregunta 3: En pacientes con ACVi ¿Cuáles son las escalas más útiles para evaluar la severidad del ataque cerebrovascular isquémico?
De la evidencia a la decisión:
La severidad ACVi es un factor predictor importante para el pronóstico funcional y de respuesta al aplicar medidas de reperfusión en el paciente 21. Para la valoración del déficit neurológico se han desarrollado diferentes escalas: National Institutes of Health Stroke Scale (NIHSS), Canadian Neurological Scale (CNS), Scandinavian Neurological Stroke Scale (SNSS), Unassisted TeleStroke Scale (UTSS) y National Stroke Project- Stroke severity (NSP-SS). Se evaluó la escala NIHSS, debido a que es la única estudiada para predecir la respuesta terapéutica en términos de sensibilidad y especificidad, del ACVi 21,22.
Mansour 2014 3 (n=127) encontró que la valoración diagnóstica de NIHSS, para la discapacidad mayor a los 3 meses en pacientes con ACVi no trombolizados, con puntaje de 22 a más, presentaron una sensibilidad de 76% y especificidad de 87%. Además, en la valoración diagnóstica de la mortalidad mayor a 3 días, la escala NIHSS presentó una sensibilidad de 84% y especificidad de 69%.
Para la evaluación de discapacidad mayor a los 3 meses en pacientes con ACVi trombolizados con la escala de NIHSS, se consideró el estudio de Cooray 2015 23 (n=44331), quien encontró que la escala presentó una sensibilidad del 69,4% y especificidad del 73,4% (rankin 0-2).
En base a lo presentado, el GEG decidió emitir una recomendación condicional a favor al uso de la escala NIHSS, debido a que presenta una moderada validez diagnóstica para evaluar la severidad del paciente con ACVi. Además, presenta una buena aceptación de los pacientes/médicos, adecuado uso de recursos y una certeza de la evidencia baja.
Puntos de BPC:
El GEG consideró sugerir que los profesionales de la salud involucrados en la atención de pacientes con ACVi cuenten con capacitación y/o certificación de la escala NIHSS, esto debido a la importancia de uniformizar la apreciación de los pacientes desde su ingreso al hospital, los resultados postrombólisis y durante su seguimiento hospitalario 24. Además, se consideró importante que para la valoración de los pacientes con ACVi, a parte de la escala NIHSS se considere el territorio vascular comprometido (circulación anterior o posterior) y la ubicación del infarto (izquierda-derecha), esto debido a que la escala NIHSS evalúa parámetros clínicos y no considera el volumen o dimensiones del infarto; así también NIHSS tiene pocos ítems para evaluar los infartos que se producen en la circulación posterior, pero estos pueden ser definidos por las estructuras anatómicas comprometidas. Por último, se sugiere que los pacientes con puntaje NIHSS mayores o iguales a 25 puntos deben considerarse cuadros severos de ACVi, debido a que estos pacientes no tendrían buenos resultados incluso si es que se realiza tratamiento de reperfusión arterial endovenosa 5.
Pregunta 4: En pacientes con ACVi ¿Cuál es la terapia de reperfusión arterial más efectiva y segura?
De la evidencia a la decisión:
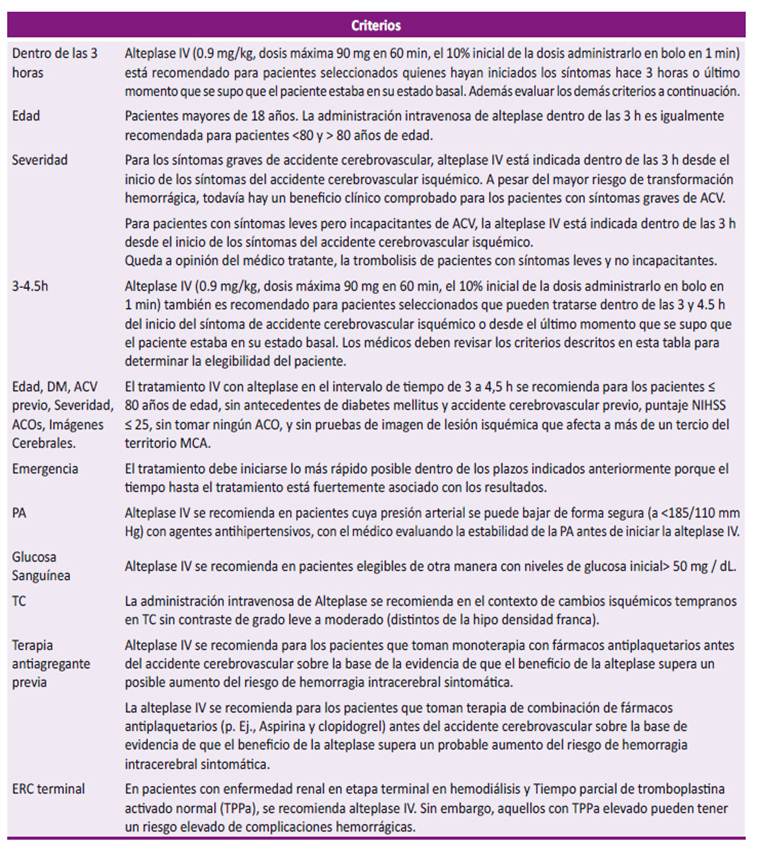
La terapia de reperfusión arterial se emplea para restaurar la irrigación arterial obstruida, principalmente por trombo, que es la causa del ACVi. Entre los métodos disponibles para esta terapia están: la trombólisis (Tabla 3) y la trombectomía (Tabla 4). Ambas terapias presentan diferencias en su rango de efectividad y eventos adversos 25,26). Por este motivo, es necesario evaluar la eficacia y seguridad de estas dos alternativas de reperfusión arterial.
Se realizaron dos preguntas PICO:
Se seleccionaron dos RS, Wardlaw 2015 25 y Lambrinos 2016 26, debido a su adecuada calidad metodológica (AMSTAR-2: 13/16).
4.1 Trombólisis endovenosa antes de las 4,5 horas versus no trombólisis. La RS de Wardlaw 2015 (n=10187) encontró que los pacientes que recibieron trombólisis endovenosa antes de las 4,5 horas presentaron menor posibilidad de discapacidad o mortalidad según la escala ranking modificada (ERm) de 3 a 6 (OR: 0,85; IC95% 0,78 - 0,93), y mayor posibilidad de hemorragia intracraneal (OR: 3,75; IC95% 3,11 - 4,51) en comparación con el que grupo que no lo recibió. Sin embargo, cuando se evaluó la posibilidad de hemorragia intracraneal, los pacientes en ambos grupos fueron muy heterogéneos en sus características basales, presentando un riesgo basal bajo (menor de 10%) de hemorragia tanto en el grupo de intervención y control.
En base a lo presentado, la trombólisis endovenosa antes de las 4,5 horas evidencia un perfil de eficacia y seguridad adecuada respecto a no emplearla con una certeza de la evidencia moderada. Además, presenta una buena aceptación de los pacientes/médicos, adecuado uso de los recursos a largo plazo. Por este motivo, el GEG decidió emitir una recomendación fuerte a favor de su uso.
4.2 Trombectomía versus trombólisis endovenosa. La RS de Lambrinos 2016 (n= 1278) encontró que el uso de la trombectomía en pacientes con ACVi de vaso grande y hasta 6 horas de iniciado los síntomas presentaron menor discapacidad, según la ERm de 1 a 2 (OR: 2.39; IC95%: 1,88 - 3,04) y mayor posibilidad de hemorragia intracraneal (OR: 2,39; IC95% 1,88 - 3,04) en comparación de los pacientes a los que se les realizó la trombólisis endovenosa.
En síntesis, la trombectomía mecánica presenta un adecuado perfil de eficacia y seguridad en comparación con la trombólisis con una certeza de la evidencia moderada a alta; sin embargo, presenta problemas con la factibilidad y un mayor empleo de los recursos (elevados costos). Por este motivo, el GEG decidió emitir una recomendación condicional a favor.
Puntos de BPC:
El GEG sugiere que pacientes con ACVi elegibles para trombólisis endovenosa la dosis de rTPA es 0,9 mg/kg, con dosis máxima de 90 mg, considerando los criterios de elegibilidad (Tabla 3) y que, si estos se cumplen, este tratamiento se debe iniciar lo antes posible, debido a la importancia de un manejo de tratamiento temprano, lo que resulta en una mejora funcional y mejor calidad de vida. Además, pacientes con ACVi de vaso grande con menos de 6 horas de evolución se sugiere evaluar algunos factores importantes para elección de la trombectomía mecánica 26. Así también, pacientes con ACV y oclusión del segmento M2 y M3 de la arteria cerebral media, arteria cerebral anterior o posterior, arteria vertebral y basilar, sean candidatos para trombectomía mecánica debido a que han evidenciado mejoras en el resultado funcional.
Pregunta 5: En pacientes con ACVi ¿Cuáles son los tratamientos diferentes a la reperfusión (prevención secundaria) más efectivos y seguros?
De la evidencia a la decisión:
Las personas que con ACVi presentan mayor riesgo de recurrencia, que suele ser más grave, discapacitante y más costoso que el evento inicial. En la prevención secundaria los tratamientos reducen el riesgo de recurrencia e incluyen la terapia antitrombótica y control de los factores de riesgo causales (presión arterial (PA), frecuencia cardiaca/respiratoria, saturación de oxígeno, temperatura y glicemia) 27,28.
El GEG considera que es necesario conocer cuáles son las alternativas terapéuticas, diferentes a la reperfusión, más efectivas y seguras. Se presentan la evidencia con las recomendaciones, puntos BPC 12 y una nota de implementación.
Tratamiento de reperfusión
5.1 Monitoreo continuo versus intermitente. Se consideró la RS de Ciccone 2013 27, debido a que presentó una adecuada calidad metodológica (AMSTAR-2: 15/16) (n=354), y encontró que el monitoreo fisiológico continuo redujo la posibilidad de muerte o discapacidad a los tres meses (OR: 0,27; IC95%: 0,13 - 0,56) y la duración de la hospitalización (DM: 5,24; IC 95%: -10,51 a 0,03) en comparación con el grupo al que se le realizó el monitoreo intermitente.
El GEG decidió emitir una recomendación condicional a favor al uso del monitoreo continuo, debido a que presenta mayores beneficios con menor posibilidad de muerte y discapacidad; sin embargo, la certeza de la evidencia es baja, presenta problemas de factibilidad y genera un mayor uso de recursos.
Punto BPC:
El GEG sugiere que en pacientes con ACVi, el monitoreo continuo no invasivo incluye las funciones vitales, debido a la importancia de tener un registro continuo de las principales variables fisiológicos entre las 48 y 72 horas de la admisión de los pacientes 27.
5.2 Modificación de la PA versus no modificación. La RS de Bath 2014 28 con adecuada calidad metodológica (AMSTAR-2: 12/16) (n=17,011), encontró que modificar o no la PA generó similares: posibilidades de muerte o dependencia a los 30 días (OR: 1.00; IC del 95%: 0,92 - 1,08), muertes tempranas (≤ 1 mes) (OR: 1,00; IC 95%: 0,73 - 1,38), muerte tardía (> 1 mes) (OR: 0,95; IC del 95%: 0,78 - 1,16) y deterioro neurológico (< 1 mes) (OR: 0,58; IC 95%: 0,09 - 3,82) en comparación con el grupo control.
El GEG decidió emitir una recomendación condicional en contra a la modificación de la PA, debido a que no se evidenció algún beneficio. A pesar de la aceptación de los pacientes, modificar la PA implica un mayor empleo de los recursos, presenta una certeza de la evidencia muy baja.
Punto BPC:
El GEG sugirió 4 BPC sobre la modificación de la presión arterial.
En pacientes con ACVi que no reciban terapias de reperfusión y que presenten PA igual o mayor a 220/120 mmHg, deberían disminuirse en un 15% en las primeras 24 horas, debido a que constituyen una indicación de tratamiento temprano pero cauteloso que ha evidenciado ser segura para reducir la muerte y dependencia, evitando una reducción abrupta de la PA 5,29. Además, pacientes con ACVi candidatos a terapias de reperfusión, deberían mantener una PA menor a 185/110 mmHg y los que reciben la terapia de reperfusión, se debe mantener una PA menor a 180/105 mmHg durante las primeras 24 horas para evitar el riesgo de hemorragia intracraneal 5,30. Así mismo, en pacientes con ACVi valorar el inicio de antihipertensivos orales o habituales luego de las 24 horas del inicio del evento debido a que ha demostrado seguridad en términos de mortalidad y dependencia 5. Por último, la hipotensión y la hipovolemia deben ser estabilizadas para mantener los niveles de perfusión tisular adecuados 5.
5.3 Efecto del control glicémico versus no control. La RS de Bellolio 2014 31 se seleccionó debido a que presentó una adecuada calidad metodológica (AMSTAR-2:15/16) (n=1583), y encontró que los pacientes controlados estrictamente con insulina (72 a 135 mg/dL) presentaron similares posibilidades de muerte o dependencia mayor severa (OR: 0,99; IC del 95%: 0,79 - 1,23), similar déficit neurológico (OR: 1,03; IC 95%: 0,81 - 1,32), mayor frecuencia de eventos adversos como hipoglicemia (OR: 14,06; IC 95%: 6,6 a 32,2) y gran elevación de hipoglicemia sintomática (OR: 18,4; IC del 95%: 9,1 a 37,3) en comparación con el grupo al que no se le controló la glicemia.
En base a lo evidenciado, el GEG decidió emitir una recomendación condicional en contra del control glicémico, debido a que el control glicémico no reduce la posibilidad de muerte o discapacidad. Además, implica un mayor uso de los recursos, presenta baja aceptación de los pacientes/médicos y una certeza de la evidencia baja.
Punto BPC
En GEG sugiere que pacientes con ACVi, el monitoreo de los niveles de glicemia estrecho para prevenir la hipoglicemia, debido a que si se presenta puede causar severos daños neurológicos 5.
5.4 Efecto de la hipotermia terapéutica versus control. La RS de Den Hertog 2009 32 se seleccionó debido a que presentó una adecuada calidad metodológica (AMSTAR-2:12/16) (n=423), y encontró que los pacientes tratados con hipotermia terapéutica presentaron similares posibilidades de muerte o dependencia mayor (OR: 0,92; IC 95%: 0,59 - 1,42), similares posibilidades de muerte por cualquier causa (OR: 0,9; IC 95%: 0,5 - 1,5) y similar posibilidades de infecciones (OR: 1,46; IC 95%: 0,82 - 2,61) en comparación con el grupo control.
En base a lo presentado, la hipotermia terapéutica no evidencia algún beneficio en la reducción de muerte o discapacidad. Además, implica un mayor uso de recursos, presenta problemas de factibilidad, baja aceptación de los pacientes/médicos y una certeza de la evidencia muy baja. Por este motivo, el GEG decidió emitir una recomendación fuerte en contra de su uso.
Punto BPC
El GEG sugiere que en pacientes con ACVi se sugiere mantener la normotermia, debido a que con temperaturas elevadas (> 38°C) está asociado a daños neurológicos e incremento de la muerte intrahospitalaria 5.
5.5 Terapia antiagregante simple versus placebo. La RS de Sandercock 2014 33 se seleccionó por su adecuada calidad metodológica (AMSTAR-2:13/16) (n= 41 483), y encontró que los pacientes tratados con antiagregantes presentaron menor posibilidad de muerte (OR: 0,95; IC 95%: 0,91 - 0,99), menor recurrencia de ACV (OR: 0,77; IC 95%: 0,69 - 0,87), similar posibilidad de hemorragia intracraneal (OR: 1,23; IC 95%: 1,00 - 1,50), y mayor posibilidad de hemorragia extracraneal (OR: 1,69; IC 95%: 1,35 - 2,11) en comparación con el grupo placebo.
En base a lo presentado, la antiagregación simple presenta menor posibilidad de muerte o discapacidad, su uso presenta una buena aceptación por los pacientes/médicos, es factible de aplicar y presenta una calidad de la evidencia moderada. Por este motivo, el GEG decidió emitir una recomendación fuerte a favor de su uso.
Punto BPC
En pacientes con ACVi que no recibieron terapia trombolítica, iniciar la terapia antiagregante plaquetaria dentro de las primeras 48 horas del inicio de los síntomas. De la misma manera, en pacientes con ACVi que recibieron terapia trombolítica, iniciar el tratamiento antiagregante posterior a 24 horas de la administración de la terapia trombolítica, debido a que ha demostrado que reduce el riesgo de recurrencia de ACV y presenta pocos eventos adversos (hemorragias) 5. Además, en pacientes con ACVi usar Ácido Acetil Salicílico (AAS) (160 a 300 mg VO), luego administrar 100 mg/24h. Como alternativa, considerar el uso de 300 mg Clopidogrel, luego administrar 75 mg/24h, debido a que ha evidenciado que no incrementa el riesgo de hemorragia 5,34,35.
5.6 Terapia antiagregante dual versus simple. La RS de Liu 2016 36 se seleccionó por su adecuada calidad metodológica (AMSTAR-2:13/16) (n=8969), y encontró que los pacientes tratados con antiagregación doble presentaron menor posibilidad de recurrencia de ACVi (OR: 0,70; IC 95%: 0,60 - 0,81), menor posibilidad de eventos vasculares mayores (OR: 0,70; IC 95%: 0,60 - 0,81), similar posibilidad de hemorragia intracraneal, (OR:1,29; IC 95%: 0,56 - 2,93) y hemorragia extracraneal masiva (OR: 1,44; IC del 95%: 0,72 - 2,88).
En base a lo presentado, a pesar que la antiagregación dual presenta mayores beneficios, la certeza de la evidencia es muy baja, presenta problemas de factibilidad y su uso implica un mayor empleo de los recursos. Por este motivo, el GEG emitió una recomendación condicional en contra .
Punto BPC
El GEG sugiere que en pacientes con ACVi considerar el uso de doble antiagregación como tratamiento de corto plazo (21 días a 3 meses) en ciertos casos de ACVi o AIT con estenosis de ≥ 50% de arteria carótida interna, cerebral media y posterior, vertebral y basilar por 3 meses, debido a que se ha evidenciado que reduce el riesgo de recurrencia de ACV sin que se eleve considerablemente el riesgo de sangrado 37.
5.7 Terapia anticoagulante inmediata versus placebo o terapia antiagregante:
5.7.1 Terapia anticoagulante inmediata versus placebo. La RS de Sandercock 2015 34 se seleccionó por su adecuada calidad metodológica (AMSTAR-2:14/16) (n=23,748), y encontró que los pacientes tratados con anticoagulantes presentaron similar posibilidad de muerte o dependencia mayor (OR: 0,99; IC 95%: 0,93 - 1,04), menor posibilidad de recurrencia de ACV (OR: 0,76; IC 95%: 0,65 - 0,85), mayor posibilidad de hemorragia intracraneal (OR: 2,55; IC 95%: 1,95 - 3,33) y extracraneal masiva (OR: 2,99; IC 95%: 2,24 - 3,99) en comparación con el grupo placebo.
5.7.2 Terapia anticoagulación inmediata versus terapia antiagregante. La RS de Berge 2002 38 se seleccionó por su adecuada calidad metodológica (AMSTAR-2:) (n=16 558), y encontró que los pacientes tratados inmediatamente con anticoagulantes presentaron similares posibilidades de muerte o dependencia mayor (OR: 1,07; IC 95%: 0,99 a 1,15), similar posibilidad de muerte durante el periodo de tratamiento (OR: 1,04; IC del 95%: 0,92 a 1,19), similar posibilidad de recurrencia de ECV (OR: 1,09; IC 95%: 0,89 a 1,33), y mayor posibilidad de hemorragia intracraneal (OR 2,27; IC del 95%: 1,49 a 3,46) y extracraneal (OR: 1,94; IC 95%: 1,20 a 3,12) en comparación con el grupo tratado con antiagregantes.
Según lo evidenciado, el empleo de la terapia de anticoagulación inmediata no reduce la posibilidad de muerte o discapacidad e incrementa el número de eventos adversos (calidad de la evidencia moderada). Además, genera un mayor uso de los recursos y presenta problemas de factibilidad. Por este motivo, el GEG decidió emitir una recomendación fuerte en contra.
Punto BPC
El tratamiento anticoagulante en pacientes con ACVi de etiología cardioembólica suele realizarse entre los 4 y 14 días debido a que es importante considerar el tiempo de enfermedad, severidad y extensión del infarto cerebral, según la ley de Diener.
5.8 Estatinas versus placebo. La RS de Chroinin 2013 39 se seleccionó por su adecuada calidad metodológica (AMSTAR-2: 8/16) (n=113 148), y encontró que los pacientes tratados con estatinas redujeron la posibilidad de muerte a los 90 días (OR: 1,41; IC del 95%: 1,29 a 2,56), presentaron mayor posibilidad de beneficio funcional a los 30 días (OR 1,64; IC del 95%: 1,14 a 2,36) y 90 días (OR: 1,41; IC del 95%: 1,29 a 2,56) en comparación con el placebo.
En síntesis, las estatinas reducen la posibilidad de muerte y presentan mayor beneficio funcional. Además, presentan una buena aceptación por parte de los pacientes/médicos; sin embargo, genera un incremento de los recursos y la certeza de la evidencia es muy baja. Por este motivo, el GEG decidió emitir una recomendación condicional a favor de su empleo.
Pregunta 6: En pacientes con ACVi ¿Cuáles son las intervenciones de neuroprotección más efectivas y seguras?
De la evidencia a la decisión:
En las personas con ACVi, el "área de penumbra" es aquella zona que rodea al área infartada, y que puede convertirse en esta última 40. Se postula que la citicolina, sulfato de magnesio, manitol, hemodilución y células madre interrumpen los procesos bioquímicos y hemodinámicos que producen este daño e incrementarían la presencia de células progenitoras en las áreas de isquemia 40,41.
Por este motivo, el GEG consideró importante conocer si estas intervenciones denominadas "neuroprotectoras" son efectivas y seguras.
Para esta pregunta clínica se realizaron cinco preguntas PICO:
Efecto de la citicolina. La RS de Shi 2016 40 (n=4039) fue seleccionada por su adecuada calidad metodológica (AMSTAR-2: 11/16), y encontró que la citicolina, a diferentes concentraciones (500 a 2000 mg) y con un seguimiento de 12 semanas a 3 meses, no redujo la posibilidad de muerte (OR: 0,91; IC95% 0,07 - 1,09), ni la dependencia (OR: 1,02; IC95% 0,87 - 1,24) frente al grupo placebo.
Considerando que la citicolina no reduce la posibilidad de muerte o dependencia y presenta una adecuada aceptación de los pacientes/médicos. Sin embargo, genera un mayor uso de recursos y presenta una certeza de la evidencia baja. Por este motivo, el GEG decidió emitir una recomendación condicional en contra de su uso.
Efecto del sulfato de magnesio. Para esta pregunta no se encontraron RS; por ello, se seleccionó el ECA de Saver 2015 41 (n=1700), encontró que el sulfato de magnesio no redujo la posibilidad de muerte (OR: 0,99; IC95% 0,76 - 1,29) ni mejoró la discapacidad mínima o nula (ERm de 0 a 1) (OR: 0,98; IC95% 0,81 - 1,20) a los 90 días frente al grupo placebo.
Considerando que el sulfato de magnesio no reduce la posibilidad de muerte o discapacidad con una certeza de la evidencia alta, pero su uso presenta poca factibilidad, implica un incremento de los recursos y no es aceptado por los pacientes/médicos. Por este motivo, el GEG decidió emitir una recomendación fuerte en contra.
Efecto del manitol. Se consideró la RS de Bereczki 2007 42 (n=226) por su buena calidad metodológica (AMSTAR-2: 14/16), encontró que el manitol no redujo la posibilidad de muerte ni la dependencia (OR: 1,28; IC95% 0,64 - 2,56) frente a la terapia estándar.
Por lo tanto, el manitol no reduce la posibilidad de muerte o dependencia. Además, presenta una adecuada factibilidad y es aceptado por los médicos especialistas; sin embargo, es posible que no sea aceptado por los pacientes, así como, presenta una certeza de la evidencia es muy baja. Por este motivo, el GEG decidió emitir una recomendación condicional en contra.
Efecto de la hemodilución. Se consideró la RS de Chang 2014 43 (n=4174) por su buena calidad metodológica (AMSTAR-2: 15/16), encontró que la hemodilución no redujo la posibilidad de muerte al primer mes (RR: 1,05; IC95% 0,93 - 1,20) ni la muerte o dependencia a los seis meses (RR: 0,96; IC 95% 0,85 - 1,07).
Según lo evidenciado, la hemodilución no reduce la posibilidad de muerte o dependencia a los seis meses. Además, presenta una adecuada factibilidad y es aceptado por los médicos; sin embargo, es posible que no sea aceptado por los pacientes y presenta una certeza de la evidencia baja. Por este motivo, el GEG decidió emitir una recomendación condicional en contra.
Efecto de las células madre. La RS de Wang 2016 44 se seleccionó por su adecuada calidad metodológica (AMSTAR-2: 11/16), y encontró que la terapia con células madre no redujo la posibilidad de muerte (RR: 0,59; IC 95% 0,29 - 1,19) ni la discapacidad (ERm) (0,40; IC 95% -0,14 - 0,93) en comparación con el grupo placebo.
En base a lo presentado, la terapia con células madre no reduce la muerte ni la discapacidad, a pesar de ser factible, presenta un mayor uso de los recursos y la certeza de la evidencia es baja. Por este motivo, el GEG decidió emitir una recomendación condicional en contra.
Pregunta 7: En pacientes con ACVi ¿es eficaz y seguro la intervención quirúrgica (craneotomía o hemicraniectomía) frente al tratamiento estándar?
De la evidencia a la decisión:
El ACVi extenso o maligno es el ACVi que se produce por la oclusión de las arterias cerebrales de mediano calibre, presenta gran edema cerebral que incrementa la presión intracraneal (PIC), generando un cuadro clínico neurológico severo que se asocia a una discapacidad mayor o muerte 45,46. El tratamiento estándar para reducir la PIC consiste en el empleo de agentes hiperosmóticos, ventilación artificial e hiperventilación, hipotermia terapéutica, posición elevada de la cabeza y el empleo de sedantes. Por otro lado, la cirugía descompresiva con extirpación del tejido óseo (cráneo) y la incisión de la duramadre, permite reducir la PIC 47. Sin embargo, existe controversia sobre cuál es la técnica más adecuada y segura para prevenir desenlaces clínicos y desbastadores en los pacientes con ACVi 45.
Para responder a esta pregunta se seleccionó la RS de Alexander 2016 45 con adecuada calidad metodológica (AMSTAR-2: 15/16) (n=388), y encontró que el grupo con hemicraniectomía presentó una mayor probabilidad de supervivencia a los 12 meses (RR: 2,05; IC del 95%: 1,54 - 2,72), mayor probabilidad de supervivencia con discapacidad leve a moderada a los 12 meses (RR: 1,58; IC del 95%: 1,02 - 2,46), y con discapacidad moderada a los 12 meses (RR: 2,25; IC del 95%: 1,51 - 3,35) frente al tratamiento estándar.
Considerando que la intervención quirúrgica presenta mayores beneficios. El GEG decidió emitir una recomendación fuerte a favor de su realización, debido a que presenta una certeza de la evidencia moderada y a largo plazo genera un menor uso de recursos, pero la aceptación de los pacientes/médicos es baja.
Puntos de BPC:
El GEG consideró que los pacientes con ACV extenso o maligno requieren de una evaluación especialista para identificarlo tempranamente y definir las acciones terapéuticas. Además, monitorizar la PIC para mejorar la toma de decisiones 5. Además, se consideró que la intervención quirúrgica descompresiva debe iniciarse lo más pronto posible, dentro de las 48 horas y no más de 96 horas, debido a que reduce la mortalidad y aumenta el éxito de un resultado funcional favorable 48-52. Además, que a los pacientes mayores de 60 años con ACVi extenso o maligno se considera realizar la craniectomía descompresiva después de una cuidadosa consideración del estado funcional premórbido, esto debido a que se ha evidenciado que este tratamiento reduce la mortalidad sin incrementar el riesgo de discapacidad severa 50,53. Por último, el GEG consideró que para pacientes con ACVi extenso o maligno infratentorial que presenten un deterioro neurológico por compromiso tronco cerebral se considera la realización de una intervención quirúrgica descompresiva debido a que reduce la mortalidad 5,54.
Pregunta 8: En pacientes con ACVi ¿cuáles son las intervenciones más efectivas y seguras para la rehabilitación del paciente con ataque cerebrovascular isquémico de origen arterial durante los primeros 15 días posteriores al inicio de los síntomas?
De la evidencia a la decisión:
Las personas que sobreviven a un ACVi presentan distintos tipos y grados de discapacidad que pueden ser; motora, sensitiva, sensorial o cognitiva. La prevención terciaria consiste en terapias que reducen esta discapacidad y mejoran la funcionalidad a los pacientes. Las terapias de rehabilitación temprana incluyen principalmente la física (recuperación motora) y de alimentación/nutrición (recuperación funcional) 2.
Por este motivo, el GEG considera importante conocer cuáles son las intervenciones de rehabilitación más efectivas y seguras.
Para esta pregunta clínica se realizaron cinco preguntas PICO:
La primera pregunta PICO comparó el uso de sonda nasogástrica sistémica/restrictiva. Se seleccionó el ECA de Food 2005 55 (n=859), no encontró diferencia en la reducción de la posibilidad de muerte (OR: 0,79; IC95%: 0,61 a 1,04) o discapacidad/muerte (OR: 0,94; IC95% 0,68 a 1,31) entre el uso de la sonda nasogástrica sistémica y restrictiva.
El GEG decidió emitir una recomendación condicional a favor al uso de la SNG en pacientes con ACVi que no pueden deglutir de forma segura, debido a que presenta una adecuada aceptación de los pacientes/médicos con una certeza de la evidencia baja. Además, el GEG decidió emitir una recomendación condicional en contra al uso sistémico de sonda nasogástrica en todos los pacientes con ACVi para garantizar su alimentación, debido a que presenta una buena aceptación de los pacientes/médicos, pero implica un mayor uso de los recursos y una certeza de la evidencia baja.
La segunda pregunta PICO evaluó el uso de los complementos nutricionales. La RS de Geeganage 2012 56 (n=4391) encontró que la administración de complementos nutricionales no redujo la muerte (OR: 0,58; IC 95%: 0,28 a 1,21) ni las úlceras por presión (OR: 1,06; IC95%: 0,94 a 1,20) en comparación con el grupo placebo.
El GEG decidió emitir una recomendación condicional en contra al uso de complementos nutricionales debido a que no se evidencia un beneficio de su empleo, debido a que presenta una adecuada aceptación de los pacientes/médicos, pero genera un mayor uso de los recursos y presenta una certeza de la evidencia baja.
La tercera pregunta PICO evaluó el empleo de la terapia del lenguaje y habla. La RS de Kelly 2010 57 (n=376) encontró que la terapia del lenguaje y habla (TLH) favoreció la comunicación funcional (DME 0,28; IC95%: 0,06 a 0,49) y comprensión lectora (DME 0,29; IC95%: 0,03 a 0,55) a comparación de no usarla.
Considerando que la terapia de lenguaje y habla favorece la comunicación y el lenguaje expresivo, es factible, presenta una buena aceptación de los pacientes/médicos y la certeza de la evidencia es baja. El GEG decidió emitir una recomendación condicional a favor de su uso.
La cuarta pregunta PICO evaluó el manejo de la disfagia con intervenciones conductuales. La RS de Geeganage 2012 56 (n=6779) encontró que las intervenciones conductuales reducen la posibilidad de disfagia (OR: 0,52; IC95% 0,30 - 0,88) pero no la neumonía (OR: 0,5; IC95%: 0,24 a 1,04) ni la mortalidad (OR: 1,05; IC95% 0,63 a 1,75) en comparación con la no aplicación de intervenciones conductuales.
Considerando que el manejo de la disfagia reduce la posibilidad de las complicaciones, es factible de realizar, tiene buena aceptación de los pacientes/médicos y presenta una certeza de la evidencia baja. El GEG decidió emitir una recomendación condicional a favor de su uso.
La quinta pregunta PICO comparó el efecto del inicio precoz vs inicio tardío de la rehabilitación física. La RS de Lynch 2014 58 (n=227) encontró que los pacientes que comenzaron su rehabilitación en los primeros 3 días redujeron la discapacidad en 15,3% (p<0,001) en comparación a quienes lo realizaron posteriormente. Sin embargo, el grupo a los que se les realizó una movilización precoz (24 horas) presentaron resultados similares en la mortalidad a los tres meses (RR: 1,21; IC95%: 0,76 - 1,65) y la discapacidad (Rankin de 0 a 2) (RR: 0,80; IC95%: 0,58 - 1,02) en comparación con los pacientes que tuvieron una movilización tardía.
Por lo tanto, el GEG decidió emitir una recomendación condicional a favor, debido a que el inicio precoz de la rehabilitación física reduce la discapacidad, presenta una buena aceptación de los pacientes/médicos y es factible de realizar. Sin embargo, esto implica un mayor uso de los recursos y presenta una certeza de la evidencia baja.
Puntos de BPC:
El GEG-local consideró importante mencionar que en pacientes con ACVi se sugiere realizar una evaluación de la deglución, nivel de conciencia, comprensión y ejecución de órdenes motoras, debido a que los pacientes puedan recuperar algunas funciones de forma secuencial y esto mejora su calidad de vida. Además, en pacientes con ACVi desnutridos o en riesgo de desnutrición se sugiere iniciar la alimentación enteral temprana para disminuir la progresión de este cuadro, manteniendo un adecuado aporte calórico. Para el soporte adicional con terapias de lenguaje/habla, el cuidador debe estar capacitado. Así también, la rehabilitación temprana domiciliaria (ejercicios de deglución, cambios de posicionamiento del paciente para recibir la alimentación) para pacientes con ACV estables es importante para reducir el riesgo de adquirir infecciones nosocomiales y facilitar su reinserción en actividades de vida diaria.