Sr. Editor,
La correcta identificación de fallecidos por COVID-19 se convierte en una necesidad epidemiológica y social durante esta pandemia, proporcionando cifras de vital importancia para que los epidemiólogos y bioestadísticos puedan determinar una tasa de letalidad más precisa en nuestro país (por menor presencia de falsos negativos), elaborar proyecciones de la enfermedad y emprender medidas que eviten el colapso de los sistemas de salud 1.
En la mayoría de países, la detección de casos de COVID-19 post mortem se basa en la recomendación de los Centers for Disease Control and Prevention (CDC) de los Estados Unidos, donde el diagnóstico de un caso sospechoso debe basarse en el resultado de una prueba de RT-PCR mediante un hisopado orofaríngeo o muestras de tejido pulmonar 2. Sin embargo, en países como el Perú, esta sugerencia se torna inviable debido a la limitada oferta de laboratorios moleculares que procesen estas muestras, lo que deviene en demoras en el manejo de los cadáveres, afectación emocional de la familia y del personal asistencial debido a la conservación de los cuerpos en el establecimiento de salud o en la morgue.
El 4 de abril de 2020, el Ministerio de Salud modificó la Directiva Sanitaria N° 087-MINSA/2020/DIGESA para el manejo de cadáveres por COVID-19, en la que se establece que toda muerte sospechosa debe ser manejada como un caso confirmado 3. Esto implica una mejora en los procesos de atención que se llevaban hasta ese momento, pero no brinda la confirmación necesaria de la causa de muerte, lo que potencialmente podría significar una distorsión en las estadísticas poblacionales. En este contexto, la posibilidad de aplicar otros métodos diagnósticos en casos post mortem con sospecha no confirmada de COVID-19, puede surgir como una alternativa razonable.
Con el objetivo de describir la evidencia disponible que sustente la posibilidad de uso de pruebas serológicas en personas que fallecen por sospecha de COVID-19, se llevó a cabo una búsqueda sistemática de literatura en MEDLINE/PubMed y Google Académico (ver estrategias de búsqueda en Material suplementario). Se buscó indicadores como el tiempo promedio transcurrido entre el inicio de síntomas y el fallecimiento, o la relación entre la severidad de los casos y la probabilidad de encontrar títulos detectables de IgG o IgM (alternativa actual por identificación serológica), en estudios previamente publicados. Se encontraron diez estudios realizados tanto con apoyo de modelos matemáticos (n=5), como con datos epidemiológicos de pacientes hospitalizados (n=5); en el primer caso, las estimaciones del tiempo entre el inicio de síntomas y el fallecimiento oscilan entre 16,1 días (IC 95% (intervalo de confianza al 95%): 13,1-20,2) hasta 22,3 días (IC 95%: 18,0-82,0) después del inicio de los síntomas; mientras que, los datos epidemiológicos encuentran una mediana entre 10,0 días (RIQ (rango intercuartil): 7,0-13,0) a 21,0 días (RIQ: 17,0-27,5), con un estudio que estima un promedio de 22,3 ± 9,2 días (Tabla 1).
Tabla 1 Publicaciones que calcularon el tiempo entre la aparición de síntomas y la muerte en pacientes con COVID-19.
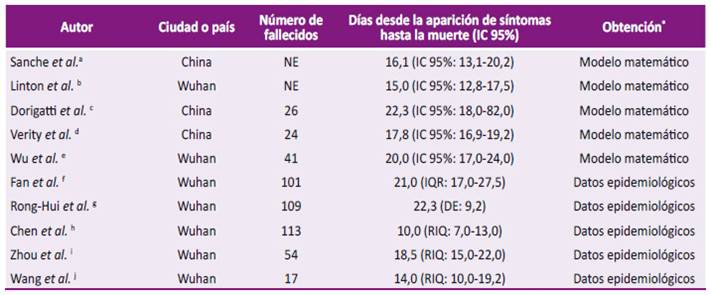
* Sanche et al. Emerging Infectious Diseases journal - CDC. 2020; 26 (7); b Linton et al. Available Case Data. J Clin Med. 2020;9(2); c Dorigatti I et al. Imperial College London; 2020; d Veriti R et al. The Lancet Infectious Diseases. Elsevier; 2020;0(0); e Wu et al. Nature Medicine. Nature Publishing Group; 2020;1-5; f Fan et al. medRxiv. Cold Spring Harbor Laboratory Press; 2020;2020.03.09.20033068; g Du et al. Ann Am Thorac Soc. 2020; h Chen et al. BMJ. British Medical Journal Publishing Group; 2020;368; i Zhou et al. The Lancet. Elsevier; 2020;395(10229):1054-6; j Wang et al. J Infect. 2020.
* En el caso de datos epidemiológicos se presentan medidas de tendencia central, mientras que los modelos matemáticos presentan estimaciones. NE: no estimado; RIQ: rango intercuartil, asociado a mediana; DE: desviación estándar asociado a promedio; IC 95%: intervalo de confianza al 95%, asociado a promedios en casos de data epidemiológica.
De acuerdo a lo encontrado en estudios previos, se conoce que a partir del día siete después del inicio de los síntomas, las pruebas serológicas basadas en la detección de IgM/IgG producido por el huésped durante la infección, pueden tener una mayor sensibilidad que el RT-PCR 4. Estudios previos, como el de Zhao et al., estimaron que las pruebas serológicas de inmunoensayo tuvieron una sensibilidad de 94,3% (IgM) y 79,8% (IgG), en comparación al RT PCR obtenido de hisopado nasofaríngeo, que detecta solamente el 45,5% de casos 5. Por su lado, Vidal-Anzardo et al., en un estudio en Lima-Perú, encontraron que los valores de sensibilidad de pruebas serológicas rápidas llegaban a un 50% después de la segunda semana, siendo necesario resaltar que estos valores fueron preliminares y que se calcularon en una muestra heterogénea 6.
Asimismo, se encontraron cuatro estudios que abordaron dentro de sus objetivos secundarios, el análisis entre la severidad de los casos y los títulos de IgG o IgM. Zheng et al.7, no encontraron diferencias en los niveles de anticuerpos producidos en dos grupos de pacientes: no severos (34 pacientes) y severos (22 pacientes) (p=0,130 para IgM, y p=0,620 para IgG). Sin embargo, Zhao et al.5 evidenciaron diferencias entre los títulos de anticuerpos (en general) y la severidad del cuadro en 173 pacientes calificados como críticos (n=32) y no críticos (p=0,004). Adicionalmente, se encontraron tres manuscritos que estaban en situación de pre-imprenta, que también muestran resultados consistentes con una relación directa entre el incremento de los anticuerpos y el desenlace de fatalidad, tanto en los casos de los niveles de IgM 8, IgG 9 y la combinación del ratio linfocitosneutrófilos y los niveles de IgG 10.
Al realizar las búsquedas sistemáticas antes mencionadas, no se encontró estudios previos que hayan evaluado el rendimiento diagnóstico de estas pruebas en fallecidos, ni experiencias institucionalizadas similares en otros países. Al respecto, solo la CDC ha mencionado que debido a que los test serológicos rápidos aún no han sido validados para el diagnóstico de COVID-19 por sí mismos, el uso de pruebas serológicas post mortem debe considerar información adicional como el tiempo transcurrido desde el inicio de síntomas 2. Basado en ello, consideramos que, si bien la evidencia no es suficiente para formular una recomendación directa, se deben generar iniciativas de investigación que contribuyan a solucionar esta problemática. Esta medida podría ser de utilidad, sobre todo en casos de fallecimientos súbitos no institucionalizados, en los que resultados de esta prueba, en conjunto con la información clínica disponible, podrían apoyar a la toma de decisiones en el equipo de salud y el inicio rápido del protocolo COVID-19 acorde a la normatividad vigente; más aún en entornos en los que el acceso a pruebas moleculares se encuentra limitado.















