INTRODUCCIÓN
En los primeros ocho meses de la pandemia por el virus SARS- CoV-2 más de 30 000 peruanos perdieron la vida 1. La evidencia procedente de reportes y estudios de cohortes de pacientes con neumonía por el SARS-CoV-2 indican una mayor letalidad en adultos mayores de 65 años (odds ratio (OR): 3,80), del sexo masculino (OR: 1,50), con comorbilidades cardiovasculares (OR: 2,50), y cuadros clínicos severos 2-4. Asimismo, la evidencia respecto al tratamiento de la neumonía por el SARS-CoV-2 indica que algunos medicamentos como hidroxicloroquina (HCQ) y azitromicina (AZM) no tendrían ningún beneficio, pero aún contradictorios respecto a otros, tales como los corticoides, enoxaparina (ENX) y el lopinavir/ritonavir (LPV/r) 5,6.
En el Perú aún no se disponen de estudios representativos que evalúen los factores asociados a la mortalidad de la neumonía por el SARS-CoV-2. Un estudio de serie de casos en un hospital de referencia nacional de Lima mostró que, de 17 pacientes hospitalizados por neumonía a causa del SARS-CoV-2, el 77% fueron de sexo masculino, 35% fueron adultos mayores, 24% tenían hipertensión arterial (HTA), y cuatro de ellos fallecieron 7. Por su parte, el Ministerio de Salud (MINSA) viene publicando documentos técnicos para orientar el tratamiento de pacientes con sospecha o confirmación de neumonía por el SARS-CoV-2 en Perú, utilizando la evidencia científica internacional disponible al momento 8.
El objetivo de esta investigación fue describir los principales factores asociados a la mortalidad en una cohorte de pacientes hospitalizados con neumonía por el SARS-CoV-2 en un hospital público de Lima, Perú.
MATERIALES Y MÉTODOS
Diseño del estudio
Se realizó un estudio de cohorte retrospectivo que se llevó a cabo en julio de 2020 e incluyó a los pacientes hospitalizados entre el 1 de abril al 1 de mayo de 2020. Se incluyeron casos confirmados o sospechosos de neumonía por el SARS-CoV-2 8, con selección de manera consecutiva no aleatoria. Se excluyeron gestantes y pacientes con enfermedades quirúrgicas concomitantes. La infección por el virus del SARS-CoV-2 se confirmó a través de pruebas rápidas o moleculares, según criterio clínico.
Ámbito de estudio
El Hospital de Emergencias de Villa el Salvador (HEVES) es un hospital público del MINSA, ubicado al sur de Lima, que fue designado desde abril de 2020 exclusivamente a la atención de pacientes con el virus del SARS-CoV-2, disponiendo 40 camas de emergencia, 160 camas de hospitalización y 30 camas de unidad de cuidados intensivos (UCI). El hospital cuenta con un equipo clínico multidisciplinario que ha venido desarrollando y actualizando protocolos de manejo local, adicionales a las directivas del MINSA y a los protocolos internacionales 8.
Variables y mediciones
Las variables fueron recolectadas en una plataforma virtual de AppSheet® usando como fuente de información la historia clínica. Se estableció como desenlace primario a la mortalidad intrahospitalaria. Entre las principales variables de interés se consideraron variables demográficas: edad, sexo, y antecedentes; variables clínicas: síntomas, signos, tiempo de enfermedad, funciones vitales, peso y talla; variables de laboratorio e imágenes: análisis de gases arteriales (AGA), hemograma, marcadores inflamatorios, de coagulación, bioquímicos, y tomografía pulmonar, evaluados al ingreso. Asimismo, se midieron variables de tratamiento: tiempo a inicio (días) y uso de antibióticos (azitromicina (AZM)), anticoagulantes (enoxaparina (ENX)), corticoides (metilprednisolona y dexametasona), antivirales (LPV/r) e HCQ durante su estancia en emergencia y hospitalización. Se clasificó a los pacientes con neumonía por el SARS-CoV-2 al ingreso en leve (frecuencia respiratoria (FR) <30, saturación de oxígeno en oximetría de pulso (SatO2) >93%, relación de presión arterial de oxígeno y fracción inspirada de oxígeno (PaO2/FIO2) >300), moderado (FR ≥30, SatO2 ≤93%, PaO2/FiO2300-201), severo (PaO /FiO 200-101, proteína C reactiva (PCR) 5-249 mg/dL, linfocitos <800/mm3) y crítico (PaO /FiO PCR >250 mg/dL) según criterios adaptados de China 9,10. Se usó un score de severidad tomográfico tomando en cuenta la clasificación propuesta por el Instituto Nacional de Enfermedades Respiratorias de México (11) en leve (1 a 5 puntos), moderada (>5 a 15 puntos) y severa (>15 puntos), la cual se realizó por dos médicos neumólogos expertos para todos los casos. Asimismo, se clasificó la extensión porcentual pulmonar tomográfica en leve (<25%), moderado (25%-50%), severo (50%-75%) y crítico (>75%).
Para analizar los tratamientos, se utilizaron los días transcurridos entre el inicio de síntomas y el inicio del tratamiento recibido y el total de días recibidos durante la hospitalización. En el caso de los corticoides, adicionalmente se separó en el análisis el uso en pulsos y no pulsos, y se calculó la dosis total de corticoides considerando la equivalencia de dexametasona y metilprednisolona 12, ya que la elección dependió de su disponibilidad. En el caso de ENX, se calculó la dosis total, dado que los pacientes la recibieron de forma profiláctica o como anticoagulación plena. El uso de HCQ, AZM, y ENX estuvo incluido en el protocolo de manejo inicial del HEVES, por lo que su prescripción fue generalizada, mientras que las indicaciones de LPV/r y corticoterapia sistémica quedaron bajo criterio médico.
Análisis estadístico
Se usaron estadísticos descriptivos, tales como porcentajes y medidas de tendencia central. En aquellas variables numéricas con una distribución normal se utilizó la media y la desviación estándar (DE), y en aquellas con una distribución no normal se utilizó la mediana y el rango intercuartil (RIC). Los análisis bivariados entre las variables independientes y el desenlace primario (mortalidad) se llevaron a cabo con la t de Student (variables numéricas continuas con una distribución normal), la prueba de U de Mann-Whitney (variables numéricas continuas con una distribución no normal), y la prueba exacta de Fisher (variables categóricas). En el análisis de regresión de Poisson se calcularon los riesgos relativos (RR) crudos con sus respectivos intervalos de confianza (IC) al 95% de los factores asociados a mortalidad, y se incluyeron en un modelo multivariado aquellas variables más relevantes para el desenlace estudiado siguiendo un criterio epidemiológico y estadístico. Finalmente, se utilizó el estimador de Kaplan-Meier para evaluar las curvas de supervivencia según la severidad clínica al ingreso. Se utilizó el programa estadístico Stata versión 16.1 (Statacorp, TX, USA).
Consideraciones éticas
Este proyecto de investigación fue aprobado por el Comité Institucional de Ética e Investigación del HEVES, con código 001-2020. El protocolo fue registrado en la base de datos del Instituto Nacional de Salud del Perú 13.
RESULTADOS
En el mes de abril del 2020, de un total de 412 pacientes hospitalizados, se incluyó a 122 pacientes con sospecha o confirmados para neumonía por el SARS-CoV-2 (Tabla 1). El 70,5% fueron de sexo masculino, con un promedio de edad de 55,8 años (rango 18-87). La mediana de tiempo de duración de síntomas fue de 7,0 días (RIC 6-10), y el de tiempo de hospitalización fue de 8,5 días (RIC 6-12). La mortalidad de nuestra muestra fue de 36,9%. De un total de 56 (45,9%) pacientes que requirieron de atención en la unidad de cuidados intensivos (UCI), sólo 9 (16,1%) alcanzaron una cama UCI, con una mediana de tiempo de espera de 2 días (RIC 1-3). Casi el total de pacientes que ingresaron con una severidad clínica moderada sobrevivieron, mientras que la mayoría de los críticos fallecieron (p<0,001) (Tabla 1). Se observaron diferencias significativas en las medianas de tiempo desde inicio de síntomas a resultado positivo en las pruebas rápidas para SARS-CoV-2 (prueba estadística de Kruskal-Wallis, p=0,033). Así, las medianas y RIC de tiempo en días a prueba de SARS-CoV-2 positiva para la prueba molecular (n=73) fue de 7 5-10, mientras que para la prueba rápida IgM (n=29) fue de 4,5 3-7, para la prueba rápida IgM/IgG (n=6) fue de 7 6-10, y para la prueba rápida IgG (n=5) fue de 11 9-13.
Tabla 1 Características de los participantes incluidos en el estudio.
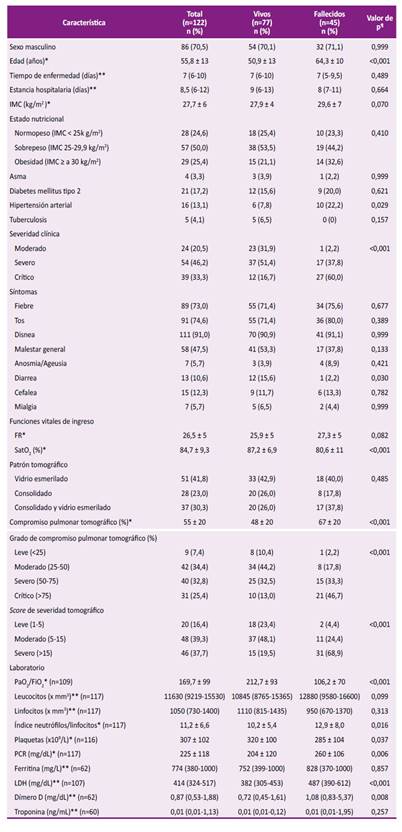
* Media ± DE; **Mediana (RIC); ¶ Variables categóricas: prueba exacta de Fischer; variables continuas de distribución normal: t de Student; variables continuas de distribución no normal: prueba U de Mann Whitney. aIMC: índice de masa corporal; PAM: presión arterial media; T: temperatura; FC: frecuencia cardíaca; FR: frecuencia respiratoria por minuto; SatO2: saturación oxígeno; PaO2/FiO : índice presión arterial de oxígeno / fracción inspirada de oxígeno; PCR: proteína C reactiva; LDH: lactato deshidrogenasas.
Se observaron diferencias estadísticamente significativas entre los sobrevivientes y fallecidos respecto a la edad, antecedentes de HTA, SatO2 en oximetría de pulso, índice PaO2/FiO2 en el AGA, conteo de plaquetas, índice neutrófilos/linfocitos (INL), PCR, dímero D (DD), LDH, y en la extensión de compromiso pulmonar y severidad tomográficos (Tabla 1). Respecto a tratamiento, se observó diferencias entre los sobrevivientes y fallecidos respecto a la dosis total usada de ENX profiláctica, la duración y la dosis total del tratamiento con corticoides, y la duración del tratamiento con LPV/r. Asimismo, si bien no hubo diferencias significativas, se observó que los sobrevivientes, en comparación a los que fallecieron, iniciaron más tempranamente LPV/r (Tabla 2).
Tabla 2 Caracterización de los tratamientos recibidos según condición de egreso.
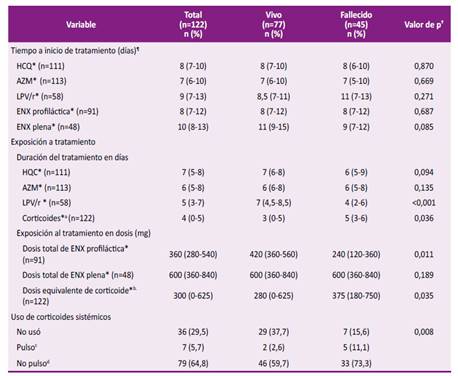
*Mediana (RIC); ¶ Tiempo transcurrido en días desde el inicio de los síntomas hasta el inicio del medicamento; † Variables categóricas: prueba exacta de Fischer; variables continuas de distribución no normal: prueba U de Mann Whitney. a Se agrupó el uso de los corticoides dexametasona y metilprednisolona. b Se calculó la dosis total de corticoides considerando la bioequivalencia de dexametasona y metilprednisolona, ya que la elección dependió de su disponibilidad 12. c Dosis de metilprednisolona mayor o igual a 500 mg/día. d Dosis de metilprednisolona igual a 125 mg/ día o dexametasona igual a 16 mg/día. Se excluyeron a los pacientes que recibieron pulsos de corticoide. HCQ: hidroxicloroquina; AZT: azitromicina; LPV/r: lopinavir/ritonavir; ENX: enoxaparina.
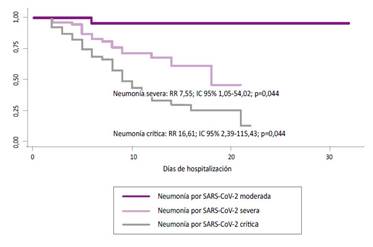
Se encontró que las variables edad, HTA, score de severidad y porcentaje de compromiso pulmonar tomográficos, INL, PCR, el DD y exposición (días) corticoide sistémico incrementaron el RR de muerte, mientras que mayores niveles de SatO2 en oximetría de pulso y de índice de PaO2/FiO2, así como la exposición a LPV/r y ENX profiláctica redujeron el RR muerte, con resultados estadísticamente significativos. No se encontraron resultados estadísticamente significativos para la exposición a HCQ y AZM. El análisis ajustado mostró que los factores edad, IMC, HTA, el índice de PaO2/FiO2, la exposición a corticoides y a LPV/r estuvieron asociados a mortalidad en nuestra cohorte de pacientes con neumonía por el SARS-CoV-2 (Tabla 3). Finalmente, el gráfico de Kaplan-Meier muestra las curvas de supervivencia según la severidad clínica al ingreso de los pacientes hospitalizados por neumonía por el SARS-CoV-2 (Figura 1).
Tabla 3 Factores clínicos y de tratamiento asociados a mortalidad por neumonía por SARS-CoV-2.
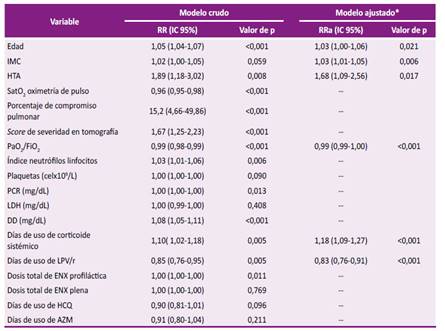
* El modelo incluyó las variables edad, sexo, IMC, hipertensión arterial, PaO2/FiO2, y la exposición (días de tratamiento) a corticoides sistémicos y LPV/r (n=53). Se optó por seleccionar la variable PaO2/FiO2 y desestimar las variables SatO2 en oximetría de pulso, porcentaje de compromiso pulmonar y score de severidad en la tomografía debido a de ellos, el primero es un marcador de laboratorio objetivo utilizado ampliamente para medir el compromiso clínico en los procesos pulmonares. No se incluyeron los análisis de laboratorio porque su medición estuvo relacionada a la disponibilidad de los reactivos. No se incluyó a la ENX profiláctica porque el tamaño del efecto fue mínimo.
DISCUSIÓN
Nuestros resultados muestran que los factores edad, HTA e IMC se asociaron a un mayor riesgo de muerte en los pacientes hospitalizados por neumonía por el SARS-CoV-2, los cuales son compatibles con los hallazgos de estudios en cohortes de otros países 14-16. Así, se requiere de una mayor evidencia que confirme o descarte que estos factores, u otros trastornos metabólicos como la diabetes mellitus 16, están asociados a una mayor mortalidad por neumonía por el SARS-CoV-2, ya que su prevención y manejo temprano podría reducir dicho riesgo.
También se identificó que los niveles registrados al ingreso de SatO2 en la oximetría de pulso y del PaO2/FiO2 en el AGA se asociaron a un mayor riesgo de muerte en nuestra cohorte de pacientes con neumonía por el SARS-CoV-2. De manera similar, diferentes estudios observacionales han asociado una mayor mortalidad con niveles de SatO por debajo de 88% y 90% 4,17 o con niveles de PaO /FiO por debajo de 200 3,18. En ese sentido, sugerimos llevar a cabo estudios de validación para determinar si los niveles de SatO2 y PaO2/FiO2 registrados al ingreso hospitalario podrían ser usados como factores pronósticos de mortalidad en los pacientes con neumonía por el SARS-CoV-2.
El análisis bivariado de los resultados de laboratorio encontró diferencias estadísticamente significativas entre sobrevivientes y fallecidos en los niveles al ingreso de los marcadores de inflamación PCR y LDH, en el INL, el conteo de plaquetas y el DD. Asimismo, el análisis de factores de riesgo mostró que la PCR, el INL y el DD se asociaron a un mayor riesgo de muerte con resultados estadísticamente significativos. Otros estudios previos también han encontrado diferencias entre sobrevivientes y fallecidos hospitalizados por neumonía por el SARS-CoV-2 en los niveles de la PCR, LDH y el INL 19-21, los cuales se explicarían por la hiperactivación de la inmunidad innata y un estado de hiperinflamación en los pacientes infectados por el SARS- CoV-2 22,23. Asimismo, otros estudios han descrito trastornos de la hemostasia, consecuencia de la disfunción endotelial inducida por dicha infección, lo que produce un estado de hipercoagulabilidad e hiperviscosidad que conllevan a un mayor consumo plaquetario y liberación de DD 24,25. También se ha reportado que las alteraciones del DD y la trombocitopenia estarían asociadas a una mayor mortalidad en los pacientes con neumonía por el SARS-CoV-2 26,27. En ese sentido, se requieren de mayores estudios que evalúen si estos marcadores de laboratorio pueden ser usados como predictores de muerte o mal pronóstico en los pacientes hospitalizados por neumonía a causa del SARS-CoV-2.
Nuestros resultados mostraron que el porcentaje de extensión del compromiso pulmonar se asoció a un mayor riesgo de muerte, mientras que no se presentaron diferencias estadísticamente significativas entre los patrones radiológicos de los sobrevivientes y fallecidos. Es reconocida la alta sensibilidad de la tomografía para el diagnóstico precoz de la neumonía por el SARS-CoV-2, así como su utilidad en la evaluación de la severidad y el seguimiento 28. En contraste a nuestros resultados, otros estudios han descrito que tanto la extensión como el patrón radiológico predominante serían determinantes para definir la severidad del compromiso pulmonar, proponiendo un modelo con estas dos características radiológicas para predecir la mortalidad 29. Así, el Instituto Nacional de Enfermedades Respiratorias de México 11, tomando en cuenta dichos hallazgos, propuso clasificar el score de severidad tomográfico en leve (1 a 5 puntos), moderado (>5 a 15 puntos) y severo (>15 puntos), el cual ha presentado una asociación estadísticamente significativa con un mayor riesgo de muerte en nuestra cohorte. Se requieren de mayores estudios que validen esta clasificación radiológica como predictor de muerte o mal pronóstico en los pacientes hospitalizados por neumonía a causa del SARS-CoV-2.
En relación con los tratamientos, es importante destacar que el diseño del presente estudio no permite derivar conclusiones acerca de la eficacia y seguridad de los medicamentos, sino que permiten generar hipótesis preliminares para que sean evaluados en estudios más amplios. Así, se encontró resultados estadísticamente significativos respecto a la exposición a corticoides, LPV/r y ENX profiláctica y su asociación con la mortalidad, mientras que no se encontró resultados estadísticamente significativos con la exposición a HCQ y AZM. Estos hallazgos tienen un alto riesgo de sesgos, principalmente debido al hecho de que la indicación de algunos de los tratamientos se puede haber relacionado a gravedad clínica valorada por el médico tratante. Respecto a los corticoides, los resultados mostraron que su uso, especialmente en forma de pulsos, así como una mayor duración de tratamiento, se asociaron a un mayor riesgo de muerte. Cabe indicar que las dosis usadas en el periodo en el cual se llevó a cabo el estudio fueron altas, con dosis de metilprednisolona entre 125 mg a 500 mg diarios, así como de dexametasona entre 12 mg a 20 mg diarios, lo cual puede haber sido perjudicial en los pacientes que se encontraban en una fase inicial de la infección por el SARS-CoV-2. Estos hallazgos serían compatibles con estudios previos en pacientes con SARS y MERS que mostraron que el uso de corticoides retrasa el aclaramiento viral 6, y estudios preliminares en pacientes con neumonía por el SARS-CoV-2 que sugieren que el uso de corticoides está asociado a un mayor riesgo de muerte 30. En esta misma línea, los hallazgos preliminares de un ensayo clínico aleatorizado (ECA) han mostrado que las dosis bajas de corticoides (dexametasona 6 mg) reduce la mortalidad de los pacientes hospitalizados por neumonía a causa del SARS-CoV-2 hasta en un 20% 31, por lo que se requieren de mayores estudios que definan el balance riesgo beneficio de los corticoides en este grupo de pacientes.
Por otro lado, los resultados mostraron que la exposición a LPV/r y ENX a dosis profilácticas estuvieron asociados a un menor riesgo de muerte en los pacientes con neumonía por el SARS- CoV-2. Con respecto a LPV/r, un ECA mostró que su uso redujo la mortalidad hasta en un 8% 32, y un estudio no aleatorizado mostró un beneficio en síntomas y en aclaramiento viral, en pacientes hospitalizados por neumonía a causa del SARS-CoV-2 33. De forma similar, aún no se cuenta con evidencia definitiva en relación al perfil de eficacia y seguridad de ENX a dosis profilácticas o plenas en pacientes infectados por el SARS-CoV-2, aunque se recomienda la anticoagulación oportuna profiláctica en ausencia de contraindicaciones absolutas para todos los casos que requieran hospitalización por neumonía a causa del SARS- CoV-2, siendo la heparina de bajo peso molecular (HBPM o ENX) el mayormente recomendado 21,34. En ese sentido, debido a que aún existe controversia en relación con la efectividad de LPV/r y ENX, se sugiere que se esperen los resultados de ECAs amplios diagnóstico en el ambiente hospitalario, estos resultados podrían orientar a los clínicos para su interpretación.
En el gráfico de Kaplan-Meier se puede apreciar el comportamiento de la SG según la severidad clínica de la neumonía por el SARS- CoV-2. Pocos estudios han propuesto una clasificación clínica de la severidad de esta enfermedad, siendo una de las más reconocidas la planteada por el grupo chino que utiliza parámetros ventilatorios para agrupar a los pacientes con neumonía por SARS-CoV-2 en leve, moderado, severo y crítico 10,37. Los especialistas del HEVES consideran, adicionalmente a los parámetros ventilatorios, como FR, SatO en oximetría de pulso, e índice de PaO /FiO en que evalúen su eficacia y seguridad en el manejo de los pacientes con neumonía por el SARS-CoV-2. Finalmente, no se encontró ninguna relación entre el uso de HCQ y AZM con la mortalidad de nuestros pacientes con neumonía por el SARS-CoV-2. Múltiples estudios han sugerido que estos medicamentos no tendrían ningún beneficio, ni en la mortalidad ni en el aclaramiento viral, en el manejo de los pacientes con neumonía por SARS-CoV-2 5,35, por lo que, a la fecha, ya no se viene recomendando su uso.
El análisis de las pruebas diagnósticas del SARS-CoV-2 mostró diferencias estadísticamente significativas entre el tiempo a resultado positivo de las pruebas rápidas de los marcadores IgM, IgM/IgG e IgG. En línea con nuestros resultados, un estudio indicó que las pruebas rápidas podrían arrojar un resultado positivo IgM dentro de los cinco días de iniciado los síntomas (< 40% de sensibilidad), y un resultado positivo IgG luego de once días de iniciado los síntomas (98% de sensibilidad) 36. Si bien estos hallazgos son preliminares, ya que se requieren de mayores estudios de validación de las pruebas rápidas como método el AGA, a los resultados del marcador inflamatorio de la PCR.
Así, nuestros hallazgos sugieren que el ingreso hospitalario con neumonía por SARS-CoV-2 en un estado severo o crítico estaría asociado a aumento en siete y 16 veces, respectivamente, en el RR de muerte comparado con un estado moderado, lo cual plantea la hipótesis para futuras investigaciones de que un manejo temprano podría mejorar los desenlaces clínicos en estos pacientes.
Los resultados del presente estudio se deben interpretar teniendo en cuenta los sesgos inherentes a su diseño. Se debe considerar, por ejemplo, la temporalidad retrospectiva de la recolección de datos, la dificultad para el seguimiento de todos los pacientes que ingresaron a UCI, y el pequeño tamaño de muestra que podría limitar el poder estadístico. Asimismo, es importante considerar que los modelos de análisis multivariado no fueron ajustados por múltiples confusores, por lo que estos resultados se deben considerar como preliminares, y deben interpretarse como medidas de asociación, y no como medidas de causalidad.
En conclusión, nuestros resultados sugieren que los factores edad, IMC, HTA, índice PaO2/FiO2, y la exposición a corticoides y LPV/r estuvieron asociadas a la mortalidad en nuestra cohorte de pacientes con neumonía por SARS-CoV-2. Estos hallazgos sugieren que las personas adultas mayores, con HTA y con mayores niveles de IMC, deben extremar los cuidados para evitar el desarrollo de cuadros graves de neumonía por SARS-CoV-2. Asimismo, nuestros hallazgos sugieren que, en el manejo de pacientes con neumonía por SARS-CoV-2, la exposición temprana a LPV/r estaría asociado a un menor riesgo de muerte, mientras que el uso de dosis altas de corticoides estaría asociado a un mayor riesgo de muerte. Resaltando la polémica sobre los diseños y limitaciones de los estudios publicados, se necesitan de ECA que sostengan o refuten los hallazgos, mientras que los clínicos y los pacientes deben ser conscientes del balance riesgo beneficio de estos medicamentos, antes de prescribir y consentir su administración.