INTRODUCCIÓN
La microangiopatía trombótica (MAT) se caracteriza por presentar anemia hemolítica microangiopática, trombocitopenia, esquistocitos en el frotis de sangre periférica, y daño de órganos de intensidad variable 1-4. En los pacientes trasplantados las MAT pueden deberse a una recurrencia de enfermedad previa al trasplante o a una causa nueva (MAT de novo), esto último se observa en menos del 1% 1-5.
Dentro de las causas más frecuentes para una MAT de novo, tenemos a las infecciones (bacterianas o virales), rechazo mediado por anticuerpos (RMA) y toxicidad por inhibidores de la calcineurina, la cual no es dosis-dependiente, siendo esta última la causa más frecuente 5,6. En los primeros meses del trasplante es difícil diferenciar las MAT causadas por RMA de las originadas por toxicidad por inhibidores de la calcineurina 5,6, esto es muy importante ya que el abordaje terapéutico será diferente.
El manejo de las MAT de novo dependerá de la causa, teniendo en los casos asociados a los agentes anticalcineurínicos, la retirada de éstos. Esta conducta junto con otras medidas ha demostrado ser el tratamiento más eficaz 5-8. En esta oportunidad, reportamos el caso de una paciente trasplantada renal que desarrolló microangiopatia trombótica como complicacion relacionada al uso de tacrolimus, su diagnóstico, manejo y posterior evolución.
REPORTE DE CASO
Se reporta el caso de una mujer de 33 años con enfermedad renal crónica secundaria a vasculitis ANCA-p, en dialisis peritoneal desde el 2017. Recibe trasplante de riñón derecho proveniente donante cadavérico (donante femenina de 41 años), en abril del 2018, con inmunosupresión de inducción a base de timoglobulina, metilprednisolona, micofenolato mofetil y tacrolimus (Tabla 1).
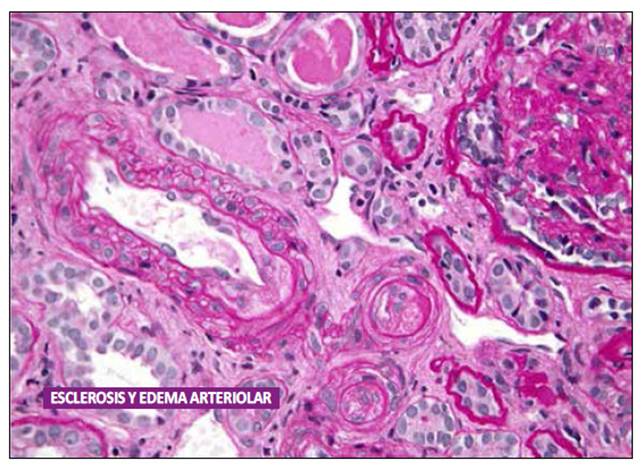
En el postrasplante inmediato presentó diuresis espontánea y disminución de creatinina hasta 1,47 mg/dL. La terapia de mantenimento se basó en prednisona, tacrolimus y micofenolato de mofetilo. Dos meses después se hospitaliza por aumento de azoados (Cr: 3,19 mg/dL) secundario a una pielonefritis aguda por Proteus vulgaris, con carga viral para CMV negativa. Ante la falta de respuesta al tratamiento antibiótico y persistiendo la elevacion de azoados, se realiza biopsia renal en junio del 2018, donde se reportan hallazgos sugestivos de rechazo crónico activo mediado por anticuerpos, patrón morfológico de glomeruloesclerosis focal y segmentaria, hialinosis nodular arteriolar y datos sugerentes de daño vascular con C4d negativo y anticuerpos donante específico (ADE) negativos (Figura 1).
Tabla 2 Evolución de resultados de exámenes de laboratorio.
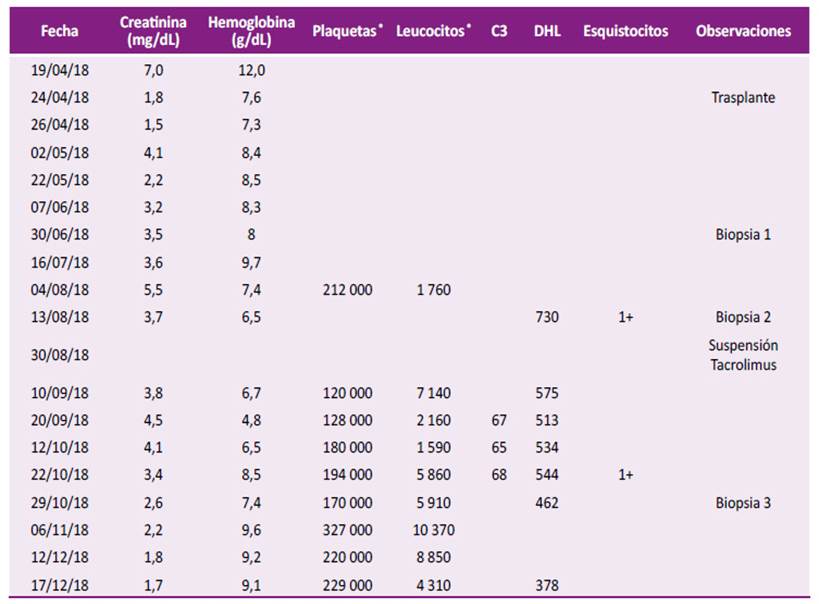
* Valores absolutos. C3: componente 3 del complemento; DHL: lactato deshidrogenasa.
Se inicia tratamiento con pulsos de metilprednisolona, plasmaferesis e inmunoglobulinas y se obtiene mejoria parcial. En julio del 2018, cursa con dolor abdominal, deposiciones liquidas, fiebre, anemia severa (Hb: 5mg/dL) y oliguria. En la analitica presenta bicitopenia: leucopenia y anemia severa, esquistocitos, complemento C3 bajo, DHL elevada y creatinina en 5,5 mg/dL por lo que se sospecha de microangiopatía trombótica (MAT).
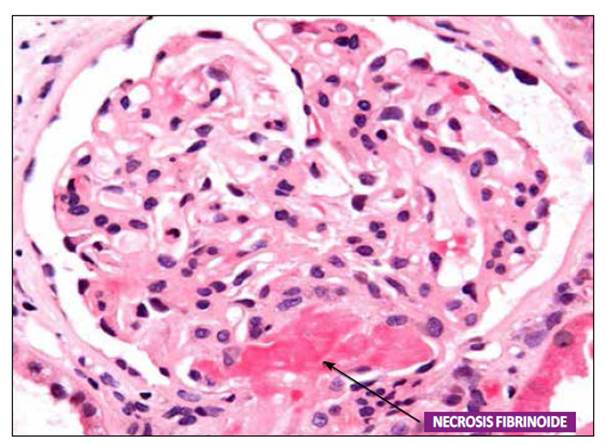
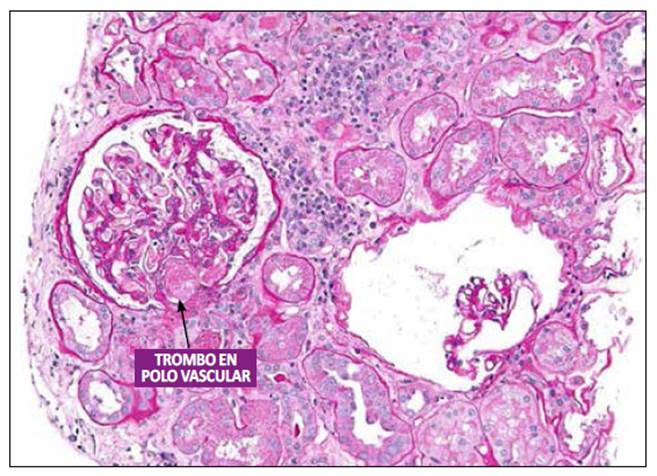
Se realiza nueva biopsia renal en agosto del 2018, diagnosticándose MAT con desdoblamiento yengrosamiento deasas capilares, trombos hialinos en glomérulo a nivel de hilio vascular (Figura 2) y hialinosis subendotelial de la arteriola y otro glomérulo con mesangiolisis global, inmunofluorescencia negativa y C4d negativo, con carga viral negativa para CMV. En octubre del 2018 persiste con anemia, leucopenia y plaquetopenia, encontrándose carga viral para CMV en 75000 copias. Con este diagnóstico se suspende el tacrolimus y se inicia tratamiento con ganciclovir intravenoso con lo que se obtiene remisión completa de la infección por CMV a las tres semanas (carga viral en 69,7 copias). Se obtiene mejoria progresiva de la funcion renal con valores de creatinina en 1,7 mg/dL y hemoglobina en 9,6 mg/dL. Se realiza biopsia del injerto renal a fines de octubre del 2018 por control de MAT, dicha biopsia determinó que la duplicación de la membrana basal de los capilares glomerulares, la necrosis fibrinoide y la esclerosis perihiliar estaría en relación a cronicidad de microangiopatía trombótica secundaria a tacrolimus (Figura 3). La paciente hasta el momento del reporte se encuentra recibiendo tratamiento inmunosupresor con micofenolato mofetil y prednisona, manteniendo niveles de creatinina en 1,7 mg/dL, hasta febrero 2020.
DISCUSIÓN
La patogenia del MAT se centra en la activación de las células del endotelio vascular, el daño por activación leucocitaria y agregación plaquetaria 6. Existen diferentes factores desencadenantes que incluyen bacterias, virus, toxinas y drogas (inhibidores de la calcineurina), injuria isquemia-reperfusión, RMA y activación o disregularización del complemento en la aparición del MAT 7-10. El caso clínico planteó dos problemas diagnósticos, el primero estuvo centrado en diferenciar si se trataba de una MAT recurrente o de novo. El SUH recurrente según la literatura se manifiesta con MAT sistémico como es el caso de la paciente y ocurre en el trasplante temprano 9-11, mientras que el MAT secundario es de afectación renal preferentemente y de aparación tardía (después del año), sin embargo, la paciente no tenía ancedente de SUH como causa de su enfermedad renal crónica. Por otro lado, no se pudieron realizar estudios para determinar si se trata de una deficiencia de algún factor del complemento como el factor H o I que oriente hacia un diagnóstico de recurrencia de enfermedad (MAT).
Dentro de las causas de MAT de novo que se consideraron en la paciente tenemos el RMA, infección por CMV y la toxicidad por tacrolimus 8-11. La biopsia renal no presentó hallazgos de C4d y los ADE fueron negativos, datos que descartan el diagnóstico de RMA. En el caso de infección por CMV, las manifestaciones clínicas como la plaquetopenia, esquistocitos con DHL elevados y el deterioro de la función renal se manifiestan antes de la elevación de la carga viral y se mantuvieron posteriormente al tratamiento con ganciclovir. Además, la biopsia renal no evidenció hallazgos de infección por CMV (inclusiones intranucleares).
Al encontrar mejoría de la función renal con descenso de la creatinina y remisión de la anemia y plaquetopenia luego de la suspensión del tacrolimus, podemos decir que se trata de una MAT secundaria a esta droga 10,12,13. Por otro lado, la MAT podría tratarse de una entidad infradiagnosticada que debe ser tomada en cuenta en los pacientes trasplantados.