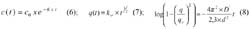Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de la Sociedad Química del Perú
versión impresa ISSN 1810-634X
Rev. Soc. Quím. Perú v.71 n.1 Lima ene./mar. 2005
Adsorción de CU(II) por quitosano en polvo y perlas de gel
Jaime A. Flores1; Abel E. Navarro2; Karim P. Ramos3; Lily Chang3; Neptali Ale1; Martha Ly3; Holger J Maldonado.1,3.
1 Unidad de Postgrado, Facultad de Química e Ing. Química, Universidad Nacional Mayor de San Marcos, Av. Venezuela s/n, Lima 1, Perú
2 Department of Chemistry, The City College of New Cork, New Cork, NY, US 10031
3 Departmento de Química, Facultad de Ciencias y Filosofía, Universidad Peruana Cayetano Heredia, Av. Honorio Delgado 430, Lima 31, Perú
RESUMEN
El biopolímero quitosano, modificado químicamente, se usó para pruebas de adsorción de Cu(II) en soluciones acuosas mediante estudios de equilibrio y cinética. Mientras el equilibrio se ajusta al modelo de Langmuir, la cinética a los mecanismos de difusión. Las velocidades de adsorción se evaluaron por ecuaciones de seudo orden. Así mismo, se propone un modelo cinético con el aporte de las variables de modelo de equilibrio.
Palabras clave: Adsorción, equilibrio, cinética, mecanismo, quitosano, perlas de gel.
ABSTRACT
Chemically modified chitosan biopolymer was used to evaluate the adsorption for Cu(II) from diluted solutions by means of equilibrium and kinetic studies. The equilibrium fits the Langmuir model, while the kinetics the difussion mechanisms. The adsorption rates were evaluated through the pseudo-order equations. In addition, a kinetic model is proposed by using the parameters of the equilibrium adsorption.
Keywords: Adsorption, equilibrium, kinetics, mechanism, chitosan, gel beads.
I. INTRODUCCIÓN
En los últimos años se observa un mayor énfasis en el estudio de los procesos de adsorción de metales pesados de las aguas de deshecho utilizando adsorbentes de origen biológico 1-4
El quitosano, poli(2-glucosamina), extraído de la quitina es considerado un buen adsorbente de metales 5,6 . Modificaciones físicas y químicas se han desarrollado para mejorar su calidad, capacidad y selectividad adsorbente 7-10 . Estudios previos indican que el quitosano, en forma de perlas de gel, de 2.5mm de diámetro tienen una área BET de 250–800m 2 .g -1 en comparación con 1–2m 2 .g -1 que tiene el quitosano en forma de escamas de 2mm 11 . Con una mayor área superficial se asegura la disponibilidad de más sitios de adsorción; se espera lograr mayores capacidades con las perlas que con partículas de quitosano nativo. Sin embargo, la posibilidad de alcanzar la misma capacidad mediante la reducción en el diámetro de partícula no ha sido considerado en trabajos previos.
En la presente investigación se describe cómo las modificaciones físicas producen variaciones en las capacidades de adsorción y sus mecanismos estableciendo condiciones óptimas para la adsorción de Cu(II) con quitosano.
II. MATERIALES Y MÉTODOS
Quitosano en escamas, Aber Technologies, Plouvien, France, grado de acetilación 87% y peso molecular 125000g.mol -1 . El material fue molido y tamizado, obteniéndose las siguientes partículas de diámetro: d i , i=1-5: 0<d 1 <75µ m, 75? m<d 2 <125µ m, 125? m<d 3 <212µ m, 212? m<d 4 <2000µ m y 0<d 5 <212µ m. Se utilizó CuSO 4 .5H 2 O, NaNO 3 , NaOH, HNO 3 cc, CH 3 CO 2 Hcc, grado reactivo, J.T. Baker y agua desionizada obtenida por ósmosis reversa, Tipo I.
La preparación de las perlas de gel (GB) consiste en precipitar el biopolímero desde una solución diluida de ácido orgánico mediante el goteo a flujo lento y constante sobre una solución alcalina 5 . 4g de quitosano-d 5 se disuelven en 100ml de sol. ácido acético 4%. La solución filtrada se transfiere por goteo sobre 500ml de NaOH 2.5N con agitación moderada. La solución alcalina se agita 12 horas y finalmente las perlas se enjuagan varias veces con agua desionizada hasta pH neutro y se almacenan en agua. El contenido de agua en el quitosano en forma de polvo y perla se pesa 0,5g y se coloca en una estufa a 105 o C por 2 horas hasta peso constante 7 .
El peso del adsorbente se calculó en base seca y el pH, medido con un pHmetro Chem Cadet 5986-25 Cole Parmer, se mantuvo constante en todas las pruebas de equilibrio y cinética ajustando el pH con NaOH ó HNO 3 0.5, 1.0 ó 5.0N. Las muestras filtradas en papel Whatman N o 42 se diluyeron con HNO 3 1% y la concentración se midió con el espectrómetro de absorción atómica a la llama, de modelo Analyst 100 Perkin Elmer a 365nm en el rango lineal 0-5 mg.l -1 .
Las pruebas de equilibrio se realizaron por duplicado, a temperatura ambiente (25 o C) y el volumen final fue de 200ml de sol. Cu(II) en botellas plásticas de 500ml con tapa colocadas en un agitador orbital Big Bill Digital Thermolyne a 250 rpm por 72 horas.
El estudio del efecto del pH se realizó con una sol. Cu(II) 50mg.l -1 conteniendo NaNO 3 0.05N y 40mg de quitosano, d 1 y d 2 . El pH se ajustó en el rango de 2–5.5 con HCl 1M y NaOH 2M.
En el estudio del efecto del tamaño de partícula y las modificaciones físicas se utilizaron pesos de adsorbente de 10-200mg, en tamaños d 1 -d 4 , con sol. Cu(II) 50mg.l -1 .
El efecto de la concentración de metal se estudió con 10mg de quitosano en polvo d 1 , d 4 y quitosano en forma de perlas de gel utilizándose soluciones de Cu(II) de concentraciones 5–100mg.l -1 a pH 5.30.
Las pruebas de cinética se realizaron utilizando volúmenes de 300ml de sol. Cu(II) 50mg.l -1 a pH 5.30 y 15mg de adsorbente d 1 y perlas de gel.
III. RESULTADOS Y DISCUSIÓN
El contenido de agua del quitosano en polvo es 10.1 % y de las perlas de 95.3%. El mayor contenido de agua en las perlas confirma un carácter hidrofilico de éstas 11 . Así, la superficie adsorbente fue extendida y se dispone de más centros de adsorción.
3.1 Efecto del pH:
De acuerdo al equilibrio (1) el comportamiento del adsorbente en solución es una función del pK a (~6.20).
R-NH3+ + H2O ↔ R-NH2 + H3O+
Similarmente, la solubilidad teórica del Cu(II) se calcula usando el pK w y pK ps del Cu(OH)2 (~20) que para usos prácticos se resume en la ecuación (2) como la concentración de saturación de Cu(II) (SCC) en función del pH:
SCC = 63550 x10 8-2x pH mg.l -1 (2)
La correspondencia entre los valores experimentales y aquéllos de la ecuación (2) y confirmados por las pruebas del blanco, indican que el pH óptimo de adsorción es de 5.30.
3.2 Efecto del tamaño de partícula y las modificaciones químicas del quitosano:
La Figura 1 muestra cómo a menor tamaño de partícula mayor es la adsorción; lo cual está en conformidad con las características de los adsorbentes de menor porosidad. A pesos mayores a 200mg, tanto el quitosano-d 1 como las perlas, eliminan casi el 100% del cobre. Esta es una primera condición útil (0,2g de quitosano son necesarios para eliminar todo el cobre desde la sol. de Cu(II) de 50mg.l -1 a pH 5.30). Similares capacidades de adsorción a bajos pesos sugieren que las partículas de polvo son permeables a los iones Cu(II) a altas concentraciones y confirman al quitosano d 1 como un tamaño de partícula adecuado para desarrollar similares capacidades a las perlas.
3.3 Efecto de la concentración del metal.
Langmuir y Freundlich 12 describen un proceso de adsorción en monocapa sin interacciones laterales entre las moléculas de adsorbato. Freundlich considera que la interacción es sobre una superficie energéticamente heterogénea. Las ecuaciones (3) y (4), respectivamente, establecen ambos modelos y los valores de capacidad de adsorción, q, se calculan mediante la ecuación (5) del balance de masas.
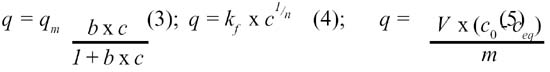
con q, mg.g -1 ; q m máxima capacidad adsorbente, mg.g -1 ; b constante de afinidad, l.mg -1 ; c concentración remanente de metal, mg.l -1 ; k f constante de capacidad; n constante de intensidad; V volumen de solución, l; c 0 concentración inicial de adsorbato, mg.l -1 y m masa de adsorbente, g.
De acuerdo a los resultados de la Tabla 1 el proceso en quitosano en polvo-d 1 y las perlas se ajustan al modelo de Langmuir. Además, debemos resaltar que nuestros resultados están entre las capacidades de adsorción más altas reportadas previamente (40-222mg.g -1 ), aunque diferentes condiciones y fuentes de adsorbato han sido usadas en cada caso 13-15 . La adsorción con quitosano d 4 fue pobre a lo largo de todo el rango de concentraciones con una tendencia a concentraciones mayores a 60 mg.l -1 , q m <150mg.g -1 .
Guibal y colaboradores determinaron que la adsorción sobre una partícula no-porosa, tal como el polvo quitosano-d 1 , se desarrolla con una penetración de 40-60? m 16 . Como el diámetro de nuestra partícula es menor que 75 µ m la penetración involucraría todo el diámetro y así un número de sitios de adsorción cercanos al de las perlas que participan en el proceso.
Además, los cálculos del número total de centros activos sugieren que el mecanismo final es de intercambio iónico. A pH 5.30 el quitosano posee alrededor de 90% de sus centros activos en la forma protonada -NH 3 + y sólo 10% son no-iónicos, -NH 2 15 ; éstos pueden enlazar un equivalente de no más de 0.7mmolesCu(II)/ g mediante el acomplejamiento o quelación. Debido a que representan no más de 45mgCu(II)/g el intercambio iónico podría ser uno de los mecanismos finales para enlazar cobre .
3.4 Cinética de adsorción.
La cinética de adsorción con biopolímeros obedece a mecanismos de difusión: difusión externa por transporte del adsorbato desde la capa externa a la superficie del adsorbente e intraparticular desde la superficie del adsorbato hasta los sitios de adsorción. Por ello, para evaluar el mecanismo predominante se usan modelos de difusión tales como la ecuación de difusión externa de Fick 11 (6) , la cual se aplica en los primeros minutos del proceso. Donde c(t) es la concentración remanente a tiempo t y c 0 la concentración inicial. Por otro lado, la difusión intraparticular puede ser aproximada al modelo empírico de Weber 17 , su función de potencias (7) se extiende entre 5-20% del proceso: q(t) es capacidad a tiempo t y k w constante de Weber, mg.g -1 .h -0.5
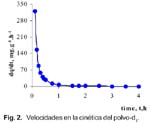
El modelo de Urano (8)18,19 se ajusta a la cinética en un rango más amplio, hasta el 60%, donde q e es la capacidad en el equilibrio, D el coeficiente de difusión, cm 2 .h -1 y d el diámetro de partícula, cm. Como se muestra en la Fig. 2, capacidades similares en el equilibrio se logran con polvo-d 1 , pero el polvo alcanza el equilibrio notablemente más rápido, 4 y 18 horas, respectivamente. Aunque esto sugiere una difusión externa en el caso del polvo, los datos en la Tabla 2 indican que la difusión intraparticular es importante como mecanismo de adsorción en ambos, polvo y perlas, siendo predominante en el caso de las perlas. Así, una correlación puede hacerse entre los estudios de equilibrio y cinética. En el primero se postuló que toda la masa de las partículas toma parte en la adsorción; este hecho convierte lo que es comúnmente considerado un mecanismo de difusión externa por partículas no porosas en una difusión intraparticular debido a la conveniente disminución en el tamaño de la partícula adsorbente.
Las velocidades del proceso se calcularon mediante los modelos de pseudo orden (9) 2,20-22 , como se muestra en la Tabla 3. Los datos de las pruebas de cinética se ajustaron mejor al modelo de pseudo 2do orden y sus parámetros confirman lamayor velocidadinicial(10)para elprocesoquetiene lugarenelquitosano en polvo (Tabla 4). Además, las constantes de capacidad en el equilibrio, q e , obtenidas por linearización de los modelos, son similares en ambos procesos y confirman los valores observados en las pruebas de cinética.
Un mayor análisis de la ecuación de seudo 2do orden en el caso del polvo permite separar las etapas en que se desarrolla el proceso. Esto se observa clara-mente al dibujar la velocidad de adsorción en cualquier momento, (10), en la Fig. 2 ycompararla conelrangode validezdelosmecanismos en la Tabla2. Similarmente a las ecuaciones de Fick y Urano obtenidas, las velocidades de seudo 2do orden decrecen marcadamente en los primeros 30 minutos como en un mecanismo de difusión externa y luego se mantiene un lento decrecimiento como en una difusión intraparticular. La pobre porosidad del polvo-d 1 puede generar que primero se saturen los sitios activos externos mientras la adsorción es notablemente rápida y luego se desarrolla la difusión intraparticular a lo largo del 75% del proceso con un lento decrecimiento de las velocidades de adsorcióntambiéngenerado por el impedimento estérico de las especies hidrolizadas H 3 O + que son liberadas en el intercambio iónico.
La información de las pruebas de equilibrio y cinética nos permite proponer un modelo cinético que incluye los parámetros de equilibrio considerando que las pruebas de cinética son una condición en el equilibrio de interacción quitosano-Cu( II). Así, q e en el modelo de seudo 2do orden se convierte en un posible valor q en elmodelodeLangmuir. Arreglos matemáticos adecuados proveen nuestra ecuación de cinética (11) mediante el reemplazo de q e=q m .b.c/(1+b.c) en la ecuación de seudo 2do orden:
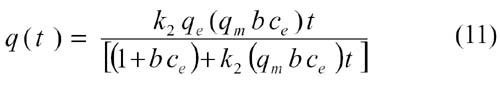
Donde las variables corresponden a ambos modelos. Al comparar los datos experimentales con las curvas obtenidas, Fig. 3, se observa una mayor aproximación al proceso del polvo-d 1 (R 2 =0.98) que al de las perlas (R 2 <0.60).
IV. CONCLUSIONES
De acuerdo con nuestros objetivos iniciales, el polvo de quitosano con diámetro de partícula menor que 75? m es útil para alcanzar capacidades de adsorción de Cu(II) tan altas como las perlas (q m ~200 mg.g -1 ) a pH 5.30. La ecuación de equilibrio de Langmuir caracteriza al proceso, mientras el mecanismo de adsorción final se sugiere que es por intercambio iónico, así como fue calculado mediante el balance de masas.
Nuestro análisis explica una correlación cuantitativa entre los resultados de equilibrio y cinética mediante el modelamiento de la interacción Cu(II)-quitosano y demuestra que el polvo sigue un mecanismo de difusión externa e intraparticular y similar a las perlas la mayoría de sus centros activos están disponibles para enlazar iones Cu(II). Finalmente, nuestra propuesta de modelo cinético, usando una combinación de las ecuaciones de Langmuir y de seudo 2do orden, aproxima los resultados obtenidos y así confirma las similitudes en los resultados de los estudios de equilibrio y cinética.
V. AGRADECIMIENTOS
Al Laboratorio de Biosorción y Productos Naturales del Dpto de Química en la Univ. Peruana Cayetano Heredia y a la Biblioteca de la Soc. Peruana de Química.
VI. REFERENCIAS
1.Volesky, B.; Holan, Z.R.; Biotechnol. Prog., 11(1995), 235 [ Links ]
2. Gundogan, R.; Acemioglu, B; Alma, M; J. Colloid Interface Sci., 269(2004), 303 [ Links ]
3. Niu, H.; Volesky, B.; Process Metallurgy, 11B(2001), 189 [ Links ]
4. Seki, H.; Suzuki, A.; J. Colloid Interface Sci., 246(2002), 259 [ Links ]
5. Guibal, E.; Larkin, A.; Vincent, T.; Tobin, J; Ind. Eng. Chem.. Res., 38(1999), 4011 [ Links ]
6. Guzmán, J.; Saucedo, I.; Navarro, R.; Revilla, J.; Guibal, E.; Langmuir, 18(2002),1567 [ Links ]
7. Dambies, L.; Guibal, E.; Roze, A.; Colloids Surfaces A: Physicochemical Eng. Aspects , 170(2000), 19 [ Links ]
8. Wan Ngah, W.; Il, K.; Ind. Eng. Chem. Res., 38(1999), 1411 [ Links ]
9. Ly, M.; Maldonado, H.; Horna, O.; Guibal, E.; Hydrometallurgy, 71(2003), 191 [ Links ]
10. Ly, M.; Maldonado, H.; Horna, O.; Guibal, E.; Process Metallurgy, 11B(2001), 119 [ Links ]
11. Guibal, E.; Milot, C.; Tobin, J.; Ind. Eng. Chem. Res., 37(1998), 1454 [ Links ]
12. Volesky, B.; Hydrometallurgy, 71(2003), 179 [ Links ]
13. Ng, J.; Cheung, W.; McKay, G.; J. Colloid Interface Sci., 255(2002), 64 [ Links ]
14. Wan Ngah, W.S.; Endud, C.; Mayanar, R.; React. Funct. Polym., 50(2002), 181 [ Links ]
5. Schmuhl, R.; Krieg, H.M.; Keizer, K.; Water SA, 27(2001), 1-7
16. Guibal, E.; Jansson, M.; Saucedo, I.; Le Cloirec, P.; Langmuir, 11(1995), 591 [ Links ]
17. Weber, W.J.; Morris, J.C.; J. Sanit. Eng. Div., 89(1963), 31 [ Links ]
18. Urano, K.; Tachikawa, H.; Ind. Eng. Chem. Res., 30(1991), 1897 [ Links ]
19. Urano, K.; Yamamoto, E.; Tonegawa, M.; Fujie, K.; Water Res., 25(1991), 1459 [ Links ]
20. Ho, Y.S.; McKay, G.; Trans IChemE, 77(1999), 165 [ Links ]
21. Ho, Y.S.; McKay, G.; Wase, D.A.J.; Foster, C.F.; Ads. Sci. Technol., 18(2000), 639 [ Links ]
22. Ferreira, S.; Andrade, H.; dos Santos, H.; J. Colloid Interface Sci., 270(2004), 276 [ Links ]