Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de la Sociedad Química del Perú
versión impresa ISSN 1810-634X
Rev. Soc. Quím. Perú v.76 n.4 Lima oct./dic. 2010
TRABAJOS ORIGINALES
Síntesis y caracterización de nanopartículas de ferrita de cobalto obtenidas por el proceso sol-gel
Synthesis and characterization of cobalt ferrite nanoparticles obtained by sol-gel process
Juan Montes de Ocaa* ; Llojan Chuquisengoa ; Hugo Alarcóna
a Universidad Nacional de Ingeniería, Laboratorio de películas delgadas. *jmontesdeocaav@yahooes
RESUMEN
En el presente trabajo se realizó una coprecipitación de sales de hierro (II) y cobalto (II) en medio alcalino y de nitratos, usando como surfactantes al bromuro de cetiltrimetilamonio (CTAB) y al ácido oleico, para así obtener una dispersión homogénea de tamaños de partícula. El análisis estructural se realizó por difracción de electrones, concluyendo que la estructura era FCC, mientras que el análisis morfológico se realizó por microscopía electrónica, obteniéndose un tamaño de partícula de 4 y 10 nm para el ácido oleico y el CTAB, respectivamente. Los espectros FTIR confirmaron algunos picos característicos de la ferrita de cobalto, así como el tipo de coordinación del surfactante a la superficie de la partícula.
Palabras clave: proceso sol-gel, nanopartículas, ferrita de cobalto, CTAB, ácido oleico.
ABSTRACT
In order to achieve a monodispersed distribution of particle diameters, a coprecipitation process of iron (II) and cobalt (II) salts in alkaline and nitrate media was perform, using cethyltrimethylammonium bromide (CTAB) or oleic acid as surfactants. The structural characterization of the precipitate was made by electron diffraction, concluding that the structure of the solid was FCC, whereas the morphological characterization was made by transmission microscopy, obtaining 4 nm and 10 nm main diameters with oleic acid and CTAB, respectively. The FTIR spectra confirmed some characteristic peaks of the cobalt ferrite and the type of coordination of the surfactants onto the particle surface.
Key words: sol-gel process, nanoparticles, cobalt ferrite, CTAB, oleic acid.
INTRODUCCIÓN
La ferrita de cobalto es un óxido doble de hierro (III) y cobalto (II), cuya fórmula química es CoFe2O4. Es ampliamente estudiada por su elevada anisotropía magnética, moderada magnetización de saturación, buena estabilidad química y dureza mecánica. La ferrita de cobalto presenta una estructura tipo espinela inversa, es decir, es una red cúbica centrada en las caras (FCC) de aniones oxígeno, en la cual los iones Fe (III) ocupan todos los huecos tetraédricos y la mitad de los octaédricos, mientras que los iones Co (II) ocupan la otra mitad de los huecos octaédricos 1,2, según se esquematiza en la figura 1:
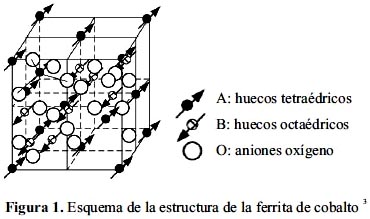
La ruta de síntesis utilizada en este trabajo fue el proceso sol-gel. A pesar que los fundamentos en los que se basa se conocen desde hace ya mucho tiempo, gran parte de su desarrollo corresponde a las últimas dos décadas, en las cuales se ha realizado una gran cantidad de trabajos en este tema. Aunque se han dado muchas definiciones para el proceso sol-gel, éste se puede resumir como un conjunto de técnicas que nos permiten tener control de los procesos químicos involucrados durante la formación del material que se desea obtener. Estas técnicas permiten, entre otras cosas, el ahorro energético debido a que no se necesita excesivo calentamiento o uso de sistemas de alto vacío.
PARTE EXPERIMENTAL
Materiales y reactivos
Los reactivos usados en el presente trabajo se resumen en la tabla 1.
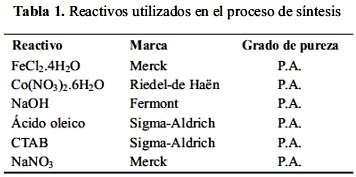
Todos los materiales de vidrio utilizados fueron lavados con HCl caliente para eliminar cualquier resto de óxidos remanentes. Las soluciones se prepararon con agua bidestilada, la cual fue hervida por media hora y desaireada con N2 por 5 minutos. El proceso completo de síntesis se realizó en atmósfera de nitrógeno para evitar la oxidación no controlada del Fe(II) 4-8.
Procedimiento
Se prepararon soluciones según la tabla 2.
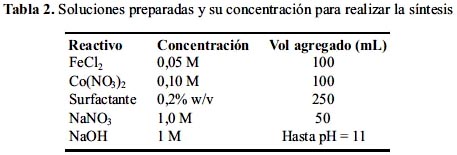
El ácido oleico se preparó saponificándolo con NaOH 5M en caliente (70°C). El agregado de NaOH a la mezcla reaccionante se realizó gota a gota con agitación constante dentro de un glovebox en atmósfera de nitrógeno. Luego de agregar el hidróxido hasta pH 11 se trasvasó la muestra a un frasco cerrado y se le dejó calentar en la estufa a 95°C por 16 horas. Las muestras para el FTIR se lavaron precipitándolas con ayuda de un electroimán hasta que la prueba de cloruros diese negativa. Los análisis TEM y difracción de electrones se realizaron directamente sobre el sol obtenido.
RESULTADOS Y DISCUSIÓN
Resultados
Se obtuvo un sol de color negro que por precipitación producía un sólido negro-marrón finamente dividido.
Los análisis que se realizaron se listan a continuación.
Microscopía electrónica de transmisión (TEM)
Las micrografías TEM obtenidas para las muestras sin surfactante (usado como control), con CTAB y con ácido oleico, se muestran en la figura 2.
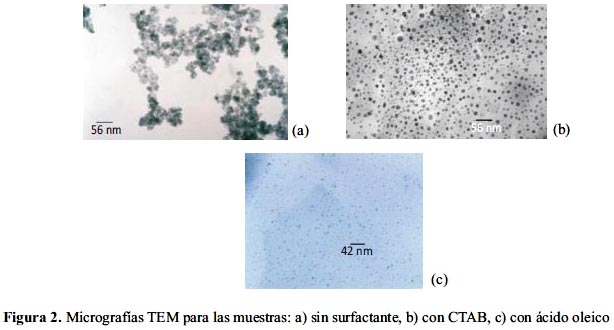
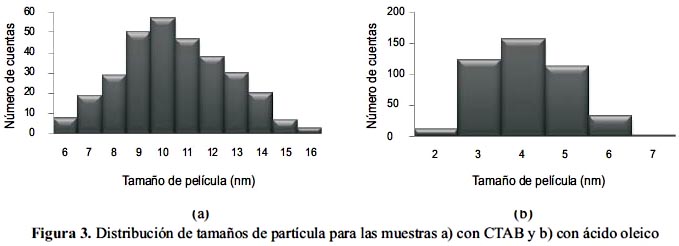
Además, para las dos muestras con surfactante se ha calculado la distribución de tamaños de partícula, las cuales se muestran en la figura 3.
Difracción de electrones
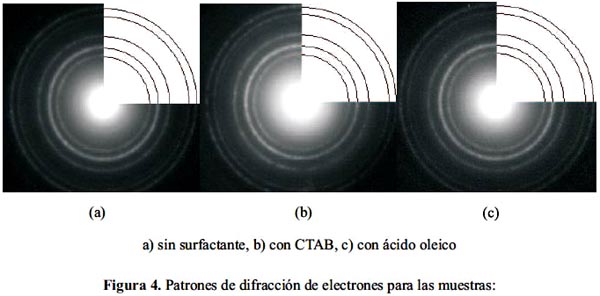
Los patrones de difracción de electrones para las muestras analizadas se muestran en la figura 4.
Espectroscopía infrarroja por transformada de Fourier (FTIR)
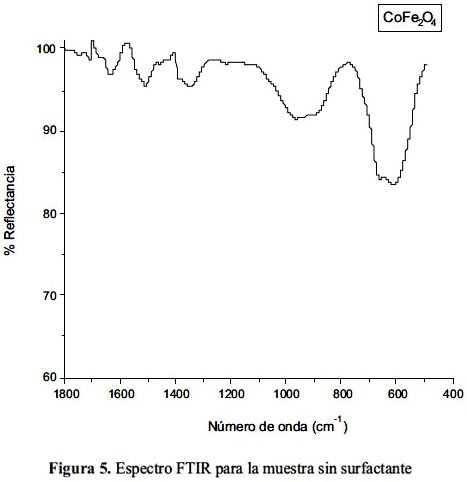
El espectro para el sólido obtenido sin surfactante se muestra en la figura 5.
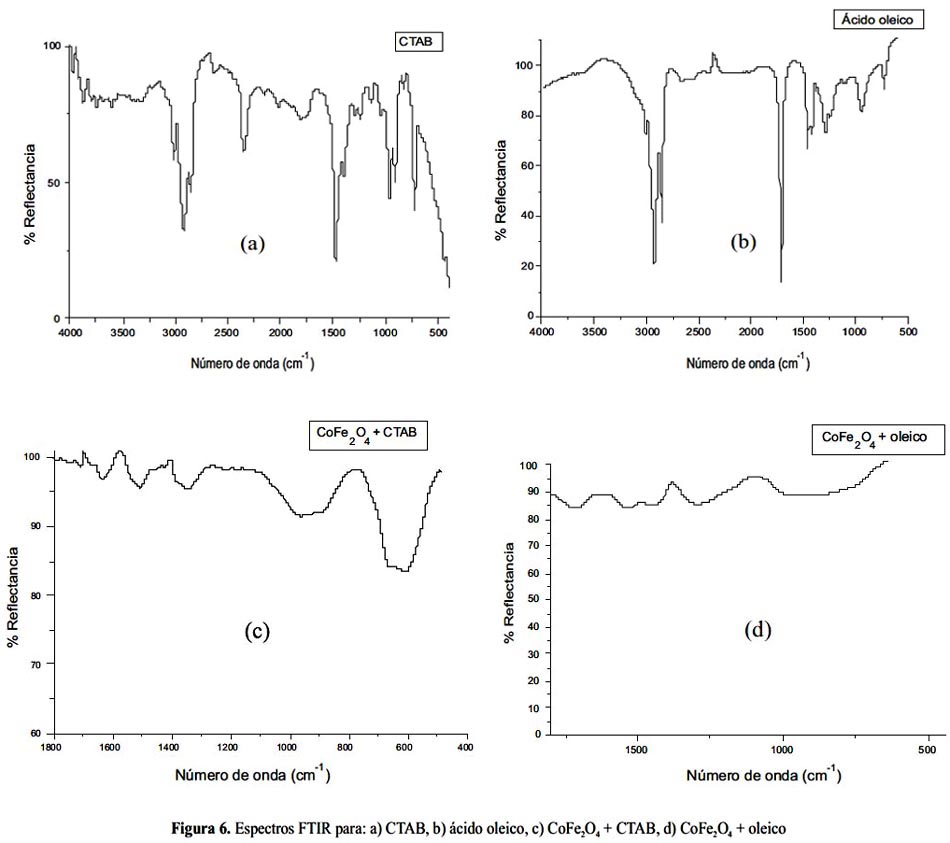
Los espectros para los dos surfactantes puros y de las partículas obtenidas con dichos surfactantes se muestran en la figura 6.
DISCUSIÓN
El análisis por difracción de electrones corrobora una estructura cúbica centrada en las caras (FCC), propia de la ferrita de cobalto en las tres muestras analizadas. Las asignaciones de los índices de Miller para cada una de las circunferencias concéntricas son: [111], [200], [220], [311] y [222].
Las micrografías TEM muestran una fuerte aglomeración de las partículas obtenidas sin surfactante, no sólo por el hecho de que no tienen un agente estabilizador, sino porque al presentar propiedades magnéticas, el movimiento Browniano las hace estar suficiente tiempo en contacto como para que la fuerza magnética las haga coagular, formándose dichos aglomerados. Por el contrario, cuando se usa surfactante para estabilizarlas, no se muestra aglomeración de partículas, sino más bien se muestran más separadas y homogéneas. De la figura 3 se puede calcular los parámetros estadísticos de la distribución, resumidos en la tabla 3:
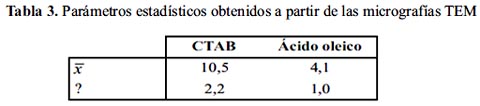
Para el caso del ácido oleico, no sólo se muestra una distribución más homogénea, sino también un menor tamaño medio de partícula.
El análisis por FTIR del sólido muestra 2 picos característicos de la ferrita de cobalto, los cuales se encuentran alrededor de 600 cm-1, atribuidos a enlaces metal-oxígeno en la ferrita9. Para los sólidos obtenidos usando surfactante, no hay diferencia entre los picos obtenidos usando CTAB con respecto a los picos obtenidos sin surfactante. Esto implica el hecho de que el CTAB no posee propiedades para coordinarse a la superficie del sólido obtenido, sino que se mantiene unido por fuerzas electrostáticas a éste, y que con los lavados sucesivos se elimina en el sobrenadante. Por otro lado, el espectro del sólido obtenido con ácido oleico como surfactante muestra una fuerte disminución del pico del carbonilo con respecto al espectro del ácido oleico puro. Esto nos permite deducir que el ácido oleico (en su forma desprotonada) se ha coordinado a la superficie de la partícula en su forma bidentada (por los dos oxígenos del carboxilato), corroborado por la reducción del pico del carbonilo debido a los efectos de resonancia que traen consigo el cambio de simetría correspondiente a la estructura bidentada. Esta coordinación debe ser una unión química más fuerte que la del CTAB debido a que la señal no se elimina con los procesos de lavado.
CONCLUSIONES
Se obtuvo nanopartículas de ferrita de cobalto mediante el proceso sol-gel usando surfactantes, lo cual se corroboró por estudios de difracción de electrones y FTIR. Cuando se usó ácido oleico, se obtuvo nanopartículas de 4,1 ± 1,0 nm en las cuales el surfactante permanecía adherido a la nanopartícula aún después del proceso de lavado.
Cuando se usó CTAB, se obtuvo nanopartículas de 10,5 ± 2,2 nm. Como comparación, se realizó una prueba sin surfactante, en la cual se observan partículas más grandes y aglomeradas, con lo cual se destaca la función del surfactante en la obtención de partículas monodispersas y más pequeñas.
AGRADECIMIENTOS
Los autores agradecen al Instituto de Investigación de la Facultad de Ciencias - UNI, al CONCYTEC y Cátedra de Nanomateriales - UNI, por su apoyo económico para la realización del presente trabajo.
BIBLIOGRAFÍA
1. Smart, L.; Moore, E. 'Química del Estado sólido'. Addison-Wesley Iberoamericana, Estados Unidos, 1995.
2. West, A. 'Basic Solid State Chemistry'. Thomson Press, Great Britain, 1984.
3. Daliya S.; Ruey-Shin J. Chem Eng., 2007, 129, 51–65.
4. Regazzoni, A.; Matijevic, E. J. Colloids Surf., 1983, 6, 189-201.
5. Sugimoto, T.; Matijevic, E. J. Colloid and Interf. Science, 1980, 74.
6. Regazzoni, A.; Matijevic, E. National Association of Corrosion Engineers, 1982, vol. 38, Nº 4.
7. Liu, C.; Rondinone, A.; Zhang, Z. Pure Appl. Chem. 2000, 72.
8. Vayssières, L.; Chanéac, C.; Tronc, E.; Jolivet, J. J. Colloid and Interf. Science, 1998, 205.
9. Calero, V. 'Synthesis and characterization of cobalt-substituted ferrite nanoparticles using reverse micelles'. Tesis de Maestría en Ingeniería Química. Universidad de Puerto Rico, 2005.
Recibido el 27-10-2010













