Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista de la Sociedad Química del Perú
versão impressa ISSN 1810-634X
Rev. Soc. Quím. Perú v.78 n.1 Lima jan./jun. 2012
TRABAJOS ORIGINALES
Análisis proximal, características fisicoquímicas y actividad antimicrobiana del musgo blanco (Sphagnum maguellanicum Brid.) proveniente de Junín, Perú
Proximate composition, physicochemical properties and antimicrobial activity of white moss (Sphagnum maguellanicum Brid.) from Junín, Perú
David Condoria , Marco Piñatellib , Rafaela Elíasc , Rosario Rojasa*
a Unidad de Investigación en Productos Naturales, Laboratorios de Investigación y Desarrollo, Facultad de Ciencias y Filosofía, Universidad Peruana Cayetano Heredia;
b Inkamoss;
c Laboratorio de Ecotoxicología, Laboratorios de Investigación y Desarrollo, Facultad de Ciencias y Filosofía, Universidad Peruana Cayetano Heredia
* Autor de correspondencia:
RESUMEN
En las zonas altoandinas del Perú crece abundantemente el musgo Sphagnum maguellanicum, el cual es cosechado y secado por las comunidades de Junín para ser luego exportado a bajo precio, principalmente como sustrato para el cultivo de orquídeas. El objetivo del presente estudio fue el determinar la composición química proximal, las principales características fisicoquímicas y la actividad antibacteriana del musgo Sphagnum maguellanicum procedente de Junín; así como el de realizar un estudio preliminar de su capacidad de adsorción del ion metálico Cu+2; con miras a identificar su potencial para el desarrollo de productos derivados con mayor valor agregado.
Se encontró que el musgo peruano posee un pH ácido (4,5 - 6,0), gran capacidad de absorción de agua (hasta 47 veces su peso seco a las 24 horas), buena adsorción de iones cobre, gran cantidad de fibra y carbohidratos; así como una buena actividad antimicrobiana in vitro contra las bacterias Staphylococcus aureus y Streptococcus faecalis. Estas características hacen de este musgo un posible candidato para el desarrollo de filtros removedores de metales y bacterias.
Palabras clave: musgo, Sphagnum maguellanicum, antimicrobiano, análisis proximal.
ABSTRACT
In the highlands of Peru grows abundantly Sphagnum maguellanicum moss, which is harvested and dried by the communities of Junín, to be exported at a low price, mainly as substrate for the culture of orchids. The objective of the present study was to determine the proximate chemical composition, the main physico-chemical characteristics and the antibacterial activity of Sphagnum maguellanicum from Junín; as well as to carry out a preliminary study of its metallic ion Cu+2 adsorption capacity; with the aim of identifying its potential for the development of derived products with greater added value. We found for the Peruvian moss acid pH values (4,5 - 6,0), great absorptivity of water (up to 47 times its dry weight after 24 hours), good metallic ion adsorption, high content of fiber and carbohydrates; as well as a good antimicrobial activity in vitro against Staphylococcus aureus and Streptococcus faecalis. These characteristics make Peruvian moss a possible candidate for the development of filters for the removal of metals and bacteria.
Key words: moss, Sphagnum maguellanicum, antimicrobial, proximate composition.
INTRODUCCIÓN
A nivel mundial, el género Sphagnum comprende más de 150 especies de musgos, con una distribución particular debida a las condiciones ambientales y de suelos que les confieren características morfológicas y físicoquímicas propias.1
En general, las especies de musgo Sphagnum se caracterizan por su gran capacidad de absorción de humedad,2 captación de metales pesados 3 y actividad antibacteriana4. Sin embargo, hay que tener en cuenta que la potencia de estas actividades depende de la especie estudiada y del lugar de procedencia del musgo.1
Hasta el momento se han reportado para el Perú cuatro especies, siendo la de mayor abundancia la especie Sphagnum maguellanicum, la cual crece en las zonas altoandinas, con altos índices de humedad, precisamente donde se encuentra la población más pobre del país. El musgo se cosecha a mano, luego se seca en tendales, se prensa y empaca para ser comercializado en el mercado internacional, utilizándose principalmente como retenedor de agua, como sustrato de propagación para el cultivo de orquídeas, decoración de maceteros y empaquetado de flores o portainjertos.2
Este recurso natural, de alto valor ambiental y gran potencial económico, actualmente no es aprovechado en forma sostenible. Es por lo tanto necesario desarrollar, mediante la investigación, una alternativa que les permita a las comunidades altoandinas aprovechar el recurso en forma sostenida, convirtiendo así al Sphagnum, hoy aprovechado sólo como materia prima, en un instrumento para el mejoramiento de calidad de vida.
El objetivo del presente estudio fue determinar la composición química proximal, las principales características fisicoquímicas y la actividad antibacteriana del Sphagnum maguellanicum procedente de Junín; así como el de realizar un estudio preliminar de su capacidad de adsorción del ion metálico Cu+2 con miras a identificar su potencial para el desarrollo de productos derivados con mayor valor agregado.
PARTE EXPERIMENTAL
Colección e identificación de muestra
Se colectó dos muestras, de aproximadamente 200 g cada una, de musgo fresco, las cuales fueron puestas a secar a temperatura ambiente y bajo sombra. Las muestras fueron colectadas en abril del 2011 en la región de Junín, e identificadas por la Ing. Dominga Zúñiga.
Densidad aparente
Las muestras de gametofitos fueron colocadas en un frasco de volumen conocido. Posteriormente, este frasco destapado fue secado en una estufa (45oC) hasta peso constante. Por último, para obtener la densidad de la muestra se anotó su peso seco y éste se dividió por el volumen del frasco.1 Este análisis se realizó por triplicado.
Determinación de pH y conductividad
Los valores de pH y conductividad se obtuvieron exprimiendo 0,5 g de cada una de las muestras de musgo rehidratado. A continuación se midió el pH y conductividad del líquido obtenido, por medio de un pH-metro (Thermo Electron Corp.) y un conductímetro (Cole Palmer Instrument Co.), respectivamente.1 Estos ensayos fueron realizados por triplicado.
Capacidad de absorción de agua
Para este ensayo1 se realizó primero el secado de las muestras en una estufa a 105oC por 10 minutos y luego a 80oC por varias horas, hasta obtener un peso constante. Para medir la captación de agua por los gametofitos del musgo, se colocó 1 g de muestra seca en un vaso de precipitados de 250 mL previamente pesado. Luego se añadió 100 mL de agua destilada y se dejó reposar por 30 segundos. Transcurrido este tiempo, se escurrió el musgo con un colador y se procedió a colocarlo en el vaso de 250 mL. Finalmente se determinó el peso del agua captada por 1 g de musgo seco.
En un segundo ensayo se siguió el procedimiento anterior, pero esta vez se puso en contacto el musgo con el agua destilada por un período de 24 horas. Cada uno de los ensayos fue realizado por triplicado.
Ensayo de retención de Cu+2
Una de las muestras de musgo fue molida finamente hasta obtener partículas de 8 mm. Un gramo de dicha muestra fue colocada en un erlenmeyer y expuesta a 200 mL de una solución de CuSO4 . 5H2O (100 mg/L). La mezcla fue mantenida bajo agitación (100 rpm) por un período de 72 horas, al cabo de las cuales se procedió a filtrar. El filtrado obtenido fue sometido a análisis por ICP-MS (Espectrometría de Masas con fuente de Plasma de Acoplamiento Inductivo) para determinar la concentración remanente de Cu+2; mientras que la cantidad del ion metálico retenido por el musgo fue calculada por diferencia de concentraciones.5 Este ensayo fue repetido 5 veces.
Análisis químico proximal
Se determinó el contenido de humedad, grasas, proteínas, cenizas y fibra cruda de a cuerdo a procedimientos estándares de la AOAC.6 Todas las determinaciones fueron realizadas por triplicado. El contenido de carbohidratos fue calculado por diferencia (100% menos el contenido de los otros componentes ya mencionados).
Preparación de extractos
El extracto acuoso del musgo se obtuvo por cocimiento por 30 minutos de 20 g de musgo seco con 100 mL de agua destilada; mientras que el extracto etanólico se obtuvo por maceración a temperatura ambiente de 20 g de musgo en 100 ml de etanol por 3 días. Los extractos obtenidos fueron sometidos a filtración y evaporación total del solvente. Finalmente, los extractos crudos obtenidos se diluyeron en sus respectivos solventes a una concentración de 80 mg/mL.
Actividad antimicrobiana de los extractos
Los microorganismos de ensayo fueron 2 bacterias gram positivas: Staphylococcus aureus ATCC 6538, Streptococcus faecalis ATCC 10536 y dos bacterias gram negativas: Escherichia coli ATCC 8739 y Proteus vulgaris.
Cada uno de los cultivos fue repicado en medio TSA (DIFCO); luego incubados en estufa a 37ºC por 24 horas. A partir de esos cultivos jóvenes se prepararon los inóculos por suspensión en agua peptonada estéril al 0,1%, equivalente al tubo 0,5 de la escala de Mac Farland (108 UFC/mL).
La evaluación de la actividad antimicrobiana se llevó a cabo utilizando el método disco-placa-cultivo, con discos de papel filtro de 6 mm de diámetro y 0,6 mm de espesor.7 Estos discos fueron impregnados con 20 µL de los respectivos extractos (equivalente a 1,6 mg del extracto crudo), dejándose luego evaporar el solvente a temperatura ambiente. Como control positivo se utilizó el sulfato de estreptomicina (500 UI/mL) impregnando en los discos 20 µL. Éstos se colocaron sobre la superficie de una placa con agar de 100 µL del inóculo. Luego fueron incubados a 37ºC por 24 horas, después de las cuales se procedió con la lectura de los diámetros de las zonas de inhibición.
RESULTADOS Y DISCUSIÓN
En la tabla 1 se muestran los rangos de las principales características fisicoquímicas obtenidas para dos muestras de S. maguellanicum colectado en Junín. El musgo se destaca por tener una densidad muy baja, un pH en rango ácido y una capacidad de absorber agua, a las 24 horas, de hasta 46 veces con respecto a su peso seco.
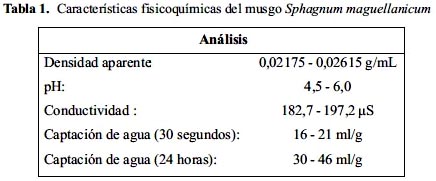
Vásquez1 evaluó muestras de Sphagnum maguellanicum chileno proveniente de 4 localidades (Los Ulmos, Cordillera Perlada, Quilquico y Lago Vargas), obteniendo como resultados valores de pH (3,82 - 4,11) más ácidos y captaciones de agua menores (22 a 27 veces su peso seco a las 24 horas) que el musgo peruano. No hay diferencia en los otros parámetros fisicoquímicos evaluados en ambos musgos.
En el presente trabajo se hizo un estudio exploratorio sobre la capacidad del musgo para retener iones como el Cu+2. Se obtuvo que por cada gramo de musgo S. maguellanicum se puede absorber hasta 19,3 mg de dicho ion metálico. Estos resultados sugieren que el musgo podría ser un buen candidato para el desarrollo de filtros removedores de metales; sin embargo, se precisa realizar estudios más detallados sobre la cinética de adsorción del ion cobre, así como de otros iones metálicos.
La tabla 2 muestra los resultados del análisis químico proximal del musgo Sphagnum maguellanicum proveniente de Junín, el cual contiene una gran cantidad de fibra cruda (39,1 - 43,3%) y carbohidratos (30,0 - 36,9%), que explican su gran capacidad de absorber agua
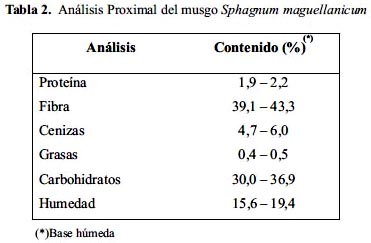
La procedencia del musgo afecta la composición química del mismo. Por ejemplo, el musgo S. maguellanicum proveniente de Chile destaca por su mayor contenido de fibra (56,0%) y menor contenido de carbohidratos (20,9%)8, en comparación con el musgo peruano. Los autores sugieren la aplicación del Sphagnum como fibra dietaria en la preparación de productos de panadería.9-10 Sin embargo, según Vásquez1, las muestras de S. maguellanicum provenientes de cuatro diferentes localidades de Chile mostraron contenidos de fibra cruda (39,2 - 47,1) similares a las obtenidas en el presente trabajo.
Se evaluó la actividad antimicrobiana in vitro del extracto acuoso y etanólico de S. maguellanicum, obteniéndose que ambos poseen muy buena actividad contra bacterias gram positivas (Staphylococcus aureus y Streptococcus faecalis) y nula actividad contra las gram negativas. En el test de difusión en agar, la actividad de ambos extractos contra los gérmenes gram positivos es, inclusive, similar a la del antibiótico estándar estreptomicina (tabla 3).
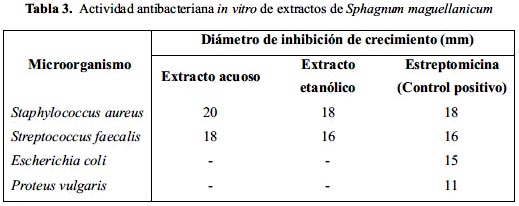
Montenegro y colaboradores11 encontraron que el musgo S. maguellanicum de Chile posee actividad contra un amplio espectro de bacterias, como por ejemplo: Azotobacter vinelandii, Erwinia carotovora subsp. carotovora, Enterobacter aerogenes, Escherichia coli, Pseudomonas aeruginosa, Salmonella typhi, Vibrio cholerae y Staphylococcus aureus.
CONCLUSIONES
El musgo Sphagnum maguellanicum, proveniente de las comunidades de Junín posee un pH ácido, gran capacidad de absorción de agua (hasta 47 veces su peso seco), buena adsorción de iones cobre, gran cantidad de fibra y carbohidratos; así como una buena actividad antimicrobiana in vitro, especialmente contra bacterias gram positivas. Estas características hacen del musgo peruano un posible candidato para el desarrollo de filtros removedores de metales y bacterias.
AGRADECIMIENTO
El presente trabajo de investigación fue llevado a cabo gracias al auspicio del FINCyT (Proyecto 118-10-FINCyT-PITEI-2010: Desarrollo de productos con valor agregado a partir del Sphagnum (musgo blanco) proveniente de comunidades de la región de Junín).
BIBLIOGRAFÍA
1. Vásquez, J. Características anatómicas, propiedades físico-químicas y capacidad de retención de agua en gametofitos de Sphagnum maguellanicum Brid. en un gradiente longitudinal. Tesis Título Químico Farmacéutico. Universidad Austral de Chile. Valdivia, Chile. 2008, 130 pp.
2. Tapia, C. Crecimiento y productividad del musgo Sphagnum magellanicum Brid. en turberas secundarias de la provincia de Llanquihue, Chile. Tesis Licenciatura en Agronomía. Universidad Austral de Chile. Valdivia, Chile. 2008, 83 pp.
3. Ho, Y.S., McKay, G. The kinetics of sorption of divalent metal ions onto Sphagnum moss peat. Water Research. 2000, 34, 735-742.
4. Singh, M., Rawat, A.K.S., Govindarajan, R. Antimicrobial activity of some Indian mosses. Fitoterapia. 2007, 78, 156-158.
5. Kobya, M., Demirbas, E., Senturk, E., Ince, M. Adsorption of heavy metal ions from aqueous solutions by activated carbon prepared from apricot stone. Bioresource Technology. 2005, 96, 1518-1521.
6. AOAC. Association of Official Analytical Chemistry. Official Methods of Analysis, 18th Edition, Revision 3. Washington DC. USA., 2010.
7. Rojas, A., Hernández, L., Pereda-Miranda, R., Mata, R. Screening for antimicrobial activity of crude drug extracts and pure natural products from Mexican medicinal plants. Journal of Ethnopharmacology. 1992, 35, 275-283.
8. Villarroel, M., Biolley, E., Yáñez, E., Peralta, R. Caracterización químico nutricional del musgo Sphagnum maguellanicum. Archivos Latinoamericanos de Nutrición. 2002, 52, 393-399.
9. Villarroel, M., Acevedo, C., Yáñez, E., Biolley, E. Propiedades funcionales de la fibra del musgo Sphagnum magellanicum y su utilización en la formulación de productos de panadería. Archivos Latinoamericanos de Nutrición. 2003, 53, 400-407.
10. Villarroel, M., Reyes, C., Hazbun, J., Karmelic, J. Optimización de una formulación de queques (cakes) con características funcionales a partir de almidones resistentes, Sphagnum magellanicum y harina desgrasada de avellana (Gevuina avellana Mol). Archivos Latinoamericanos de Nutrición. 2007, 57, 56-61.
11. Montenegro, G., Portaluppi, M.C., Salas, F.A., Díaz M.F. Biological properties of the Chilean native moss Sphagnum magellanicum. Biological Research. 2009, 42, 233-237.
Recibido el 16-12-2011
Aprobado el 24-01-2012













