Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de la Sociedad Química del Perú
versión impresa ISSN 1810-634X
Rev. Soc. Quím. Perú v.78 n.2 Lima abr./jun. 2012
TRABAJOS ORIGINALES
Reactividad del bis-(2,4-dinitrofenil)-éter y del análogo tioéter frente a aniones carboxílicos y tiocarboxílicos
Reactivity of bis-(2,4-dinitrophenyl)-ether and analog thioether from carboxylic and thiocarboxylic anions
Ignacio Martín Galloa, Ana María Caresanaa, Jorge Cappettaa, Director Dr. César Alfonso Michelia
a* Instituto de Química Básica y Aplicada (IQBA) – Centro de Investigaciones Científicas y Enseñanza Experimental (CICEE) – Facultad de Ciencias Exactas, Químicas y Naturales (FCEQyN) - Universidad de Morón. Cabildo 134, Morón (1708) Prov. Buenos Aires, República Argentina. (54-11) 5627-2000. ignaciogallo@yahoo.com.ar
RESUMEN
Se busca establecer el orden de reactividad relativa del bis-(2,4-dinitrofenil) éter y del bis(2,4-dinitrofenil) tioéter, frente a los aniones acetato, tioacetato, benzoato y tiobenzoato en metanol - acetona (1:1), siguiendo el desarrollo de dichas reacciones por HPLC. Los aniones acetato, tioacetato, benzoato y tiobenzoato actúan como reactivos nucleofílicos frente a ambos sustratos, atacándolos mediante un mecanismo de sustitución nucleofílica aromática bimolecular o, de manera indirecta, activando la nucleofilia del metanol, componente de la mezcla solvente.
Para la interpretación de los datos obtenidos de los cromatogramas, se construyen gráficos de concentración versus tiempo para los sustratos y los principales productos de reacción, previa interpolación de las áreas de sus correspondientes picos, en curvas de calibración construidas con soluciones de testigos. Los resultados de la investigación indican una mayor reactividad del tioléter respecto al éter, confirmando resultados ya publicados, basados en el seguimiento de las mismas reacciones por TLC; además, hay diferencias en el grupo de reacciones dadas por acetato y tioacetato versus benzoato y tiobenzoato, debidas a diferencias de impedimentos estéricos entre los grupos acetilo y benzoílo.
También aparecen diferencias de reactividad muy significativas cuando actúa el oxígeno de aniones carboxílicos o el azufre de aniones tiocarboxílicos como nucleófilo.
Palabras clave: sustitución nucleofílica aromática; reactividad de diaril éteres nitrados; reactividad de diaril tioéteres nitrados; reactividad de aniones carboxílicos y tiocarboxílicos; reacciones de acilación.
ABSTRACT
It is pretended to establish the relative order of reactivity of bis-(2,4-dinitrophenyl) ether and bis-(2,4-dinitrophenyl) thioether, towards acetate, thioacetate, benzoate and thiobenzoate anions in methanol – acetone (1:1), by following the development of said reactions by HPLC. Acetate, thioacetate, benzoate and thiobenzoate anions act as nucleophilic reagents towards both substrates, attacking them by means of a bimolecular nucleophilic aromatic substitution mechanism or, indirectly, activating the nucleophilicity of methanol, solvent mixture component.
For the interpretation of data obtained from chromatograms, concentration vs. time graphs are built for the substrates and the main products of the reactions, after interpolating the corresponding peak areas in calibration curves built with standard solutions. Research results indicate a higher reactivity of the thioether with respect to ether, confirming results already published; also there are differences in the acetate and thioacetate vs. benzoate and thiobenzoate reactions group due to differences of steric impediments between these groups. There are also very significant reactivity differences when the carboxylic oxygen anion acts or thiocarboxylic sulfur anion as nucleophile.
Key words: nucleophilic aromatic substitution; reactivity of diaryl ethers nitrated; reactivity of diaryl thioether nitrated; reactivity of carboxylic anions and thiocarboxylic; acylation reactions.
INTRODUCCIÓN
La investigación sobre la química comparada del bis-(2,4-dinitrofenil) éter y del bis-(2,4- dinitrofenil) tioéter surgió a partir de una serie de estudios acerca de la reactividad de aniones tiocarboxílicos frente al 1-flúor-2,4-dinitrobenceno y su análogo clorado. Los resultados publicados a este respecto1,2,3 permitieron proponer la siguiente secuencia de reacciones (confirmada por TLC y HPLC contra testigos):
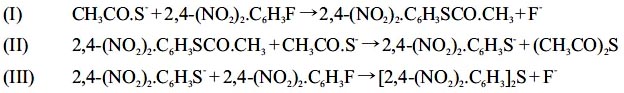
Esta secuencia se produce de manera análoga con el anión tiobenzoato (confirmado por TLC). Las distintas etapas pueden ser controladas y adaptadas para el aislamiento y posterior caracterización del tioéster y del tioéter formados, de acuerdo al nucleófilo empleado, el pH y el solvente de reacción; en metanol, el uso de ácido tiobenzoico como nucleófilo conlleva la precipitación del tiobenzoato de 2,4-dinitrofenilo, mientras que el uso de tiobenzoato, ácido tioacético o tioacetato provocan la precipitación del bis-(2,4-dinitrofenil) tioéter; en acetona, no se observa precipitado alguno, pero pueden detectarse las mismas sustancias en las aguas madres.
De acuerdo a lo esperado, el uso de 1-cloro-2,4-dinitrobenceno como sustrato retarda las reacciones (I) y (III).
Una vez determinada esta secuencia de reacciones, se marcó el objetivo de estudiar de manera comparada el comportamiento del tioéter y su éter análogo, en lo que hace a su facilidad de formación y su estabilidad en las condiciones de reacción ensayadas. Para el estudio comparado de su formación, se buscó llevar a cabo aisladamente la reacción (III) para formar el bis-(2,4-dinitrofenil)-tioéter, y su reacción análoga para la formación del bis-(2,4dinitrofenil)-éter (empleando 2,4- dinitrofenóxido como nucleófilo). Para el estudio de su estabilidad, se buscó comparar la facilidad de su descomposición por el ataque del anión metóxido.
Resultados ya publicados en cuanto a esta comparación3 indican que el bis- (2,4- dinitrofenil) éter se forma con mayor dificultad que el tioéter análogo; de hecho, se ha determinado que la reacción análoga de (III) no se produce en solución acetónica, y debe emplearse el método por fusión, descrito en la bibliografía, para su síntesis. Mientras tanto, el bis-(2,4-dinitrofenil) tioéter sí se forma mediante la reacción (III) en solución acetónica. Además, se confirmó por TLC y por HPLC contra testigos, la menor reactividad del éter respecto del tioéter frente al ataque del ion metóxido en acetona5.
En base a lo anteriormente expuesto, se considera de interés comparar los resultados mencionados con los que pudieran obtenerse haciendo uso de nucleófilos carboxílicos y tiocarboxílicos sobre los mismos sustratos.
Atales efectos se ensayaron las ocho combinaciones posibles:
-
Bis-(2,4-dinitrofenil) tioéter con tioacetato
-
Bis-(2,4-dinitrofenil) éter con tioacetato
-
Bis-(2,4-dinitrofenil) tioéter con tiobenzoato
-
Bis-(2,4-dinitrofenil) éter con tiobenzoato
-
Bis-(2,4-dinitrofenil) tioéter con acetato
-
Bis-(2,4-dinitrofenil) éter con acetato
-
Bis-(2,4-dinitrofenil) tioéter con benzoato
-
Bis-(2,4-dinitrofenil) éter con benzoato
para evidenciar eventuales diferencias de comportamiento de los nucléofilos elegidos, en base a las diferencias de impedimento estérico entre acetilo y benzoílo y las diferencias características de los átomos de azufre y oxígeno.
Es decir, se trata de determinar:
-
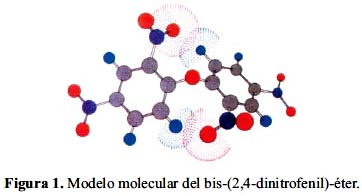
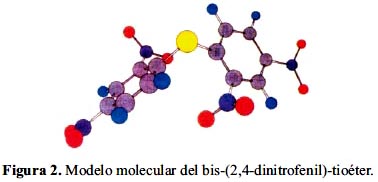
Los efectos del impedimento estérico no solamente aportado por la estructura de uno o ambos sustratos (figuras 1 y 2) sino también por la estructura de los nucleófilos benzoílicos y acetílicos involucrados.
-
Los efectos de la distinta densidad electrónica de los átomos de oxígeno y de azufre en su acción nucleofílica.
Se espera así poder establecer una escala del factor reactividad/selectividad de los cuatro aniones frente a ambos éteres (oxigenado y sulfurado).
Luego, de aquellas reacciones que ocurran en fase homogénea, podrán compararse sus reactividades por seguimiento contra testigos de reactivos intermedios y productos, en lo que hacen a sus variaciones de concentración en función del tiempo, previa realización de las curvas de calibración correspondientes; a los efectos se tomarán de las aguas de reacción alícuotas iguales a tiempos progresivos, que una vez diluidas oportunamente para congelar la reacción, serán procesadas por HPLC para determinar las correspondientes concentraciones de las sustancias presentes en cada una de las mencionadas alícuotas.
Mediante la comparación de los gráficos concentración versus tiempo, a continuación obtenidas, se intentará establecer en qué grado influyen las nucleofilias de oxígeno y azufre de los grupos carboxílicos y tiocarboxílicos en el desarrollo de las mencionadas reacciones, como así también hasta dónde las diferencias de impedimento estérico del fenilo (benzoato y tiobenzoato) respecto del metilo (acetato y tioacetato) pueden intervenir en la diferencia de reactividad prevista allí donde se manifieste.
A modo ilustrativo, se muestran los modelos moleculares, donde se pone en evidencia la diferencia, debida al impedimento estérico, en los carbonos electrofílicos de ambos sustratos:
PARTE EXPERIMENTAL
Diseño del trabajo
Resumen metodológico
Teniendo en cuenta experiencias anteriores referentes a los trabajos ya mencionados, se eligió como solvente de reacción la mezcla metanol - acetona (1:1), la misma ha sido elegida para obtener una buena solubilidad de reactivos y productos de reacción y a la vez un efecto de solvatación sobre los nucleófilos no demasiado intenso, pero suficiente como para que las reacciones no se desarrollen con excesiva rapidez; además, la mezcla elegida no produciría un efecto nivelador significativo ante las diferencias que se pretenden evidenciar a nivel comparativo.
Las reacciones en estudio se llevaron a cabo en igualdad de condiciones experimentales y repetidamente, pero debido a la diferencia de reactividad de los aniones tiocarboxílicos (tioacetato y tiobenzoato) versus la reactividad de los aniones carboxílicos (acetato y benzoato) frente a los dos éteres, se tuvo que efectuar tomas de muestras a tiempos distintos según fueran aniones carboxílicos o tiocarboxílicos.
Para el caso del anión tioacetato se tomaron muestras a los 0, 23, 155, 240, 340 y 400 minutos; para el anión tiobenzoato se tomaron muestras a los 0, 1, 25, 100 y 155 minutos.
Luego, para el anión acetato y benzoato se tomaron muestras de aguas madres de reacción de distintos días con y sin reflujo de 2 y 4 horas.
En cada caso, el seguimiento de la reacción se realizó extrayendo alícuotas del medio de reacción según el esquema anterior de tiempos, diluyéndolas en fase móvil (buffer pH=3, acetonitrilo 50:50) en proporción 1/10, e inyectándolas en el cromatógrafo de RP-HPLC para su separación y cuantificación.
La dilución cumple la función de detener el progreso de la reacción, evitando así que la reacción prosiga dentro del cromatógrafo, y asegurando que las concentraciones de los compuestos cuantificados sean las correspondientes al momento de la toma de la alícuota. Por otra parte, el buffer de la fase móvil facilita la separación de los compuestos aniónicos, protonándolos (por ejemplo, el 2,4-dinitrotiofenóxido, producto en la descomposición del bis-(2,4-dinitrofenil) tioéter, se protona formando 2,4- dinitrotiofenol).
La cuantificación de los compuestos se logró interpolando las áreas integradas de los picos correspondientes a los sustratos en comparación y a los principales productos de su descomposición (cuyos tiempos de retención fueron verificados previamente empleando soluciones de testigos), en curvas de calibración, realizadas con soluciones de concentraciones conocidas (dentro del rango aproximado de concentraciones de trabajo) de los correspondientes testigos.
Los datos obtenidos permitieron graficar curvas de concentración vs. tiempo para cada compuesto cuantificado. A partir de dichas curvas se procedió a la interpretación y comparación de las reacciones.
Condiciones cromatográficas
-
Cromatógrafo: HEWLETT PACKARD Ti-SERIES 1050.
-
Detector: HP1050 VARIABLE WAVELENGTH UV/VIS DETECTOR 79853.
-
Longitud de onda empleada para las mediciones: 254nm.
-
Integrador: HEWLETT PACKARD HP3396 SERIES II INTEGRATOR
-
Fase fija: HyChrom Ace C18; L=10cm; DY= 4,6mm; dp= 3μm.
-
Fase móvil (cromatografía isocrática): Buffer pH=3: acetonitrilo 50:50 (filtrada por membrana de 0,45 μm y desgasificada con vacío).
-
Caudal: 1,3mL/min.
-
Volumen de inyección: 20 μL.
Compuestos
Los compuestos, cuyo seguimiento se efectuó por HPLC a lo largo de las reacciones, son los reactivos y productos más importantes de las mismas, cuyos tiempos de retención (Rt) se determinaron a partir de soluciones de testigos: bis-(2,4-dinitrofenil) éter (Rt ~ 5,58min.); bis-(2,4-dinitrofenil) tioéter (Rt ~ 7,23min.); 2,4-dinitroanisol (Rt ~ 2,50 min.); 2,4-dinitrotiofenol (Rt ~ 1,80 min.); 2,4-dinitrofenol (Rt ~ 1,70 min.); acetato de 2,4dinitrofenilo (Rt ~ 2,87 min.); benzoato de 2,4-dinitrofenilo (Rt ~ 6,71 min.); benzoato de potasio (Rt ~ 1,54 min.); tioacetato de 2,4-dinitrofenilo (Rt ~ 3,58 min.); tiobenzoato de 2,4dinitrofenilo (Rt ~ 9,14 min.); tiobenzoato de potasio (Rt ~ 2,87 min.).
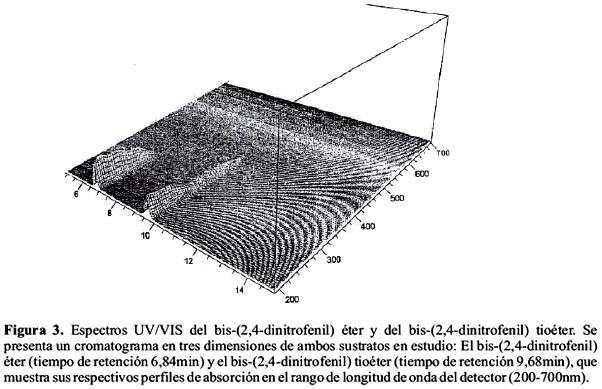
La longitud de onda de 254nm fue elegida para el detector por corresponder a un máximo en el espectro de absorción de los dos sustratos, permitiendo la mayor precisión posible en su medición (figura 3.).
RESULTADOS Y DISCUSIÓN
Formulación de la reacción del bis-(2,4-dinitrofenil) éter y bis-(2,4-dinitrofenil) tioéter con anión tioacetato.
Se desarrolló las reacciones completas del bis-(2,4-dinitrofenil) éter y bis-(2,4 dinitrofenil) tioéter con el anión tioacetato para mayor comprensión de lo que después se observa cualitativamente en las cromatografías TLC y cuantitativamente en la cromatografía HPLC.
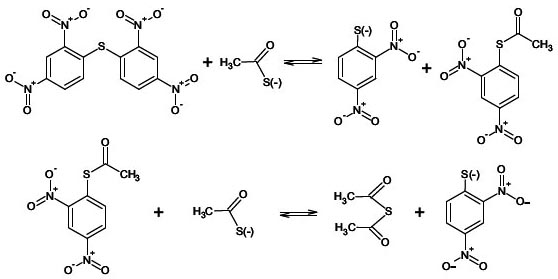
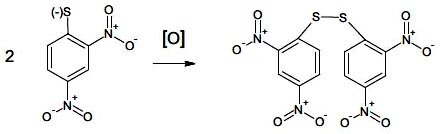
Bis-(2,4-dinitrofenil) sulfuro con anión tioacetato
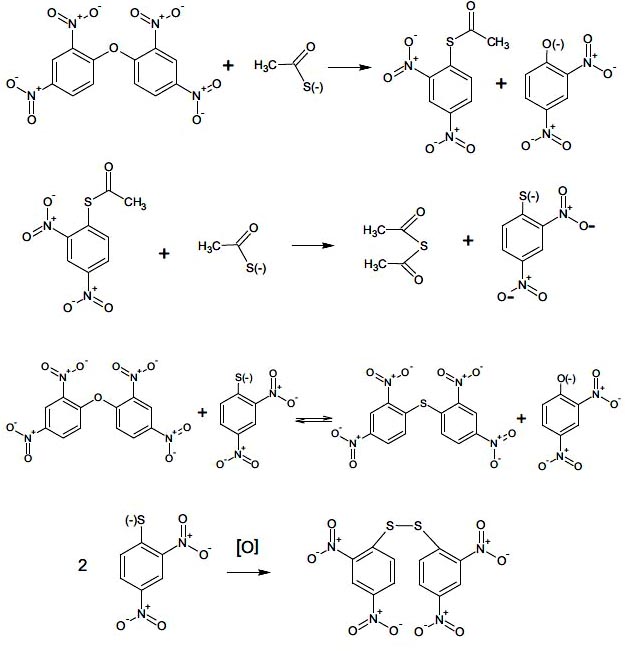
Bis-(2,4-dinitrofenil) éter con anión tioacetato
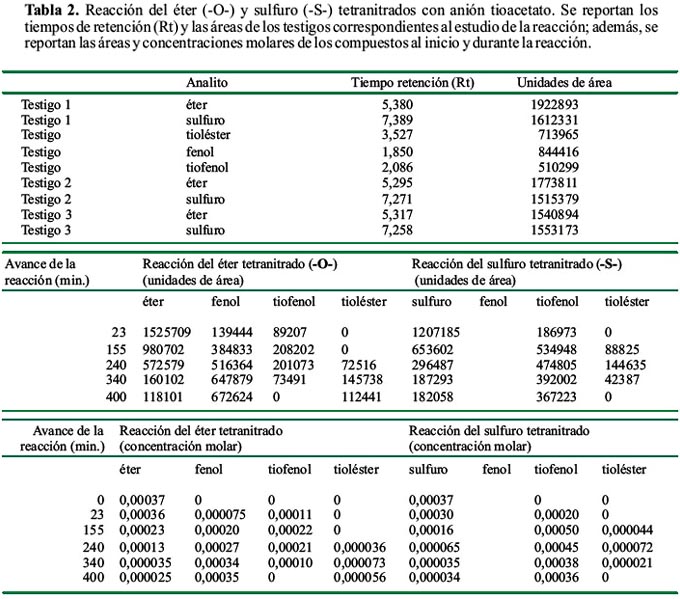
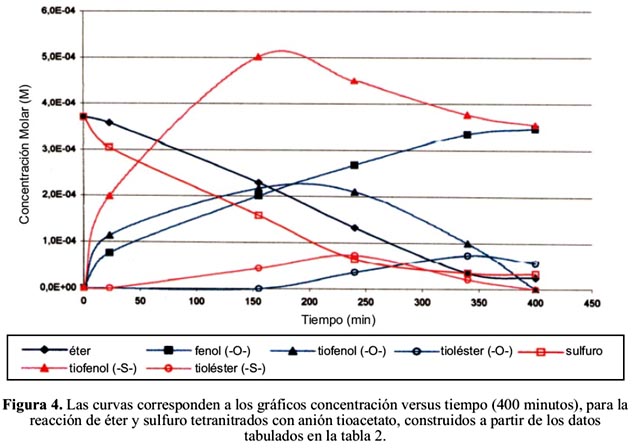
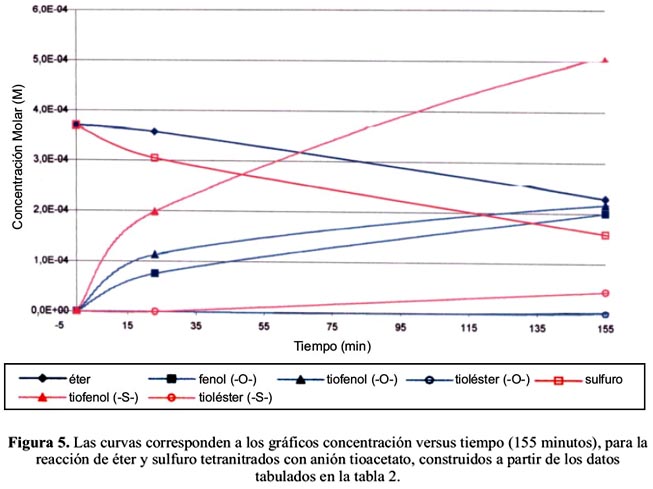
Interpretación de la reacción del bis-(2,4-dinitrofenil) éter y bis-(2,4-dinitrofenil) tioéter con anión tioacetato.
La variación de concentración del 2,4-dinitrotiofenol proveniente de la reacción con bis-(2,4dinitrofenil) éter (aprox. a los 100 min.), indica a paridad de tiempo una concentración de 2,4 dinitrotiofenol, que es aproximadamente la mitad de la presentada por el 2,4-dinitrotiofenol proveniente de la reacción con el bis-(2,4 dinitrofenil) tioéter.
Esto se justifica teniendo en cuenta que el 2,4-dinitrotiofenol en la reacción con el bis-(2,4dinitrofenil) tioéter se forma por descomposición del tioléster intermediario (tioacetato de 2,4-dinitrofenilo), por el ataque nucleofílico que el mismo tioacetato conduce sobre el bis(2,4-dinitrofenil) tioéter.
En el caso de la reacción con bis-(2,4-dinitrofenil) éter, el 2,4-dinitrotiofenol se forma sólo como consecuencia de la descomposición del tioléster intermediario. Por otra parte, el 2,4dinitrofenol y el 2,4-dinitrotiofenol provenientes de la reacción con el bis-(2,4-dinitrofenil) éter, presentan una variación de la concentración prácticamente coincidente.
Cabe resaltar que, después de los primeros 150 minutos, la oxidación del 2,4-dinitrotiofenol a bis-(2,4-dinitrofenil) disulfuro formado en las dos reacciones, hace decrecer sus respectivas concentraciones (gráfico con tiempos largos) haciéndose prevalente el proceso oxidativo respecto a la formación de tiofenol.
La presencia del bis-(2,4-dinitrofenil) disulfuro es claramente evidenciado en las TLC presentadas que se discuten por separado.
Las curvas correspondientes al tioléster decrecen en ambas reacciones; presentan el comportamiento acampanado característico de los intermedios, y su aparición algo tardía se atribuye a su inestabilidad que requiere un tiempo (parcial agotamiento del nucleófilo) para poder presentar una acumulación algo significativa.
Teniendo en cuenta, además, que este tipo de tioléster es bastante lábil, su acumulación resulta escasa respecto al máximo alcanzable si no hubiera descomposición. Por tal razón, ambas curvas acampanadas expresan concentraciones bajas; además, indican que se forma antes el tioléster proveniente del bis-(2,4-dinitrofenil) tioéter (más reactivo) que el tioléster proveniente del bis-(2,4-dinitrofenil) éter (menos reactivo).
Aunque no se ha podido detectar la presencia de tioanhídrido acético ni por TLC, ni por HPLC, hay motivos justificados de su presencia como intermedio muy reactivo6.
Interpretación de la reacción del bis-(2,4-dinitrofenil) éter y bis-(2,4-dinitrofenil) tioéter con anión tiobenzoato.
Correspondería una formulación análoga para la reacción de ambos éteres con anión tiobenzoato.
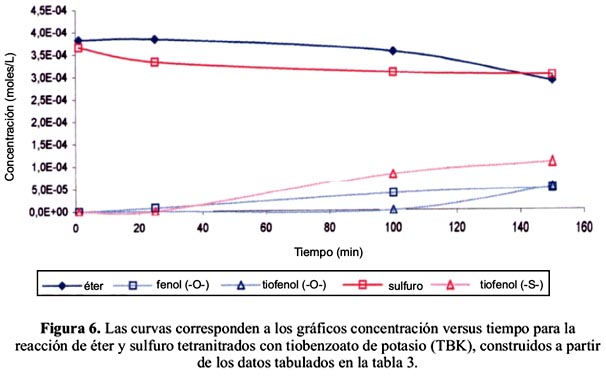
El comportamiento de ambas curvas (tabla 3 y figura 6) es, en general, semejante al presentado en la comparación anterior (mismas reacciones, mismos mecanismos), pero todo ocurre con mayor lentitud.
El impedimento estérico diferente que presentan las moléculas de bis-(2,4-dinitrofenil) éter y bis-(2,4-dinitrofenil) tioéter, es la causa de esto, que mayormente se evidencia usando anión tiobenzoato como nucleófilo.
Por otra parte, la diferencia relativa de reactividad que presentan bis-(2,4-dinitrofenil) éter y bis-(2,4-dinitrofenil) tioéter con el anión tioacetato, es más acentuada que la diferencia relativa correspondiente cuando se atacan bis-(2,4-dinitrofenil) éter y bis-(2,4 dinitrofenil) tioéter con anión tiobenzoato. Esto sería consecuencia del diferente impedimento estéreo que presenta el anión tiobenzoato respecto al anión tioacetato y que dificultaría también la interacción tiobenzoato con bis-(2,4-dinitrofenil) tioéter.
En cuanto al tioléster (tiobenzoato de 2,4-dinitrofenilo), éste se comporta también de manera análoga, pero apareciendo parcialmente por acumulación (por agotamiento del nucleófilo) sólo hacia el final y sólo en la reacción con el bis-(2,4-dinitrofenil) tioéter.
Aunque no se ha podido detectar la presencia de tioanhídrido benzoico ni por TLC, ni por HPLC, en nuestro trabajo, hay referencias en trabajos anteriores de su presencia en la reacción del tiobenzoato de 2,4-dinitrofenilo con tiobenzoato de potasio (ambos a una concentración inicial 1x10-2 M), detectado por HPLC6.
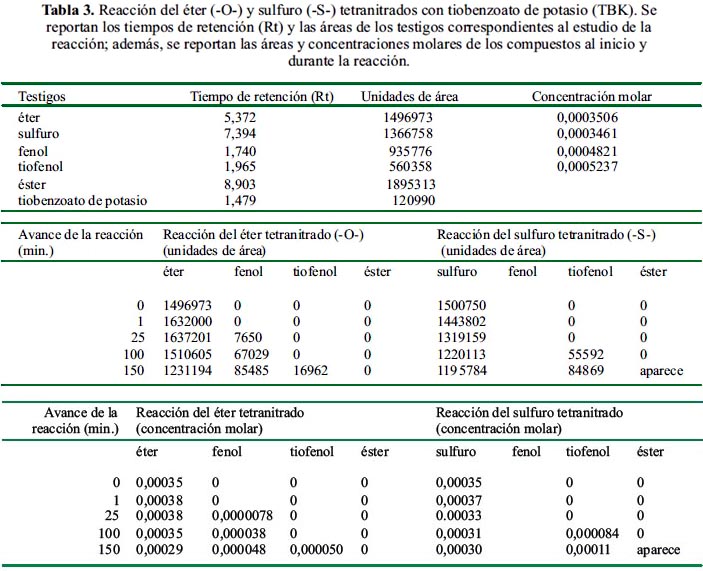
Formulación de la reacción del bis-(2,4-dinitrofenil) éter y bis- (2,4-dinitrofenil) tioéter en presencia de aniones acetato y benzoato.
Bis-(2,4-dinitrofenil) sulfuro con acetato presente
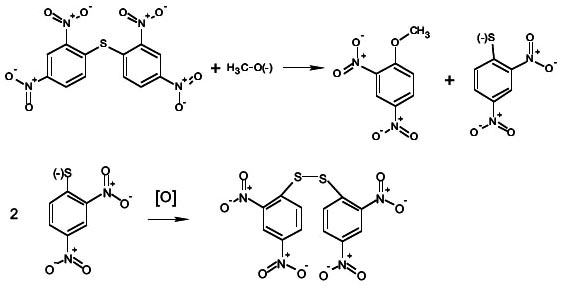
Bis-(2,4-dinitrofenil) éter con acetato presente
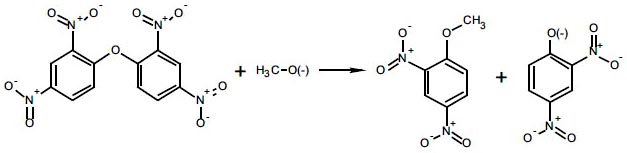
Interpretación de la reacción del bis-(2,4-dinitrofenil) éter y bis-(2,4-dinitrofenil) tioéter con aniones acetato y benzoato.
Del simple análisis de las áreas tabuladas (tabla 4), sin recurrir a las concentraciones correspondientes, surge evidente una reactividad nula para las cuatro reacciones hasta 5 días de seguimiento. Debió recurrirse al reflujo para observar dicha reacción.
La menor nucleofilidad del oxígeno, respecto al azufre, deja en segundo plano sea la diferencia en el impedimento estérico entre ambos éteres, sea la diferencia en el impedimento estérico que pueden proporcionar los radicales benzoílo y acetilo.
De las reacciones puestas a reflujo, a paridad de tiempo, se registra presencia de 2,4dinitroanisol que es mayor en el caso de la reacción con bis-(2,4-dinitrofenil) tioéter y anión acetato, menos en la reacción de bis-(2,4-dinitrofenil) éter con anión acetato, aun menos en la reacción de bis-(2,4-dinitrofenil) tioéter con el anión benzoato y todavía menos en la reacción del bis-(2,4-dinitrofenil) éter con el mismo anión.
El comportamiento del 2,4-dinitrofenol es análogo a las diferencias presentadas con el 2,4dinitroanisol.
El seguimiento del 2,4-dinitrotiofenol no es atendible en estas condiciones por la violenta oxidación que sufre con el reflujo.
Para interpretar la aparición del anisol nos remitimos al estudio5 donde ambos éteres se analizaron frente al ataque del anión CH3O- y también nos referimos6 a cuando el anión CH3O-, o el mismo metanol supuestamente ayudado por los aniones carboxílicos y tiocarboxílicos, pueden atacar sustratos activados para la SNAr y para la SN sobre carbono acílico y carbono benzoílico.

CONCLUSIONES
-
En general, éter y sulfuro reaccionan directamente con los aniones tiocarboxílicos, mientras no lo hacen con los carboxílicos. En este último caso, el impedimento estérico de los aniones carboxílicos se suma al escaso carácter nucleofílico de ambos respecto a los tiocarboxílicos.
-
En las reacciones conducidas con los aniones tiocarboxílicos se observa una mayor reactividad del tioéter respecto al éter (impedimento estérico que presentan ambos éteres). Cuantitativamente esto se puede apreciar al analizar las concentraciones de los éteres a los 20-25 minutos de reacción en ambas reacciones:

-
Cuando se usa anión tioacetato, la diferencia de reactividad entre ambos éteres es más marcada que cuando se usa anión tiobenzoato (diferencia de impedimento estérico presentada por el acetilo y benzoílo, respectivamente), como se aprecia en el cuadro anterior.
-
El ataque nucleofílico que sufren éter y tioéter en presencia de aniones carboxílicos es debido al metanol de la mezcla solvente (formación de 2,4-dinitroanisol) con la ayuda que le otorgan ambos aniones (acetato en mayor grado que el benzoato). La diferencia de concentración que el 2,4-dinitroanisol alcanza en las cuatro reacciones corrobora la diferencia de reactividad de ambos éteres como fuera determinada haciendo uso del anión metóxido5. En ese caso el impedimento estérico del anión metóxido frente a los sustratos, resultaba relativamente pequeño y su carga más intensamente concentrada que en los oxígenos de los aniones carboxílicos que estudiamos aquí.
-
En cambio, la diferencia en las reactividades y en los productos formados detectada en este trabajo, cuando se usan aniones carboxílicos, podría ser debida: 1) en cuanto hace a la diferencia en las reactividades: por el diferente impedimento estérico presentado por éter y tioéter frente a los aniones carboxílicos; 2) en cuanto hace a los productos formados detectados: por la diferente ayuda que ambos aniones aportan, más el acetato y menos el benzoato, para incrementar la fuerza nucleofílica del metanol.
AGRADECIMIENTOS
A los Sres. Decano, Dr. Aquiles Ferranti, y Vicedecano, Dr. Néstor Boschetti, y demás autoridades de la Facultad de Ciencias Exactas, Químicas y Naturales (FCEQyN) de la Universidad de Morón (UM) por el constante apoyo que nos han brindado durante el desarrollo del presente trabajo de investigación.
BIBLIOGRAFÍA
1. Micheli, C. y Foligno, L. "Estudio de la reactividad del anión tioacetato hacia sustratos monohalogenados (1F, 1Cl) 2,4-dinitrados del benceno en metanol y en acetona". Anuario Latinoamericano de Educación en Química; San Luis, Argentina, volumen IV, pp. 5 – 9; 1990.
2. Micheli, C. y Foligno, L. "Estudio de la reactividad del anión tioacetato hacia sustratos monohalogenados (1F,1Cl) 2,4-dinitrados del benceno en metanol y en acetona, IIº parte". Anuario Latinoamericano de Educación en Química; San Luis, Argentina, volumen IV, pp. 195 – 209; 1991.
3. Micheli. C. y Foligno, L. "Aniones tiocarboxílicos con sustratos aromáticos activados: una reacción versátil". Anuario Latinoamericano de Educación en Química; San Luis, Argentina, volumen X, pp. 242 -246; 1998.
4. Micheli, C., Wright, V., Goicochea, D. y Fasoli, H. "Síntesis y descomposición por vía nucleofílica de feniléter y feniltioéter tetranitrados", Revista de la Facultad de Ciencias Exactas, Químicas y Naturales, 2007; (5):65 -68.
5. Micheli, C., Wright V., Gallo, I., González P. y Sciarrotta E. "Introducción al estudio de la reactividad del bis (2,4-dinitrofenil)-éter y del bis (2,4-dinitrofenil)-tioéter frente al anión metóxido en acetona". Revista de la Facultad de Ciencias Exactas, Químicas y Naturales, 2010; (8):35 -50.
6. Micheli, C. y colaboradores. "Reactividad comparada de aniones carboxílicos y tiocarboxílicos con sustratos aromáticos activados". Presentado en la Secretaría de Ciencia y Técnica (SeCyT) de la Universidad de Morón (UM) (código de Proyecto A09008/08), aprobado con evaluación externa, aún no publicado.
Recibido el 23-04-2012
Aprobado el 03-05-2012




![Síntesis de nanopartículas de oro obtenidas por reducción de H[AuCl4]](/img/es/prev.gif)








