Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de la Sociedad Química del Perú
versión impresa ISSN 1810-634X
Rev. Soc. Quím. Perú v.79 n.1 Lima ene./mar. 2013
TRABAJOS ORIGINALES
Polimerización de compuestos antociánicos presentes en el colorante de la hierba santa (Cestrum hediondinum D.) y prueba de adsorción de iones Aluminio (III)
Polymerization of anthocyanin compounds present in the coloring of the yerba santa (Cestrum hediondinum D.) and proof of ion adsorption aluminum (III)
Rossana Georgina Juárez Montiel*, Nilda Pinto Apaza1, Teresa Cano de Terrones1
1 Facultad de Ciencias Naturales y Formales, Universidad Nacional de San Agustín de Arequipa, Santa Catalina 117
* juarezroxanag@gmail.com
RESUMEN
Del colorante de la "hierba santa" Cestrum hediondinum D., se separó seis fracciones. El sólido de la fracción C presenta ëmax.546 nm (BI), 282 nm (BII) y un hombro a 328 nm. El precipitado de la fracción A, ëmax. 520 nm (BI), 280 nm (BII); ambos polimerizan con formaldehído en medio ácido oxálico a un pH entre 3,0 a 4,0. Esto es confirmado por el estudio espectroscópico IR de los sólidos obtenidos, los que muestran la aparición de bandas 1452 cm-1 y 778 cm-1, correspondientes al grupo metileno. El estudio espectroscópico IR del sólido polimérico de la fracción C con tricloruro de aluminio nos muestra bandas fuera del intervalo normal 2993 cm-1 y 2465,72 cm-1 y la variación en las señales 1312 cm-1 y 1073 cm-1, todas relacionadas a los enlaces C-O y O-H fenólicos. El estudio SEM del sólido polimérico de la fracción C con aluminio (III) no muestra una adsorción uniforme.
Palabras clave: Cestrum hediondinum D., antocianina, polifenoles, polimerización.
ABSTRACT
Of the coloring of the "hierba santa" Cestrum hediondinum D., they separated six fractions. The solid of the fraction C ëmax 546 nm (BI), 282 nm (BII) and a shoulder to 328 nm. The precipitate of the fraction A, ëmax 520 nm (BI), 280 nm (BII); polymerised with formaldehyde in oxalic acid at a pH between 3,0 to 4,0. Is This confirmed by the IR spectroscopic study of the obtained solids those that show the appearance of bands 1452 cm-1 and 778 cm-1, corresponding to the methylene group, which would confirm the polymerization. The IR spectral studies of solid polymer of the fraction C with aluminum trichloride shows us bands outside of the normal interval 2993 cm-1 and 2465,72 cm-1 and the variation in the signs 1312 cm-1 and 1073 cm-1 all related to the connection C-O and O-H phenols. The study SEM of the solid polymer of the fraction C with aluminum (III), not being uniform the adsorption.
Keywords: Cestrum hediondinum D., polyphenol, anthocyanin, polymerization.
INTRODUCCIÓN
La hierba santa, cuyo nombre científico es Cestrum hediondinum D., es una planta silvestre que en Arequipa la encontramos en los distritos de Sabandía, Characato, Chiguata, Mollebaya y a lo largo de las riveras del río Chili; es un arbusto muy ramificado, de olor desagradable, de hojas elípticas lanceoladas, flores tubulosas de color verdusco-amarillento. El fruto es una baya ovoide, violácea-negrusca, dispuesta en racimos, que presenta un colorante que es la mezcla de cinco compuestos antociánicos al estado de glicósidos.1
Debido a su estructura, los compuestos antociánicos pueden ser usados como ligandos en la coordinación de iones metálicos, por lo que la diversidad de colores en las flores es explicada por la formación de quelatos entre el metal y la sal flavilio de color rojo de la antocianina. Los metales más comunes en complejos con antocianinas reportados son: Sn, Cu, Fe, Al, Mg, y K 2. Asimismo, se ha demostrado que en el vino, tanto los antocianos como los taninos pueden unirse por medio de una reacción en la que interviene el acetaldehído. Esto da lugar a productos enlazados por puentes de etilo (T-etil-T), aductos de tanino-antocianos (T-etil-A) y antocianos entre sí (A-etil-A).3
Tomando en consideración lo anterior se planteó el objetivo de polimerizar los compuestos antociánicos presentes en el colorante de la hierba santa (Cestrum hediondinum, D.) y probar su aplicación en la adsorción de iones aluminio.
PARTE EXPERIMENTAL
La materia prima fue los frutos maduros de la especie vegetal Cestrum hediondinum, D. "hierba santa". La muestra fue recolectada entre las siete y diez horas en el distrito de Characato – Arequipa, en latitud (º) -16,40; longitud (º) -71,52 y elevación (msnm) 2413, siendo la temperatura promedio de 20 ºC.
Extracción de antocianinas por maceración simple en refrigeración a 4 ºC
Se pesó 100 gramos de hollejo estabilizado seco y pulverizado y se extrajo con 1000 mL de solvente etanol:agua 70:30, por 48 horas. Terminado el tiempo de maceración, se decantó y se realizó la filtración al vacío utilizando para los lavados porciones etanol-agua. El filtrado fue concentrado a una temperatura no mayor a 30 ºC para evitar la degradación.4
Separación por cromatografía en columna de los compuesto antociánicos
20 mL de la solución concentrada del filtrado se mezclaron 20 g de sílicagel 60 (0,063-0,200 mm). La mezcla fue secada a temperatura ambiente, pulverizada en un mortero de porcelana y colocada en una columna cromatográfica; previamente es empacada con sílicagel y saturada con el propan-2-ol. Se eluyó con propan-2-ol, etanol absoluto, etanol al 98% y agua destilada y se colectó diferentes fracciones.
Caracterización por espectroscopía UV-VIS de antocianinas; barrido espectral de 200-800 nm
Se pesó 0,01 g de muestra proveniente de las fracciones colectadas y se disolvió en 10 mL de metanol espectroscópico Uvasol® (Merck), adicionando 3 gotas de solución acuosa de HCl al 50%, y se realizó el barrido espectral de 200 a 800 nm, previa calibración con el blanco.
Espectroscopía UV-Vis con el empleo de reactivos diagnósticos
Se empleó metóxido de sodio, tricloruro de aluminio, tricloruro de aluminio/ácido clorhídrico y acetato de sodio, tal como lo indica la literatura.5
Caracterización por espectroscopía de infrarrojo (IR) de las antocianinas
Los espectros fueron registrados en espectrofotómetros con transformada de Fourier Perkin- Elmer a partir de muestras sólidas (Universidad Nacional Mayor de San Marcos).
Síntesis de polímeros
Se mezcló 20 g de antocianina, 3,5 g de una solución acuosa de formaldehído al 37% de pureza y 50 mL de metanol; la mezcla se calienta a reflujo en un baño maría con movimiento hasta la formación de una solución homogénea; luego se añade 1 g de ácido oxálico y se calienta por 1 hora; se añade metanol (50 mL) y se prosigue con el calentamiento 1 hora más. Luego se filtra y lava el precipitado con etanol.
Caracterización del polímero
Se determinó los grupos funcionales por espectroscopía IR y la solubilidad por la variación del índice de refracción del solvente.
Se colocó 0,01 g del polímero en un tubo de ensayo provisto de tapa al que se añade 2,0 mL de disolvente. Se agita continuamente y se mide el índice de refracción del líquido; se utilizó un refractómetro Abbé.6
Caracterización estructural del polímero: Microscopía electrónica de barrido
La muestra fue metalizada con oro. La observación punto por punto fue realizada con un microscopio electrónico de barrido, el SEM XL20 de PHILIPS, equipado con detector de electrones retrodispersados y microanalizador de difracción de rayos X por energía dispersiva EDAX DX-4i del Centro de Microscopía electrónica de la UNSA.
Pruebas de adsorción de iones metálicos aluminio (III) por interacción sólido- líquido
Se colocó en contacto 10 mL de una disolución metanólica de AlCl3 0,2 M preparada a partir de tricloruro de aluminio anhidro, con 0,1 g de polímero a temperatura ambiente durante 24 horas con agitación constante; luego el polímero es filtrado, lavado con metanol y secado, para su análisis por espectroscopía IR y SEM.
RESULTADOS Y DISCUSIÓN
Separación por cromatografía en columna de los compuestos antociánicos
Se obtuvo seis fracciones codificadas como A, B, C, D, E, F. La fracción D eluída con etanol de 98º muestra la mayor concentración de compuestos antociánicos. Siendo la fracción A y D inestables y la F insoluble en metanol.
A continuación se verán los resultados correspondientes a la fracción C y al precipitado de la fracción A.
Caracterización espectroscópica UV-Vis de antocianinas
Los resultados experimentales para la fracción C se muestran en la tabla 1.
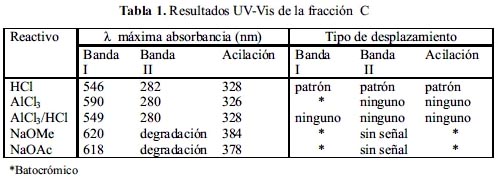
El espectro UV-Vis obtenido en un espectrofotómetro UV-Vis 8452 A Hewlett Packard corresponde a un compuesto antociánico por las características de las bandas I y II, posiblemente derivado de la delfinidina (ëmáx. 546 nm, 282 nm), presentando una señal adicional correspondiente a un compuesto acilado, que por el valor sería del ácido cafeico4, el cual estaría anulando el efecto del azúcar. Los resultados con los reactivos diagnóstico, evidencian grupos OH en posición orto y sensibles a la ionización, con grupos OH libres en el anillo A, posiciones C5 y C7.
En la tabla 2 se presentan los resultados experimentales para el precipitado de la fracción A.
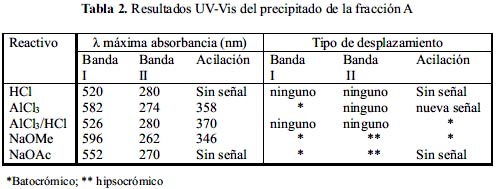
Igualmente, se deduce que la antocianina presenta grupos o-hidroxilo en el anillo B, sensibles a la ionización con metóxido de sodio; los grupos OH del anillo A muestran una variación hipsocrómica con metóxido de sodio y acetato de sodio en la señal así como una disminución en la absorbancia.
Elección de las antocianinas monoméricas
El monómero antociánico para el proceso de polimerización debe cumplir con el requisito estructural de presentar un OH en C7, y o-hidroxilos para la coordinación con el ion Al (III).
De acuerdo a los resultados, (tabla 3), podemos concluir que para el proceso de polimerización se elige la fracción C etanólica por tener grupos OH en posición orto y los grupos OH de las posiciones C5 y C7 libres y el precipitado de la fracción A propan-2-ol por tener grupos OH en posición orto e indicios de OH libre en la posición C5 y C7.

Caracterización por espectroscopía de infrarrojo (IR) de las antocianinas
Antocianina de la fracción C
El espectro IR corresponde a un compuesto aromático con grupos hidroxilos. No ha presentado bandas para grupos metóxilos (2850cm-1, 2815 cm-1, 1237cm-1 y 1272cm-1).
Antocianina precipitada de la fracción A
El espectro IR corresponde a un compuesto aromático con grupos hidroxilos. No ha presentado bandas para grupos metóxilos (2850 cm-1,2815 cm-1, 1237 cm-1 y 1272cm-1).
Síntesis de polímeros
La técnica de polimerización empleada cumple con las siguientes condiciones de reacción:
-
Estructurales:
Relación molar de la antocianina y el formaldehído:
Medio de la reacción:
pH:
El ion flavilio se comporta como un electrófilo siendo su forma pseudobase carbinol la que es más susceptible al ataque electrofílico del ion hidroximetilencarbono en sus posiciones nucleofílicas C6 y C8.
El pH está dentro del rango 3,5- 4,1 del vino tinto, en el que se da reacciones de condensación hacia la forma A+-etil- AOH.7
Catalizador:
Temperatura:
Caracterización fisicoquímica de los sólidos obtenidos
Análisis del espectro IR del sólido polimérico de la fracción C
De acuerdo a las señales en el espectro IR obtenido, podemos indicar que hay polimerización por la aparición de nuevas bandas en 1452 cm-1 y 779 cm-1 correspondientes a los grupos metileno (figura 1).
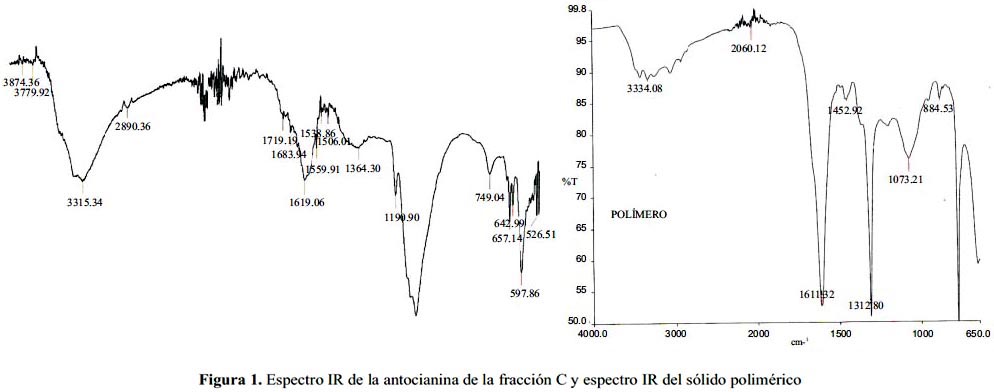
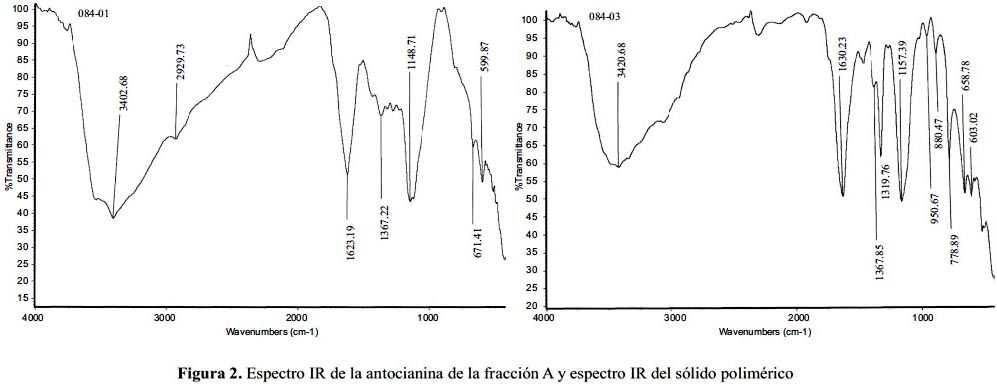
Análisis del espectro IR del sólido polimérico del precipitado de la fracción A De acuerdo a las señales en el espectro IR obtenido podemos indicar que hay polimerización por la aparición de nuevas bandas en 1460 cm-1 y 778 cm-1 correspondientes a grupos metileno en el sólido obtenido (figura 2).
Mecanismo de reacción
De acuerdo a los resultados experimentales obtenidos se propone un mecanismo de polimerización que implica formación de uniones metilénicas entre antocianos. Se toma en consideración al anillo A, ya que para explicar la polimerización de los antocianos únicamente los anillos A o C toman parte en las reacciones de polimerización.8 Las antocianinas difieren en el patrón de sustitución en el anillo B, por lo que los distintos sustituyentes de anillo B no deberían tener ningún afecto en el ratio de polimerización de unos antocianos u otros.9
La polimerización termina cuando la molécula en crecimiento se hace insoluble en el disolvente y precipita.
De acuerdo a los resultados experimentales podemos indicar que los polímeros obtenidos sobrepasan el grado de oligómeros, es decir, las ocho unidades residuales de antocianinas, por lo que precipitan.10
También se puede concluir que las moléculas poliméricas contienen unidades residuales de antocianinas al estado de iones flavilio evidenciado por el color púrpura de los sólidos obtenidos.11
El pH de 3 a 4, en el proceso de polimerización, asegura la presencia del equilibrio entre los iones flavilio con sus pseudobases carbinol.
Solubilidad
La muestra polimérica de la fracción C etanólica fue sometida a disolventes del orden hidrofílico a lipofílico, registrándose el índice de refracción cada veinticuatro horas durante cuatro días. De los disolventes ensayados se pudo observar la variación progresiva del índice de refracción del hexano, concluyéndose que el sólido polimérico es insoluble en agua y etanol, acetato de etilo y parcialmente soluble en hexano por lo que se confirma el cambio en la estructura de la antocianina ya que la molécula monoméricas de antocianina es soluble en agua y etanol cuando están al estado de glicósidos y solubles en etanol al estado de aglicona.
Caracterización estructural SEM del polímero
Los sólidos poliméricos obtenidos a partir de antocianinas glicosídicas presentan el problema de hidratación, no pudiéndose tomar imágenes adecuadas, por lo que se optó por polimerizar la aglicona de la fracción C etanólica, registrándose las imágenes en el SEM, las cuales nos muestran un sólido poroso (figura 3).

Pruebas de adsorción de iones aluminio (III)
La pruebas se realizaron con el polímero obtenido a partir de la fracción C etanólica; la solución metanólica de tricloruro de aluminio estuvo en contacto con el sólido polimérico por 24 horas a temperatura ambiente; luego fue filtrado y lavado con metanol. Al secar el sólido polimérico, inicialmente de color púrpura, cambió a azul lo que ya evidencia la coordinación de los grupos o-hidroxilo con los iones Al3+.
Espectro IR de adsorción de iones aluminio (III)
El espectro IR muestra una señal 2993 cm-1 que está fuera del intervalo normal, indicando un equilibrio con la formación de un quelato; la señal 2465,72 cm-1 está también fuera del intervalo normal relacionada al estiramiento del enlace O-H.
La variación en las señales 1312 cm-1 y 1073 cm-1 también están relacionadas con los enlaces O-H y C-O.
De acuerdo a las señales en el espectro obtenido podemos indicar que la interacción de las antocianinas poliméricas con los iones aluminio afecta las bandas correspondientes a los grupos – OH fenólicos.
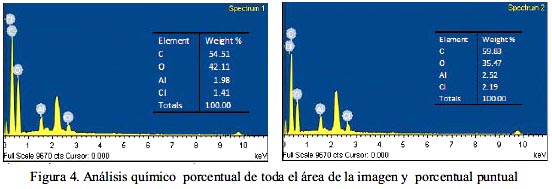
Análisis SEM de adsorción de iones aluminio (III)
La figura 4 muestra la composición químico porcentual SEM del polímero con el ion aluminio (III); se confirma la adsorción del ion Al3+, y que no es uniforme en toda la muestra.
CONCLUSIONES
-
Del colorante de la hierba santa se separaron seis fracciones. La caracterización UV-Vis dio como resultado que las fracciones corresponden a compuestos antociánicos y que presentan grupos o-dihidroxilos en el anillo B, lo que permite la complejación con el ion Al3+, excepto la fracción acuosa E. La caracterización IR confirma la presencia de grupos hidroxilos.
-
El sólido de la fracción C de ëmáx. 546 nm (BI), 282 nm (BII) y un hombro a 328 nm, y el precipitado de la fracción A de ëmáx. 520 nm (BI), 280 nm (BII), polimerizan con formaldehído en medio ácido oxálico a un pH de 3,0 a 4,0. Esto es confirmado por el estudio espectroscópico IR de los sólidos obtenidos, los que muestran la aparición de bandas 1452 cm-1 y 778 cm-1, correspondientes al grupo metileno, lo que confirma la polimerización.
-
El sólido polimérico de la fracción C etanólica es parcialmente soluble en hexano, lo que indica una modificación estructural de la antocianina inicial soluble en agua y etanol.
-
El estudio espectroscópico IR de la muestra polimérica de la fracción C que es sometida a la acción de una solución de tricloruro de aluminio, nos muestra bandas fuera del intervalo normal a 2993 cm-1 y 2465, 72 cm-1, y la variación en las señales 1312 cm-1 y 1073 cm-1, todas relacionadas con los enlaces C-O y O-H fenólicos.
-
El estudio SEM del sólido polimérico de la fracción C con aluminio (III) no muestra una adsorción uniforme.
AGRADECIMIENTOS
Agradecemos a la Unidad de Posgrado de Facultad de Ciencias Naturales y Formales, por el apoyo prestado para la realización de este trabajo de investigación.
REFERENCIAS
1. Juárez Montiel R. Extracción, Purificación e Identificación del colorante de la Hierba Santa (Cestrum hediondinum, D.) [Tesis de Licenciatura]. Arequipa, Perú, Universidad Nacional de San Agustín de Arequipa; 1993.
2. Rein M. Copigmentation reactions and color stability of berryanthocyanins. University of Helsinki, Finlandia, 2005. http://ethesis.helsinki.fi/julkaisut/maa/skemi/vk/rein/copigmen.pdf
3. Cheynier, V. El color de los vinos tintos. Wine Internet Technical Journal, 2003;4: 1-9.
4. Antocianos y Betaninas colorantes naturales de aplicación Industrial. Publicación del Programa Iberoamericano de Ciencia y Tecnología para el Desarrollo (CYTED) y la Comisión Nacional Científica y Tecnológica de Chile (CONICYT). Red. IVD Sustancias Fitoquímicas de Aplicación Industrial Subprograma IV: Biomasa como fuente de Productos Químicos y Energía Proyecto IV.10. Santiago de Chile, 2003
5. Lock de Ugaz O. Investigación Fitoquímica. Lima-Perú. Pontificia Universidad Católica del Perú. Fondo Editorial. 1988.
6. Armelin Elain. Síntesis y Caracterización de Nuevas Poliesteramidas: Estudio de sus Propiedades. [Tesis Doctoral]. Barcelona, España: Universidad Politécnica de Cataluña ; 2002.
7. Ribereau-Gayon P, Glories Maujean A. Dubourdieno. Tratado de Enología. Química del vino, estabilización y tratamientos. Argentina: Ediciones Mundiprensa; 2003.
8. Cheynier V. Moutounet, M. Sarni- Manchado, P. Los compuestos fenólicos. En enología: Fundamentos científicos tecnológicos. Argentina. Ediciones Mundiprensa, p. 114-136. 2000.
9. Garcia-Beneytez E, Revilla E, Cabello F, Anthocyanin pattern of several red grape cultivars and wines made from them. European Food Research and Technology, 2002; 215: 32-37.
10. Santos-Buelga C, Bravo-Haro S, Rivas-Gonzalo J. C. Interactions between catechin and malvidin-3-monoglucoside in models solutions. Z Lebensm Unters Forsch, 1995; 201: 269-274.
11. Atanasova V, Fulcrand H, Le Guernevé C, Cheynier V, Moutounet M, Structure of a new dimeric acetaldehyde malvidin 3-glucoside condensation product. Tetrahedron Letters, 2002; 43: 6151-6153.
Recibido el 08-11-2012
Aprobado el 25-01-2013













