Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista de la Sociedad Química del Perú
Print version ISSN 1810-634X
Rev. Soc. Quím. Perú vol.83 no.2 Lima Apr./Jun. 2017
TRABAJOS ORIGINALES
Uso de edulcorantes comerciales como una alternativa a la reducción de 5-Hidroximetil-2- Furfural (HMF) en galletas modelo
Use of commercial sweeteners as an alternative to the reduction of 5-Hydroxymethyl-2-Furfural (HMF) in model cookies
Nils Huamán Castilla*a, Erik Allccaa, Nilton Leóna, Gladys Yupanquib
a Escuela Profesional de Ingeniería Agroindustrial, Universidad Nacional de Moquegua (UNAM), Av. Ancash s/n, Moquegua, Perú,
b. Escuela de Posgrado Universidad Nacional Agraria La Molina, e-mail: nilefox@gmail.com; Teléfono: +51-958890808
RESUMEN
El presente estudio tuvo por objetivo evaluar la influencia del uso de edulcorantes comerciales tales como estevia y sucralosa para reducir la formación de 5-hidroximetil-2-furfural (HMF) en galletas modelo, para tal efecto se prepararon tres muestras con sacarosa, stevia y sucralosa. Los resultados muestran que la adición de sacarosa promueve la formación de HMF con valores promedio de 15,29 ± 0,34 mg/kg, mientras que la adición de estevia mitigó la formación de HMF en ~ 60% con valores promedio de 6,49 ± 0,5 mg/kg. No obstante, la adición de sucralosa, contrariamente al comportamiento de la stevia, promueve la formación HMF en niveles 55,9 ± 2,99 mg/kg. Estos resultados nos indican que el uso de estevia reduce el contenido de HMF en galletas modelo, promoviendo la obtención de alimentos inocuos y seguros para consumo humano.
Palabras clave: sacarosa, sucralosa, estevia, HMF.
ABSTRACT
The present study aimed to evaluate the influence of commercial sweeteners such as stevia and sucralose to reduce formation of 5-hydroxymethyl-2-furfural (HMF) in model cookies. Three samples were prepared with sucrose, stevia and sucralose. The results show that the addition of sucrose promotes the formation of HMF with mean values of 15,29 ± 0,34 mg / kg, while the addition of stevia mitigates the formation of HMF in ~ 60% with mean values of 6,49 ± 0,5 mg / kg. However, the addition of sucralose contrary to stevia behavior promotes HMF formation at levels of 55,9 ± 2,99 mg / kg. These results indicate that the use of stevia reduces the HMF content in model cookies, promoting the obtaining of safe foods for human consumption.
Key words: sacarosa, sucralosa, stevia, HMF.
INTRODUCCIÓN
Los productos de panificación, tales como galletas y panes, son definidos como la transformación de la harina con la adición de agua y otros agentes, tales como levaduras y edulcorantes que promueven, además de la textura, características sensoriales particulares; pues, en general, el aspecto del color en la superficie es el primer parámetro de calidad evaluado por el consumidor y es crítico en la aceptación del producto, también es asociado con el aroma y el nivel de satisfacción1.
La formación del color amarillo dorado en galletas es debido al pardeamiento no enzimático, el mismo que es una reacción química que se produce durante el proceso de horneado, conocido como la reacción de Maillard, cuyos productos finales de este mecanismo de reacción son conocidos como melanoidinas. Cuando los sistemas alimenticios contienen azúcares reductores y aminoácidos, y son tratados a altos niveles de temperatura (> 120°C) la reacción de Maillard es promovida, pero esta reacción también depende de la actividad de agua y pH2. Un reciente estudio evaluó el tipo de harina, temperatura y pH en la formación de melanoidinas en la superficie del pan, encontrando que tal comportamiento puede ser explicado por un modelo de primer orden3.
La interacción de azúcares reductores (glucosa y fructosa) y aminoácidos u otros grupos de compuestos que contengan nitrógeno, durante el proceso de horneado, es asociado a la formación de 5-hidroximetil-2-furfural (HMF) vía reacción de Maillard y degradación de azúcares, el cual es altamente dependiente del nivel de actividad de agua, mostrando reacciones altas a niveles superiores de 0,4; lo que trae como consecuencia la formación de HMF4. No obstante, el HMF es un compuesto químico considerado como un contaminante tóxico que recientemente ha traído mucho interés debido a su alta toxicidad, y ha sido reconocido como posible compuesto mutagénico y carcinogénico en alimentos5. Los productos horneados, como las galletas, pueden contener HMF en niveles de 11,8 a 87,7 mg/kg6. Ha sido demostrado que una ingesta oral de 0,08 a 500 mg/kg de peso corporal es rápidamente absorbido por el sistema digestivo en ratas y ratones, estas concentraciones son citotóxicas, dañan la mucosidad de las membranas celulares, seguido de la aparición de células cancerosas7. Por ello, el objetivo de este trabajo de investigación es evaluar la influencia del uso de edulcorantes comerciales para mitigar la formación de HFM en galletas modelo.
PARTE EXPERIMENTAL
Tres muestras de galleta modelo y un control fueron preparadas con 70g de almidón (95% de pureza); 0,5 g de gluten y 15 g de mantequilla (98% grasa); para la primera muestra (M1) se añadieron 25 g de sacarosa, para la segunda muestra (M2) se sustituyó parcialmente el contenido de sacarosa con 12,5 g y 1,18 g de estevia, de la misma forma, para la tercera muestra (M3) se añadieron 12,5 g de sacarosa y 1,18 g de sucralosa, un control fue preparado sin la adición de edulcorantes. Las masas fueron preparadas en una laminadora de masas (modelo malta 1000) cuyo espesor de cada muestra fue de 2,75 cm. El horneado se realizó en un horno convector eléctrico marca Moretti modelo ML-4, la temperatura de horneado fue de 180°C por un tiempo de 20 min; las galletas horneadas fueron enfriadas y envasas en bolsas de polipropileno de alta densidad para su conservación y posterior análisis.
Análisis de HMF: la metodología de análisis es según lo propuesto por Toker et al (2013)8; se pesó 1 g de muestra previamente molida, la cual se colocó en un tubo de centrífuga de 50 mL, se adicionó 20 mL de agua destilada, se agregaron 1,5 mL de carrez I (15g de K4[Fe(CN)6] x3H2O en 100 mL de agua); se agitó por 2 min, posteriormente se agregó 1,5 mL de carrez II (30g de ZnSO4x7H2O en 100 mL de agua), luego se centrifugó por 15 min a 6000 rpm. Una vez finalizada esta etapa se tomó 2 mL del sobrenadante y se filtró por un filtro de 0,22 μm (nylon), la muestra filtrada fue depositada en un vial de 3 mL para su posterior análisis por HPLC-DAD. Las condiciones de análisis cromatográfico, mediante HPLC DAD, fueron fase móvil: ácido acético al 1% y acetonitrilo (proporción 95/5%); el flujo de la fase móvil fue de 1 mL/min, longitud de onda del detector = 284 nm; Inyección de 20 μL; Columna AcclaimTM 120, C-18, 5 μm, 120 Å y 4,6 x 150 mm.
Análisis sensorial: la aceptabilidad general (color, sabor y apariencia) de las galletas modelo se realizaron mediante la metodología propuesta por Bala (2015)9 en una escala de 5 puntos. El panel sensorial involucrado (jueces semi-entrenados) pertenecen a la Escuela Profesional de Ingeniería Agroindustrial de la UNAM. Las muestras se calificaron sobre una escala de 5 puntos, donde: 5 significa altamente aceptable y 0 completamente inaceptable.
Para el análisis estadístico fue usado el programa Statgraphics Plus for Windows 4.0 (Herndon, VA, USA). Para estudiar los efectos de la adición de edulcorantes sobre la reducción de HMF, se aplicó un análisis de varianza (ANOVA) y las diferencias significativas en las variables de respuesta se evaluaron con un nivel de significancia de p ≤ 0,05.
RESULTADOS Y DISCUSIÓN
Un reciente estudio evaluó las condiciones óptimas en la medición de HMF mediante HPLC-DAD, dicho trabajo indica que el tiempo de retención para este compuesto es de ~5 min usando una columna C 18. Adicionalmente, los resultados al usar un HPLC-DAD tienen una confiabilidad del 98%, cuyo margen de error se debe en demasía a la azeotropia propia del alimento8. La Figura 1 muestra el análisis cromatografico de HMF en las galletas modelo usando un HPLC-DAD con columna C 18, se puede observar que las tres muestras de sacarosa (M1), stevia (M2) y sucralosa (M3) tienen el mismo tiempo de retención, pero diferentes picos de absorbancia, esto es debido a la diferente concentración de HMF presente en cada muestra.
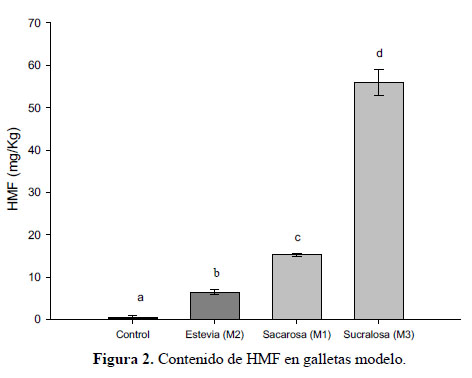
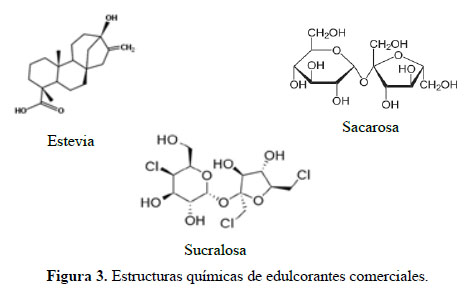
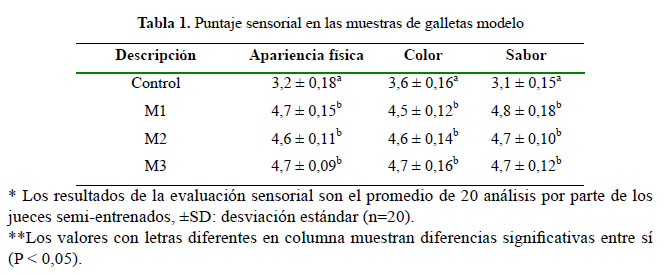
La Figura 2 muestra las concentraciones de HMF en sacarosa (M1), estevia (M2) y sucralosa (M3). El contenido de HMF en la muestra de sacarosa (M1) varía de 14,9 a 15,6 mg/kg, al respecto, la estructura química de este compuesto no es la de un azúcar reductor (Figura 3). Sin embargo, diversos estudios demostraron que las altas temperaturas (>120°C) promueven la ruptura del enlace glucósidico liberando azúcares reductores, tales como glucosa y fructosa, los mismos que interactúan con los grupos amino de las proteínas para formar HMF vía reacción de Maillard10. No obstante, debido a las altas temperaturas de horneado (180°C) es posible que la sacarosa también se haya degradado vía la ruta de la caramelización o deshidratación de azúcares para formar HMF. El contenido de HMF en la muestra de estevia (M2) varía de 6,49 a 7 mg/kg (Figura 2), al respecto es importante mencionar que la estructura química de este compuesto no es la de un azúcar reductor tales (Figura 3), por ende no interactúa con los grupos amino de las proteínas para formar HMF vía reacción de Maillard10. Por otro lado, la muestra de estevia (M2), debido a la sustitución parcial, contiene un 12,5 g de sacarosa, esto explicaría la concentración de HMF detectada en esta muestra6,11. * Los resultados analíticos están expresados en miligramos de HMF por gramo de galleta modelo y son el promedio de tres repeticiones, ±SD: desviación estándar (n=3) **Los valores con letras diferentes muestran diferencias significativas entre sí (P<0,05) El contenido de HMF en la muestra de sucralosa (M3) varía de 52,9 a 58,9 mg/kg, dicho contenido fue mayor en comparación con las muestras M2 y M1 (Figura 2). Al respecto, es importante mencionar que la sucralosa es el nombre común de un edulcorante artificial cuyo nombre quimico es 1,6-dicloro-1,6-dideoxi-B-fructofuranosil-4-cloro-4deoxi-x-dgalactopiranosa o 4,1´,6´-triclorogalactosucrosa (Figura 3). Este compuesto es sintetizado a partir de la sucrosa (sacarosa), cuya conformación es diferente a la estructura molecular de la sacarosa, pues tiene unidos átomos de cloro en su estructura química, esto hace que la sucralosa sea un compuesto termoestable12. Sin embargo, un estudio demostró que en temperaturas más allá de los 119°C ocurría una descomposición térmica de dos etapas en la sucralosa13. Esta reactividad de la sucralosa se debe a los tres átomos de cloro que están presentes en su estructura (C-Cl); La primera etapa se da alrededor de los 130°C donde los átomos de cloro son liberados y por cada átomo de cloro se liberan dos moléculas de agua; la segunda etapa ocurre entre los 140 – 160°C, consiste en la reacción del cloro con la molécula de agua, donde forma cloruro de hidrógeno13. La formación de cloruro de hidrógeno hace que el pH del medio baje hasta niveles de 3 a 4, sumado a las altas temperaturas promueven que el enlace glicósidico se rompa liberando fructopiranosil (fructosa) y galactopiranosil (glucosa) que son azúcares reductores14. Este tipo de hidrólisis explicaría la formación de HMF en las galletas modelo a partir de sucralosa. Los parámetros cinéticos de los azúcares reductores en la reacción de Maillard fueron determinados por un estudio que estableció un orden jerárquico de la preferencia de la reacción Maillard por estos azúcares, estando en orden de mayor a menor la fructosa, ribosa, xilosa, arabinosa y glucosa, respectivamente, esta afinidad por la reacción se explica por la unión que realizan estos azúcares con el grupo amino de la lisina (NH2), la preferencia radica en el peso molecular y la mayor afinidad al grupo aldehído libre para reaccionar de las aldosas (xilosa, ribosa y ribosa), a diferencia de la fructosa que presenta un grupo cetónico el cual es más reactivo10. Del panel de jueces semi-entrenados (Tabla 1), muestra que las galletas modelo preparadas con sacarosa, estevia y sucralosa no presentan diferencias significadas entre sí (P < 0,05) demostrando que la sustitución parcial de edulcorantes tales como estevia y sucralosa por sacarosa en un margen del 14% permiten conservar la aceptabilidad general en galletas modelo. Similares resultados fueron reportados en diversos estudios, donde mencionan a edulcorantes tales como estevia, inulina, xilitol, maltitol y sucralosa, que gracias a su poder edulcorante permiten sustituir parcialmente el contenido de sacarosa en productos de panificación, evitando alterar la percepción sensorial de dichos productos15. CONCLUSIONES El uso de edulcorantes como la estevia mitiga la formación de HMF en galletas modelo debido a su estructura química particular, la sacarosa promueve la formación de HMF por dos vías alternas de caramelización y reacción de Maillard por hidrólisis parcial de su estructura. Sin embargo, la sucralosa contrariamente al comportamiento de la estevia promueve la formación HMF en niveles superiores al de la sacarosa, debido a las altas temperaturas del proceso de horneado y la liberación de cloruro de hidrógeno que promueven la hidrólisis de este compuesto. AGRADECIMIENTO Los autores agradecen al PhD. Franco Pedreshi Plasencia, del Departamento de Ingeniería Química y Bioprocesos de la Pontificia Universidad Católica de Chile. BIBLIOGRAFÍA 1. Pedreschi F, León J, Mery D, Moyano P, Pedreschi R, Kaack K, et al. Color development and acrylamide content of pre-dried potato chips. J Food Eng. 2007; 79 (3): 786–93. [ Links ] 2. Purlis E, Salvadori VO. Modelling the browning of bread during baking. Food Res Int. 2009; 42 (7): 865–70. [ Links ] 3. Broyart B, Trystram G, Duquenoy A. Predicting colour kinetics during cracker baking. J Food Eng. 1998; 35 (3):351–68. [ Links ] 4. Ameur LA, Trystram G, Birlouez-Aragon I. Accumulation of 5-hydroxymethyl-2- furfural in cookies during the backing process: Validation of an extraction method. Food Chem. 2006; 98 (4): 790–6. [ Links ] 5. Ulbricht RJ, Northup SJ, Thomas JA. A review of 5-hydroxymethylfurfural (HMF) in parenteral solutions. Toxicol Sci. 1984; 4 (5): 843–53. [ Links ] 6. Ramírez-Jiménez A, García-Villanova B, Guerra-Hernández E. Hydroxymethylfurfural and methylfurfural content of selected bakery products. Food Res Int. 2000; 33 (10): 833–8. [ Links ] 7. Archer MC, Bruce WR, Chan CC, Corpet DE, Medline A, Roncucci L. Aberrant crypt foci and microadenoma as markers for colon cancer. Environ Health Perspect. 1992; 98:195-197. [ Links ] 8. Toker OS, Dogan M, Ersoz NB, Yilmaz MT. Optimization of the content of 5-hydroxymethylfurfural (HMF) formed in some molasses types: HPLC-DAD analysis to determine effect of different storage time and temperature levels. Ind Crops Prod. 2013; 50: 137–44. [ Links ] 9. Bala A, Gul K, Riar CS, Yildiz F. Functional and sensory properties of cookies prepared from wheat flour supplemented with cassava and water chestnut flours. Cogent Food Agric. 2015; 1 (1): 101-109. [ Links ] 10. Laroque D, Inisan C, Berger C, Vouland É, Dufossé L, Guérard F. Kinetic study on the Maillard reaction. Consideration of sugar reactivity. Food Chem. 2008; 111 (4): 1032–42. [ Links ] 11. Capuano E, Fogliano V. Acrylamide and 5-hydroxymethylfurfural (HMF): A review on metabolism, toxicity, occurrence in food and mitigation strategies. LWT - Food Sci Technol. 2011; 44 (4): 793–810. [ Links ] 12. Linden A, Muhammad Sofian AS, Lee CK. 4,1′,6′-Trichloro-4,1′,6′-trideoxysucrose monohydrate. Acta Crystallogr Sect C Cryst Struct Commun. 2002; 58 (12): 711–714. [ Links ] 13. Bannach G, Almeida RR, Lacerda LG, Schnitzler E, Ionashiro M. Thermal stability and thermal decomposition of sucralose. Eclet Quim. 2009; 34 (4): 21–6. [ Links ] 14. Rahn A, Yaylayan VA. Thermal degradation of sucralose and its potential in generating chloropropanols in the presence of glycerol. Food Chem. 2010; 118 (1): 56–61. [ Links ] 15. Struck S, Jaros D, Brennan CS, Rohm H. Sugar replacement in sweetened bakery goods. Int J Food Sci Technol. 2014; 49 (9): 1963–76 [ Links ] Recibido el 24-02-17 Aprobado el 22-07-17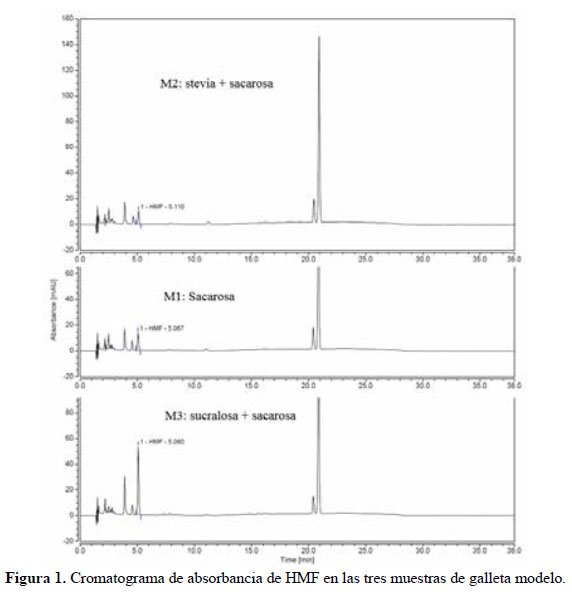





![Theoretical characterization and design of efficient photoactive materials based on Anthra[2,3-c]Pyrrole and Anthra[2,3-c]Thiophene derivatives aimed towards organic solar cells](/img/en/next.gif)







