INTRODUCCIÓN
En el Perú, la producción de arroz, según el Instituto Nacional de Innovación Agraria (INIA), ocupó un área sembrada y cosechada de 0,38 millones de hectáreas durante el 2014, estimando una generación aproximada de 0,34 millones de toneladas de cascarilla de arroz1.
La valorización de la cascarilla de arroz, residuo lignocelulósico, debe superar barreras naturales como la cercanía física y asociación química entre la lignina y los polisacáridos de la pared celular; así como el grado de cristalización de los polímeros de celulosa2, 3,4, y para ello se debe realizar pretratamientos químicos, con al finalidad de exponer a la celulosa al ataque enzimático y posterior fermentación alcohólica para la obtención de la producción de etano de segunda generación 5,6.
El pretratamiento alcalino-peróxido es aplicado para la remoción de la lignina por saponificación de los enlaces éster, logrando en algunos casos hasta un 50 % de remoción 7,8. La inclusión del peróxido en medio alcalino favorece la delignificación por la oxidación con radicales hidroxilo y superóxidos 9,10. El pretratamiento ácido permite la disolución de la hemicelulosa y redistribución de la lignina, aumentando la digestibilidad de la celulosa 6. El efecto de altas temperaturas y elevada acidez pueden degradar las pentosas y hexosas formando furfural y 5-hidroximetilfurfural compuestos inhibidores de la hidrólisis enzimática y fermentación 8,11. La aplicación del pretratamiento silicato-peróxido busca promover la formación de enlaces entre los grupos silicatos de la superficie rugosa y tricomas de la superficie de la cascarilla de arroz con los silicatos proporcionados por el pretratamiento generando huecos en la epidermis que expongan a la celulosa a un ataque enzimático posterior 2.
Posterior al pretratamiento de la cascarilla de arroz, se realiza la hidrólisis enzimática, mediante una mezcla de enzimas que constan principalmente de celulasas, ß-glucosidasas y hemicelulasas de tipo xilanasas 12,13. Como una medida de la eficiencia de la hidrólisis, se utiliza el parámetro de la sacarificación, que relaciona el contenido de los azúcares reductores en el hidrolizado con el contenido de azúcares totales en la cascarilla de arroz 12,14,15,16.
La presente investigación tuvo por objetivo evaluar el efecto de los pretratamientos químicos sobre la hidrólisis enzimática de la cascarilla de arroz.
PARTE EXPERIMENTAL
Materiales
La cascarilla de arroz fue recolectada en la Asociación Peruana de Molineros de Arroz y Molino Sudamérica en mayo del 2017 Lambayeque - Perú. El material presentó un tamaño de 9,2 - 10,7 mm de largo por 2,1 - 3,8 mm de ancho, para evitar un gasto energético adicional se eliminó el proceso de molienda, otros autores reportan que al utilizar la cascarilla molida hasta 1,2 mm, se favorece notoriamente la liberación de azúcares totales 17. Las muestras fueron conservadas al vacío en bolsas de 5 kg de capacidad y almacenadas en oscuridad hasta su análisis.
Los reactivos utilizados para los pretratamientos fueron: hidróxido de potasio (85 %, Merck, Alemania), ácido acético glacial (100 %, Merck, Alemania), peróxido de hidrógeno (50 %, Maquimsa S.A., Perú), silicato de potasio (23 % SiO2, Klaida, Perú). Para la hidrólisis enzimática se utilizó una mezcla de celulasas, con alto nivel de β-glucosidasas y hemicelulasas (Cellic® CTec2).
Pretratamiento de la cascarilla de arroz
Se realizaron nueve pretratamientos alcalino-peróxido utilizando mezclas (1:1) de hidróxido de potasio al 2, 4 y 6 % p/v y peróxido de hidrógeno al 5, 10, 15 % v/v; nueve pretratamientos ácido-peróxido utilizando mezclas (1:1) de ácido acético glacial al 5,10 y 15 % v/v y peróxido de hidrógeno al 5, 10 y 15 % v/v; y nueve pretratamientos silicato-peróxido utilizando mezclas (5:2) de silicato de potasio al 5, 10 y 15 % p/v y peróxido de hidrógeno al 5, 10, 15 % v/v, como se observa en tabla 1.
Tabla 1 Pretratamientos aplicados a la cascarilla de arroz.
| Pretratamientos | ||||||
| Alcalino-peróxido | Ácido-peróxido | Silicato-peróxido | ||||
| % KOH - % H2O2 | % CH3COOH - % H2O2 | % K2SiO3 - % H2O2 | ||||
| T1-Alc | 0 - 0 | T1-Ac | 0- 0 | T1-S | 0- 0 | |
| T2-Alc | 2 - 5 | T2-Ac | 5- 5 | T2-S | 5- 5 | |
| T3-Alc | 4 - 5 | T3-Ac | 10-5 | T3-S | 10-5 | |
| T4-Alc | 6 - 5 | T4-Ac | 15-5 | T4-S | 15-5 | |
| T5-Alc | 2-10 | T5-Ac | 5-10 | T5-S | 5-10 | |
| T6-Alc | 4-10 | T6-Ac | 10- 10 | T6-S | 10- 10 | |
| T7-Alc | 6-10 | T7-Ac | 15- 10 | T7-S | 15- 10 | |
| T8-Alc | 2-15 | T8-Ac | 5-15 | T8-S | 5-15 | |
| T9-Alc | 4-15 | T9-Ac | 10- 15 | T9-S | 10- 15 | |
| T10-Alc | 6-15 | T10-Ac | 15- 15 | T10-S | 15- 15 | |
Se utilizó una carga de 10 % p/v de cascarilla de arroz en la solución deslignificante de cada pretratamiento, el tiempo de incubación fue de 3 h a 70 °C18. Se seleccionó un pretratamiento óptimo de cada solución deslignificante (alcalino-peróxido, ácido-peróxido, silicato-peróxido) en base a la mayor concentración de azúcares totales en el lixiviado, para su caracterización morfologíca mediante SEM e hidrólisis enzimática.
Determinación de azúcares totales (AT)
La determinación de AT se realizó en el lixiviado de las muestras como una medida indirecta de la eficiencia de cada pretratamiento. Se utilizó el método de DuBois, que se basa en la deshidratación de los azúcares al reaccionar con el ácido sulfúrico formando derivados de furfural. La formación del complejo coloreado se encuentra entre amarillo y naranja y presenta una absorbancia máxima a 490 nm19. Para la cuantificación se utilizó un espectrofotómetro modelo Evolution 300 UV-Vis Thermo Fisher Scientific.
Caracterización morfológica de la cascarilla de arroz pretratada
Las muestras de los pretratamientos óptimos y una muestra no pretratada fueron observadas por la parte interna y externa de su superficie utilizando microscopia electrónica de barrido (SEM). Las imágenes fueron obtenidas utilizando un microscopio electrónico modelo Q250 Analytical. Para el análisis las muestras fueron secadas y cubiertas con una película de oro, se utilizó una aceleración de voltaje de 20 kV. Las imágenes fueron obtenidas a 35 y 260 magnificaciones.
Hidrólisis enzimática (HE)
La cascarilla de arroz pretratada fue hidrolizada enzimáticamente con diferentes relaciones enzima/sustrato: 0,1; 0,2 y 0,3 mL de enzima por gramo de sustrato, similar a lo reportado por Salcedo et al.20; utilizando una carga de 5 % p/v, 50 mM de buffer acetato de sodio, pH de 5, a 50º C por 72 horas y agitación de 150 rpm. Se trabajó con una mezcla de enzimas: celulasas, con alto nivel de β-glucosidasas y hemicelulasas (Cellic® CTec2). Este mezcla de enzimas posee un alto rendimiento de conversión, efectiva a altas concentraciones de sólidos, tolerante a inhibidores, compatible con múltiples materias primas y pretratamientos, posee una alta concentración y estabilidad 13. Al finalizar, se almacenó el hidrolizado enzimático a 4 °C para determinar la cantidad de azúcares reductores así como el porcentaje de sacarificación.
Determinación de azúcares reductores (AR) y sacarificación
La determinación de AR fue realizada utilizando el método del DNS, el método se basa en la reacción redox que ocurre entre los azúcares reductores y el ácido 3,5-dinitrosalicílico, la cual produce una coloración naranja y presenta una absorbancia máxima a 540 nm 21,22. Para la cuantificación se utilizó un espectrofotómetro modelo Evolution 300 UV-Vis Thermo Fisher Scientific.
La sacarificación es un parámetro importante para evaluar la capacidad de un sustrato para formar azúcares reductores. Este parámetro relaciona el contenido de azúcares reductores en el hidrolizado enzimáticos y la concentración potencial de azúcar del sustrato con o sin pretratamiento, se determina mediante la ecuación (1) 7,15,23.
La concentración potencial de azúcares en la cascarilla de arroz se basó en la determinación del contenido de celulosa y hemicelulosa, obtenida por diferencia entre la masa total y el contenido de lignina, humedad y cenizas, conforme a lo establecido por el reporte técnico de la National Renewable Energy Laboratory OF United States NREL/TP-510-42618.
RESULTADOS Y DISCUSIÓN
Pretratamiento de la cascarilla de arroz
Los resultados óptimos para cada pretratamiento fueron: T10-Alc, T9-Ac y T10-S. El análisis estadístico del ANOVA y el LSD-Fisher presentan diferencia significativa (p<0,05) en cada caso. En la figura 1 se muestra la comparación de AT en mg/g.
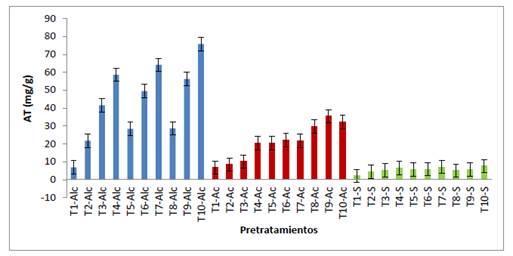
Figura 1 Azúcares totales (mg/g) en el lixiviaado de la cascarilla de arroz sometida a pretratamientos.
El pretratamiento es la etapa más importante, pues tiene un impacto en el rendimiento y eficiencia de la hidrólisis enzimática. En esta etapa se eliminan algunos componentes constitutivos de la cascarilla como la lignina que dificulta la actividad enzimática y disminuye la cristalinidad de las fibras de celulosa; también se remueve la hemicelulosa de los residuos lignocelulósicos 5,6.
El pretratamiento T10-Alc (H2O2 15 % v/v, pH de 11, 70 °C y 3 h de incubación para 10% de sustrato) de la cascarilla de arroz presentó el mejor resultado liberando hasta 75,9 mg/g de azúcares totales, este resultado es mayor al encontrado para el tratamiento alcalino 60 mg/g (H2O2 0% v/v, pH de 11,5, 35 °C y 24 horas de incubación para 15 % de sustrato) e hidrólisis enzimática (pH de 5, 45 °C, 72 h, 0,4 mL/g) y menor que el tratamiento con alcalino-peróxido 249 mg/g (H2O2 7,5 % v/v, pH de 11,5, 35 °C, 24 horas de incubación para 15 % de sustrato) e hidrólisis enzimática (pH de 5, 45 °C, 72 h, 0,4 mL/g) reportado por Saha y Cotta 17. A tiempos cortos de pretratamiento, temperaturas altas de incubación mejoran el rendimiento de los azúcares liberados similar a lo reportado por Saha y Cotta 17 cuando evalúa a las temperaturas de 25 y 35 °C obteniendo un resultado de 149 y 211mg/g, respectivamente. El incremento de la dosis de álcali mejora la liberación de azúcares totales desde 28,7 (T8-Alc) hasta 75,9 mg/g (T10-Alc) similar a lo reportado por Saha y Cotta25, que logra un incremento hasta del 83 %, cuando utiliza piedra caliza como álcali. Asimismo, se reporta que mediante el pretratamiento alcalino se mejora la digestibilidad de la celulosa y una menor degradabilidad de azúcares en relación al pretratamiento ácido 25,26. Mediante el pretratamiento alcalino se produce la saponificación de los enlaces éster de la lignina, provocando la hidrólisis de la lignina, hemicelulosa y celulosa8 evita la fragmentación de los polímeros de hemicelulosa, remueve lignina y hemicelulosa aumentando la accesibilidad de las enzimas a la celulosa 6,8,27, sin degradar tanto los azúcares 27, es por ello que es más eficiente que los otros pretratamientos. Aunque este pretratamiento presenta como desventaja que algunas bases se conviertan en sales y estas se incorporan en la biomasa27. Se reporta que el pretatamiento alcalino-peróxido es más eficaz para mejorar la digestibilidad de los residuos en la hidrólisis enzimática, es decir, se obtiene mayor solubilidad de lignina y hemicelulosa, y una mayor conversión a pH de 11,5; en comparación del pretratamiento alcalino 26,28.
El pretratamiento T9-Ac (H2O2 15 % v/v, pH de 2,6, 70 °C y 3 h de incubación para 10% de sustrato) liberó hasta 35,5 mg/g de azúcares totales, este resultado es mayor a 15 mg/g (H2O2 0% v/v, pH menor a 2, 121 °C, 15 min de incubación para 15 % de sustrato) reportado por Saha et al.11, pero inferior a 65 mg/g determinado por Wi et al.29 al utilizar ácido sulfúrico (H2O20% v/v, pH menor a 2, 80 °C, 120 min de incubación para 10 % de sustrato) e hidrólisis enzimática (pH de 5, 37 °C, 72 horas de incubación, actividad de la celulasa y xilanasa de 79 kFPU/mL y 592 IU/mL). El pretratamiento con ácido depende de la temperatura, tiempo, concentración y tipo de ácido utilizado para la obtención de azúcares fermentables 6,27. Este pretratamiento no resulta efectivo para la eliminación de la lignina, siendo tóxico, corrosivo y peligroso, requiriendo de procesos resistentes a la corrosión, lo que provoca un encarecimiento de costes 26,28. Se reporta que durante el pretatamiento ácido caliente, generalmente las hemicelulosas se hidrolizan 8,26 y los azúcares libres resultantes pueden degradarse a furfural provenientes de pentosas y a 5-hidroxi-metilfurfural provenientes de hexosas8. Estos compuestos son inhibidores de los microorganismos, y su producción significa la pérdida de azúcares fermentables 8,26. Estudios realizados por Wi et al.29 en paja de arroz (relación de 1:1 de H2O2 y CH 3COOH, 80 °C y 2 h de incubación, para 10 % de sustrato) e hidrólisis enzimática (pH de 5, 37 °C, 72 h, actividad de la celulasa y xilanasa de 79 kFPU/mL y 592 IU/mL) lograron mejores resultados de hasta 110 mg/g de azúcares totales, debido a que el pretratamiento con ácido acético y peróxido de hidrógeno es más eficiente para eliminar lignina antes de la hidrólisis enzimática 8,29, además no requiere de elevadas temperaturas, es menos corrosivo como los ácidos fuertes y disminuye la generación de inhibidores en el proceso de la fermentación.
El pretratamiento T10-S (H2O2 15% v/v, pH neutro, 70 °C y 3 h de incubación para 10% de sustrato) liberó hasta 7,6 mg/g de azúcares totales, este resultado es menor a cualquiera de los pretratamientos probados alcalino-peróxido o ácido-peróxido, también es menor a 15,0 mg/g reportado por Wi et al.29 cuando solo se aplica una molienda como pretratamiento, sin la aplicación de otros reactivos, e hidrolisis enzimática (pH de 5, 37 °C, 72h, actividad de la celulasa y xilanasa de 79 kFPU/mL y 592 IU/mL).
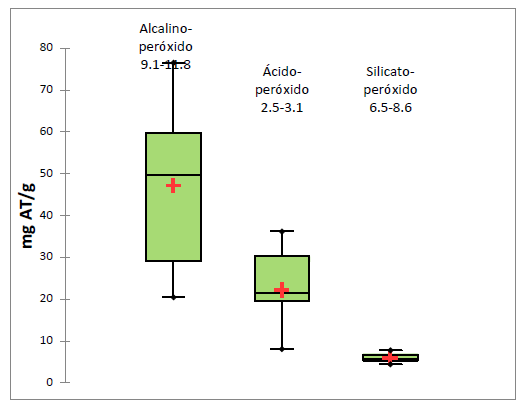
En la figura 2 se observa el rango de valores de pH encontrados en los lixiviados de los pretratamientos de la cascarilla de arroz, estos fueron; alcalino-peróxido: 9,1-11,8, ácido-peróxido: 2,5-3,1 y silicato-peróxido: 6,6-8,6. Los valores de pH hallados en el pretratamiento alcalino-peróxido se asemejan a los valores reportados, en donde se indica que la eficiencia de la deslignificación está en relación a los valores de pH, valores de 11,5-11,6 son más efectivos y valores menores a 10 son insignificantes y valores de más de 12,5 no muestran efecto sobre la digestibilidad enzimática17,26,30. El control del valor de pH entre 4 y 7 puede mejorar la suceptibilidad de la celulosa a las enzimas, disminuye la cristalinidad de la celulosa, disminuye la asociación de la celulosa con la lignina y evita la formación de la degradación de los monosacáridos a furfurales e hidroximetilfurfurales que interfieren en el proceso de hidrólisis enzimática y en el proceso fermentativo31.
Caracterización morfológica de la cascarilla de arroz
El análisis por microscopia de barrido electrónico de la epidermis interna de la cascarilla de arroz sin pretatratamiento presentó una superficie lisa, cerosa y brillosa, acorde con lo planteado por Zou y Yang2, donde la lignina y la hemicelulosa mantienen unidas a las fibras de celulosa (figura 3a); el pretratamiento con T10-Alc presentó una superficie muy rasgada con parcial desintegración de la fibra debido a la remoción de la lignina y la hemicelulosa similar a lo reportado por Brígida et al.24 (figura 3b), el pretratamiento con T9-Ac presentó una superficie rasgada, donde se ha removido la capa cerosa de ácidos grasos y se observa la formación de fosas donde se ha removido la pared celular (figura 3c), en el pretratamiento T10-S se observó que el silicato proveniente de la solución del pretratamiento forma una película sobre la superficie de la cascarilla de arroz que evita el ataque del peróxido sobre la fibra (figura 3d).
Hidrolisis enzimática
Los sustratos obtenidos de los pretratamiento seleccionados, T10-Alc, T9-Ac y T10-S fueron hidrolizados enzimáticamente con 0, 0,1, 0,2 y 0,3 mL de enzima Cellic Ctec2 por gramo de cascarilla de arroz, utilizando buffer acetato de sodio 50 mM, pH de 5, 50º C y 72 h de hidrólisis. En la figura 4 se observa que la mayor concentración de azúcares reductores a las 72 h de hidrólisis, se logra cuando se trabajó con la cascarilla proveniente del pretratamiento T10-Alc (H2O2 15 % v/v, pH de11, 70 °C y 3 h de incubación para 10 % de sustrato).
Mediante las comparaciones múltiples de LSD-Fisher se analizó los tratamientos enzimáticos que provenían de los pretratamientos T10-Alc, T9-Ac y T10-S, presentando diferencia significativa (p<0,05) solo para el pretratamiento alcalino-peróxido en relación a los otros tratamientos.
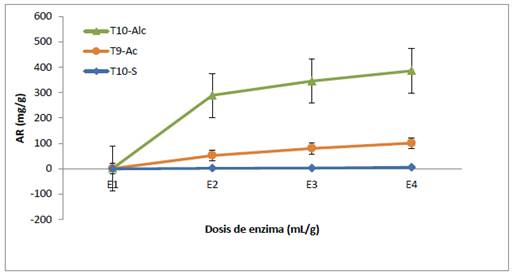
Figura 4. Azúcares reductores (mg/g) en la hidrólisis enzimática (dosis de enzima E1: 0, E2: 0,1, E3: 0,2 y E4: 0,3 mL/g Ctec2, 50 mM de buffer acetato de sodio, pH de 5, 50 ºC por 72 h, carga 5 % p/v) de los pretratamientos T10-Alc (H2O2 15 % v/v, pH de 11, 70 °C por 3 h, carga 10 % p/v), T9-Ac (H2O2 15 % v/v, pH de 2,6, 70 °C por 3 h, carga 10 % p/v) y T10-S (H2O2 15 % v/v, pH 7,5, 70 °C por 3 h, carga 10 % p/v).
La concentración de azúcares reductores en mg/g proveniente del pretratamiento T10-Alc (6 % KOH - 15 % H2O2, 70°C, 3 h y carga del 10 % p/v) e hidrólisis enzimática (pH de 5, 50 °C por 72 h, 0,3 mL/g, con una carga 5% p/v) alcanza valores de 399,9 mg/g, este valor es superior a 60 mg/g cuando se trabajó con pretratamiento alcalino (0% v/v H 2O2, pH de 11,5, 35 °C por 24 h) e hidrólisis enzimática (pH de 5, 45 °C por 72 h, 0,4 mL/g, con una carga 5% p/v) y de 260 mg/g de azúcares reductores cuando se trabajó con pretratamiento peróxido alcalino (7,5 % v/v H2O2, pH de 11,5, 35 °C por 24 h) e hidrólisis enzimática (pH de 5, 45 °C por 72 h, 0,4 mL/g, con una carga 5 % p/v) reportado por Saha y Cotta 17. Se obseva que en presencia del peróxido y alta temperatura en el pretratamiento se obtiene mayor cantidad de azúcares reductores, estas relaciones también lo reporta Saha y Cotta30.
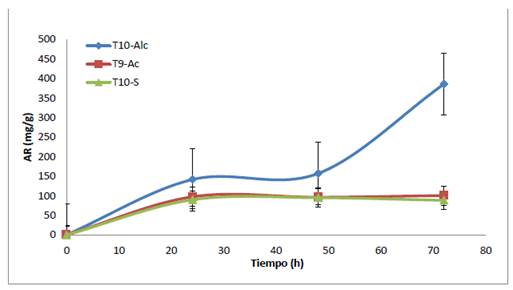
En la figura 5 se observa mayor concentración de azúcares reductores a mayor tiempo de incubación de hidrólisis enzimática para el pretratamiento T10-Alc, semejante resultado reportó Saha y Cotta30 al obtener un máximo rendimiento de azúcares, trabajando bajo las condiciones mencionadas anteriormente y con una dosis de 0,12 mL/g de enzima, variando los tiempos de incubación de 3 h a 120 h, obteniendo 190 mg/g y 353 mg/g de AR, respectivamente; aún así, estos valores reportados no llegan a superar el valor hallado en el presente trabajo de 399,88 mg/g, teniendo como desventaja el largo tiempo de incubación pero eficientes al usar una menor concentración de enzima.
Porcentaje de sacarificación
Para obtener el porcentaje de sacarificación se aplicó la Ec. (1), que relaciona el contenido de azúcares reductores en el hidrolizado enzimáticos y la concentración potencial de azúcar del sustrato con o sin pretratamiento. El contenido potencial de azúcares (celulosa y hemicelulosa) en la cascarilla de arroz fue de 54,75 % valor similar a lo reportado por Yu et al.23, este valor se obtuvo de la diferencia entre la masa total y el contenido de lignina 18,02 %, la humedad 8,78 % y cenizas 18,45 %, como se observa en la tabla 2.
Tabla 2 Composición química de la cascarilla de arroz.
| Componente | Contenido (%) |
| Lignina | 18,02 ± 0,87 |
| Humedad | 8,78 ± 0,41 |
| Cenizas | 18,45 ± 0,38 |
| Celulosa+ Hemicelulosa | 54,75 ± 0,01 |
Nota: Resultados ± desviación estándar para dos muestras por triplicado
Los mejores resultados encontrados fue para el pretratamiento T10-Alc (6% KOH - 15% H2O2, 70°C, 3 h y carga del 10 % p/v) e hidrólisis enzimática (pH de 5, 50 °C por 72 h, 0,3 mL/g, con una carga 5 % p/v) que alcanzó una sacarificiación de 73,2 %, este resultado es similar a 73 % reporatado por Saha y Cotta17 (7,50 % v/v H2O2, pH de 11,5, 35 °C; 24 h, con carga de 15 % p/v), e hidrólisis enzimática (pH de 5, 45 °C, 72 h, 0,12 mL/g y carga de 10 % p/v), utilizando una mezcla de enzimas cellulasa, β-glucosidasa y xylanasa, cuando se utiliza cascarilla de arroz como sustrato.
CONCLUSIONES
El pretratamiento alcalino-peróxido, tiene mayor efecto en el acceso de las enzimas celulasas, ß-glucosidasas y xilanasas en la cascarilla de arroz facilitando la sacarificación de la celulosa y hemicelulosa, en azúcares reductores que podrían ser fermentados en el proceso de obtención de etanol 2G. Sin embargo, el uso de diversos medios puede tener un impacto en el gasto energético del proceso.