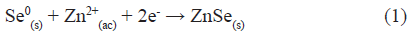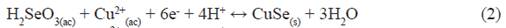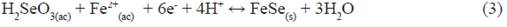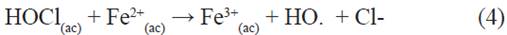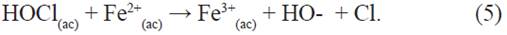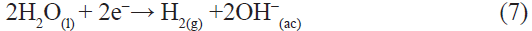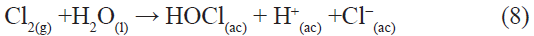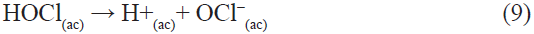INTRODUCCIÓN
En el pasado, los sistemas de saneamiento municipal para el tratamiento de efluentes de industria textil eran efectivos para eliminar los colorantes insolubles en agua. Sin embargo, con el uso creciente de colorantes solubles en agua, los tratamientos biológicos convencionales no logran la eliminación adecuada de estos compuestos1.
La fotocatálisis heterogénea es un proceso capaz de reducir la concentración de contaminantes orgánicos hasta un nivel donde no representen una amenaza al sistema biótico donde llegan los efluentes acuosos e inclusive es posible la mineralización ya que es un proceso no selectivo, lo que permite que contaminantes no biodegradables puedan ser tratados dentro de aguas residuales en las que aparecen muchos compuestos orgánicos2. Por otra parte, el tratamiento por oxidación electroquímica es una tecnología emergente utilizada para la eliminación de contaminantes orgánicos e inorgánicos del agua y aguas residuales por oxidación directa o indirecta. Para el primer caso, en un proceso de oxidación anódica directa, los contaminantes se adsorben primero en la superficie del ánodo y luego se destruyen por la reacción de transferencia de electrones anódica. Luego, en el segundo caso, en un proceso de oxidación indirecta, los oxidantes fuertes como el HClO/Cl2, O3 y H2O2 se generan electroquímicamente, consecuentemente los contaminantes se destruyen en el bulk de la solución por reacción de oxidación por la especie generada en el electrodo. Asimismo, todos los oxidantes se generan in situ y se utilizan inmediatamente3. La eficiencia fotocatalítica se puede mejorar aplicando un potencial electroquímico a un fotocatalizador. El proceso denominado fotoelectrocatálisis conduce a una mejor separación de los portadores de carga, lo que conduce a una foto- oxidación mejorada de los compuestos orgánicos4.
Dicho esto, esta investigación se realizó con el propósito de plantear un método alternativo para descontaminar aguas de colorantes orgánicos mediante la unión de dos técnicas: fotocatálisis y electrocatálisis. Consiguientemente, películas delgadas de materiales fotoactivos depositados sobre sustratos conductores son materiales muy prácticos y relativamente baratos de reproducir, fueron usadas como catalizadores aprovechando las propiedades ópticas del semiconductor seleniuro de zinc, y con la ayuda de un potencial eléctrico para la generación de especies activas de cloro, potenciadas con la presencia del ion cloruro en el medio, para promover una degradación eficiente.
PARTE EXPERIMENTAL
Electrodeposición
Para la electrodeposición de todas las películas se utilizó un sistema de tres electrodos, figura 1A. Como sustrato FTO (óxido de estaño dopado con flúor) electrodo de trabajo de dimensiones 2 cm x 3,5 cm, como contraelectrodo se utilizó un alambre de platino de dimensiones 4 cm x 1 mm y como electrodo de referencia Ag/AgCl (KCl 3,5 M), se trabajó a una temperatura de 70°C y a un de pH controlado de 2,5.
Se trabajó con un potenciostato Autolab PGSTAT 204, primero se realizó la voltametría cíclica para obtener el potencial de deposición adecuado y luego utilizando la cronoamperometría se realizó la electrodeposición. Los voltagramas mostrados se trabajaron a pH de 2,5 con una velocidad de barrido de 50 mV/s excepto donde se muestra con condiciones diferentes.
Se realizó una limpieza química a los sustratos para tener una superficie homogénea que permita la formación de la película sobre la superficie del FTO, primero se sumergió en un baño de HCl y lejía (1/1 v/v) por 10 min, así también, se limpió con detergente caliente lavándolo con agua destilada y por último se llevó las películas a un baño con isopropanol y etanol 1/1 en ultrasonido.
Los reactivos empleados en la síntesis y sus concentraciones trabajadas fueron: ZnSO4.7H2O (Parmeac, 50 mmol L-1), FeSO4.7H2O, SeO2, KCl y polivinilpirrolidona PVP (Aldrich Sigma, 10, 1, 100 mmol L-1 y 4 g L-1), CuSO4.5H2O, anaranjado de metilo (Riedel-de Haen, 1, 0,05 mmol L-1), H2SO4 (Fermont, 98 % (m/m)). Todos de grado PA.
La solución de trabajo consistió en un baño con solución precursora de zinc, ZnSO4, y SeO2, regulando el pH a 2,5 con ácido sulfúrico, también se añadió PVP para mejorar la homogeneidad de las películas. Por otro lado, para sintetizar las películas ZnSe-Fe y ZnSe- Cu, a la solución de trabajo inicial se añadieron los iones Fe2+ y Cu2+ respectivamente, en forma de sales. Todas las soluciones fueron preparadas con agua ultrapura (18MΩ) y se controló la temperatura con un termostato a 70 °C.
Para la película de ZnSe, se determinó primero el potencial de deposición de sus especies precursoras Zn2+ y Se4+, de manera independiente y luego juntas, bajo las condiciones de trabajo mediante voltametría cíclica. Luego el ZnSe se depositó por cronoamperometría con el potencial determinado anteriormente, la electrodeposición para este caso fue de 60 min a un potencial de -0,8 V. Seguidamente, para las películas modificadas con iones Fe2+ y Cu2+, se realizó la electrodeposición por cronoamperometría con los potenciales de -0,8 V y -0,7 V para hierro y cobre, respectivamente, debido a que estas daban las mejores eficiencias catalíticas, para un tiempo de deposición de 60 min.
Caracterización
Las películas fueron caracterizadas tal como fueron obtenidas del baño químico, sin tratamiento previo, Se caracterizó por UV-Vis DRS en el rango de 200 a 800 nm en un equipo CARY 60 Agilent Technologies con accesorio de esfera integradora. Se caracterizó por espectroscopia Raman desde el rango de 150 a 900 cm-1 en un equipo Horiba Scientific con láser de 532 nm. Se caracterizó por XRD con un equipo X´pert MPD Philips, equipado con una fuente de Cu Kα (λ = 1.5418 Å), con ángulo de barrido (2θ) desde 20 a 80°. Para realizar la técnica SEM se utilizaron dos equipos SEM EVO MA 10 Zeiss Oxford 20 mm y XMAX SU8230 Hitach con un rango desde 2,5 um hasta de 200 nm. Para realizar la técnica EDS se usó el equipo EVO MA 10 acoplado al microscopio electrónico.
Fotoelectrocatálisis
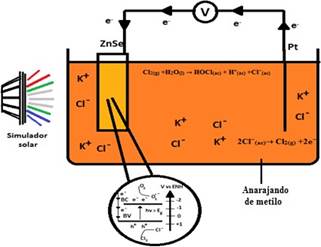
Las pruebas de electrocatálisis y fotoelectrocatálisis fueron realizadas con la técnica de cronoamperometría a potencial constante -1 V, la concentración de anaranjado de metilo fue constante = 5x10-5 mol L-1, además los ensayos fueron realizados a temperatura ambiente 298 K. Se hicieron pruebas de degradación para el colorante anaranjado de metilo utilizando el sistema de la figura 1B, y se utilizó KCl 0.1 mol L-1 como electrolito soporte. No se modificó el pH para ningún caso.
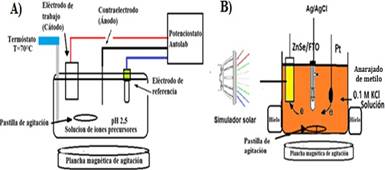
Figura 1 A) Diagrama del sistema tres electrodos utilizados en la electrodeposición. B) Diagrama esquemático del sistema para la decoloración de AM.
Se retiraron alícuotas cada cierto tiempo, se hicieron barridos de 220 a 600 nm y se midieron las absorbancias a 465 nm a diferentes tiempos, para finalmente compararse los rendimientos catalíticos de las diferentes películas a temperatura ambiente. Se utilizaron dos focos simuladores: uno que emite radiación en todo el espectro visible con una potencia de 300 W al cual llamaremos luz visible y el segundo un foco LED color azul con potencia de 40 W al cual llamaremos luz azul, además para la luz visible se tuvo que utilizar un sistema de refrigeración para no alterar la temperatura de la catálisis y que los resultados sean los más homogéneos posibles.
RESULTADOS Y DISCUSIÓN
Voltametría cíclica
En la figura 2 se presenta el mecanismo para la formación de la película, primero el óxido de selenio reacciona con el agua para formar el ácido selenioso H2SeO3, luego este en presencia del ácido se reduce para formar selenio metálico, que se deposita como sólido rojizo-naranja, por último, este reacciona con el zinc presente en el baño acuoso para formar seleniuro de zinc5 a -0,8V, (ec. 1), como una película delgada que presenta una coloración amarillo- naranja.
El zinc se logró reducir a -0,8 V, con un potencial de reducción menor al -1,2 V encontrado en la figura 2, este potencial más positivo6 se debe a la energía ganada en la formación del ZnSe, cuando en el baño de deposición está presente el selenio. A este potencial se le conoce como potencial de co-deposición.
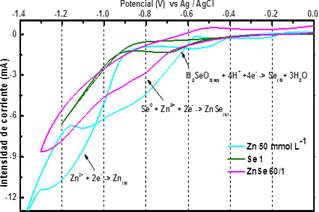
Figura 2 Voltametría cíclica Zn = 50 mmol L-1, T = 70 °C, Se = 1 mmol L-1, T = 23 °C y Zn/Se 60/1 mmol L-1, T = 70 °C.
Así también, el pH desempeñaba un papel fundamental debido a que pH mayores de 2,5 favorecía la reducción de zinc hasta la formación de zinc metálico y desfavorecía la reducción de selenio, sin embargo, a pH menores de 2,5 la deposición de selenio se veía muy favorecida, depositándose una gruesa película de selenio rojo, en cuanto al zinc este no tiende a depositarse7 sobre el electrodo a pH menores a 2,5.
Las soluciones fueron purgadas con nitrógeno gaseoso para evitar la formación de óxidos metálicos. Se proponen las siguientes reacciones cuando se agregan los metales al sistema hibrido7.
En la figura 3A, se puede notar el pico de reducción de cobre a -0,43 V de Cu2+ a Cu+. La reacción propuesta es el número 2 a -0,85V, aproximadamente, dándose la reducción de cobre formando el seleniuro correspondiente, y a su vez se forma la película de ZnSe a -0,8V. En la figura 3B, no se aprecian los picos de reducción del hierro como en el caso del cobre, ya que es de muy baja intensidad de corriente. La formación de la película donde se ve un desplazamiento positivo a -0,68 V, reduciendo el hierro y formando el compuesto FeSe dentro de la película de ZnSe, como mostrado en la ec. 3. La inserción en la figura 3B, corresponde a la voltametría cíclica de la especie Fe2+ bajo las condiciones de deposición, se puede notar dos picos de reducción de Fe2+ a Fe+ y Fe2+ a Fe. Además, experimentalmente se vio la deposición de una ligera capa de hierro metálico, con todo lo anterior expuesto queda demostrado que el hierro se reduce sobre la película.
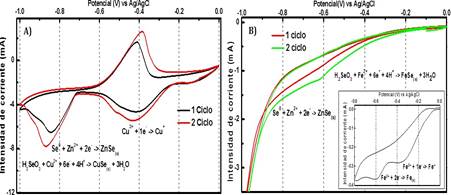
Figura 3 Voltametría cíclica A) Cu = 1 mmol L-1, Se = 1 mmol L-1, Zn = 50 mmol L-1, purgado con N , T = 70 °C B) Fe = 10 mmol L-1, Se = 1 mmol L-1, Zn = 50 mmol L-1, purgado con 2(g)N2(g), velocidad de barrido = 25 mV s-1, T = 70 °C. La inserción en la figura B corresponde a la voltametría cíclica Fe = 5 mmol L-1, T = 70 °C, purgado con N .2(g)
La película de ZnSe presenta un máximo de absorción a aproximadamente a 546 nm <> 2,27 eV. En el caso del sistema híbrido ZnSe-Fe, se observa un pico de absorción a 544nm <> 2,28 eV, aproximadamente, no se observa un cambio aparente en la longitud de onda debido a la baja presencia del Fe2+ en el sistema híbrido. Por último, en el sistema híbrido ZnSe-Cu, se puede observar un pico a aproximadamente 595 nm <> 2,08 eV, que correspondería al máximo de absorción de la película.
Se hizo un estudio superficial de las películas delgadas de ZnSe, ZnSe-Fe y ZnSe-Cu por microscopía electrónica de barrido, los resultados se muestran en la figura 4. Las cuales indican que las partículas tienden a ser esféricas, especialmente en el caso del sistema híbrido ZnSe y ZnSe-Fe, las cuales presentan un tamaño promedio de 400 nm y 300 nm, aproximadamente, y en el caso del sistema híbrido ZnSe-Cu también se presentan nanopartículas cuasiesféricas que presentan un tamaño de 450 nm, aproximadamente. El tamaño promedio de las películas está un poco mayor a lo hallado en la literatura 100-200 nm8, esto posiblemente a la adición del surfactante PVP y la mayor concentración de zinc
Se analizaron las películas delgadas por EDS, los porcentajes mostrados están en relación a la masa relativa del elemento. En la película de ZnSe, se encontró la presencia de selenio (24,3 %) así como una pequeña fracción de zinc (1,7 %), lo cual nos sugiere una relación estequiométrica de ZnSe de 1/14,3. Luego, para la película de ZnSe-Fe se pudo notar, de igual modo, la presencia excesiva de selenio (32,9 %) y una pequeña fracción de zinc (3,9 %) la cual genera una relación estequiométrica Zn/Se de 1/17,3 pero no se encontró la presencia de hierro. Por último, en la película de ZnSe-Cu, se encontró la presencia de cobre (12,9%), selenio (25 %) y zinc (5,6 %) haciendo el mismo cálculo, como en los casos anteriores, obtenemos una relación estequiométrica de Zn/Se/Cu 1/4,5/2,3, esto nos da a entender que el cobre se deposita de una manera más efectiva que el hierro.
En la figura 5A se muestran los espectros Raman de las películas sintetizadas. Se puede observar el pico característico del selenio trigonal9 a 230 cm-1, mientras que el pico a 251 cm-1 corresponde al modo de estiramiento A1 de la fase de selenio amorfo9, esto da como evidencia que hay fases de selenio que no han reaccionado con el zinc, sin embargo, el pico de ZnSe no se puede visualizar debido a que el límite de detección del equipo no permite distinguir el pico del selenio trigonal. En la película de ZnSe-Fe, se observa el pico característico del ZnSe a 236 cm-1 y además el pico a 183 cm-1 corresponde al modo de vibración del Se-Se10. De manera similar en la película de ZnSe-Cu, se puede apreciar el pico del ZnSe a 239 cm-1, esta vibración es característica del ZnSe8 y es el fonón tipo longitudinal óptico, esta vibración varía entre 234 cm-1 hasta 239 cm-1 dependiendo del tamaño de las partículas, entonces se puede afirmar que, para el caso de los dopajes con Fe y Cu, las fases de selenio elemental están en menor cantidad y no son detectables por esta técnica.
En la figura 5B, se muestran los difractogramas de las películas de FTO, ZnSe, ZnSe-Fe y ZnSe-Cu. Para la primera película de ZnSe, se muestran dos planos, el primero a un ángulo de 27,4° pertenece al plano (111) y el ángulo 44,8° se aproxima al plano (220) de la película de ZnSe10. Además, en la película de ZnSe-Fe se tiene un pico a un ángulo a 34,8° que podría ser el plano característico (111) del FeSe11, asimismo se encontró la presencia de una banda a 27,4° que sería del plano (111) de ZnSe y una banda de baja intensidad a 44,5° que correspondería al plano (220) del ZnSe.
Finalmente, para ZnSe-Cu, la banda a 27,4° del plano (111) se presentó con muy baja intensidad, pero el pico característico a 44,7° del plano (220) del ZnSe, fue más intenso. La distancia interplanar fue calculada por la ley de Bragg para los ángulos 27,4°, 34,8° y 44,8° dando como resultados 3,25 Å, 2,02 Å y 2,58 Å, respectivamente.
Los demás picos de gran amplitud son debidos al sustrato FTO marcados con un asterisco.
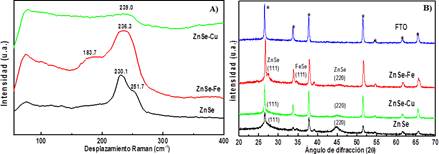
Figura 5 A) Espectro Raman de las películas sintetizadas ZnSe, ZnSe-Fe y ZnSe-Cu B) Patrones de difracción de rayos X para las películas sintetizadas.
La alta proporción de selenio presente en la película se debe al método de síntesis, cuando depositamos el seleniuro de zinc se necesita primero el selenio (0) precursor que se obtiene a partir del ácido selenioso, entonces este paso es determinante en la síntesis porque dependiendo de cuanto selenio pase a reaccionar con el zinc se formará una fase donde la relación estequiométrica de zinc y selenio sean 1/1, aunque esto parece no ocurrir en el sistema hibrido de ZnSe-Cu, donde por cada mol de selenio está presente una mol de zinc y una mol de cobre, al parecer la reacción con cobre sería más efectiva que con zinc y forme una nueva fase. Y en el caso del sistema híbrido de ZnSe-Fe no puede ser detectado hierro por esta técnica. Se puede concluir que por espectroscopía Raman, DRX y EDS se mostró la presencia en exceso de selenio elemental.
Fotoelectrodegradación del anaranjado de metilo
En la figura 6, se observa la actividad electrocatalítica de todas las películas. Se aprecia que el sistema híbrido de ZnSe-Fe no es tan efectivo, mientras que con cobre aumentó en comparación con la película de ZnSe-Fe. Se resalta que la película de ZnSe es la que presenta mayor rendimiento electrocatalítico, alcanzando una decoloración de 96,5 % en 45 min de catálisis. Las diferencias entre los rendimientos catalíticos se deben principalmente a las conductividades de las películas, esto determina la cantidad de corriente en la superficie del electrodo.
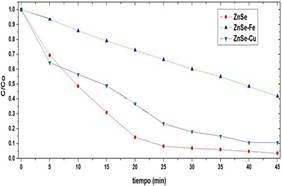
Figura 6 Electrodegradación de AM con diferentes catalizadores, KCl = 0,1 mol L-1, AM = 5x10-5 mol L-1, potencial aplicado = -1V.
En la figura 7 se muestran la fotoelectrodegradación del AM, con irradiación luz azul en la figura 7A. Para el caso de los dopante de Fe2+ y Cu2+ se mostró rendimientos similares, esto debido al factor de fotocatálisis y que las películas absorben en esta región del espectro visible. Finalmente, para la película de ZnSe se obtuvo el mejor rendimiento catalítico, reduciendo el tiempo de decoloración hasta 35 min. Además, para el caso de la película de ZnSe-Cu, se observa una reducción notoria en la región UV el espectro de absorción del AM, lo que podría sugerir una menor presencia de productos intermediarios que absorben en esta región. En este caso, se esperaba que con la presencia de los metales dopantes se mejoraría, sin embargo, la baja intensidad de esta fuente de irradiación, así como la baja cristalinidad del semiconductor (mostrado en la figura 5B) y la menor conductividad de las películas podrían reducir su eficiencia en la fotoelectrocatálisis.
Con el fin de mejorar la eficiencia catalítica se cambió de fuente de irradiación para una más potente de 40 W a 300 W. En la figura 7B se muestran los rendimientos de todas las películas por fotoelectrocatálisis, se puede apreciar que el sistema híbrido ZnSe-Cu es el que decolora totalmente al anaranjado de metilo en 25 min, seguidos del sistema híbrido ZnSe-Fe y ZnSe donde decoloran totalmente al contaminante, donde el primero muestra un ligero aumento en su eficiencia respecto al segundo.
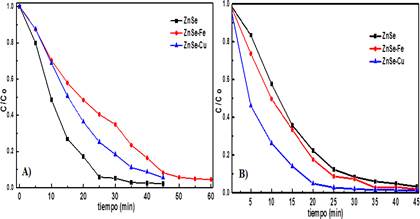
Figura 7 Electrofotodegradación de AM con diferentes catalizadores, A) luz azul B) luz visible, KCl = 0,1 mol L-1, AM = 5x10-5 mol L-1, potencial aplicado = -1V.
Este notorio aumento en el caso del ZnSe-Cu y menos notable en el caso de ZnSe-Fe, se debe al factor fotocatalítico, donde al haber mayor potencia de la fuente y en todo el espectro visible, habrá una tendencia de los portadores de carga a saltar de la banda de valencia a la banda de conducción. Además, cabe mencionar que para la degradación de AM con la película de ZnSe-Fe, el espectro de AM en la región UV, (no mostrado), presentó baja intensidad, lo que sugiere menor presencia de productos en esta región. Así también, la electrocatálisis podría disminuir el tiempo de recombinación, lo que aumenta la catálisis mostrando el beneficio de asociar ambos procesos para aumentar la eficiencia catalítica.
Este buen desempeño catalítico podría comprobarse con análisis de carbono orgánico total, que podría sugerir la mineralización del colorante. Este aumento, cuando se asocian ambos procesos, podría deberse a una menor recombinación de portadores de cargas debido al dopaje de la estructura de bandas del ZnSe, así como una menor saturación de sitios activos. Además, también se podría producir una reacción tipo-Fenton, ec. 4 y 5, entre el Fe de la película y el hipoclorito en solución12.
Esta asociación positiva de procesos se debería a que el cobre al tener mayor cantidad de electrones varía la energía de banda prohibida a una de menor energía λmax = 595 nm <> 2,08 eV que es favorable en el momento de realizar una fotocatálisis. Así también, el cobre actuaría como una trampa de electrones disminuyendo el fenómeno de la recombinación13. Asimismo, se sabe que el cobre es un ion que presenta actividad Fenton, lo que contribuiría con la reacción tipo Fenton al igual que el caso anterior. El semiconductor ZnSe es de naturaleza intrínseca, y por tanto la cantidad de portadores de carga que puedan estar en la superficie será muy pobre. Sin embargo, al modificar la película con metales de transición se favorece la creación de nuevos defectos, así como nuevos estados de energía donde puedan darse los saltos electrónicos para generar una corriente de portadores de carga.
En la figura 8, se propone un mecanismo para la generación de radicales debido a la fotoexcitación de electrones de la banda de valencia hacia la banda de conducción en la película de ZnSe, donde al recibir un fotón, de mayor energía que el band gap óptico λmax= 546 nm, se promueve el movimiento de portadores de carga de modo que sea posible la generación de radicales O2-.. Al analizar el nivel de bandas del semiconductor ZnSe, el nivel de valencia no sería lo suficientemente oxidante para generar radicales hidroxilos, E° = 2,73 V, donde E° es el potencial estándar de reducción, más sí lo suficiente como para oxidar al ion cloruro, E° = 1,36 V, por lo que se podría sugerir que, en la banda de valencia, termodinámicamente sería más favorable la generación de cloro en vez de la generación de radicales hidroxilos.
Así también, la película funcionó como cátodo, donde se favorecería el transporte de electrones hacia su superficie, flujo de electrones del ánodo hacia el cátodo, aportando más electrones a la banda de valencia que fueron perdidos en la fotocatálisis. Este aumento de electrones en la superficie del catalizador, podría ser corroborado por medición de fotocorriente en presencia de los dos simuladores, lo cual podría ser sugerido para un trabajo futuro. Cabe resaltar que ninguna de las películas sufrió algún proceso ni de fotocorrosión ni electrocorrosión, lo que aumenta el potencial de las películas para su posterior aplicación y reutilización.
La actividad electrocatalítica está dada por las ecuaciones 6, 7, 8 y 9. El ion cloruro está presente en gran cantidad en la solución y es debido a este, que especies cloradas pueden reaccionar con el colorante degradando el enlace azo y de este modo decolorándolo. Se produce la electrogeneración de las especies OH- y Cl con el colorante anaranjado de metilo. [3] los cuales reaccionan directamente
En el ánodo: (platino)
En el cátodo: (FTO potencial -1V)
Mientras que en bulk de la solución:
A su vez, debido a la fotocatálisis, se generan los radicales HO. que podrían tener una oxidación indirecta a su vez, actuando en el mecanismo paso a paso generando especies activas de cloro14, ácido hipocloroso e iones hipoclorito, dióxido de cloro, clorato, perclorato, etc.
CONCLUSIONES
Se consiguió la electrodeposición de películas delgadas de ZnSe modificadas con hierro y cobre mediante la técnica de electrodeposición, con presencia del precursor de selenio (0). Se obtuvieron micropartículas de forma cuasiesféricas de aproximadamente 300 - 500 nm. Así también la presencia de hierro se comprobó por el plano del seleniuro de hierro y cobre mediante los análisis de los voltagramas, y el espectro de EDS.
Se consiguió mejorar la degradación de anaranjado de metilo, llegando a una decoloración total en un tiempo de 25 min y una eficiencia de 99 % de degradación con el proceso de fotoelectrocatálisis.
Este aumento se debió a factores como menor recombinación de portadores de carga debido a la modificación de bandas por metales de transición y el flujo de electrones del ánodo.