INTRODUCCIÓN
El estudio de varias especies de La familia Verbenaceae han permitido evidenciar su utilidad en la medicina tradicional en malestares del aparato digestivo, aparato reproductor femenino, sistema músculo esquelético y nosologías dependientes de la cultura1 como antioxidantes, esto debido a compuestos fenólicos contenidos en especies como Aloysia citriodora Palau, esta especie contiene un alto porcentaje de fenólico y estos componentes, generalmente poseen una mayor actividad antioxidante2, por otro lado, se ha logrado identificar mediante cromatogramas provenientes de la infusión de las hojas un perfil de polifenoles caracterizados por la presencia de ácido cafeico y flavonoides3, los extractos alcohólicos y acuosos poseen actividad antiinflamatoria, atribuida a la presencia de theviridosido, un glucósido iridoide, además, otro componente común en la familia VERBENACEAE, la actividad analgésica se debe a la presencia de verbascósido y en cuanto a la actividad antipirética, el extracto acuoso es ligeramente superior al del paracetamol4.
Como agentes antimicrobianos y antimicóticos, los aceites esenciales y extractos de plantas han formado las bases de muchas aplicaciones, que van desde la preservación, procesados de carne hasta productos farmacéuticos, es así como el aceite esencial de tomillo no solo actúa como agente antibacteriano si no también minimiza la oxidación de lípidos además de mejorar sus características sensoriales incluso mejorando la salubridad del producto hasta por dos semanas en almacenamiento refrigerado5, además, otros estudios demuestran la amplia actividad antimicrobiana de especies de la familia VERBENÁCEA, como es el caso del aceite esencial de la Aloysia triphylla mostrando efectos sobre el trypanosoma cruzi siendo un tratamiento alternativo frente a los escasos fármacos para su tratamiento6. Estudios realizados en Venezuela muestran el amplio espectro antibacteriano contra patógenos genito- urinarios y hacen notable su uso con bajas dosis6 y el aceite de la Aloysia gratissima es un antibacteriano efectivo contra Staphylococcus aureus y M. luteos e incluso mostró actividad antiedematogena con un gran porcentaje de inhibición de la inflamación siendo esto último aplicado de manera tópica7 también muestra actividad antimicrobiana contra Escherichia coli y Bacillus subtillis8.
En cuanto a la composición de los aceites la identificación de los analitos se apoya en el uso de la cromatografía gases acoplada a espectrometría de masas9, la detección en la Aloysia Triphylla da como componentes principales como 1,8-cineol (12,4%), geranial (9,9%), 6-metil-5-hepten-2-ona (7,4%) y neral (6,9%) analizado por CG-EM10, por otro lado, para la Aloysia gratissima se logró identificar también metabolitos secundarios de la clase de terpenos, un total de 14 componentes y siendo los principales componentes identificados isopinocamphone (trans -3-pinanona) (25.4%), limoneno (15.1%) y guaiol (12.7%)11.
Finalmente, la presente investigación tiene por objetivo, extraer y caracterizar al aceite esencial de la Aloysia aloysioides Loes & Moldenke y evaluar la actividad antibacteriana; además, este estudio será un aporte a la flora peruana ya que no hay ningún estudio fitoquímico de esta planta.
PARTE EXPERIMENTAL
Material vegetal
La muestra en estudio de Aloysia aloysioides Loes & Moldenke (ver figura 1), fueron recolectadas en junio de 2019 en el distrito de Tintay provincia de Aymaraes, Abancay (Perú).
Identificación de la muestra
La identificación botánica se realizó en el Museo de Historia Natural de la Universidad Nacional Mayor de San Marcos, por el Mg. Asunción Cano Echevarría, quien nos proporcionó el nombre científico como Aloysia aloysioides Loes & Moldenke (constancia N° 124-USM-2019).
Extracción del aceite esencial
La muestra fue sometida a una destilación, por el método de arrastre de vapor de agua, usando 673 gramos, durante 2 horas, usando un equipo semiindustrial de acero inoxidable de 20 litros de capacidad. El aceite esencial obtenido se secó con sulfato de sodio anhidro.
Cromatografía de gases (CG)
fue realizado con un cromatógrafo de Agilent ® Technologies 7890A GC-System equipado con una columna capilar DB5-MS, 30mx0.25 nm i. d., con film de Polidimetil Siloxane (J & W LTM Column module) de un espesor de 0,25 μm. La temperatura inicial de la columna es de 60ºC durante 5 minutos, aumentando de 60ºC a 200ºC, con una rampa de aumento de temperatura de 4ºC/min, en la siguiente rampa de temperatura aumenta de 200ºC hasta los 280ºC con una rampa de crecimiento de 10ºC/min; la temperatura final se mantiene constante durante 35 minutos. La temperatura del inyector es de 250ºC, el detector se encuentra a una temperatura de 180ºC. El gas de arrastre es Helio con un caudal de 1 mL/min, el volumen de inyección de la muestra es de 1μL.
Cromatografía de gases acoplada a espectrometría de masas (CG-EM)
realizado en un detector acoplado al cromatógrafo, corresponde a un Agilent ® Technologies 5975C, Inert XL MSD con detector Triple-Axis, operando en las condiciones indicadas anteriormente, con un voltaje de ionización de 70 eV y con la fuente iónica a una temperatura de 230ºC. A análisis se realiza aproximadamente en 110 min.
Análisis de los resultados
se realizó con el software Chemstation para el análisis de las áreas obtenidas para los varios componentes, la identificación de los espectros de masas de cada pico se realiza con las siguientes bases de datos: Nist Mass Spectral Software, y Wiley.
Análisis Microbiológico
Cepas microbianas
Para el ensayo de actividad antimicrobiana se utilizaron 3 cepas bacterianas y una cepa fúngica (hongo). Todas las cepas utilizadas fueron cepas patógenas aisladas de muestras clínicas humanas proporcionadas por el laboratorio de Microbiología de la Facultad de Farmacia y Bioquímica - UNMSM. Las cepas bacterianas fueron Escherichia coli y Pseudomonas aeruginosa (Gram negativas) y Staphylococcus aureus (Gram positivo) y Candida albicans (hongo).
Preparación de inóculos y ensayo de actividad antimicrobiana
La técnica utilizada fue difusión en pozo en agar. Se realizó en el laboratorio de Microbiología de la Facultad de Farmacia y Bioquímica, Universidad Nacional Mayor de San Marcos. Los microorganismos almacenados en agar inclinado se cultivaron en agar tripticasa soya (TSA) paras las bacterias y en agar Sabouraud dextrosa para el hongo, se incubaron a 37 ºC x 24 h. Después de este tiempo se realizó la preparación de las suspensiones microbianas en suero fisiológico a 0,5 de escala de McFarland. De cada suspensión microbiana se tomó 50 µL y se mezcló con 20 mL de agar Mueller Hinton licuado estéril a 45 ºC para las bacterias y agar Sabouraud para Candida albicans, luego se pasó a placas Petri estéril, se dejó solidificar y se realizó 3 pozos de 6 mm de diámetro en cada placa utilizando un sacabocados estéril. En un pozo de las placas se colocó 100 µg de la muestra (crema), en el segundo pozo se colocó 50 µL (25 µg/mL) de solución gentamicina (control +) para las bacterias y fluconazol (control +) para Candida albicans y en el tercer pozo se colocó 50 µL de suero fisiológico (control -). Las placas de fueron incubadas a 37 ºC entre 24 a 48h en este tiempo se verificó la presencia de los halos de inhibición alrededor de los pozos. En las placas con presencia de halos de inhibición se midieron el diámetro de los halos en milímetros (mm). Los ensayos para la muestra se realizaron por duplicado12,13.
RESULTADOS Y DISCUSION
Se obtuvo un aceite de olor cítrico con leve color amarillo, con un rendimiento de 0,38 %, respecto al material muestra inicial, la índice refracción del aceite esencial fue 1,477 y la densidad promedio fue de 0,8525 g/ml.
Análisis espectroscópico
Espectroscopía infrarroja
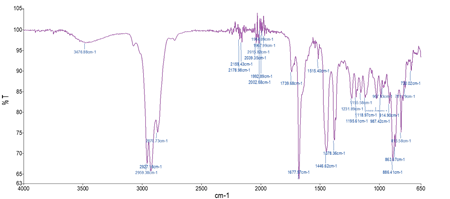
En la figura 2, se muestra el espectro FT-IR del aceite esencial de Aloysia aloysiodes Loes & Moldenke, que permitirá identificar los grupos funcionales contenidos en los componentes químicos del aceite esencial
En la Tabla N° 1 se muestran los componentes identificados mediante espectroscopia IR, tales como los dimetilos terminales presentes en el citral, la α-tujona y la 6-metil-5-hepten-2-ona. El estiramiento del enlace C=O en 1739 y 1677 cm-1 es característico del grupo carbonilo y evaluado junto con la torsión C―H que se aprecia a 1378 cm-1, indican la presencia de aldehídos, posiblemente con enlace C=C en su cadena principal debido al pico en 1677 cm-1; esto coincide con la estructura del citral, este compuesto está presente en el aceite esencial de cedrón. Además, se pueden observar picos de absorción a 1446 cm-1, característicos de torsión de tijeras de radicales metilenos (-CH2-) de compuestos cíclicos pequeños (C5-C8). Así mismo, hay picos de absorción en 2959 y 1446 cm-1, que corresponden a grupos metileno terminales (=CH2), como los hallados en la molécula del limoneno o el espatulenol. Los picos de absorción en 1195 y 1118 cm-1 son indicio de la presencia de alcoholes secundarios y terciarios debido al estiramiento del enlace C-OH14. Además, se observa que alrededor de 2000 cm-1, hay varios picos pequeños, el cual nos indica que el aceite esencial tiene aromáticos.
Tabla 2 Bandas de absorción del espectro infrarrojo del aceite esencial de “Lima-Lima”.
| Bandas cm-1 | Grupo funcional | Observaciones |
| 3476 | O-H | Una banda de tensión O-H enlazado a un aromático |
| 2959 | -CH3 | Doblete debido a las vibraciones de tensión asimétricaysimétrica del C-H independiente de la molécula |
| 2959-2870 | ‒CH3, ‒CH2‒ | Vibración de alargamiento de enlaces C - H característico de compuestos orgánicos.Valor es útil para determinar la hibridación del átomo de carbono, corresponde a carbono sp3 (alcano o posibles grupos alquilo) |
| 2870 | ‒CH2‒ | Vibraciones simétricas del átomo de hidrógeno,independiente del tamaño de la molécula. |
| 1738 | (C=O) | Vibración de alargamiento del carbonilo (C=O) valor característico de aldehídos y cetonas. |
| 1446 | CH2‒ | Flexión de carbono - hidrógeno. |
| 1446 | ‒CH3 | Característico del grupo metilo. |
| 1378 | ‒CH3, ‒CH2‒ | Característico del isopropil (dos grupos metilo en el mismo carbono) |
| 1364 | ‒CH3 | Alcano, metilo - geminal. |
| 987 | Alifáticos | Bandas muy débiles con difícil designación. |
| 914 -967 | Alifáticos | Bandas muy débiles con difícil designación. |
| 815 -840 | =C‒H | Alquenos, hidrocarburos aromáticos. |
| 730 -781 | C‒H | Debido a vibraciones del carbono - hidrógeno |
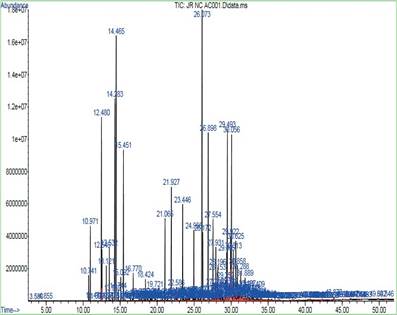
La identificación de los componentes presentes en el aceite esencial mediante CG-EM, se realizó comparando los tiempos de retención y los espectros de masas mediante búsqueda computarizada en la librería con las siguientes bases de datos: Nist Mass Spectral Software, y Wiley. En la figura 3, tenemos el cromatograma del aceite esencial.
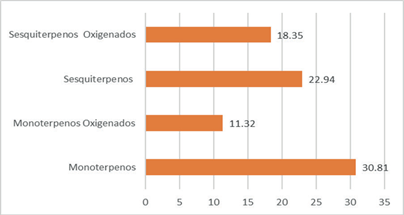
Respecto de composición, de los treinta componentes identificados, el 30,81% monoterpenos, monoterpenos oxigenados de 11,32 %, sesquiterpenos 22,94 % y finalmente con un 18,35% de sesquiterpenos oxigenados estos mostrados en la figura 3. Los componentes mayoritarios identificados fueron: β-Cariofileno (10,88 %), limonelo (9,9 %), p-cimeno (7,22%), Oxido de cariofileno (5,98 %), Nerolidol (4,96 %) y α-humuleno (4,92 %). Este aceite guarda estrecha relación con el aceite esencial De Aloysia thyphylla siendo esta de la misma familia estudiada en Argentina el β-Cariofileno (3,3%) y otra en Venezuela, β-Cariofileno (2,1 %).
Tabla 3 La composición del aceite esencial de Lima-Lima.
| Componente | Abundancia % | RT | Fórmula global |
|---|---|---|---|
| β-Cariofileno | 10,88 | 26,07 | C15H24 |
| limonelo | 9,49 | 14,46 | C10H16 |
| p-cimeno | 7,22 | 14,28 | C10H14 |
| Oxido de cariofileno | 5,98 | 30,06 | C15H24O |
| Sabineno | 5,61 | 12,48 | C10H16 |
| Nerolidol | 4,96 | 29,49 | C15H26O |
| α-humuleno | 4,92 | 26,9 | C15H24 |
| Y-terpineno | 3,8 | 15,45 | C10H16 |
| Citral | 3,67 | 21,93 | C10H16O |
| Gemacreno D | 2,22 | 27,33 | C15H24 |
| Espatulenol | 2,14 | 29,92 | C15H24O |
| neral | 2,29 | 21,06 | C10H16O |
| Acetato de Mirtenilo | 2,31 | 23,45 | C12H18O2 |
| α-pineno | 1,72 | 10,97 | C10H16 |
| α-felandreno | 1,18 | 13,53 | C10H16 |
| β -pineno | 1,05 | 12,55 | C10H16 |
| Acetato de Geranilo | 1,62 | 24,96 | C12H20O2 |
| α-Chamigreno | 1,72 | 26,1 | C15H24 |
| Biciclogermacreno | 1,31 | 27,55 | C15H24 |
| Germacreno B | 1,2 | 29,39 | C15H24 |
| Guaiol | 1,24 | 30,18 | C15H26O |
| Oxido Humuleno | 1,59 | 30,37 | C15H24O |
| Endo-1-bourbananol | 0,94 | 30,51 | C15H26O |
| Cadinol Isomero | 0,83 | 31,29 | C15H26O |
| β-Mirceno | 0,74 | 13,12 | C10H16 |
| Hidrato de Sesquisabineno | 0,67 | 29,14 | C15H26O |
| Butirato de Geranilo | 0,82 | 28,11 | C14H24O2 |
| β-Bisaboleno | 0,69 | 28,15 | C15H24 |
| Linelool | 0,61 | 16,77 | C10H18O |
| otros componentes (>0,5%) | 17,1 | ||
| TOTAL | 99,9 |
El componente mayoritario es el beta-Cariofileno, con casi 11 % del aceite esencial, además, se verificó la presencia del limoneno, se concluyó que este componente de la planta es el que le proporciona al aceite de lima-lima un sabor y olor agradable, pues su contenido es importante, aunque menor al beta-Cariofileno. Como se puede apreciar la figura 4, el contenido de Sesquiterpenos y Monoterpenos presentes en el aceite de esencial de lima- lima expresado en porcentajes, cuya diferencia entre ambos componentes es del 7.87%, que hace notable la cantidad elevada de Sesquiterpenos presentes en la Aloysia peruviana y la distingue de otras especies Aloysias reportadas en estudios previos.
Evaluación de la actividad antibacteriana
En la tabla 4 se evidencia que para la muestra existe halo de inhibición solo para Staphylococcus aureus, no existe halos de inhibición para Escherichia coli, Pseudomonas aeruginosa y Candida albicans. Se concluye que el aceite esencial tiene actividad antimicrobiana contra Staphylococcus aureus (Gram positivo) pero no tiene ninguna actividad antimicrobiana contra Escherichia coli y Pseudomonas aeruginosa (Gram negativos) y Candida albicans (hongo). Es preciso indicar que, la muestra fue enfrentada a las cepas clínicas, los cuales son diferentes a las cepas estándar (ATCC). Las cepas clínicas pueden ser mucho más resistentes a comparación de las cepas estándar, pero realizar el ensayo con cepas clínicas se acercan a la realidad si se tiene previsto aplicar el aceite en algún producto.
De acuerdo con los valores obtenidos se observa que el aceite esencial de Aloysia aloysioides Loes & Moldenke no presentó actividad que otras especies de Aloysia de su misma familia, ya que diversos estudios indican que si son bioactivos frente a Candida albicans, Pseudomonas aeruginosa y Escherichia coli(Demo et. al, 2005 y Duarte et. al, 2007). Esta diferencia se puede atribuir a variación en la composición química del aceite la ausencia del geranial y el porcentaje mínimo de neral el cual en el caso del aceite esencial de Lima -lima no supera el 3%, también, otro factor a tomar en cuenta es la proporción de Monoterpenos y Sesquiterpenos es muy cercana no mayor al 7,87 %, finalmente esta composición podría estar influenciada también por las condiciones del medio ambiente donde crece la planta, esto fue demostrado en estudios previos en otras Aloysias.
Tabla 4 Actividad antibacteriana del aceite esencial de
| Microorganismos | Diámetro de halos de inhibición (mm) | ||||
|---|---|---|---|---|---|
| Fluconazol (control +) | Gentamicina (control +) | Suero fisiológico (Control -) | Muestra 1 | Muestra 2 | |
| Escherichia coli | --- | 30 | 0 | 0 | 0 |
| Pseudomonas aeruginosa | --- | 25 | 0 | 0 | 0 |
| Staphylococcus aureus | --- | 26 | 0 | 19 | 19 |
| Candida albicans | 23 | --- | 0 | 0 | 0 |
CONCLUSIONES
El aceite esencial de Aloysia aloysioides Loes & Moldenke, obtenido por el método de destilación por arrastre con vapor de agua, posee un rendimiento RAE% de 0,38%. El análisis fisicoquímico del aceite esencial, nos revela que es un líquido de color ligeramente amarillento, olor cítrico herbáceo, sabor ligeramente dulce y cítrico, soluble en alcohol al 96%, el índice de refracción es 1,4798, la densidad de 0,8561 g/mL.
Se han identificado y cuantificado 208 compuestos empleando la Cromatografía de Gases acoplada a Espectrometría de Masas (CG-EM) en la muestra de aceite esencial de A. aloysioides Loes & Moldenke, de estos, 6 son los compuestos mayoritarios, estos son: β-Cariofileno (10,88 %), limonelo (9,9 %), p-cimeno (7,22%), Oxido de cariofileno (5,98 %), Nerolidol (4,96 %) y α-humuleno (4,92 %).
Este aceite esencial es una fuente de sustancias con actividad antibacteriana que podría ser usado en preparaciones farmacéuticas y aplicaciones en la Industria Alimentaria para el tratamiento de infecciones causadas por Staphylococcus aureus. Por otro lado, este es el primer reporte de actividad antibacteriana del aceite esencial de A. aloysioides Loes & Moldenke contra patógenos.