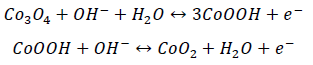INTRODUCCIÓN
El avance en el desarrollo de sistemas de almacenamiento de energía abre la puerta al aprovechamiento de diversas fuentes de energía renovable como alternativa a la dependencia de combustibles fósiles. En este contexto, los sistemas de almacenamiento electroquímico, que incluyen baterías, supercapacitores (SCs), celdas de combustible y celdas electroquímicas 1, se destacan por su capacidad para almacenar y liberar energía mediante procesos de carga y descarga eléctrica. La eficacia de los procesos electroquímicos depende en gran medida del tipo de electrodos utilizados, lo que hace imperativo desarrollar electrodos que cumplan con requisitos específicos como: una alta difusión iónica, estabilidad química frente a ciclos de carga y descarga, capacidad de almacenamiento iónico, elevada conductividad y transferencia de electrones 2. En los SCs, su eficiencia está influenciada por múltiples factores, en donde destacan el comportamiento electroquímico de sus electrodos, las propiedades del electrolito y la ventana de potencial de los electrodos. La optimización de estos factores se convierte en una necesidad para mejorar tanto el transporte electrónico como la difusión iónica en estos sistemas 3. En los últimos años, el desarrollo de electrodos para supercapacitores ha centrado su atención en materiales altamente porosos, ya que proporcionan sitios activos propicios para diversas reacciones químicas y mejoran el transporte de iones en la superficie, lo que, a su vez, mejora la difusión del electrolito 4. Entre estos materiales, los metal-organic frameworks (MOFs) se destacan como una de las clases de materiales porosos más relevantes en la actualidad debido a su abundancia de sitios activos, la capacidad de ajustar sus distribuciones de poros y la posibilidad de controlar sus morfologías 5. No obstante, los MOFs en su forma bulk presentan limitaciones, como una baja conductividad eléctrica, la presencia de microporos inaccesibles para el electrolito y, por lo tanto, una baja difusión iónica. Con el fin de mejorar sus propiedades electroquímicas, se han empleado los MOFs como precursores o como soportes para desarrollar materiales carbonosos, óxidos metálicos y compósitos de diversos tipos 6. Tratamientos térmicos, como la pirólisis, permiten obtener materiales porosos derivados de los MOFs controlando la temperatura y las tasas de calentamiento, manteniendo la alta porosidad y estructura del material 7. De manera similar, los clústeres metálicos presentes en los MOFs pueden transformarse durante el tratamiento térmico, generando nanopartículas metálicas y/u óxidos metálicos dispersos en todo el material carbonoso 8. Un tipo de MOF de gran interés son las redes zeolíticas de imidazol, conocidas como zeolitic imidazolate frameworks (ZIFs). En particular, el ZIF-67, que se basa en iones metálicos de cobalto (Co2+) y el ligando orgánico 2-metilimidazol, los cuales en coordinación forman clústeres poliédricos con estructura cúbica 9. Su uso está orientado principalmente a la generación de óxidos de cobalto porosos; por ejemplo, Saraf et al. realizaron un tratamiento de calcinación simple al ZIF-67 para obtener nanopartículas de Co3O4 con una capacitancia específica de 190 F g-1 y elevada retención de la capacitancia (71 % luego de 5000 ciclos) 10. La combinación de tratamientos térmicos para el ZIF-67 puede permitir sintetizar derivados con propiedades particulares, por ejemplo, el tratamiento térmico en atmósfera inerte permite la obtención de carbones oxidados con capacitancias específicas de 332,3 mF cm211. La versatilidad del uso de ZIF-67 como precursor de óxidos de cobalto es tan amplia, que se han sintetizado Co3O4 en matrices de celulosa combinadas con NTC para el desarrollo de materiales con excelente transferencia electrónica y capacitancia específica de 665 mF cm212. Además, la optimización de los parámetros de calcinación permite la preparación de óxidos porosos con estructuras dodecaédricas como los sintetizados por Zhang et al. que exhiben capacitancias específicas de hasta 1100 F g-1, y retienen su capacitancia específica en un 95 % luego de 6000 ciclos de carga-descarga 13, siendo una estrategia prometedora para la obtención de materiales mixtos de óxidos con matrices carbonosas altamente eficientes en supercapacitores. En este trabajo, se analizaron las propiedades del ZIF-67 y los óxidos de cobalto obtenidos mediante su tratamiento térmico, con el objetivo de evaluar su viabilidad como electrodos en supercapacitores híbridos.
PARTE EXPERIMENTAL
Síntesis de ZIF-67 a temperatura ambiente
Se disolvieron 436,5 mg de Co(NO3)2•6H2O (SigmaAldrich, 98%) en 10 mL de solución (1:1 metanol (SigmaAldrich, 99,9%)/etanol (SigmaAldrich, 99,5%)) y 494,7 mg de 2- metilimidazol (SigmaAldrich, 99%) en 10 mL de solución (1:1 metanol/etanol), ambas soluciones se mezclaron bajo agitación vigorosa por 5 min, la mezcla se mantuvo en reposo por 24 h a temperatura ambiente. Luego, los cristales obtenidos se lavaron por triplicado con etanol y luego se secaron a 80 °C por 6 h 14.
Obtención de óxidos de cobalto
Los parámetros elegidos para el calentamiento del ZIF-67 fueron temperatura, tiempo y rampa de calentamiento, siendo de 350 y 450 °C por 1, 2 y 3 h usando rampas de 1 y 5°C min-1; respectivamente 10,13,14. Basado en los 3 parámetros elegidos para la optimización de calcinación de ZIF-67, se realizó la matriz de experimentos mostrada en la .
Preparación de electrodos modificados
Para el estudio electroquímico de los materiales obtenidos fue necesario modificar electrodos de carbón vítreo (GCE) con los óxidos obtenidos de la calcinación de ZIF-67 siguiendo tres etapas: inicialmente se realizó la preparación de la tinta de óxidos de cobalto con 2 mg del material que se dispersó en 400 µL de H2O ultrapura, 100 µL de isopropanol y 20 µL de Nafion (5 % m/v) por 10 min en ultrasonido; posteriormente se realizó la limpieza del GCE a través del pulido por 20 min en alúmina de 0,3 y 0,05 µm. Finalmente, se agregaron 10 µL de la tinta en alícuotas de 5 µL al GCE, usando una lámpara IR para el secado.
Tabla 1 Matriz de experimentos modificando los parámetros para la calcinación de ZIF-67.
| Codificación | Tiempo / h | Temperatura / °C | Rampa / °C min-1 |
| CoO-1 | 1 | 350 | 1 |
| CoO-2 | 1 | 350 | 5 |
| CoO-3 | 1 | 450 | 1 |
| CoO-4 | 1 | 450 | 5 |
| CoO-5 | 2 | 350 | 1 |
| CoO-6 | 2 | 350 | 5 |
| CoO-7 | 2 | 450 | 1 |
| CoO-8 | 2 | 450 | 5 |
| CoO-9 | 3 | 350 | 1 |
| CoO-10 | 3 | 350 | 5 |
| CoO-11 | 3 | 450 | 1 |
| CoO-12 | 3 | 450 | 5 |
Caracterización fisicoquímica y estructural
La identificación de los grupos funcionales se realizó a través de los espectros infrarrojos por transformada de Fourier (FTIR), medidos a temperatura ambiente entre 650 y 4000 cm-1 con la técnica de ATR, usando un espectrofotómetro IR Shimadzu, complementados también con la técnica de espectroscopía Raman (Zplora, HORIBA Scientific) con una intensidad de láser de 532 nm. Los patrones de difracción de rayos X (DRX) fueron realizados a temperatura ambiente en un difractómetro D8 Advance (Bruker, USA) usando radiación de CuKα (λ = 1,54059 Å). Comparativamente los patrones de difracción fueron simulados por el programa VESTA utilizando las estructuras de ZIF-67 (COD N°7236367) y Co3O4 (COD N° 9005898). La morfología de los cristales preparados fue observada por microscopía electrónica de barrido (SEM) usando un microscopio electrónico HITACHI Japón, SU8230.
Estudios electroquímicos
Todos los estudios electroquímicos se realizaron en un potenciostato (μAutolab tipo III, Autolab/Eco chemie) usando una celda de 3 electrodos, con alambre de platino como contraelectrodo, electrodo de Hg/HgO/NaOH (3 mol L-1) comercial como electrodo de referencia, y un electrodo de carbón vitreo (GCE) como electrodo de trabajo. Las técnicas de voltamperometría cíclica (CV) y curvas galvanostáticas de carga y descarga (GCD) se realizaron para evaluar las diferentes propiedades electroquímicas del electrodo modificado en medio alcalino de 1 mol L-1 de KOH.
RESULTADOS Y DISCUSIÓN
Caracterización fisicoquímica y estructural de ZIF-67 y óxidos derivados
La síntesis del ZIF-67 genera cristales fucsias precipitados en la solución. Luego de la calcinación del material se observó la formación de un polvo negro-grisáceo con puntos brillantes que dependen de las condiciones de síntesis. La espectroscopía IR del ZIF-67 permitió evaluar la coordinación de los ligandos orgánicos con los iones metálicos como se observa en la Figura 1a. El pico a 2929 cm-1 es asociado a las vibraciones del C-H alifático (grupo CH3), mientras que el pico ubicado a 997 cm-1 corresponde a las vibraciones de estiramiento del Co-N 15, relacionado a la coordinación del cobalto con el ligando 2-metilimidazol. Las otras bandas corresponden a las vibraciones de la red cristalina del ZIF-67 y el ligando 2-metilimidazol. Complementariamente, los patrones de difracción para el ZIF-67 (Figura 1b) muestran las mismas fases cristalinas que los patrones simulados para el ZIF-67, confirmando la síntesis del material, siendo el pico ubicado a 7,25 ° el de mayor intensidad relacionado al plano cristalino (011) 16.

Figura 1 a) Espectro IR del ZIF-67 (inserto: estructura molecular del ZIF-67), b) Comparación de los difractogramas del ZIF-67 obtenido experimentalmente y simulado, c) Espectro Raman del CoO-1 derivado de la calcinación del ZIF-67 (inserto: diagrama estructural del Co3O4), d) Comparación de los difractogramas del Co3O4 obtenido experimentalmente y simulado.
La naturaleza del óxido de cobalto (CoO-1) obtenido a las condiciones de 350 °C por 1 h con rampa de 1 °C min-1 se estudió con espectroscopia Raman (Figura 1c) en la cual se identifican 5 bandas a 183, 470, 510, 608 y 678 cm-1. Estos picos activos en Raman generalmente se relacionan a la estructura de espinela típica del Co3O4, la cual tiene una conformación del tipo: 𝐶𝑜2+(𝐶𝑜3+)2𝑂2− 4 (con un grupo espacial 𝑂7), con 𝐶𝑜2+ y 𝐶𝑜3+ ubicados en los espacios tetraédricos y octaédricos, respectivamente. Este tipo de espinela tiene una celda primitiva de 14 átomos, y al ser parte del grupo de simetría 𝑂ℎ solo presenta 3 modos activos en Raman: A1g, Eg y F2g17. El modo vibracional a 684,5 cm-1 (A1g) se atribuye a los sitios octaédricos de la estructura, mientras que los modos vibracionales Eg y F2g son atribuidos a las vibraciones combinadas de los sitios octaédricos y tetraédricos 7. La Figura 1.d muestra los patrones de difracción de rayos X para el CoO-1, confirmando la completa transformación del ZIF-67 a una fase pura de Co3O4 luego de la calcinación. Se evidencian los principales picos de difracción ubicados en un ángulo 2θ = 19,0°; 31,3°; 36,8°; 44,8°; 55,7°; 59,4°; 65,2°; 77,3° y 78,4°
correspondientes a los planos de reflexión (111), (220), (311), (400), (422), (511), (440),(533) y (622) del Co3O418.

Figura 2 Imágenes (a) SEM y (b) SEM-EDS, (c-e) imágenes del mapeo elemental EDS de Co, C y N, respectivamente; y (f) Análisis EDS del ZIF-67.
La morfología superficial del ZIF-67 se analizó a través de las imágenes SEM (Figura 2). La Figura 2a muestra que las partículas de ZIF-67 están en un rango de tamaño de 200 -
400 nm. En la Figura 2 b-f se presenta la información elemental de la muestra, evidenciando que los átomos de cobalto están dispuestos en toda la superficie del material al igual que el nitrógeno en una relación Co:N de 0,258, bastante cercana a la relación existente en la fórmula molecular del ZIF-67 (𝐶768𝐻960𝑁384𝐶𝑜96), con una relación teórica Co:N de 0,25 19; la diferencia principalmente se debe a que el análisis EDS se realizó solo sobre una región de la superficie y para obtener información más precisa se requiere analizar diversos puntos del material y calcular el promedio de ellos. En el análisis elemental (Figura 2 f) no se evidencia la presencia de oxígeno, despreciando así la influencia del medio ambiente en los resultados obtenidos y asociando todo el nitrógeno detectado al ZIF-67.

Figura 3 Imágenes (a) SEM y (b) SEM-EDS, (c-e) imágenes del mapeo elemental EDS de Co, O y C, respectivamente; y (f) Análisis EDS del CoO-1.
En la Figura 3 se muestra las imágenes SEM-EDS para el CoO-1. El tamaño de las partículas de CoO-1 se mantiene en el rango de 200 - 400 nm, con una morfología poliédrica. La principal diferencia con el ZIF-67 se evidencia en el análisis elemental (Figura 3f) mostrando un alto contenido de oxígeno (40,3%) con una relación Co:O de 0,45. Para el CoO-1 no se evidencia la presencia de átomos de nitrógeno, lo que se puede relacionar con la degradación del ligando 2-metilimidazol debido a la calcinación. La información obtenida por el análisis SEM-EDS, en conjunto con la presencia de enlaces Co-O (Figura 1c) y la estructura cristalina (Figura 1d), confirman la obtención de óxidos de cobalto (Co3O4) luego de la calcinación del ZIF-67.
Caracterización electroquímica de ZIF-67 y óxidos derivados
A través de la técnica de voltamperometría cíclica se puede estudiar y evaluar el comportamiento electroquímico del ZIF-67 en medio básico, y compararlo con el óxido de cobalto obtenido por su carbonización para así relacionar las condiciones de calcinación con el cambio en las propiedades electroquímicas del material.
La Figura 4 muestra la voltamperometría cíclica para el ZIF-67 (línea negra), para una ventana de potencial de trabajo (0,40 - 0,62 V) la única reacción redox observable es la evolución de oxígeno para potenciales mayores a 0,55 V debido a la oxidación del agua, según:
El comportamiento electroquímico del ZIF-67 para un potencial de 0,40 a 0,55 V indicaría que se trata de un material del tipo doble capa eléctrica (EDCL) el cual utiliza la separación de cargas en las interfaces electroquímicas entre el electrodo y el electrolito20. Bajo estas condiciones, para el ZIF-67 se tiene una capacitancia específica de 39,9 F g-1 (5 mV s-1). La calcinación de ZIF-67 permite la obtención de óxidos de cobalto 21; sin embargo, las características fisicoquímicas y estructurales dependerán directamente del método de síntesis del ZIF-67 y los parámetros de la calcinación (tiempo, temperatura, rampa de calentamiento) para la formación del óxido 10. Para comprender mejor la influencia de los parámetros de calcinación del ZIF-67 en las características y propiedades de los óxidos de cobalto, se realizaron 12 condiciones experimentales diferentes mostradas en la Tabla 1, siendo el CoO-1 el primer material sintetizado, con unas condiciones experimentales de 350 °C por 1 h, con una rampa de 1 °C min-1. En la Figura 4 (línea roja) se muestra la voltamperometría cíclica del CoO-1 y ZIF-67, evidenciando el cambio en el comportamiento electroquímico luego de que el ZIF-67 se ha sometido a calcinación, pues el CoO-1 exhibe una cupla redox cuasireversible (∆ = 60 ). El CoO-1 solo presenta corrientes no faradaicas a potenciales menores de 0,425 V; con un pico de reducción a 0,49 V y de oxidación a 0,50 V (cupla redox) probablemente relacionado con los procesos electroquímicos que realiza el Co3O4 en medio alcalino, descrito en las siguientes reacciones 21:
Por ello, se describe al CoO-1 como un material pseudocapacitivo puesto que presenta un comportamiento en donde el potencial redox del material depende de la superficie recubierta por la especie activa electroquímicamente. Bajo estas condiciones, el material exhibe una capacitancia de 186,3 F g-1 a 10 mV s-1 en 1 mol L-1 KOH, que puede estar relacionada con la porosidad y estructura química estable, permitiendo la adecuada difusión iónica del electrolito 22.
Estudio electroquímico de los óxidos de cobalto obtenidos
La evaluación de los parámetros de síntesis se realizó comparando las capacitancias específicas de los materiales obtenidos. En base a los resultados, se observa que uno de los parámetros más importantes en la calcinación de ZIF-67 es la rampa de calentamiento. La Figura 5, presenta las voltamperometrías para los óxidos de cobalto calcinados a una rampa de calentamiento de 1 y 5 °C min-1 y en la Tabla 2 se aprecia los valores de capacitancia para cada material. La Figura 5a y b muestra que para una rampa de 1 °C min-1, independientemente de la temperatura, un calentamiento lento de calcinación genera materiales con menores capacitancias específicas, siendo el de mayor valor el CoO-1 (186.3 F g-1). Además, al comparar las temperaturas, se observa que temperaturas más altas (450 °C) favorecen la reversibilidad y definición de las reacciones redox presentes en los óxidos de cobalto como se observa en la Figura 5b. Adicionalmente, en la Figura 5c y d se evidencia el fenómeno contrario, pues para una rampa de 5 °C min-1, un tiempo de calcinación más rápido genera materiales con mayor capacitancia específica (relación directamente proporcional), mientras que el aumento de temperatura nuevamente favorece la reversibilidad de los picos redox.

Figura 5 Voltamperometrías cíclicas para óxidos de cobalto en 1 mol L-1 KOH a 10 mV s-1 obtenidos bajo diferentes condiciones: rampa de calentamiento de 1 °C min-1 a una temperatura de a) 350 °C y b) 450 °C. Rampa de calentamiento de 5 °C min-1 a una temperatura de c) 350 °C y d) 450 °C. (Insertos: Capacitancia vs tiempo de calcinación).
Los resultados obtenidos indican que la rampa de calentamiento más rápida (5 °C min-1) tiende a aumentar la capacitancia específica para los materiales CoO-2, CoO-6 y CoO-10 calcinados a 350 °C. La Figura 5c muestra como la capacitancia aumenta acorde al tiempo que se ha sometido el material a esta temperatura, lo cual se relaciona con un mayor tiempo en reacción con el oxígeno ambiental y la posibilidad de que la coordinación entre iones metálicos con el ligando permita la formación/eliminación de diferentes grupos funcionales como óxidos de cobalto dispuestos en toda la red estructural del ZIF 23, mejorando la conductividad eléctrica y características electroquímicas del mismo. Sin embargo, para el caso de 1 °C min-1 a 450 °C se tiene el efecto contrario debido a que un mayor tiempo a esta temperatura tiene un efecto negativo en la capacitancia del material, como se observa para los materiales CoO-3, CoO-7 y CoO-11, debido a que la exposición prolongada a altas temperaturas puede generar el colapso de la red estructural de los óxidos y con ello, pérdida de porosidad disminuyendo así la difusión iónica del electrolito en la superficie y una menor transferencia electrónica en las interfases electrodo/electrolito. En base a la comparativa de capacitancias de los materiales sintetizados (Tabla 2), se tiene que las condiciones óptimas de calcinación son de 1 h a 350 °C con rampa de 1 °C min-1 obteniendo materiales de 186,3 F g-1 (CoO-1).
Tabla 2 Comparativa de capacitancias específicas para los diferentes óxidos de cobalto derivados de ZIF-67.
| Material | Capacitancia específica (F g-1) |
| ZIF-67 | 165,3 |
| CoO-1 | 186,3 |
| CoO-2 | 51,1 |
| CoO-3 | 131,7 |
| CoO-4 | 30,6 |
| CoO-5 | 104,4 |
| CoO-6 | 111,3 |
| CoO-7 | 76,7 |
| CoO-8 | 29,6 |
| CoO-9 | 110,5 |
| CoO-10 | 152,9 |
| CoO-11 | 20,7 |
| CoO-12 | 40,3 |
Evaluación electroquímica del CoO-1
El estudio de CoO-1 a diferentes velocidades de barrido por la técnica de CV se muestra en la Figura 6a. El desplazamiento de los picos redox con el aumento de la velocidad de barrido se relaciona con la cinética de transferencia electrónica 7, evidenciando que este factor debe ser mejorado para el sistema CoO-1 - GCE posiblemente a través de la incorporación de matrices carbonosas con mayor conductividad eléctrica y porosidad, aumentando así la transferencia electrónica entre electrodo/electrolito.
Las capacitancias específicas para el CoO-1 a diferentes velocidades de barrido, calculadas a partir de la Figura 6a se muestran en la Figura 6b. En comparación con materiales carbonosos, la Figura 6b muestra una dependencia inversamente proporcional de la capacitancia específica con la velocidad de barrido, esto se puede relacionar con los tiempos de contacto entre el electrodo y electrolito. Grandes velocidades de barrido brindan un tiempo pequeño para que el electrolito pueda difundir a los poros del material y realizar los procesos de transferencia electrónica; por ello, generalmente a altas velocidades de barrido se tienen solo procesos eléctricos superficiales (la difusión iónica del electrolito no es relevante), mientras que a bajas velocidades de barrido el tiempo de contacto electrodo-electrolito es mucho mayor, lo cual permite una mejor difusión iónica en la estructura porosa del material aumentando el área de contacto y con ello, la transferencia electrónica mejorando la capacitancia específica 24. La forma decreciente no lineal de la gráfica 𝐶𝑒𝑠𝑝 𝑣𝑠 𝑉 para el óxido CoO-1, generalmente indica un comportamiento pseudocapacitivo con corrientes del tipo mixta (faradaicas y no faradaicas), no cumpliendo con el comportamiento típico lineal de materiales basados en doble capa eléctrica.
Las curvas galvanostáticas de carga-descarga a diferentes densidades de corriente para el CoO-1 en 1 mol L-1 KOH se muestran en la Figura 6c. En todos los materiales podemos ver una meseta entre el potencial de 0,50 a 0,55 V, esto muestra principalmente que el proceso redox asociado es faradaico, implicando una mayor contribución del tipo batería que de doble capa eléctrica (EDLC) en los procesos de almacenamiento de carga 25. El material presenta un valor de 179,5 F g-1 para una densidad de corriente de 2 A g-1, (similar a los 186,3 F g-1 obtenidos a 10 mV s-1 por CV) evidenciando una relación existente entre la capacitancia específica con la densidad de corriente. El material también desarrolla capacitancias de 165; 152 y 140 F g-1 para densidades de corriente de 3, 4 y 5 A g-1, con una diferencia de 39 F g-1 al aumentar la densidad de corriente de 2 a 5 A g-1. La disminución de la capacitancia conforme aumenta la densidad de corriente se debe a que con una mayor entrega de potencia el material necesita menor tiempo para su cargado y con ello, el tiempo de descarga también disminuye. Para una densidad de corriente de 2 A g-1, se tiene un tiempo de carga de 25 s y un tiempo de descarga de 19 s (menor en un 24 %), lo cual puede indicar que el material tiene una carga lenta y una entrega de carga rápida, siendo necesario estudios adicionales para la determinación de la eficiencia

Figura 6 Análisis electroquímico para el CoO-1, a) Voltamperometría cíclica a diferentes velocidades de barrido, b) Gráfico de capacitancia específica vs velocidad de barrido. c) Curvas de carga-descarga a diferentes densidades de corriente. d) Retención de la capacitancia específica después de 50 ciclos. Todos los análisis se realizaron en 1 mol L-1 KOH.
Además, se estudió la estabilidad del material frente a ciclos de carga-descarga consecutivos, realizando 100 ciclos de carga-descarga con un % de retención de la capacitancia de 92 %, a 5 A g-1, como se describe en la Figura 6d. Se requiere un estudio más prolongado para evaluar la estabilidad electroquímica del CoO-1. Sin embargo, la formación de especies secundarias entre el cobalto y el electrolito pueden ser responsables de un decrecimiento de la actividad electroquímica, además de la formación de burbujas de O2 en la superficie de contacto y la estabilidad estructural del material frente a los intercambios iónicos entre el electrolito y los poros del material 26.
CONCLUSIONES
Se realizó la síntesis del ZIF-67 con el método de temperatura ambiente y su calcinación para la obtención de óxidos de cobalto (Co3O4), evaluando parámetros de tiempo, rampa de calentamiento y temperatura, identificando que las condiciones óptimas para la obtención del Co3O4 es de 350 °C por 1 h con una rampa de calentamiento de 1 °C min-1. El análisis estructural y fisicoquímico fue realizado por las técnicas de espectroscopía IR, Raman, difracción de rayos X y SEM-EDS, las cuales confirmaron la formación del ZIF- 67 por la presencia de enlaces Co-N relacionados a la coordinación del Co con el ligando 2-metilimidazol, la estructura cristalina asociada al ZIF-67 con un pico de máxima intensidad asociado al plano (011), además de la formación de cristales poliédricos, respectivamente. Mientras que la presencia de enlaces Co-O, luego de la calcinación del ZIF-67, en conjunto con la estructura cristalina asociada al Co3O4 y el alto contenido de oxígeno (43% en porcentaje atómico) en la superficie del material corrobora la obtención de óxidos de cobalto derivados.
Los óxidos de cobalto bajo las condiciones óptimas de síntesis exhibieron una capacitancia específica de 186,3 F g-1 por voltamperometría cíclica a 10 mV s-1 y de 179,5 F g-1 a 2 A g-1 por curvas de carga-descarga, con un % de retención de capacitancia de 92%, luego de 100 ciclos en 1 mol L-1 KOH. El comportamiento electroquímico del material se atribuye a la buena conductividad eléctrica del material, comportamiento pseudocapacitivo, difusión iónica efectiva del electrolito y estabilidad estructural. Por ello, el óxido de cobalto derivado de la calcinación de ZIF-67 es un potencial candidato para la modificación de matrices carbonosas que aporten estabilidad y soporte estructural, permitiendo así la construcción de materiales híbridos con excelentes propiedades para su uso en supercapacitores.