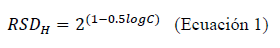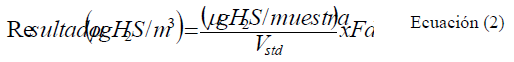INTRODUCCIÓN
La Agencia para Sustancias Tóxicas y el Registro de Enfermedades (ATSDR) explica que el ácido sulfhídrico se forma de manera natural debido a las emisiones de gases de los volcanes o grietas submarinas; se produce debido a la actividad humana, es decir por plantas industriales, plantas petroquímicas, refinerías de petróleo, plantas procesadoras de alimentos, entre otros1. El ácido sulfhídrico (H2S) conocido como sulfuro de hidrógeno o gas de alcantarilla, es un gas tóxico y venenoso, incoloro e inflamable. La presencia del H2S en el aire puede afectar a los seres humanos porque ocasiona la inhibición de la actividad de la enzima citocromo oxidasa, lo cual deriva en problemas asociados a la diabetes, isquemia, e incluso cáncer2,3. El olor típico del H2S está relacionado a sustancias podridas, es posible cuantificar su presencia en concentraciones que van desde los 0.005 a 0.3 ppm (partes de H2S en 1 millón de parte de aire)4. Cuando las concentraciones del H2S sobrepasan los valores mencionados en el ambiente, una persona puede perder la capacidad de identificarlo por el olfato, representando así un mayor peligro en la salud1,4.
Se han reportado investigaciones que evidencian la efectividad del empleo de biopolímeros en diferentes métodos para absorber selectivamente H2S presente en el aire. Uno de los biopolímeros más usados es el quitosano, derivado de la quitina, el cual se obtiene de exoesqueletos de crustáceos. Abu-Hani et al., 2017, desarrollaron films de quitosano con glicerol para ser utilizados como sensores flexibles quimioresistivos para la detección de H2S(g) hasta concentraciones de 1000 ppm5. Se obtuvo el límite de detección de H2S(g) de 15 ppm para un rango de temperaturas entre 20 - 80 °C, así también comprobaron la selectividad del sensor basado en quitosano para la detección de H2S(g) en una mezcla con otros gases como el hidrógeno (H2) y etileno (C2H4). El quitosano también ha sido empleado como matriz biopolimérica, en la cual se han cargado diferentes sustancias que incluyen iones de cobre (II), sulfato de hierro, zeolitas, nanopartículas de oro y plata1,6,7,8. Por ejemplo, los sensores colorimétricos basados en sulfato de hierro y quitosano permitieron la detección de H2S(g) mediante la visualización del cambio de color de amarillo a negro a medida del paso del tiempo de contacto con dicho gas, siendo la respuesta de detección más rápida reportada a los 30 s de exposición
a una concentración de 100 ppm de H S 1 2 (g)
Asimismo, se ha reportado el uso de biopolímeros derivados de algas marrones como el alginato, el cual fue empleado para desarrollar biorreactores que contenían microrganismos sulfuro oxidadoras como las Thiobacillus sp. para la remoción continua hasta 600 ppm de H2S(g) durante un máximo de 240 h9.
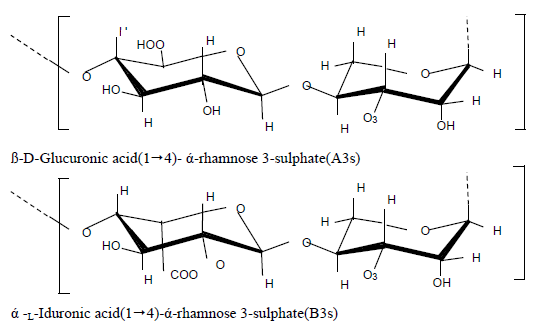
Uno de los biopolímeros que recientemente se encuentra siendo investigado para determinar sus potenciales aplicaciones en el campo biomédico, energético, remediación, entre otros, es el Ulvan10,11,12. A partir de algas verdes del género Ulva sp., se pueden extraer polisacáridos sulfatados conocidos como Ulvan que se componen de ácidos aldobiurónicos del tipo A y B, y la nomenclatura que se les designa es i) A3s= ácido β- D-glucurónico14, unido a α-Lramnosa3-sulfato, ii) B3s= ácido α-L-idurónico está enlazado1,4 al 3-sulfato de α-L-ramnosa.
El presente trabajo tiene como objetivo principal utilizar el polisacárido Ulvan como aditivo en la solución absorbente de H2S(g) a fin de optimizar las condiciones de muestreo y reemplazar a los reactivos convencionales que se suelen emplear para la detección de dicho gas. Los métodos tradicionales para la detección de H2S presente en el aire requieren del uso un tren de muestreo con una solución captadora o absorbente. Esta solución absorbente principalmente contiene sulfato de cadmio (CdSO4), que al entrar en contacto con el H2S(g) produce sulfuro de cadmio (CdS). El uso de CdSO4 puede provocar daños a nivel respiratorio, a la vez que, una constante exposición puede provocar en las personas enfermedades renales, enfermedad a los huesos, incluso enfermedades cancerígenas; sumado al daño que provoca en ecosistema afectando plantas y suelos13. Resulta necesario identificar sustancias no contaminantes que permitan disminuir el uso de CdSO4 en la solución absorbente, pero sin afectar la efectividad de la captación del H2S en el aire. Además, el uso de polisacáridos Ulvan derivados de algas verdes permitirá explotar un recurso que actualmente no se aprovecha para fines tecnológicos relacionados con la captación de contaminantes presentes en el aire.
PARTE EXPERIMENTAL
Reactivos: Materiales de partida
Se empleó arabinogalactano (polímero foto protector) (Sigma-Aldrich), sulfato de cadmio (A.C.S; JT Barker), tiosulfato de sodio anhidro ( ≥98.0%, Merck) , yodato de potasio (traceable to NIST SRM Certipur, Merck), yoduro de potasio (PA, JT Baker), cloruro férrico (PA; JT Baker) y yodo resublimado (PA; JT Baker.); etanol (PA; J. T. Baker), hidróxido de sodio (PA; Merck), ácido clorhídrico (PA; J.T. Baker), almidón (PA, Merck), ácido sulfúrico (PA, J. T. Baker), N.N-Dimetilfenilendiamina dihidrocloruro (A.C.S; Merck), Ulvan, y agua destilada.
Soluciones preparadas
Solución madre de amina: se preparó empleando H2SO4 98% con agua destilada en un ratio 25:15 (v/v) y 9.2 g de N.N-Dimetilfenilendiamina dihidrocloruro.
Solución de trabajo de amina: se elaboró con 60 mL de una mezcla 1:1 (v/v) de H2SO4 98% con agua destilada y 1 mL de la solución madre de amina.
Solución de almidón: se preparó al 0.4 % empleando agua destilada.
Solución de cloruro férrico: se preparó disolviendo 2 g en 25 mL.
Solución de tiosulfato sódico 0.1N: se disolvió 12.6910 g por cada 1 L de agua destilada.
Solución de yodato de potasio: se disolvió 1.5 g por cada 500 mL de agua destilada.
Solución de yodo (0.1N): se disolvió 12.6910 g por cada 1 L de agua destilada que contiene 100 g de solución de yodato de potasio.
Solución madre de sulfuro sódico: se pesó entre 7-7.5 g de sulfuro sódico nonahidratado en 1L de agua destilada.
Soluciones para la curva de calibración de sulfuro de hidrogeno: a partir de la solución madre de sulfuro sódico se preparó la solución stock de sulfuro de hidrogeno de 1022.5 µg H2S/mL. Dicha solución se empleó para obtener diluciones a 102.25 µg H2S mL y luego a 1.0225 µg H2S/mL. Esta última solución fue utilizada para obtener las soluciones estándar, las cuales fueron medidas a 665 nm
en el Espectrofotómetro UV-VIS (Perkin Elmer Lambda 365+) para obtener las absorbancias.
Extracción de polisacáridos Ulvan :
Se emplearon algas verdes comerciales Ulva nematoidea, las cuales fueron identificadas con el manual del Instituto del Mar del Perú - IMARPE (14). Las algas fueron lavadas con abundante agua destilada, secadas en una estufa a 40 °C, trituradas y almacenadas a 4 °C. La obtención de polisacáridos Ulvan a partir de las algas verdes es un método propio, y consistió en los siguientes pasos:
Pre-tratamiento: Por cada 34 g de alga verde seca se empleó 500 mL de etanol y se colocaron con agitación magnética constante (350 rpm) a temperatura ambiente. Luego de 24 h, se descartó el sobrenadante, y el resto de algas fueron secados a 40 °C.
Extracción: las algas obtenidas se trataron con agua destilada en un ratio de 1:35 (w/v) con agitación constante a 80 °C por 6 h. La mezcla obtenida fue centrifugada a 10,000 rpm y el sobrenadante fue recolectado y concentrado a 60 °C hasta la mitad de su volumen.
Precipitación: Los polisacáridos Ulvan fueron precipitados empleando etanol con un ratio de 1:2 (v/v) en un baño de hielo. El precipitado obtenido fue purificado con lavados usando etanol. Luego fueron secados a 40 °C en una estufa y finalmente, triturados y almacenados en un desecador.
Determinación de la concentración de H2S
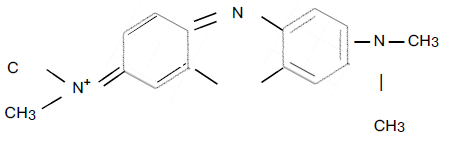
Se siguió la metodología de la COVENIN 3571:2000 Calidad de aire. Determinación de la concentración sulfuro de hidrogeno (H2S(g)) en la atmosfera. En la cual se describe el monitoreo del gas (H2S) en el aire, para lo cual se emplea un tren de muestreo con burbujeadores instalados, las condiciones de muestreo indicados en la norma son 25 °C, 50 mL de solución absorbente y flujo de muestreo 0.2 L/min durante 24 horas. La solución absorbente está compuesta por sulfato de cadmio, hidróxido de sodio y arabinogalactano. El sulfato de cadmio (CdSO4) al entrar en contacto con el H2S (g) produce sulfuro de cadmio (CdS), el cual reacciona con la solución de trabajo de amina, en presencia del cloruro férrico, para formar el Azul de metileno.
La parte de análisis se realiza colorimétricamente a 665nm, construyendo una curva de calibración: Concentración vs Absorbancia utilizando como solución madre el sulfuro sódico. A todas soluciones se le agregó 1 mL de solución de trabajo de amina y 2 gotas de la solución de cloruro férrico, posteriormente se agitó y se esperó 30 minutos para que el color azul de metileno se desarrolle.
Optimización de la solución absorbente
La composición inicial de la solución absorbente está en relación a lo reportado en la norma para la determinación de H2S(g) COVENIN 3571:2000. Se utilizó 4.3 g de sulfato de cadmio, 0.3 g de hidróxido de sodio y 10 g de arabinogalactano para 1 L de agua. De acuerdo a lo expuesto se busca optimizar la solución eliminando el máximo de componentes tóxicos posibles, de tal manera la solución absorbente sea más amigable al medio ambiente. La solución absorbente modificada, contuvo el polisacárido Ulvan en un rango desde 2 - 80 % (wt.).
Para evaluar el rendimiento, se preparó la solución absorbente original y se le realizó la inyección del gas H2S(g) en la concentración 3.51 ug/m3, luego se procedió a preparar la solución absorbente optimizándola, inyectando el gas H2S(g) a la misma concentración, para determinar el porcentaje de rendimiento se dividió el resultado obtenido por la solución absorbente optimizada sobre la solución absorbente original por cien.
Validación del método de ensayo
La NTP-ISO/IEC 17025:201715 en el ítem 7.2.2 Validación de Métodos establece validar los métodos de ensayo normalizados modificados. En el presente trabajo se realiza un cambio en el método, el tiempo de muestreo se fijó en 24 horas, tal cambio lo realizan todos los laboratorios que tienen implementado el método de la COVENIN, es un requisito del protocolo nacional de monitoreo de la calidad ambiental del aire, el cual indica que el gas H2S(g) debe ser muestreado durante 24 horas. Además, se está reemplazando un reactivo en la solución absorbente.
Directriz de Validación
La DA-acr-20D Directriz para la validación de métodos de ensayo, establece los parámetros a ser evaluados en el método de ensayo.
Veracidad: Grado de concordancia existente entre el valor medio obtenido de una gran serie de resultados y un valor aceptado como referencia. [c].
Precisión: Grado de coincidencia existente entre los resultados independientes de un ensayo, obtenidos en condiciones estipuladas. [ISO 5725-1]
Selectividad: La capacidad de un método para determinar con exactitud y e especificidad el analito de interés en la presencia de otros componentes en una matriz de la muestra bajo condiciones indicadas de la prueba16.
Sensibilidad: Es el cambio en la respuesta de un instrumento de medida dividido por el cambio correspondiente en el estímulo16.
Rango: Es el intervalo entre la más alta y la más baja concentración del analito en la muestra, para la cual se ha demostrado que el método analítico tiene un nivel apropiado de precisión, veracidad y linealidad.
Linealidad: Define la capacidad del método para obtener los resultados de la prueba proporcionales a la concentración del analito16.
Límite de detección: La concentración más baja del analito en una muestra que puede ser detectada, pero no necesariamente cuantificable bajo condiciones indicadas de la prueba16.
Límite de cuantificación: La concentración más baja de un analito que se puede determinar con aceptable precisión (repetibilidad) y exactitud bajo condiciones indicadas de la prueba16.
Robustez: Es la capacidad de un procedimiento analítico de no ser afectado por pequeñas, pero deliberadas variaciones en parámetros del método, y proporciona una indicación de su confiabilidad durante su normal uso16.
Incertidumbre: Es un intervalo asociado con un resultado de medida que expresa los valores que razonablemente pueden ser atribuido a la cantidad.
Parámetros de validación evaluados
Para la evaluación de los parámetros de validación fueron 3 analista químicos los que realizaron el ensayo en un número de 10 repeticiones, teniendo un tamaño de muestra total de 30. Como valor de referencia se realizó la inyección del gas H2S a la solución absorbente optimizada en dos concentraciones 3.51 ug/m3 y 13.54 ug/m3,
Los parámetros evaluados fueron:
Veracidad: Se evaluó en dos niveles de concentración para determinar el grado de concordancia existente entre el valor medio obtenido de cada serie de resultados y el valor de referencia.
Precisión: El grado de coincidencia se evaluó con un tamaño de muestra n=30, se expresó como porcentaje de la desviación estándar relativa de repetibilidad (%RSDr), el cual se calculó como la ratio entre la desviación estándar de repetibilidad y el valor promedio de concentración. Además, se calculó desviación estándar relativa de Horwitz mediante la ecuación (1) utilizando la concentración (C) del H2S en ug /m3 detectados.
Linealidad: se emplearon cinco niveles de solución estándar a concentraciones 0.6, 1.5, 3.0, 5.0 y 7.0 µg/muestra, preparados del estándar interno 1022.5 µg H2S/mL. Los resultados fueron analizados a través del coeficiente de correlación y el intercepto usando EXCEL
Rango: Es el intervalo entre la más alta y más baja concentración (cantidades) del analito en la muestra, para la cual se ha demostrado que el método analítico tiene un nivel apropiado de precisión, veracidad y linealidad. [Text on validation of analytical procedure. Ich harmonised Tripartite Guideline].
Límite de detección (LOD) y cuantificación (LDQ): se calcularon a partir de la varianza y desviación estándar, para un n=10, nivel de confianza del 0.05 y un valor del factor de cobertura de 4.
Especificidad: Se determinó comparando el valor esperado (3.51 ug/m3) con una serie de muestras fortificadas en ese mismo valor.
Robustez: la medida de la resistencia del método modificado se evaluó usando ANOVA (p<0.05) para un n=30 y tiempos de detección de 30 min, 60 min y 90 min.
Incertidumbre: este parámetro fue calculado según la metodología declarada en la Guía Eurachem16. En el cual del mesurando, el mesurando es el cálculo o formula que utiliza el método para emitir un resultado, identifica los factores que aportan en ella y va calculando uno por uno el aporte de cada factor.
RESULTADOS Y DISCUSIÓN
La optimización de la solución absorbente consistió en la evaluación del efecto del uso del polisacárido Ulvan en un rango desde 2 - 80 % (wt.) en reemplazo de los reactivos convencionales para la detección de H2S(g).
Primero, se obtuvo que reemplazando el 80 % (wt.) del contenido de reactivos convencionales (CdSO4, NaOH y arabinogalactano) por Ulvan generaba un rendimiento del 40 %, mientras que el uso de Ulvan al 5% permitió alcanzar un rendimiento de 94%. Una vez obtenido el porcentaje de Ulvan adecuado para la solución absorbente, se continuó evaluando la disminución del uso de otros reactivos.
En segundo lugar, se evaluó la disminución del reactivo arabinogalactano en un rango de 0 - 100 % (wt.), manteniendo el porcentaje de Ulvan constante (5 % wt.). Se obtuvo que el rendimiento para un contenido de 100 %, 50 % y 0 % (wt.), fue de 94 %, 92 % y 92 %, respectivamente. Dichos resultados respaldan que la eliminación del reactivo arabinogalactano no cambia significativamente el rendimiento de la solución absorbente. En tercer lugar, se evaluó el efecto de la disminución del contenido de NaOH en la solución absorbente en un rango de 0 - 100 % (wt.), manteniendo el porcentaje de Ulvan constante (5 % wt.). El análisis indicó que para un contenido de 100 %, 50 % y 0 % (wt.) de NaOH, se obtuvo el mismo rendimiento de 92 %, lo cual permitió indicar que el reactivo NaOH no cambia significativamente el rendimiento de la solución absorbente en la concentración evaluada.
Finalmente, se evaluó la disminución de la presencia de CdSO4. Se evaluó el contenido del CdSO4 al 100 %, 95 % y 90 % (wt.), manteniendo el porcentaje de Ulvan constante (5 % wt.). El estudio reveló que el uso de CdSO4 al 100 %, 95 % y 90 % (wt.) permitió alcanzar rendimiento con 92 %, 91 % y 75 %, respectivamente. En esta última etapa, se observó que la disminución del sulfuro de cadmio si afecta el rendimiento de la solución absorbente por tal razón se decidió reducir sólo en un 5 % el CdSO4. Este resultado fue evaluado (n=5) para determinar si es reproducible. Se obtuvo un rendimiento del 91% para dichas repeticiones concluyendo que el uso del Ulvan para la elaboración de soluciones absorbentes de H2S(g) permitió la eliminación total de 2 reactivos de los 3 componentes originales y una disminución del CdSO4. Esto puede estar relacionado a la estructura del Ulvan. Al ser un polisacárido sulfatado, puede interaccionar favorablemente con el H2S(g).
La validación del método con la solución absorbente optimizada (5 % wt. de Ulvan y 95% (wt) de CdSO4,) obtuvo los siguientes resultados:
Primero se evaluó si los conjuntos de datos presentan distribución normal, para ello se utilizó el estadístico Anderson-Darling, el cual evalúa normalidad de acuerdo a la distribución que presentan los datos. Se obtuvo como resultado que los conjuntos de datos presentan una distribución normal pues el p value de cada grupo de resultados es mayor a 0.05. (p value: 0.217, 0.178, 0.178 para el primer nivel y p value: 0.393, 0.447, 0.178 para el segundo nivel) La consistencia de datos se realizó en dos niveles, 3.5 µg H2S/m3 y 13.5 µg H2S/m3, porque de acuerdo al rango de trabajo 2 a 24 ug H2S/m3, dividir en solo 2 niveles es suficiente para demostrar exactitud en los resultados, y se obtuvo un sesgo de 0.667 % y 0.094 %, respectivamente, con un total de 30 repeticiones y a un nivel de significancia α=0.05.
La veracidad de la solución absorbente optimizada se evaluó en los mismos niveles mencionados de µg H2S/m3 y se determinó que los % de recuperación fueron de 100 % y 99 %. Ambos se encuentran dentro del rango de aceptación con un mínimo de 80 % y máximo de 120 %, al 95 % de confianza (Referencia tomada de la AOAC Appendix F: Guidelines for Stndar Method Performance Requirements p,9). A partir de ello, se estableció la veracidad de los resultados.
La precisión fue evaluada utilizando el estadístico de desviación estándar relativa de Horwitz mediante la ecuación (1) para un número de repeticiones de 30 en total entre los 3 analistas. Se determinó la varianza, la desviación estándar, el valor promedio de la concentración de H2S(g), y el el % RSDr. Se definió el criterio de decisión para un RSDr ≤ 0.67* RSDHorwitz para los dos niveles de concentración de 3.5 µg H2S/m3 y 13.5 µg H2S/m3. En ambos rangos los datos son precisos debido a que el %RSD de repetibilidad (1.53 y 0.41, respectivamente) fue menor al %RSD de Horwitz *0.67 (8.87 y 7.24, respectivamente).
En la figura 1 se muestra la curva de calibración de H2S(g), a partir de la cual se obtiene la ecuación de la curva Abs=0.078C + 0.073, donde “Abs” es la absorbancia y “C” es la concentración en µg H2S/mL. Además, se determinó que el coeficiente de determinación (R2) fue superior a 0.995. Dichos resultados confirmaron la linealidad satisfactoria del método modificado con polisacáridos Ulvan.
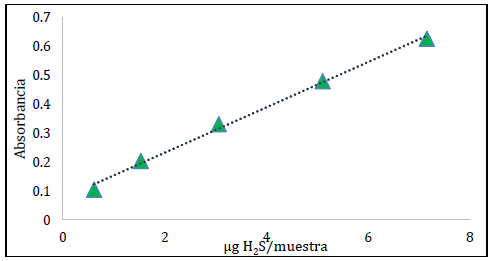
Figura 3 Imagen representativa de la curva de calibración de H2S(g). La ecuación de la curva se define como Abs=0.078C + 0.073, con un R2= 0.996.
El rango de trabajo para el método es 2.1 ug H2S/m3 a 24.7 ug H2S/m3, en este intervalo de concentración se determinó veracidad, precisión y linealidad.
El límite de detección (LOD) y cuantificación (LDQ) de H2S(g) empleando el método con la solución absorbente optimiza con polisacáridos Ulvan se determinaron a un nivel de confianza del 95 %, con 29 grados de libertad y t (de tabla para una cola al 95 % de confianza) de 2,045. Se obtuvo que el valor de LOD y LDQ fue de 0.47 µg/m3 y 1.88 µg/m3, respectivamente.
La especificidad se determinó comparando una seria de 10 resultados con el valor esperado (el valor referencial de 3.5 µg H2S/m3), con el estadístico t-student, el cual nos dio un p-value de 0.447 mayor al 0.05, lo que confirma que hay especificidad en el método.
La robustez del método propuesto se evaluó en función al tiempo de lectura que fue definido en el presente trabajo como el tiempo de reacción del color azul de metileno a 30 min, 60 min y 90 min. La concentración evaluada fue de 13.5 ug H2S/m3. Los datos obtenidos de las concentraciones de H2S(g)/m3 fueron normales y el Análisis de la Varianza (ANOVA) permitió determinar que los grupos de resultados mostrados en la tabla 1 son estadísticamente iguales (p-value ≥ 0.05). Por lo tanto, el método es robusto para el tiempo de desarrollo de color, y se pueden trabajar en cualquiera de los tiempos evaluados sin afectar la reproducibilidad de los resultados.
Tabla 1 Robustez del método propuesto empleando Ulvan en la solución absorbente de H2S(g).
| N° | Condición: Tiempo de reacción (30 min, 60 min y 90 min) del color azul de metileno | ||
| Grupo 1 | Grupo 2 | Grupo 3 | |
| 30 min | 60 min | 90 min | |
| 1 | 13.53 | 13.48 | 13.58 |
| 2 | 13.62 | 13.58 | 13.53 |
| 3 | 13.48 | 13.67 | 13.58 |
| 4 | 13.58 | 13.62 | 13.48 |
| 5 | 13.48 | 13.48 | 13.67 |
| 6 | 13.43 | 13.43 | 13.43 |
| 7 | 13.53 | 13.62 | 13.48 |
| 8 | 13.58 | 13.53 | 13.58 |
| 9 | 13.48 | 13.48 | 13.62 |
| 10 | 13.43 | 13.43 | 13.43 |
La incertidumbre del método se estimó según la metodología de la Guía Eurachem, la cuál parte con la determinación del mesurando (formula con la cual se calcula el resultado), para nuestro método se calcula de la siguiente manera:
Donde:
Resultado (ug H2S /m3): Es el resultado final que indica los microgramos de ácido sulfhídrico por metro cubico de aire.
ug H2S / muestra: Es el resultado que indica los microgramos de ácido sulfhídrico en la solución absorbente y proviene de la curva de calibración preparada con el sulfuro de sodio nonahidratado.
Vstd: Volumen estándar, el cual interviene las condiciones del monitoreo. (Caudal, tiempo, presión, temperatura). El cual bajo condiciones estándar da un resultado de 0.298 Fd: Factor de dilución.
Del mesurando se identifican los factores que contribuyen en el resultado, concentración µg H2S/muestra (que proviene de la curva de calibración, con los estándares), factor de dilución, volumen estándar (presión, temperatura, caudal y tiempo, provienen de las condiciones del muestreo) adicionando el sesgo y la precisión de los analistas (estimados previamente).
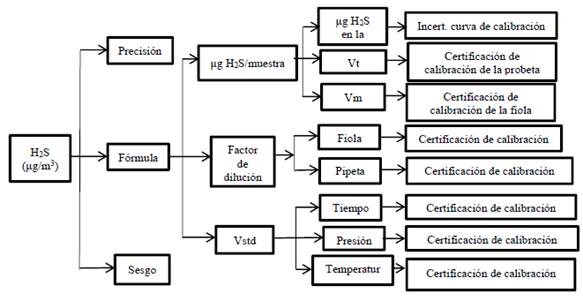
A continuación, se presenta un diagrama de los factores y de donde se obtiene su contribución a la incertidumbre:
La figura 4 indica que la contribución de incertidumbre se obtiene de los certificados de calibración de los materiales utilizados en el método, además del muestreo, la contribución del sesgo se obtiene realizando una gráfica concentración vs sesgo para cada concentración estándar evaluada 3.51 ug/m3 y 13.54 ug/m3, de aquí se obtiene la contribución del sesgo para cada resultado, similarmente para obtener la contribución de la precisión se gráfica concentración vs %RSD para cada concentración estándar evaluada. Sumando todas estas incertidumbres, se obtiene la incertidumbre combinada que al ser multiplicada por el factor de cobertura K (al 95 % de confianza) 1,96, se obtiene la incertidumbre expandida del método.
CONCLUSIONES
El uso de polisacáridos Ulvan para la elaboración de soluciones absorbentes de H2S(g) permitió la eliminación total de 2 reactivos de los 3 componentes originales y una disminución del 5 % (wt.) de CdSO4, uno de los componentes más tóxicos. La validación de la solución absorbente optimizada al 5 % wt. de Ulvan y 95 % (wt) de CdSO4, se llevó a cabo a través de los siguientes parámetros: veracidad, precisión, selectividad, rango de trabajo, linealidad, límite de detección, límite de cuantificación, sensibilidad, robustez e incertidumbre. Se determinaron los porcentajes % de recuperación (100 % y 99 %) se encontraron dentro del rango de aceptación (mínimo de 80 % y máximo de 120 %), lo cual confirmó la veracidad de los resultados. La precisión fue evaluada utilizando el estadístico desviación estándar relativa de Hortwitz para los dos niveles de concentración de 3.5 µg H2S/m3 y 13.5 µg H2S/m3. En ambos se determinó que los datos son precisos porque el %RSD de repetibilidad fue menor al %RSD de Horwitz. Consecuentemente. el método es exacto en ambos niveles evaluados pues la veracidad y la precisión cumplieron sus respectivos criterios.
A partir de la curva de calibración, se comprobó la linealidad satisfactoria del método modificado con polisacáridos Ulvan dado que el coeficiente de determinación (R2) fue superior a 0.995. Los valores límite de detección (LOD) y cuantificación (LDQ) de H2S fueron de 0.47 µg/m3 y 1.88 µg/m3, respectivamente. Las evaluaciones a distintos tiempos de desarrollo del color azul de metileno fueron robustos, y se pueden trabajar en condiciones normales sin afectar la reproducibilidad de los resultados. El método modificado y optimizado con la presencia de polisacáridos Ulvan fue validado de acuerdo a la norma NTP-ISO/IEC 17025, cumpliendo con los parámetros de validación declarados en la directriz de validación. De esta manera, se concluyó que el Ulvan representan una potencial alternativa para aplicaciones en la detección de gases contaminantes como el H2S(g).