Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Scientia Agropecuaria
versión impresa ISSN 2077-9917
Scientia Agropecuaria vol.10 no.3 Trujillo jul./set. 2019
http://dx.doi.org/10.17268/sci.agropecu.2019.03.02
ARTÍCULO ORIGINAL
Identificación morfológica de hongos micotoxigénicos en accesiones de quinua (Chenopodium quinoa Wild.) de la costa y sierra peruana
Morphological identification of mycotoxigenic fungi in accessions of quinoa (Chenopodium quinoa Wild.) of the peruvian coast and sierra
Jeniffer Guarniz-Benites; Jenny Del Carmen Valdez-Arana* ORCID iD: https://orcid.org/0000-0002-9592-6353
Facultad De Industrias Alimentaria, Universidad Nacional Agraria La Molina. Apartado postal 12-056 - Av. La Molina s/n, La Molina, Lima, Perú.
Resumen
El objetivo de la investigación fue identificar mohos micotoxigénicos en acciones de quinua (Chenopodium quinoa Willd.) cultivadas en la Costa (Lima) y la Sierra (Huancayo). El contenido de humedad (9.22-15.89%) y el contenido de saponinas (0,17-1,67%) no mostró diferencias significativas entre las accesiones de Costa y Sierra. La cuantificación de mohos en las accesiones de Costa mostró recuentos altos (75*104-10*104 ufc/g) y bajos en la Sierra (50-150 est. ufc/g), siendo estadísticamente diferentes. Existe una relación lineal negativa entre el contenido de saponinas y el recuento de mohos y levaduras en ambos grupos de accesiones de quinua. Los géneros identificados en Costa incluyen: Cladosporium (40%), Penicillium (30%), Aspergillus (20%) y Trichotecium (10%) y en Sierra: Cladosporium (50%), Penicillium (14%), Talaromyces (14%), Aspergillus (7%), Alternaria (7%) y Oidium (7%). Las aflatoxinas totales para Aspergillus ochraceus (100H53) fue 2,2 ppb y para Aspergillus fumigatus (235H70) fue 1,1-1,6 ppb. La ocratoxina A para Aspergillus ochraceus (100H53) fue de 3,7- 18,1 ppb y para Penicillium verrucosum (53H43 y 53H45) fue de 1,0 y 1,1 ppb respectivamente. Las fumonisinas para Alternaria alternata (100H53) fue 0,2 ppm por lo que todos los mohos mencionados se consideran micotoxigénicos condición que permite establecer condiciones de control y prevención en alimentos.
Palabras clave: quinua; saponina; Aspergillus; Penicillum; micotoxinas.
Abstract
The objective of the research was to identify mycotoxigenic molds in quinoa (Chenopodium quinoa Willd.), Quinoa seeds were sown in the Coast (Lima) and the Sierra (Huancayo). The moisture content (9.22-15.89%) and the content of saponins (0.17- 1.67%) showed no significant differences between the accessions of Costa and Sierra. The quantification of molds in the Costa accessions showed high counts (75*104-10*104 cfu/g) and low counts in the Sierra (50-150 est. cfu/g), being statistically different. There is a negative linear relationship between the content of saponins and the count of molds and yeasts in both groups of accessions of quinoa. The genera identified in Costa include: Cladosporium (40%), Penicillium (30%), Aspergillus (20%) and Trichotecium (10%) and in Sierra: Cladosporium (50%), Penicillium (14%), Talaromyces (14%), Aspergillus (7%), Alternaria (7%) and Oidium (7%). The "total aflatoxins" for Aspergillus ochraceus (100H53) was 2.2 ppb and for Aspergillus fumigatus (235H70) it was 1.1-1.6 ppb. The "ochratoxin A" for Aspergillus ochraceus (100H53) was 3.7-18.1 ppb and for Penicillium verrucosum (53H43 and 53H45) it was 1.0 and 1.1 ppb respectively. The "fumonisins" for Alternaria alternata (100H53) was 0.2 ppm, so all the mentioned molds are considered to be mycotoxigenic conditions that allow to establish conditions of control and prevention in foods.
Keywords: quinoa; saponin; Aspergillus; Penicillum; mycotoxins.
1. Introducción
La quinua (Chenopodium quinoa W.) es considerada por la FAO como uno de los cultivos promisorios para la humanidad, cultivo estratégico para la seguridad y soberanía alimentaria debido a su calidad nutritiva, amplia variabilidad genética en los países andinos, adaptabilidad a condiciones adversas y bajo costo de producción, la creciente demanda en los últimos años ha convertido al Perú en el primer productor y exportador mundial de quinua (Minagri, 2018). Sin embargo, el problema radica en la contaminación de los alimentos agropecuarios, la que pude darse por agentes biológicos (mohos y levaduras), residuos químicos (plaguicidas) y otros contaminantes (metales pesados y toxinas) que pueden superar los límites permitidos y poner en riesgo la salud de quien los consume, representar un obstáculo para el comercio nacional e internacional de los productos. En razón a lo expuesto y con el fin de establecer medidas de control que prevengan el desarrollo de mohos, el objetivo principal de la investigación fue Identificar morfológicamente hongos micotoxigénicos en acciones de quinua, con diferente contenido de saponinas, cultivados en Costa y Sierra del Perú, mediante métodos morfológicos y bioquímicos.
2. Materiales y métodos
Materia prima
Accesiones de quinua (5) provenientes de Lima (12°02′06″S 77°01′07″O): y (8) provenientes de Huancayo (12°04′00″S 75°13′00″O) con diferente contenido de saponinas (Tabla 3).
Programas informáticos:
App Mycelium Touch Versión 1.0, Minitab 17 Versión 3.1 y Software R-project versión 2.12.2.
Métodos de ensayo
Caracterización de las accesiones de quinua:
Determinación del contenido de saponinas: Método espectrofotométrico (Guzmán et al., 2013). Determinación del contenido de humedad (AOAC, 2005).
Cuantificación de los mohos y levaduras:
Métodos según Tournas et al. (2001).
Identificación morfológica de mohos:
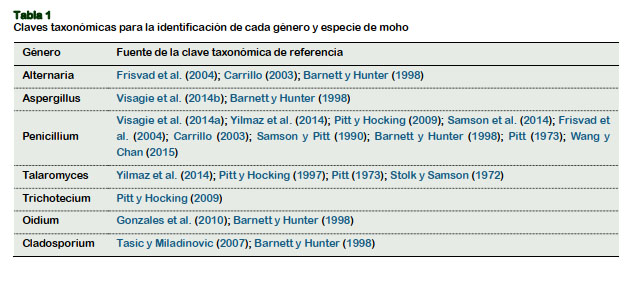
Se procedió al Recuento de esporas (Bustillo, 2010), Pruebas presuntivas en medios nutritivos: a) Caracterización microscópica (Mossel et al., 2003), b) Caracterización macroscópica mediante el empleo de Sistemas de identificación según género del moho: Aspergillus: Pitt (1997); Penicillium: Pitt (1973); Alternaria: Carrillo (2003), basados en el empleo de distintas temperaturas y medios de cultivo. La identificación de género se realizó según la "Illustrated genera of imperfect fungi" (Barnett y Hunter, 1998) y para la identificación macroscópica de las especies de los géneros Aspergillus, Penicillium y Alternaria se emplearon las claves taxonómicas según la Tabla 1.
Determinación de micotoxinas
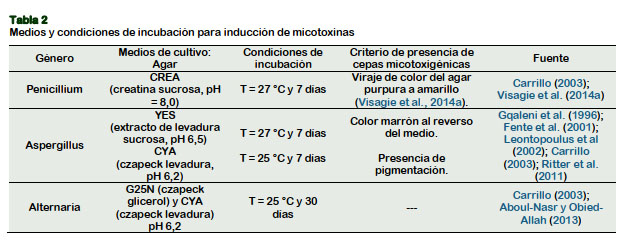
Las cepas de Aspergillus, Penicillium y Alternaria se sembraron en agar PDA para la producción de esporas (Gato, 2010). Las suspensiones de 105 esporas/ml se inocularon en medios inductores de micotoxinas (CREA, YES, CYA y G25N) (Visagie et al., 2014a). Se realizó la extracción de Ocratoxina A, Aflatoxinas Totales y Fumonisinas siguiendo Bragulat et al. (2001), Reddy et al. (2009), Aboul- Nasr y Obied-Allah (2013) (Tabla 2). Las micotoxinas fueron cuantificadas según el kit Veratox® (Neogen Corporation, 2015).
3. Resultados y discusión
Caracterización de accesiones de quinua: contenido de humedad y saponinas
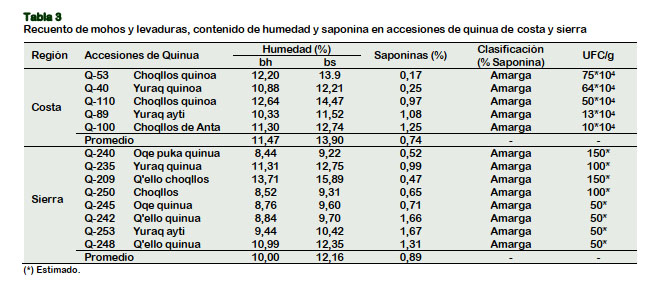
El contenido de humedad en base seca de las accesiones de quinua de la Costa estuvo en el rango 11,52 a 14,47% y de la Sierra, entre 9,22 a 15,89% (Tabla 3). Se observa que dichos valores cumplen con lo establecido por INACAL (2014), excepto en Q-100 (12,74%), Q-53 (13,90%) y Q-110 (14,47%) procedentes de la Costa; y Q-235 (12,75%) y Q-209 (15,89%) procedentes de la Sierra. Las pruebas de distribución no paramétricas de Kolmogorov-Smirnov (p = 0,1259), de Conover (p = 0,0545) y U de Mann (p = 0,171), según Berlanga y Rubio (2012), mostraron que no existen diferencias significativas entre el contenido de humedad de las accesiones de quinua de Costa y Sierra. Todas las accesiones presentaron un contenido de saponina mayor a 0,39 por ciento (Tabla 3), que coinciden con lo reportado por Ahumada et al. (2016) en quinuas de América Latina. Las pruebas de Kolmogorov-Smirnov (p = 0,5859), de Conover (p = 0,8388) y U de Mann Whitney (p = 0,4351) (Berlanga y Rubio, 2012), muestran que no existen diferencias significativas entre los contenidos de saponinas de las accesiones de quinua procedentes de la Costa con Sierra. Sin embargo, García-Parra et al. (2018) señala que el contenido de saponinas depende de la variedad, condiciones del suelo y clima. Las características físicas, químicas y microbiológicas del suelo, generan efectos sobre la síntesis de metabolitos, tales como las saponinas. Algunos estudios muestran el efecto de la salinidad e irrigación con el contenido de saponinas.
Cuantificación de mohos y levaduras
El contenido de mohos y levaduras de las accesiones de la Costa (10*104-75*104 ufc/g) fueron mayores a los de la Sierra (50- 150 est. ufc/g) (Tabla 3). Las pruebas de Kolmogorov-Smirnov (p = 0,004251), de Conover (p = 0,002088) y U de Mann Whitney (p < 2,2e-16) indica que el lugar de procedencia de las accesiones de quinua ejerció efecto en el recuento de mohos y levaduras (ufc/g) entre las accesiones de quinua de Costa y Sierra. Esta disminución en la carga microbiana es una estrategia adaptativa para mitigar los cambios ambientales como lo señalan Gonzales et al. (2017).
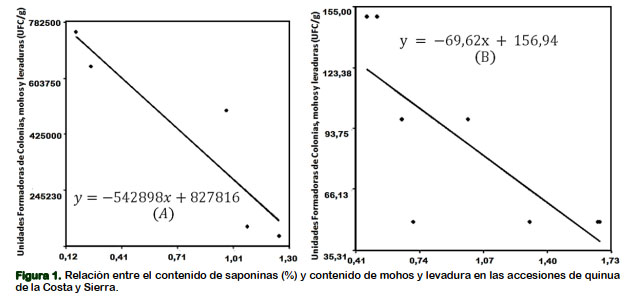
Al determinar la relación entre el contenido de saponinas (%) y el contenido de mohos y levaduras en las accesiones de quinua de Costa y Sierra empleando regresión lineal (Tabla 3 y Figura 1), se encontró que existe una relación lineal con pendiente negativa (R2 = 0,84) en el caso de las accesiones de quinua de la Costa, y para el caso de la sierra con mayor dispersión para un R2 = 0.60, que concuerda con lo reportado por Apaza et al. (2016), Pappier et al. (2008) y Stuardo y San Martin (2008).
Identificación morfológica de mohos
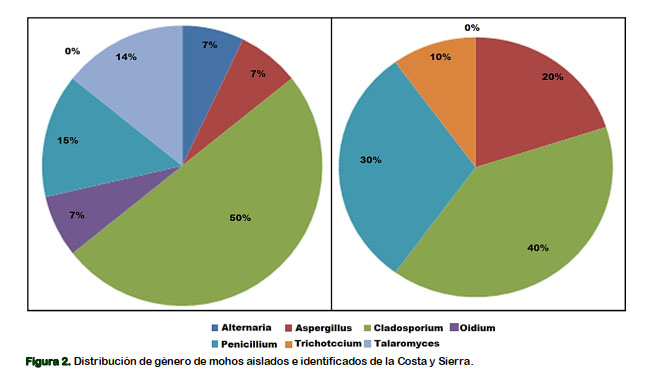
En la Figura 2 se muestra la distribución porcentual de los géneros de mohos identificados, provenientes de las accesiones de quinua de Costa y Sierra.
Los géneros de mayor incidencia en la Costa correspondieron a Cladosporium (40%), Penicillium (30%), Aspergillus (20%) y Trichotecium (10%), mientras que los géneros de mayor incidencia en la Sierra correspondieron a Cladosporium (50%), Penicillium (14%), Talaromyces (14%), Aspergillus (7%), Alternaria (7%) y Oidium (7%). Se evidencia que los géneros comunes en ambas regiones fueron los géneros Cladosporium, Penicillium y Aspergillum.
Identificación morfológica del género Alternaria (cepa 245H2)
Las principales características morfológicas se observan en la Tabla 4.
Investigaciones recientes han demostrado la incidencia de Alternaria alternata en quinua (Gonzales et al., 2017), que produce alergias por hipersensibilidad; es probablemente la especie productora de micotoxinas más importante (Pavón, 2012), entre ellas las Fumonisinas (Abbas et al., 1996; Mirocha et al., 1996).
Identificación morfológica del género Aspergillus
Las principales características morfológicas se observan en la Tabla 5.
Cepa 100H53: Identificada como Aspergillus ochraceus, especie aislada de la accesión Q100. Es una especie fuertemente productora de Ocratoxina A (Santos-Ciscona et al., 2019).
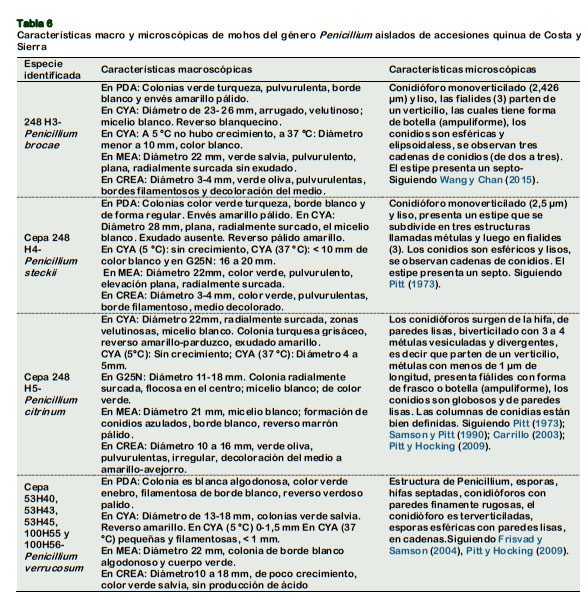
Identificación de especies del género Penicillium:
Cepas 248 H3: Identificada como Penicillium brocae.
Cepas 248 H4: Identificada como Penicillium steckii.
Cepa 248 H5: Identificada como Penicillium citrinum.
Cepa 240 H 25 y 240H27: Identificadas como Talaromyces wortmannii.
Cepa 53H40, 53H43, 53H45, 100H55 y 100H56: Identificada como Penicillium verrucosum.
Identificacion de otros géneros de mohos:
Cepa 240 H 25 y 240H27: Identificada como Talaromyces wortmannii.
Cepa 89H48: Identificada como Trichotecium sp.
Cepa 209H9: Identificada como Oidium sp.
Determinación de Aflatoxinas totales (B1, B2, G1 y G2), ocratoxina A y fumonisinas
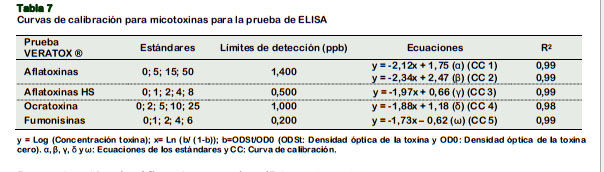
A fin de generar el contenido de micotoxinas, como etapa preliminar, se obtuvieron las curvas de calibración para los estándares de Aflatoxinas totales, Ocratoxina A y Fumonisinas, representadas por las ecuaciones y coeficiente de correlación (R2) (Tabla 7).
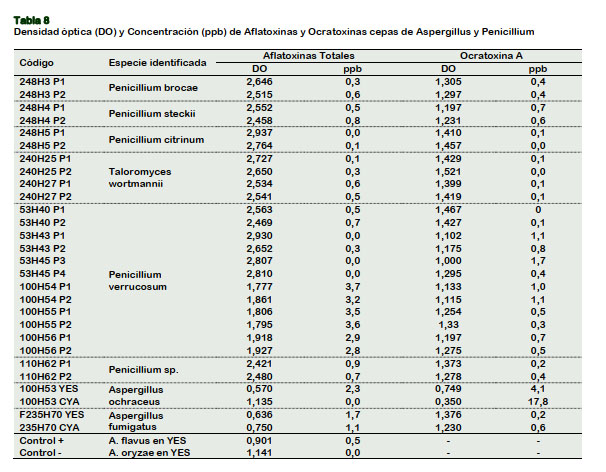
En la Tabla 8 se muestran que no hubo producción de aflatoxinas totales (B1, B2, G1, G2) por las cepas de Penicillium: 248H3, 248H5, 240H25, 53H40, 53H43, 53H45, 100H54, 100H55, 100H56 y 110H62.
Esto ocurrió debido a que las cepas identificadas como P. brocae (248H3 y 248H4), P. steckii (248H4), T. wortmannii (240H25 y 248H27) y P. verrucosum (53H40, 53H43 y 53H45) no son productoras de aflatoxinas (Peterson et al., 2003; Visagie et al., 2014b).
En la Tabla 8 se muestra que la cepa de Aspergillus flavus (control positivo) mostró ser positiva a la producción de Aflatoxinas (B1, B2, G1 y G2) bajo las condiciones culturales establecidas, coincidiendo con lo reportado por Ritter et al. (2011), Reddy et al. (2009), Leontopoulus et al. (2002) y Fente et al. (2001). Mientras que Aspergillus oryzae (control negativo) resultó negativa a la producción de aflatoxinas (B1, B2, G1 y G2). Efectivamente esta especie es una "forma domesticada" de A. flavus y no es productora de aflatoxinas (Abarca, 2000). La cepa de A. flavus tuvo una producción de 0,5 ppb de aflatoxinas bajo las condiciones establecidas, coincidiendo con Ritter et al. (2011). Las cepas 235H70 (Aspergillus fumigatus) y 100H53 (Aspergillus ochraceus) resultaron ser positivas a la producción de Aflatoxinas totales (B1, B2, G1 y G2). La cepa 253H70 produjo 1,6 ppb de aflatoxinas (YES) y 1,1 ppb de aflatoxinas (CYA), coincidiendo por lo reportado por Abarca et al. (1997) respecto a la producción de aflatoxinas por las cepas de A. fumigatus. Mientras que Aspergillus roseoglobulosus produjo 2,2 ppb de aflatoxinas (YES) y 0,0 ppb de aflatoxinas (CYA). Los resultados muestran una mayor producción de aflatoxinas en el medio YES comparada con CYA, coin- cidiendo con lo reportado por Ritter et al. (2011) y Reddy et al. (2009).
Asimismo, en la Tabla 8 se muestra que los extractos de los medios de cultivo de Penicillium: 248H3, 248H5, 240H25, 100H55, 100H56 y 110H62 no generaron ocratoxina A en las condiciones estable- cidas para las cepas de Penicillium en agar CREA. La cepa 53H43 (P. verrucosum) produjo 0,1 ppb. La producción de la cepa 53H45 (P. verrucosum) fue 1,1 ppb, mientras que la producción de ocratoxina A de la cepa 100H54 (Penicillium sp.) fue de 1,1 ppb. Efectivamente, la capacidad de producción de Ocratoxina A de las cepas de Penicillium verrucosum bajo las condiciones establecidas, ha sido reportada por Pitt y Hocking (2009). Por otro lado, es probable que el contenido de Ocratoxinas aumente con el contenido de humedad de las accesiones de quinuas Q- 53 (13,90%) y Q-100 (12,74%) (Ravelo et al., 2011).
En la Tabla 9 se observa que la producción de ocratoxina A de la cepa 100H53 (A. ochraceus) en el medio de cultivo YES (18,0 ppb) fue mayor que en el medio de cultivo CYA (4,0 ppb). Lo mismo ocurre con la producción de Ocratoxina A de la cepa 235H70 (A. fumigatus), en el medio de cultivo YES (0,6 ppb) fue mayor que en el medio de cultivo CYA (0,3 ppb). Se evidenció que el mejor medio para la producción de ocratoxina A es el medio de cultivo YES, condición encontrada por Fente et al. (2001) y Ritter et al. (2011).
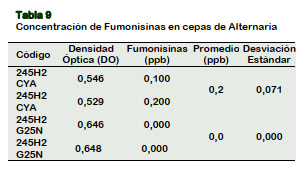
En la Tabla 9 se observa que las concentraciones de la micotoxina en los extractos de los cultivos de Alternaria: 245H2 en CYA presentó valor superior al límite establecido por el método, siendo esta cepa toxigénica, coincidiendo con lo reportado por Abbas et al. (1996) y Mirocha et al. (1996).
4. Conclusiones
Se cuantificó el contenido de hongos presentes en granos de las 13 accesiones de quinua provenientes de la Costa (Lima) y Sierra (Huancayo). Las accesiones de quinua de la Costa presentaron un rango de 75*104 y 10*104; y las de las Sierra 50 y 150 estimado. La procedencia de las accesiones condicionó la cantidad y variedad de hongos. Los géneros Cladosporium, Penicillium y Aspergillus se presentaron en la Costa y Sierra. Mientras que el género Trichotecium se presentó exclusivamente de la Costa y los generos Trichotecium, Talaromyces y Oidium en la Sierra. El contenido de saponinas de las accesiones de quinua presentó una correlación negativa con el contenido de mohos y levaduras en accesiones de Costa y Sierra. La cuantificación de aflatoxinas para algunos de los mohos del género Aspergillus, en el medio de cultivo YES, presentó desde 0,6 a 2,2 ppb de aflatoxinas totales (50%), siendo estos toxigénicos; el otro 50% fue del tipo no toxigénico; en el medio de cultivo CYA presentó desde < 0,5 a 1,1 ppb de aflatoxinas totales (50 por ciento), siendo estos toxigénicos. La cuantificación de ocratoxina para algunos de los mohos del género Penicillium, en el medio de cultivo CREA presentó desde 1,0 a 1,1 ppb de ocratoxina A (25 por ciento), siendo estos toxigénicos. Para el género Aspergillus, en el medio de cultivo CYA presentó desde < 1,0 a 3,7 ppb de ocratoxina A (50%), siendo estos toxigé- nicos. En el medio de cultivo YES presentó desde < 1,0 a 18,1 ppb de ocratoxina A (50 por ciento), siendo estos toxigénicos. La cuantificación de fumonisinas para el moho del género Alternaria, en el medio de cultivo CYA presentó 0,2 ppb de Fumonisinas (50%), siendo esta toxigénica; el otro 50% fue no toxigénico.
Agradecimientos
La presente investigación ha sido financiada por el Proyecto de Investigación Aplicada con Contrato Nº 141-FINCyT-IA-2013 "Selección de ecotipos de quinua (Chenopodium quinoa) con mayor potencial nutricional, funcional, tecnológico, sensorial y menor contenido de saponinas, cultivados en costa y sierra", del Fondo para la Innovación, la Ciencia y la Tecnología (FINCyT) del Programa Nacional de Innovación para la Competitividad y Productividad (Innovate Perú).
How to cite this article:
Guarniz-Benites, J.; Valdez-Arana, J. 2019. Identificación morfológica de hongos micotoxigénicos en accesiones de quinua (Chenopodium quinoa Wild.) de la costa y sierra peruana. Scientia Agropecuaria 10(3): 327 – 336.
Referencias bibliográficas
Abarca, L.M.; Bragulat, R.M.; Catellá, G.; Accensi, F.; Cabañes, J.F. 2000. Hongos productores de micotoxinas emergentes. Revista Iberoamericana de Micología 17: 63-68. [ Links ]
Abarca, M.L.; Bragulat, M.R.; Castellá, G.; Accensi, F.; Cabañes, F.J. 1997. New ochratoxigenic species in the genus Aspergillus. Journal of Food Protection 60(12): 1580-1582. [ Links ]
Abbas, H.K.; Duke, S.O.; Riley, W.T.; Kraus, G.A. 1996. The chemistry and biological activities of the natural products AAL-toxin and the fumonisin. Adv. Exp. Med. Biol. 391: 293–308. [ Links ]
Aboul-Nasr, M.B.; Obied-Allad, M.R.A. 2013. Biological and chemical detection of fumonisins produced on agar medium by Fusarium verticillioides isolates collected from corn in Sohag, Egypt. Microbiology 159: 1720–1724. [ Links ]
Ahumada, A.; Ortega, A.; Chito, D.; Benítez, R. 2016. Saponinas de quinua (Chenopodium quinoa Willd.): un subproducto con alto potencial biológico. Revista Colombiana de Ciencias Químico Farmaceuticas 45(3): 438-469. [ Links ]
AOAC. 2005. Official Methods of Analysis, Association of Official Analytical Chemists, Washington DC. [ Links ]
Apaza, R.; Smeltekop, H.; Flores, Y.; Almanza, G.; Salcedo, L. 2016. Efecto de saponinas de Chenopodium quinoa Willd. contra el fitopatógeno Cercospora beticola sacc. Revista de Proteccion Vegetal 31(1): 63-69. [ Links ]
Barnett, H.L.; Hunter, B.B. 1998. Illustrated genera of imperfect fungi. Fourth ed. Minnesota, EEUU. US: Burgess Publishing Company, APS. 241 pp. [ Links ]
Berlanga, V.; Rubio, M.J. 2012. Clasificación de pruebas no paramétricas. Cómo aplicarlas en SPSS. REIRE, Revista d’Innovació i Recerca en Educació 5(2): 101-113.
Bragulat, M.R.; Abarca, M.L.; Cabañez, F.J. 2001. An easy screening method for fungi producing ochratoxin a in pure culture. International journal of food microbiology 71: 139-144. [ Links ]
Bustillo, A.E. 2010. Método para cuantificar suspensión de esporas de hongos y otros microorganismos. Reporte técnico. Universidad Nacional- Palmira curso Patología de insectos. Disponible en: https://www.researchgate.net/publication/27 7870402_metodo_para_cuantificar_suspensi ones_de_esporas_de_hongos_y_otros_organi smos. [ Links ]
Carrillo, L. 2003. Los hongos de los alimentos y forrajes. Universidad Nacional de Salta, Argentina. ISBN 987-9381-19-X. 118 pp. [ Links ]
Fente, C.A.; Jaimez, J.I.; Vázquez, B.I.; Franco, C.M.; Cepeda, A. 2001. New additive for culture media for rapid identification of aflatoxin-producing aspergillus strains. Applied and enviromental. Microbiology 67(10): 4858-4862. [ Links ]
Frisvad, J.C.; Samson, R.A. 2004. Polyphasic taxonomy of Penicillium subgenus Penicillium: a guide to identification of food and airborne terverticillate penicillia and their mycotoxins. Studies in mycology 49: 1- 17. [ Links ]
Frisvad, J.C.; Frank, M.J.; Houbraken, J.; Kuijpers, A.; Samson, R. 2004. New ochratoxin a producing species of aspergillus section circumdati. Studies in mycology. 50:23-43. [ Links ]
García-Parra, M.A.; Plazas-Leguizamón, N.Z.; Carvajal, D.C.; Ferreira, S.K; David, J. 2018. Descripción de las saponinas en quinua (Chenopodium quinoa Willd) en relación con el suelo y el clima: una revisión. Informador Técnico 82(2): 241-249. [ Links ]
Gato, C.Y. 2010.Metodos de conservación y formulación de Trichoderma hazianum rifai. Fitosanidad 14(3): 189-195. [ Links ]
Gonzales, N.; Martinez, B.; Infante, D. 2010. Mildiu polvoriento en las cucurbitáceas. Protección Vegetal 25(1): 44-50. [ Links ]
Gonzalez-Teuber, M.; Vilo, C.; Bascuñán-Godoy, L. 2017. Molecular characterization of endophytic fungi associated with the roots of Chenopodium quinoa inhabiting the Atacama Desert, Chile. Genomics Data 11: 109-112. [ Links ]
Gqaleni, N.; Smith, J.E.; Lacey, J. 1996. Coproduction of aflatoxins and cyclopiazonic acid in isolates of aspergillus flavus. Food additives & contaminants 13(6): 677-685. [ Links ]
Guzmán, B.; Cruz, D.L.; Alvarado, J.A.; Mollinedo, P. 2013. Cuantificación de Saponinas en muestras de Cañihua Chenopodium pallidicaule Aellen. Revista Boliviana de Química 30(2): 131-136. [ Links ]
INACAL (Instituto Nacional de Calidad - Perú). 2014. NTP 205.062:2014. Granos Andinos. Quinua. Requisitos. 2 (ed). Lima. Perú. 28 dic 2014. 15 p. [ Links ]
Leontopoulus, D.; Siafaka, A.; Makaki, P. 2002. Black olives as substrate for aspergillus parasiticus growth and aflatoxin b production. Food Microbiology. 20: 119-126. [ Links ]
MINAGRI (Ministerio Nacional de Agricultura y Riego – Perú). 2018. Manejo agronómico prácticas de conservación de suelos, producción, comercialización y perspectivas de granos andinos. Lima. Perú [ Links ].
Mirocha, C.J.; Chen, J.; Xie, W.; Xu, Y.; Abbas, H.J.; Hogge, L.R. 1996. Biosynthesis of fumonisin and aal derivatives by alternaria and fusarium in laboratory culture. Adv. Exp. Med. Biol. 392: 213–224. [ Links ]
Mossel, D.; Moreno-García, B.; Struijk, C. 2003. Microbiología de los Alimentos. Editoral Acribia, Zaragoza, España. [ Links ]
Neogen Corporation. 2015. Manual de Procedimientos. Disponible en: http://www.Neogen.Com/En/. [ Links ]
Pappier, U.; Fernandez, V.; Larumbe, G.; Vaamonde, G. 2008. Effect of processing for saponin removal on fungal contamination of quinoa seeds (Chenopodium quinoa Willd.). International Journal of Food Microbiology 125: 153–157. [ Links ]
Pavón, M.A.; Gonzales, I.; Martin, R.; García, T. 2012. Importancia del género Alternaria como productor de micotoxinas y agente causal de enfermedades humanas. Nutrición Hospitalaria 27(6): 1772-1781. [ Links ]
Peterson, S.; Pérez, J.; Vega, F.E.; Infante, F. 2003. Penicillium brocae, a new pecies associated with the coffee berry borer in Chiapas, Mexico. Mycologia 95(1): 141-147. [ Links ]
Pitt, J.; Hocking, A.D. 1997. Fungi and spoilage: penicillium and related genera. Capitulo 7. Pag 203-338. [ Links ]
Pitt, J.I. 1973. An appraisal of identification methods for Penicillium species. Novel taxonomic criteria based on temperature and water relations. Mycologia 65(5): 1135-1157. [ Links ]
Pitt, J.I.; Hocking A.D. 2009. Fungi and Food Spoilage. 3 rd. Springer Dordrecht Heidelberg. New York, EEUUAA. [ Links ]
Ravelo, A.; Rubio, A.J.; Gutierrez, A.J.; Hardisson de la Torre 2011. La ocratoxina A en alimentos de consumo humano: revisión. Nutr Hosp. 26(6): 1215-1226. [ Links ]
Reddy, K.R.N.; Abbas, H.K.; Abel, C.A.; Shier, W.T.; Oliveira, C.A.F.; Raghavender, C.R. 2009. Mycotoxin contamination of commercially important agricultural commodities. Toxin reviews 28(2-3): 154-168. [ Links ]
Ritter, A.C.; Hoeltz, M.; Noll, I.B. 2011. Toxigenic potencial of aspergillus flavus tested in different cultre conditions. Ciencia y tecnologia de alimentos. Campinas 31(3): 623-628. [ Links ]
Samson, R.A.; Pitt, J.I. 1990. Modern concepts in penicillium and aspergillus classification. Springer science+business media New York. EEUU. [ Links ]
Samson, R.A.; Visagie, C.M.; Houbraken, J; Hong, S.B.; Hubka, V.; Klaassen, H.W.; Perrone, G.; Seifert, K.A.; Susca, A.; Tanney, J.B.; Varga, J.; Kocsubé, S.; Szigeti G.; Yaguchi, T.Y; Frisvad, J.C. 2014. Phylogeny, identification and nomenclature of the genus aspergillus. Studies in mycology 78: 141-173. [ Links ]
Santos-Ciscon, V.A.; Diepeningen, A.; Cruz, J.; Eleutéria, I.; Waalwijk, C. 2019. Aspergillus species from Brazilian dry beans and their toxigenic potential. International Journal of Food Microbiology 292: 91-100. [ Links ]
Stolk, A.C.; Samson, R.A. 1972. The Genus Talaromyces Studies on Talaromyces and related genera II. Studies in Mycology 2: 1-65. [ Links ]
Stuardo, M.; San Martin, R. 2008. Antifungal properties of quinoa (Chenopodium quinoa willd.) alkali treated saponins against botrytis cinérea. Industrial crops and products 27:296-302. [ Links ]
Tasic, S.; Miladinovic, N. 2007. Cladosporium spp. cause of opportunistic mycoses. Acta Facultatis Medicae Naissensis 24(1): 15-19. [ Links ]
Tournas, V.; Stack, M.E.; Mislivec, P.B.; Koch, H.A.; Bandler, R. 2001. Bacteriological analytical manual: BAM, yeast, molds and mycotoxins. 8th Edition. FDA. EEUU. [ Links ]
Visagie, C.M.; Houbraken, J.; Frisvad, J.C.; Hong, S-B.; Klaassen, H.W.; Perrone, G.; Seifert, K.A.; Varga, J.; Yaguchi, T.; Sanmon, Ra. 2014a. Identification and nomenclature of the genus penicillium. Studies in mycology 78: 343-371. [ Links ]
Visagie, C.M.; Hirooka, Y.; Tanney, J.B; Whitfield, E; Mwange, K.; Meijer, M.; Amend, A.S.; Seifert, K.A.; Samson, R.A. 2014b. Aspergillus, Penicillium and Talaromyces isolated from house dust samples collected around the world. Studies in Mycology 78: 63- 139. [ Links ]
Wang, Y-Z.; Chan, M-L. 2015. A Penicillium and a Talaromyces Nw to Taian. Coll. And Res. 28: 1-4. [ Links ]
Yilmaz, N.; Visagie, C.M.; Houbraken, J.; Frisvad, J.C.; Samson, R.A. 2014. Polyphasic taxonomy of the genus Talaromyces. Studies in Mycology 78: 175-341. [ Links ]
* Corresponding author
E-mail: jvaldez@lamolina.edu.pe (J. Valdez-Arana).
Received September 2, 2018.
Accepted April 29, 2019.