Introducción
El Pisco, finísimo destilado de uva producido en el Perú con más de 400 años de historia, ha incrementado su producción desde el año 2000 llegando a producir más de 7 millones de litros en 2019. De acuerdo al reglamento de la Denominación de Origen del Pisco, este puede ser producido a partir de ocho variedades de uva: Negra Criolla, Mollar, Quebranta, Uvina, Italia, Torontel, Moscatel y Albilla. Quebranta es la de mayor producción nacional y Negra Criolla es la de mayor producción en el departamento de Arequipa (Vingerhoets, 2015).
Las especies de Oregmopyga están todas presentes en el Nuevo Mundo (García et al., 2016); cinco especies presentes en el suroeste de los Estados Unidos, tres en el sureste de los Estados Unidos, una en el norte de Baja California, México y una en Perú (Miller y Stocks, 2007). Hodgson y Miller (2010) describe a Oregmopyga peruviana como plaga de la vid presente solamente en el Perú.
O. peruviana afecta los tallos leñosos de las plantas y se alojan debajo de la corteza e infestaciones fuertes puede ocasionar la muerte de la planta (Wille, 1952; Granara de Willink y Diaz, 2007). O. peruviana está presente en los departamentos de la Libertad, Lima, Ica, Arequipa, Moquegua y Tacna (Granara de Willink y Diaz, 2007). Wille (1952) menciona que O. peruviana ataca en forma importante los troncos de la vid en algunos valles vitícolas y en forma grave en el valle de Majes, Arequipa. Observaciones empíricas de campo sugieren que la infestación por O. peruviana provoca reducción de la canopia, menor tamaño de racimo, menor tamaño de baya y menor rendimiento.
Wille (1952) recomendó como método de control el pintado de los tallos de la vid en estado invernal, con una emulsión de kerosene, jabón, cal viva y agua, pero no indica los datos experimentales ni concentraciones para este control. Dadther-Huaman et al. (2019) menciona que, al utilizar imidacloprid, vinaza, clorpirifos y dinotefuran en una aproximación de manejo integrado pudo reducir la población de O. peruviana.
Se propone como tratamientos los siguientes: buprofezin, insecticida de contacto inhibidor de la síntesis de quitina (Uchida et al., 1987), en contraste con otros inhibido-res de síntesis de quitina, este compuesto actúa específicamente en insectos chupadores (Yasui et al., 1985). Clorpirifos, insecticida que actúa por contacto, ingestión e inhalación (Dorsan(r) 48 EC, Silvestre, Perú), utilizado como alternativa de tratamiento en poscosecha (Sazo, 1995). Vinaza, subproducto orgánico líquido de la fabricación del Pisco (Callejas et al., 2015), no ha sido probado anteriormente como método de control individual, estudios realizados en vinaza obtenida de la caña de azúcar presentan pH ácido y está compuesta principalmente por sulfatos, alcoholes y sustancias orgánicas volátiles (García y Rojas, 2006) que pueden ejercer un efecto en la plaga. Spirotetramat, insecticida sistémico de moviente en floema y xilema, utilizado para el control de un amplio espectro de insectos picadores chupadores, gracias a su movilidad puede controlar plagas ocultas en la planta (Mohapatra et al., 2012). Imidacloprid insecticida neonicotinoide, uno de los más utilizados a nivel mundial, puede ser aplicado a semillas, vía drench y aplicación foliar, puede controlar insectos eficientemente e incrementar la cosecha significativamente (Mohapatra et al., 2012). Mezcla de hongos Metharizium anisopliae y Beauveria bassiana (Inbiol(r), Terragenesis, Perú), existe un resurgimiento mundial de interés en el uso de hongos entomopatógenos como agentes de control biológico (Feng et al., 1994), esta mezcla de hongos ha sido utilizada para el control del "chanchito blanco" (Inbiol(r), Terra Genesis, Perú). Tiametoxam, insecticida sistémico de la segunda generación de neonicotinoides, provee un excelente control a un amplio rango de plagas como áfidos y trips, además, un fuerte efecto preventivo en transmisión de algunos virus. Tiametoxam puede ser aplicado al suelo o de forma foliar (Maienfisch et al., 2001). Dinotefuran, insecticida neonicotinoide altamente sistémico, de alta actividad insecticida y de gran espectro puede ser aplicado de forma foliar, drench y a semillas (Nauen et al., 2003).
O. peruviana constituye una plaga importante en todas las zonas vitivinícolas de la región Arequipa, sin embargo, aún no existe conocimiento suficiente sobre métodos de control de forma individual. Es necesario generar conocimientos básicos referidos a la identidad de la especie problema. En la literatura entomológica nacional y mundial sólo existen un trabajo publicado sobre la identificación de esta plaga y un trabajo de aproximación de manejo integrado, todos los demás aspectos permanecen desconocidos, lo cual representa un campo de investigación no explorado. El conocimiento actual de O. peruviana es muy limitado, hasta el momento solo se ha reportado su presencia en el Perú, especialmente en zonas áridas, de tal modo que la solución sólo se puede investigar y lograr en zonas que presentan O. peruviana, y donde representen un interés socio-económico.
Considerando la importancia que tiene la producción de variedades de uva para la elaboración de la bebida Nacional, Pisco, es importante poder obtener una mejor rentabilidad a través de métodos de control de plagas, para la cual esta investigación tuvo como objetivo determinar la eficacia individual de nueve tratamientos para el control de O. peruviana.
Materiales y métodos
Área de estudio
La investigación se realizó en el fundo Santa Rosa, anexo el Pedregal, distrito Uraca, provincia de Castilla, departamento de Arequipa, Perú, entre junio 2017 y enero 2018. Sus coordenadas geográficas: latitud sur: 16°13'08"; Longitud oeste 72°28'07" y altitud 480 m s. n. m.
Material vegetal y condiciones agronómicas
Las evaluaciones se realizaron en dos lotes con la variedad Negra Criolla y uno con la variedad Quebranta, con sistema de riego por goteo con doble manguera, sistema de conducción en espaldera con doble brazo, suelo arenoso franco. En la variedad Negra Criolla, el distanciamiento entre hileras fue de 2,5 m en un lote y 3 m en el otro. En la variedad Quebranta, el distanciamiento entre hileras fue de 3 m. En los tres lotes, el distanciamiento entre plantas fue de 1,3 m.
Condiciones meteorológicas de la zona de estudio
El anexo Pedregal, distrito de Uraca de la provincia de Castilla presenta un clima típicamente árido. La insolación diaria tiene un valor medio de 12 horas; la temperatura media es de 21 °C con una media máxima de 29 °C y una media mínima de 14 °C. La humedad relativa media es de 66% con una media máxima de 84% y una media mínima de 40%. La precipitación media anual es casi cero (5 mm durante el periodo de evaluación). Esta información meteorológica se obtuvo de una estación (HOBO micro Station, modelo ONSET) instalada en el campo experimental.
Métodos empleados
Los tratamientos, las variedades, las áreas de evaluación, el lugar de aplicación y las concentraciones sometidas a evaluación están descritos en la Tabla 1.
Cada tratamiento se evaluó de forma individual y se comparó con su testigo (sin tratamiento alguno). Los tratamientos fueron aplicados en diferentes estados fenológicos, identificados mediante la notación con letras de la A a la P según Baggiolini (1952). La zona de evaluación de los tratamientos es desde el cuello del tronco hasta la bifurcación de los brazos, para cada evaluación se retiró el ritidomo para poder observar el número de individuos de O. peruviana, proceso denominado destole. Los tratamientos de buprofezin, clorpirifos, vinaza, imidacloprid granulado dispersable (WG) y la Mezcla de hongos M. anisopliae y B. bassiana, tuvieron 3 repeticiones de 2 plantas cada una, se evaluaron cada 7 días, y se realizaron 5 evaluaciones dando un total de 30 plantas evaluadas, en los tratamientos de clorpirifos y vinaza se aplicó previamente detergente amino potásico en dosis de 87,5 g·hL-1 de agua a chorro continuo sobre los troncos para poder limpiar la zona de tratamiento y facilitar la penetración de los productos aplicados posteriormente. Los tratamientos con clorpirifos y la mezcla de hongos M. anisopliae y B. bassiana fueron aplicados acompañados del surfactante, oxirano (750 g·L-1) + poliéter (250 g·L-1) (Break Thru(r), BASF, Perú), en dosis de producto formulado de 50 ml·hL-1. Los tratamientos con spirotetramat, imidacloprid suspensión concentrada (SC), tuvieron 3 repeticiones de 2 plantas cada una, se evaluaron cada 7 días durante 5 evaluaciones, además se evaluó una sexta vez luego de un mes de la quinta evaluación dando un total de 36 plantas evaluadas. Los tratamientos con tiametoxam y dinotefuran tuvieron 3 repeticiones de 2 plantas cada una, se evaluaron cada 7 días durante 7 evaluaciones, dando un total de 42 plantas evaluadas. El testigo para cada tratamiento tuvo 3 repeticiones de 2 plantas cada una, se evaluó la misma fecha que los tratamientos. En cada evaluación se realizó el conteo de individuos por planta.
Cada tratamiento fue aplicado en una parcela experimental, en cada parcela experimental se estableció una zona de aplicación rodeada por una zona de amortiguación para evitar el efecto de borde (López-Barrera, 2004).
Tabla 1 Distribución de los tratamientos para el control de O. peruviana
| Tratamientos | Variedad | Área de evaluación (m2) | Sitio de aplicación | Concentración |
| Buprofezin | NC | 430 | Tronco destolado | 25 g-hL-1 |
| Clorpirifos | NC | 1993 | Tronco | 96 g-hL-1 |
| Vinaza | Q | 1993 | Tronco | vinaza pura |
| Spirotetramat | NC | 1576 | Suelo | 474,3 g-ha-1 |
| Imidacloprid SC | NC | 1576 | Suelo | 1435 g-ha-1 |
| Imidacloprid WG | Q | 1993 | Hojas | 17,5 g-hL-1 |
| M. anisopliae + B. bassiana | Q | 1993 | Tronco | 333,3 x 1012 UFC-hL-1 |
| Tiametoxam | NC | 1576 | Suelo | 900 g-ha-1 |
| Dinotefuran | NC | 1576 | Suelo | 680 g-ha-1 |
SC = Suspensión concentrada (formulación comercial), WG = Granulado dispersable (formulación comercial), NC = Negra Criolla, Q = Quebranta, Suelo = vía sistema de riego, UFC = Unidades Formadoras de Colonias.
Para determinar el porcentaje de control se utilizó la fórmula de Henderson y Tilton (1955), para poblaciones no uniformes.
Porcentaje de control = 100 x (1- (Ta x Cb ÷ Tb x Ca))
Donde, Ta = número de individuos después del tratamiento, Tb = número de individuos antes del tratamiento, Ca = número de individuos en el testigo después del tratamiento, Cb = es el número de individuos en el testigo antes del tratamiento.
Análisis estadístico
Se utilizó el programa estadístico SPSS(r), versión 22. Los resultados fueron sometidos a la prueba paramétrica de T de Student (p ≤ 0,05) para variables independientes. Los datos que no presentaron normalidad y homogeneidad de varianza fueron contrastados mediante la prueba no paramétrica U de Mann-Whitney.
Resultados y discusión
Tratamientos Poscosecha
Buprofezin: antes de la aplicación (a los 0 días), el número de individuos por planta del testigo (79,1) es ligeramente mayor a la del tratamiento (61,6); además, el testigo y el tratamiento tienen una desviación alta, 15,9 y 7,2 respectivamente, no existe diferencia significativa. A los 7 y 14 días, el número de individuos por planta en el tratamiento es 6,6 y 1,8 respectivamente, siendo menor a la del testigo, 55,9 y 18,3 individuos respectivamente, existe diferencia significativa para cada fecha de evaluación. Buprofezin muestra un control sobre O. peruviana y concuerda con la indicación de ser una alternativa de control para plagas similares como los "chanchitos blancos" (Sazo, 1995). Esto es debido al modo de acción del químico, que inhibe la síntesis de quitina de ninfas (Applaud(r), TQC, Perú). A los 21 días el número de individuos por planta del testigo y tratamiento disminuye, 1,3 y 0,6 respectivamente, pero existe diferencia significativa, debido a que las desviaciones son pequeñas (0,3 para el testigo y 0,1 para el tratamiento), el número de individuos del testigo disminuye a causa del destole. A los 28 días el número de individuos por planta del testigo y tratamiento son iguales (0), el testigo disminuye el número de individuos por planta por efecto del destole, control cultural que expone a los insectos a factores externos ocasionando su muerte (Figura 1a).
Clorpirifos: antes de la aplicación (0 días), el número de individuos por planta del testigo y tratamiento fueron 410,3 y 363,8, respectivamente, no existiendo diferencias significativas entre ellos. A los 7, 14, 21 y 28 días el número de individuos por planta del testigo fueron 387,3, 324,7, 334,2 y 388,3 respectivamente mientras que el número de individuos por planta del tratamiento disminuye 105,7, 46,8, 91,2 y 54,2; respectivamente, existiendo diferencias significativas para cada fecha de evaluación, evidenciando el efecto de clorpirifos para el control de hemípteros (Sazo et al., 2008). Clorpirifos posee una buena acción de vapor que permite controlar insectos que se ocultan dentro del tejido vegetal, tiene, además, un efecto de persistencia en la planta y en el suelo evitando rápidas reinfes-taciones (Dorsan(r) 48 EC, Silvestre, Perú). A partir de los 7 días, se observó un cambio en el color de los insectos, lo que indica la efectividad de clorpirifos (Bisset et al., 2011) (Figura 1b). A los 21 días se observó un incremento en la población del tratamiento debido a que para cada momento de evaluación se eligen nuevas plantas sin descortezar, teniendo poblaciones variables.
Vinaza: antes de la aplicación (0 días), el número de individuos por planta del testigo fue menor que la del tratamiento 410,3 y 571,1 respectivamente, no existiendo diferencias significativas. A los 7 días el número de individuos por planta del tratamiento empieza a disminuir (510,3), sin embargo, aún es mayor que el testigo (387,3), no existiendo diferencias significativas. A los 14 días el número de individuos por planta del testigo y tratamiento fueron, 324,7 y 167,4 respectivamente, demostrando el efecto de la vinaza, existiendo diferencias significativas. A los 21 días el número de individuos por planta del testigo y tratamiento se acercan, 334,2 y 304,2 respectivamente, no existiendo diferencias significativas, esto se debe a que, en cada evaluación, se tomaron plantas diferentes por el comportamiento de la plaga, que solo puede vivir debajo de la corteza, teniendo poblaciones variables. A los 28 días el número de individuos por planta del testigo fue 388,3 y del tratamiento de 161,7, existiendo diferencias significativas. La vinaza disminuye la población del tratamiento probablemente debido a su pH acido, concentración de sulfatos y alcoholes volátiles, como se demuestra en la vinaza de la caña (García y Rojas, 2006). Dadther-Huaman et al. (2019) también mencionan el control efectivo de la vinaza, producto alterno y económico, teniendo poblaciones bajas de O. peruviana debido a que se aplicó vinaza en dos oportunidades (Figura 1c).
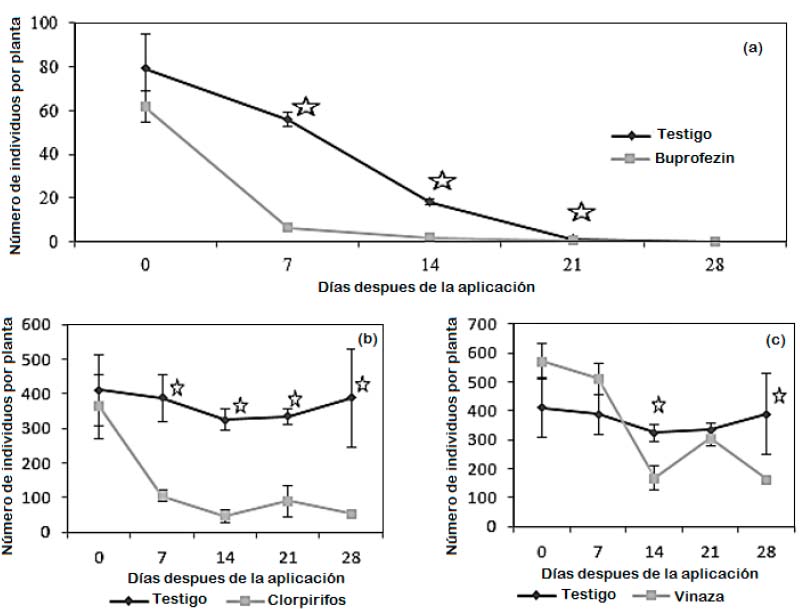
Figura 1 Población de O. peruviana (número de individuos por planta) y el tiempo, medido en días después de la aplicación, estado fenológico P (caída de hojas). (a): tratamiento con buprofezin, sobre Negra Criolla, aplicado al tronco previamente destolado; (b): tratamiento con clorpirifos, sobre Quebranta, aplicado al tronco; (c): tratamiento con vinaza, sobre Quebranta, aplicado al tronco. Estrellas muestran diferencia significativa.
Tratamientos Brotación-Floración
Spirotetramat: antes de la aplicación (0 días), el testigo y tratamiento inician con un número de individuos por planta similar, 120,8 y 112,7 respectivamente, no existe diferencia significativa. El número de individuos por planta del testigo comienza a aumentar a los 7 y 14 días, 76,8 y 188,5 respectivamente, mientras que en el tratamiento el número de individuos por planta empieza a disminuir 21,8 a los 7 días y 77,3 a los 14 días (el número de individuos a los 14 días se incrementó en relación a la de los 7 días, debido a que en cada evaluación se tomaron plantas diferentes por el comportamiento de la plaga, que solo puede vivir debajo de la corteza, teniendo poblaciones variables), no existe diferencia significativa. A los 21, 28 y 52 días el número de individuos por planta del testigo se incrementó siendo 426,7, 258 y 416 respectivamente, y el número de individuos por planta del tratamiento decayó 69,8, 6,7 y 45 respectivamente, existe diferencia significativa para cada fecha de evaluación. Spirotetramat ocasiona disminución de insectos, ya que actúa inhibiendo la biosíntesis de lípidos de tal manera que la muda no puede efectuarse (Movento(r) 150 OD, Bayer, Perú), además, gracias al movimiento de spirotetramat por floema y xilema, puede inclusive llegar a las zonas más alejadas como raíces y protegerlas contra chupadores-picadores (Mohapatra et al., 2012) (Figura 2a).
Imidacloprid concentrado soluble (SC): antes de la aplicación (0 días), los individuos por planta del testigo y tratamiento son similares, 120,8 y 121,3 respectivamente, no existe diferencia significativa. A los 7 días el testigo presenta 76,8 individuos por planta, ligeramente menor a la del tratamiento 107, no existe diferencia significativa. A los 14, 21, 28 y 52 días, el número de individuos por planta del testigo se incrementa, 188,5, 426,7, 258 y 416, respectivamente, mientras que el número de individuos por planta del tratamiento disminuye, 106,2, 87,5, 40 y 51,7 respectivamente, existe diferencia significativa. El efecto de imidacloprid se debe a su modo de acción (Kodaka et al., 1998) nuevo o no convencional para combatir plagas de insectos altamente resistentes (Elbert, 1991) (Figura 2b).
Imidacloprid granulado dispersante (WG): Antes de la aplicación (0 días), el número de individuos por planta del testigo es 84, y del tratamiento 49,3, no existe diferencia significativa. A los 7 días el número de individuos por planta del testigo se incrementa (143,2) y la del tratamiento se incrementa mucho más (208,3), sin embargo, no existe diferencia significativa debido a la heterogeneidad generada por el método de evaluación.
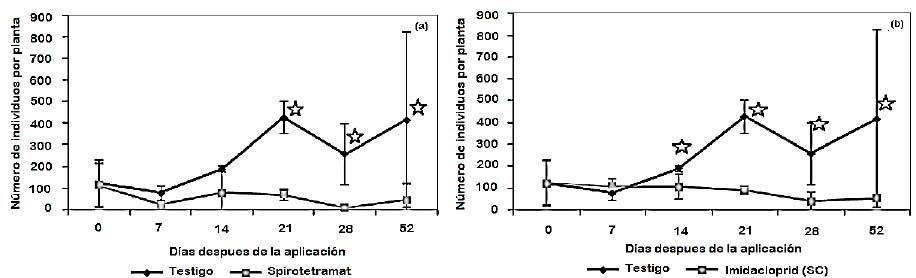
Figura 2 Población de O. peruviana (número de individuos por planta) y el tiempo, medido en días después de la aplicación, estados fenológicos F (racimos visibles), G (racimos separados) y H (botones florales separados). (a): tratamiento con spirotetramat, sobre Negra Criolla, aplicado al suelo; (b): tratamiento con imidacloprid (SC, suspensión concentrada), sobre Negra Criolla, aplicado al suelo. Estrellas muestran diferencia significativa.
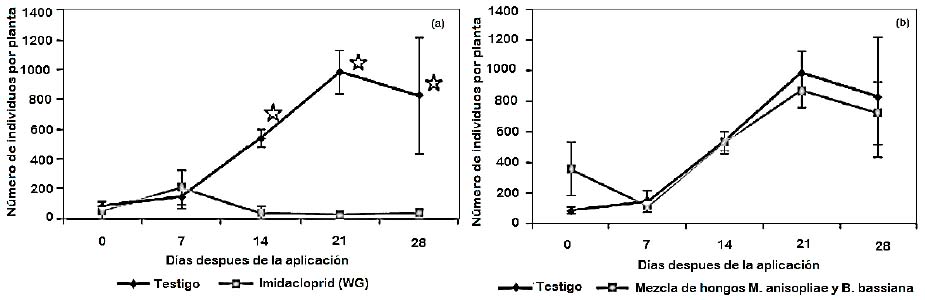
Figura 3 Población de O. peruviana (número de individuos por planta) y el tiempo, medido en días después de la aplicación, estados fenológicos F (racimos visibles), G (racimos separados) y H (botones florales separados). (a): tratamiento con imidacloprid (WG, granulado dispersable), sobre Quebranta, aplicado a las hojas; (b): tratamiento con mezcla de hongos Metarhizium anisopliae y Beauveria bassiana, sobre Quebranta, aplicado al tronco. Estrellas muestran diferencia significativa.
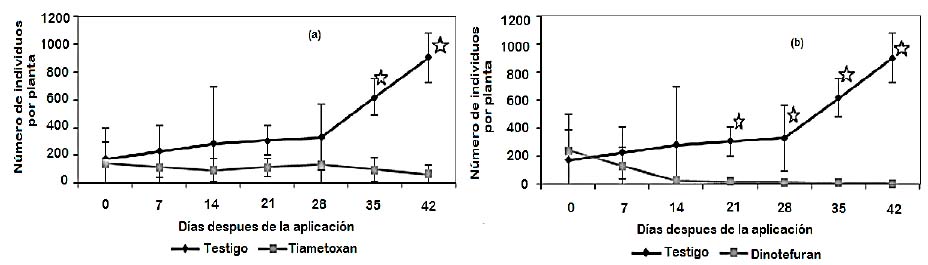
Figura 4 Población de O. peruviana (número de individuos por planta) y el tiempo, medido en días después de la aplicación, estados fenológicos K (grano tamaño guisante), L (racimo cernido), M (envero). (a): tratamiento con tiametoxam, sobre Negra Criolla, aplicado al suelo; (b): tratamiento con dinotefuran, sobre Negra Criolla, aplicado al suelo. Estrellas muestran diferencia significativa.
A los 14, 21 y 28 días el número de individuos por planta del testigo se incrementa 536,7, 985 y 826,7 respectivamente, mientras que el número de individuos por planta del tratamiento disminuye, 36, 26 y 37,7 respectivamente, existe diferencia significativa. Esto demuestra el efecto de control del imidaclo-prid debido a su alta sistemicidad del producto aplicado a las hojas (Singh et al., 2010), gracias a su modo de acción puede actuar sobre insectos resistentes a insecticidas piretiroides y fosforados (Confidor(r) 70 WG, Bayer, Perú) (Figura 3a).
Mezcla de hongos entomopatógenos ( M. anisopliae y B. bassiana ): no reduce el número de individuos por planta, no existiendo diferencias significativas. El hongo necesita entrar en contacto con la plaga, el insecto se encuentra escondido debajo del ritidomo, a pesar de que se realizaron incisiones en ciertas partes de la planta, donde se aplicó el producto. Además, pese a haber aplicado el producto en las primeras horas del día, la plaga estuvo expuesta a la radiación y las fuertes temperaturas propias de la zona (Figura 3b).
Tratamientos Floración-Envero
Tiametoxam: antes de la aplicación (0 días), el número de individuos por planta del testigo es 172 y del tratamiento 139,7, no existe diferencia significativa; a los 7, 14, 21 y 28 días el testigo incrementa el número de individuos por planta siendo, 226,8, 281,7, 306,7 y 331,7 respectivamente, mientras que la población del tratamiento es 116,2, 92,7, 111,8 y 131 respectivamente, no existe diferencia significativa. A los 35 y 42 días el número de individuos por planta del testigo aumenta, 619 y 906,3 respectivamente, mientras que el número de individuos por planta del tratamiento disminuye, 96,5 y 62 respectivamente, existe diferencia significativa. Tiametoxam es uno de los insecticidas más usados en el mundo (Coulon et al., 2018) de la familia de los neonicotinoides, de amplio espectro, que puede ser usado en hoja o suelo, ya que tiene una alta movilidad en la planta (Maienfisch et al., 2001), lo que demuestra su control sobre O. peruviana (Figura 4a).
Dinotefuran: Antes de la evaluación (0 días), el número de individuos por planta del testigo es 172 mientras que el tratamiento es 239, no existe diferencia significativa. A los 7 y 14 días el número de individuos por planta del tratamiento empieza a reducir, 132 y 25 respectivamente, mientras que el número de individuos por planta del testigo se incrementa, 226,8 y 281,7 respectivamente.
Para los 21, 28, 35 y 42 días el número de individuos por planta del tratamiento se reduce drásticamente siendo 19,2, 13,3, 9,3 y 5,3, respectivamente mientras que el número de individuos por planta del testigo se incrementa 306,7, 221,7, 619 y 906,3 respectivamente, existe diferencia significativa en cada fecha de evaluación. Se observa que dinotefuran provoca que el número de individuos por planta se reduzca por debajo de 30 a los 14 días, lo cual puede deberse a su acción estomacal, de contacto y sistémica (Kodaka et al., 1998), y a que es agonista del receptor nicotínico de acetilcolina, que afecta la sinapsis en el sistema nervioso central (Tomizawa y Yamamoto, 1993), además, dinotefuran tiene una actividad insecticida especialmente alta contra una amplia gama de insectos hemípteros y una baja toxicidad para los mamíferos (Tomlin, 2000) (Figura 4b).
Porcentajes de control
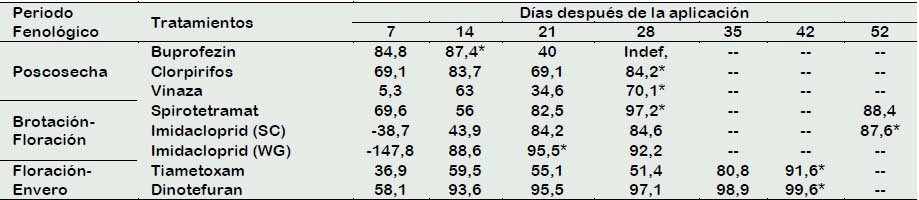
Para cada tratamiento se obtuvo el porcentaje de control en cada momento de evaluación en días después de la aplicación, la Tabla 2 presenta los resultados. De los tratamientos poscosecha (buprofezin, clorpirifos y vinaza), buprofezin muestra la mayor eficacia, con un porcentaje de control de 87,4%, en el menor tiempo (14 días), seguido de clorpirifos (84,2% en 28 días) y la vinaza presenta la menor eficacia (70,1% a los 28 días). Sin embargo, todos los tratamientos muestran porcentajes de control superiores al 70%. Con respecto al tratamiento con buprofezin, el más eficaz, requiere un previo destole, que implica un mayor costo de mano de obra.
Por otro lado, la vinaza, aunque su eficacia es menor, su disponibilidad a muy bajo costo representa una ventaja para los productores de Pisco debido a que es un subproducto de la destilación (Callejas et al., 2015). Es necesario realizar más investigaciones para determinar el modo de acción de la vinaza sobre la plaga y la entomofauna asociada a la vid.
De los tratamientos brotación-floración (spirotetramat, imidacloprid (SC) e imidacloprid (WG)), spirotetramat muestra la mayor eficacia, con un porcentaje de control de 97,2% en un periodo de 28 días. Seguido de imidacloprid (WG), que presenta un porcentaje de control de 95,5%, en un periodo de 21 días. Imidacloprid (SC) presenta la menor eficacia (87,6% a los 52 días).
Todos los porcentajes de control son mayores al 85%. A pesar de la mayor eficacia en menor tiempo de imidacloprid (WG), este tratamiento implica un mayor costo en personal para la aplicación foliar en comparación con los tratamientos imidacloprid (SC) y spirotetramat, que son inyectados directamente al sistema de riego.
Spirotetramat muestra un porcentaje de mortalidad de 88,4% a los 52 días, lo cual corrobora la persistencia indicada por el fabricante (Movento(r) 100 SC, Bayer, Chile). La alta eficacia de imidacloprid (SC) confirma la excelente absorción radicular indicada por el fabricante (Confidor(r) 350SC, Bayer, Chile).
De los tratamientos floración-envero (tiametoxam y dinotefuran), ambos muestran su mayor porcentaje de control a los 42 días, superando el 90% (dinotefuran 99,6% y tiametoxam 91,6%). Con una toxicidad relativamente baja para los mamíferos y los organismos no dirigidos (Tomlin, 2000).
Conclusiones
Todos los tratamientos, a excepción de la mezcla de hongos de M. anisopliae y B. bassiana, muestran eficacia en el control de O. peruviana, con poblaciones en los testigos significativamente superiores a las poblaciones de los tratamientos.
De los tratamientos aplicados en posco-secha, buprofezin tiene el mayor porcentaje de control 87,4%, seguido de clorpirifos 84,2%, y vinaza con 70,1%.
De los tratamientos utilizados en brotación-floración, spirotetramat tiene el mayor porcentaje de control 97,2%, seguido de imidacloprid (WG) con 95,5% e imidacloprid (SC) con 87,6%. El tratamiento con mezcla de hongos M. anisopliae y B. bassiana, no muestra control de O. peruviana.
De los tratamientos utilizados en floración-envero, dinotefuran tiene el mayor porcentaje de mortalidad de 99,6%, seguido de tiametoxam con un porcentaje de mortalidad del 91,6%.
Ocho de los nueve tratamientos tuvieron un porcentaje de control superior al 70% siendo los más eficaces dinotefuran y tiametoxam. Además, vinaza es una alternativa orgánica y económica para el control de O. peruviana.
Se recomienda realizar repeticiones de los tratamientos en las zonas afectadas por O. peruviana: Arequipa, La Libertad, Lima, Ica, Moquegua y Tacna. Asimismo, evaluar el efecto de la vinaza aplicada en diferentes periodos fenológicos.