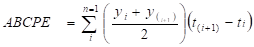Introducción
La quinua (Chenopodium quinoa Willd.) es un cultivo originario de la región andina. La cuenca del lago Titicaca ubicado entre Perú y Bolivia es considerado como centro de origen y se conserva mayor diversidad genética, cultivándose desde hace 7,000 años (Danielsen y Ames, 2014). Actualmente, la quinua es reconocida a nivel internacional por su alto contenido de proteínas como promedio contiene entre 14,33% y 15% (Rojas et al., 2016; García y Plazas, 2018). Es considerada como el único alimento del reino vegetal que provee aminoácidos esenciales con alto contenido de lisina, metionina, treonina y triptófan; siendo estos muy útil en las etapas de desarrollo y crecimiento de los niños, y puede ser utilizada en las dietas especiales para adultos mayores, deportistas de alto rendimiento, diabéticos por no contener colesterol (Navruz-Varli y Sanlier, 2016; Schmöckel et al., 2017). La quinua posee gran variabilidad y plasticidad genética que le permite tolerar y adaptarse a diferentes condiciones adversas como: heladas, suelos salinos, suelos poco fértiles, puede cultivarse desde 0 a 4000 msnm, en diferentes zonas agroecológicas del Perú y en otros países como Estados Unidos, Canadá, Italia, Marrueco, India y Egipto (Bazile et al., 2016; Thines y Choi, 2016; Eisa et al., 2017), en Turkia se comportó como resistente a la sequía (Altuner et al., 2019). A nivel nacional el cultivo de quinua ha adquirido mucha importancia para la agro exportación (Risco y Mattos, 2014). En Piura y en países como China (Hui et al., 2018), Estados Unidos (Testen et al, 2014) Egipto (Khalifa y Thabet, 2018) y en Turquía (Soylu et al., (2020) reportan que este cultivo ha sido infectado por la enfermedad del mildiu (Peronospora variabilis Gäum), ocasionando defoliación completa de la planta y pérdidas económicas a los agricultores. Investigadores cómo Testen et al. (2014) y Thines y Choi (2016) indican que las pérdidas pueden alcanzar hasta 33% en variedades tolerantes y 99% en variedades susceptibles, P. variabilis es un patógeno económicamente importante en la producción de quinua. Para el control aplican fungicidas químicos que son dañinos para la salud y medio ambiente, frente a este problema Jamiołkowska (2020), señala que extractos de plantas y algas, oligosacáridos, aminoácidos y sustancias sintéticas pueden activar mecanismos de defensa de la planta frente al ataque de patógenos. En Piura, se desconoce la etiología y manejo del mildiu, por lo que se hizo necesario realizar el presente estudio con la finalidad de detectar el inóculo primario del mildiu, describir la sintomatología y evaluar el efecto de los inductores de defensa en el control de la enfermedad.
Materiales y métodos
Lugar y periodo de ejecución
El estudio se realizó en el Laboratorio de Fitopatología, Facultad de Agronomía y en el Centro de Investigación de Producción Agrícola (CIPA) de la Universidad Nacional de Piura, ubicado a una altitud de 35 msnm, con coordenadas geográficas de 05°10’45’’ latitud Sur y 80°37’07’’ longitud Oeste, las condiciones climáticas que se registraron son T° media de 24,9 °C y HR media 80,4%.
Detección de oosporas en semillas de quinua
Se analizó 15 muestras de diferentes variedades y de diferente procedencia (Tabla 1). Para detectar oosporas se contabilizó 100 unidades de granos de quinua, se colocaron en tubos de ensayo conteniendo 1 mL de agua destilada estéril, se agitó en un agitador magnético durante 5 min. Posteriormente, con una pipeta se extrajo una alícuota de 0,25 mL y se colocó en láminas portaobjeto marcadas en cuadriculas de 3 x 3 mm, adicionando una gota de safranina, luego se observó en un microscopio compuesto (Carl Zeiss Mod. KF 2, Oberkochen, Germany) (aumento 40X) y se contabilizó el número de oosporas.
Tabla 1 Detección de oosporas de Peronospora variabilis en diferentes variedades de semillas de Chenopodium quinoa
| N° de Muestra | Variedades | Procedencia |
| 01 | Salcedo INIA | Sullana-Piura |
| 02 | Pasankalla | Puno |
| 03 | Salcedo INIA | ECOSAC - Piura |
| 04 | Witulla | Puno |
| 05 | Amarilla Marangani | DRAP - Piura |
| 06 | Salcedo INIA | CIPA-UNP |
| 07 | Blanca de Junín | DRAP - Piura |
| 08 | Amarilla de Junín | DRAP - Piura |
| 09 | Quellohua | Puno |
| 10 | Salcedo INIA | Lambayeque |
| 11 | Wila | Puno |
| 12 | Koliku | Puno |
| 13 | Blanca de Juli | Puno |
| 14 | INIA Altiplano | Puno |
| 15 | Koyto | Puno |
DRAP=Direccion Regional de Agricultura - Piura, INIA=Instituto Nacional de Innovacion Agraria.
Características morfométricas de Peronospora variabilis
Se colectaron hojas de quinua con síntomas y signos de mildiu, se prepararon montajes en el cual consistió en realizar raspados de las estructuras reproductivas con una aguja de disección estéril, se colocaron en láminas porta objetos que contenían una gota de agua destilada, se cubrió con laminilla y luego llevados al microscopio compuesto para observar y realizar mediciones micrométricas de los esporangióforos, esporangios y oosporas.
En campo
Material genético
Se empleó semilla botánica certificada, var. salcedo INIA, procedente del departamento de Lambayeque.
Inductores de defensa
Los tratamientos consistieron en la aplicación individual, combinada e intercalada de los productos (Tabla 2). Se utilizó una mochila asperjadora manual de 15 L de capacidad, se adicionaron los productos a la dosis respectiva. Los tratamientos con los productos Biosar y 3 Tac, se mezclaron con el producto Biotens que es un surfactante tenso activo; y para el tratamiento 5 se mezclaron los productos Agromos+Soil set. Las aplicaciones estuvieron basadas en la fenología del cultivo y la severidad de la enfermedad, realizándose en total 8 aplicaciones. Se empleó Diseño de Bloques Completamente al Azar (DBCA) con nueve tratamientos y cinco repeticiones. Se realizó el análisis de variancia (ANVA) y las comparaciones de medias de Tukey (α=0,05) utilizando el programa SAS (System Analysis Statistical).
Evaluación de severidad
Se identificaron 25 plantas por tratamiento, y se evaluaron tres hojas por planta al azar, en el tercio inferior, medio y superior; usando la escala descriptiva de 0 a 5 grados (Tabla 3), las evaluaciones se realizaron cada cinco días, iniciándose a los 19 a 74 días después de la siembra (dds).
Área Bajo la Curva del Progreso de la Enfermedad (ABCPE)
Con los datos de severidad se calcularon el valor del Área Bajo la Curva del Progreso de la Enfermedad (ABCPE), descrito originalmente en inglés como Area Under Disease Progress Curve (AUDPC), para lo cual se empleó la fórmula propuesta por Shaner y Finney (1977). Se realizó el análisis de va riancia (ANVA) y las comparaciones de medias de Tukey (α=0,05), usando el programa SAS (System Analysis Statistical).
Donde Yi:% de área foliar afectada por mildiu el día t ; T: periodos de evaluación; y n: número de evaluaciones.
Resultados y discusión
Detección de oosporas en semillas de quinua
Se observó la presencia de oosporas de P. variabilis en las 15 muestras analizadas (Figura 1A, 1B; Tabla 4). Las variedades; INIA-Altiplano, Salcedo INIA-Lambayeque y Kolicu presentaron el mayor número de oosporas 96, 80 y 64 respectivamente y las variedades Salcedo INIA-ECOSAC y Pasankalla presentaron el menor número de oosporas 10 y 8/100unidades de semilla. Resultados similares fueron obtenidos por Khalifa y Thabet (2018) detectaron oosporas y esporangios en las semillas de quinua en las variedades CICA y Real.
Tabla 2 Tratamientos de inductores de defensa para el control de Peronospora variabilis en el cultivo de Chenopodium quinoa. CIPA - UNP
| N° de trats. | Nombre comercial | Ingrediente activo | Dosis (L o kg / 200 L de agua) |
| 01 | Biosar | Aminoácidos y proteínas* | 1,0 |
| 02 | Biosar | Aminoácidos y proteínas | 0,5 |
| 03 | 3 Tac | Trichoderma spp* | 1,0 |
| 04 | 3 Tac | Trichoderma spp. | 0,5 |
| 05 | Agromos+Soil set | Manano oligosac. +CuSO4, Fe, Mn y Zn | 0,25 + 0,25 |
| 06 | Action FP/Pare | Fosfito de K/CuSO4-5H2O | 0,5/0,5 |
| 07 | Metalosate | Quelato de Cu* | 0,5 |
| 08 | Metalosate | Quelato de Cu | 0,35 |
| 09 | Testigo | ---- | ---- |
*= Dosis alta de los inductores de defensa.
Tabla 3 Grados de severidad de Peronospora variabilis en el cultivo de Chenopodium quinoa
| Grado de severidad | Características del área foliar afectado |
| 0 | Hojas sanas |
| 1 | 1% - 5% de área foliar afectada, pequeños puntos amarillentos |
| 2 | 6% - 15% de área foliar afectada y manchas amarillentas |
| 3 | 16% - 25% de área foliar afectada, manchas amarillentas en el haz y esporulación grisácea en el envés |
| 4 | 26% - 50% de área foliar afectada, manchas amarillentas, esporulación grisácea y pequeñas lesiones necróticas |
| 5 | 51% - 100% de área foliar afectada, amarillamiento generalizado, necrosis y defoliación |
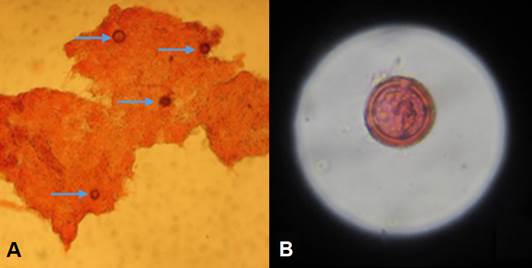
Figura 1 Estructuras de P. variabilis observadas en el microscopio compuesto aumento (40X). (A) presencia de oosporas inmersos en hojas infectadas. (B) oosporas de forma redondeada con doble pared celular.
Tabla 4 Número de oosporas detectadas Peronospora variabilis en semillas de Chenopodium quinoa
| Variedades | Procedencia | N° de oosporas /100 granos de semillas |
| INIA Altiplano | Puno | 96 |
| Salcedo INIA | INIA - Lambayeque | 80 |
| Koliku | Puno | 64 |
| Witulla | Puno | 47 |
| Blanca de Juli | Puno | 45 |
| Quellohua | Puno | 42 |
| Salcedo INIA | Cieneguillo | 42 |
| Amarilla de Junín | DRAP - Piura | 34 |
| Blanca de Junín | DRAP - Piura | 30 |
| Ccoyto | Puno | 28 |
| Amarilla marangani | DRAP - Piura | 17 |
| Wila | Puno | 16 |
| Salcedo INIA | CIPA - UNP | 15 |
| Salcedo INIA | ECOSAC - Piura | 10 |
| Pasankalla | Puno | 8 |
El-Assiuty et al. (2019) en Egipto reportan la presencia de oosporas, 90% en el pericarpio, 87% en la cubierta de las semillas y 3% en el embrión de oosporas en el pericarpio 90%, en la cubierta de las semillas 87% y 3% en el embrión. Así mismo, estudios realizados por Testen et al. (2014) indican que la semilla de quinua es una fuente de inóculo primario y medio de transmisión de las oosporas de mildiu. Investigadores como Pintore et al. (2016) y Thomas et al. (2017) señalan que las semillas de cucurbitáceas y albahaca con oosporas facilitan el movimiento del patógeno a nuevas regiones geográficas y a diferentes partes del mundo. Reportándose por primera vez mildiu causado porP. variabilisenC. quinoaen China (Hui et al., 2018). En Piura, se ha observado la presencia de oosporas inmersos en hojas infectadas de la campaña agrícola del CIPA-2014 (Figura 1A). Por otro lado, Khalifa y Thabet (2018) no detectaron oosporas en semillas de quinua de la variedad Hualhaus en Egipto. En este estudio se concluye que las semillas de quinua se comportan como fuente de inóculo primario del mildiu. Taha (2019) indica que la identificación de la fuente de inoculo es muy importante para prevenir la propagación de P. variabilis y el tratamiento de semillas con Metalaxil es muy efectivo para minimizar la incidencia del mildiu en el cultivo de cucurbitáceas (Thomas et al., 2017).
Epidemiología
Se registró los datos meteorológicos durante el desarrollo del estudio con una T° media de 24,9 °C y HR media 80,4%, estas condiciones favorecieron el desarrollo del patógeno en el departamento de Piura. Estas condiciones coinciden con las descritas por Risco y Mattos (2014), quienes reportan una T° de 15 a 25 °C y HR mayor a 80% que favorecen el desarrollo de la enfermedad de mildiu ocasionada por P. variabilis. Asimismo, en la parcela experimental del CIPA-UNP se ha observado la presencia de gotas de rocío en la superficie de hojas en primeras horas de la mañana (Figura 2). Danielsen y Ames (2014) indican que la presencia de una capa delgada de agua de rocío en las hojas a primeras horas de la mañana, permiten la germinación de esporangios, la penetración directa del patógeno sobre el tejido y el desarrollo de la enfermedad. Testen et al. (2014) observaron a los cinco días después de la inoculación (ddi) primeros síntomas y a los siete ddi observó esporulación grisácea, señalan que su periodo de incubación son seis días y es una enfermedad policíclica.
Descripción de síntomas de mildiu
34 dds se observó los primeros síntomas de la enfermedad, iniciando con la presencia de pequeños puntos amarillentos; posteriormente, tres a cuatro días se formó manchas cloróticas irregulares limitadas por las nervadura principal y lateral de la hoja (Figura 2A), después de cuatro días (38 dds) se realizó riego por inundación, creando condiciones muy favorables para el desarrollo agresivo de la enfermedad, alcanzando el tercio superior de la planta (Figura 3B), posteriormente, se observó el enrollamiento de hojas y la defoliación de la planta. Danielsen y Ames (2014) y Huamán et al. (2017), señalan que en condiciones de costa con alta humedad relativa y la siembra de variedades susceptibles, la enfermedad se presenta en forma epifitica y es más agresiva, ataca en diferentes estados fenológicos del cultivo, y en especial en plantas jóvenes ocasiona defoliación prematura, reducción del área fotosintética, y de esta manera afecta el rendimiento del cultivo. En el envés de las hojas y en la proyección de las manchas cloróticas se observó la formación de un moho grisáceo de aspecto algodonoso formado por esporangios y esporangióforos (Figura 4). Saravia et al. (2014) mencionan que la esporulación está relacionada con el grado de resistencia de las variedades, siendo abundante la esporulación en variedades susceptibles y poco o nada en variedades resistentes. En el presente estudio la variedad salcedo INIA, presentó una abundante esporulación, comportándose como susceptible en Piura.
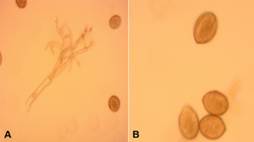
Características morfométricas de Peronospora variabilis
Se observó moho grisáceo en el envés de las hojas infectadas, constituido por esporangioforos y esporangios. Los esporangióforos midieron entre l56 y 231 µm de longitud y 8,0 y 12,3 µm de diámetro, con forma arborescente, ramificados dicotómicamente que terminan en 2 - 3 extremos flexuosos dispuestos en ángulo recto o agudo, en los que se insertan los esporangios (Figura 5A). Los esporangios fueron de forma ovoide con doble pared cuyo tamaño fue de 25,2 y 30,6 µm de largo y 18,6 y 23,6 µm de diámetro (Figura 5B) y con pedicelo. Los esporangios presentaron forma ovoide con doble pared cuyo tamaño fue 25,2 y 30,6 µm de largo y 18,6 y 23,6 µm de diámetro (Figura 5B), los esporangios presentaron pedicelo. Así mismo, se observó la formación de oosporas (Figura 1B) de forma esférica, con doble pared, oscuras, ligeramente rugosa y ondulada en la parte externa, protoplasma granulado, cuyo tamaño fue de 35 a 50 µm de diámetro. Estas características morfológicas del esporangióforos, esporangios y oosporas coinciden para la especie Peronospora variabilis por Khalifa y Thabet (2018) y Soylu et al. (2020), además realizan el primer reporte del mildiu causado por P. variabilis en C. album en la región del Mediterráneo Oriental de Turquía. P. variabilis infecta solo a las especies de Chenopodium y es un biótrofo obligado Thines y Choi (2016).

Figura 3 Síntomas de mildiu en hojas de quinua A) Manchas cloróticas irregulares, limitadas por las nervaduras en hojas, B) Ataque agresivo del patógeno.

Figura 4 (A) Signos de mildiu en hojas de quinua y (B) formación del moho grisáceo en el envés de la hoja, constituidas por esporangióforos y esporangios.
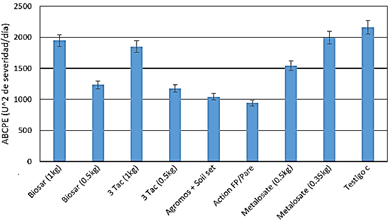
Severidad y área bajo la curva del progreso de la enfermedad (ABCPE)
A los 34 dds se presentó los primeros síntomas de la enfermedad, con menor severidad se obtuvieron con los tratamientos Agro mos+Soil set y Action FP/pare con 0,27%, y el testigo alcanzó 5,64%. A los 54 dds Action FP/pare obtuvo 40,39% y a los 59 dds el testigo alcanzó 56,07% donde en ambos se presentó mayor severidad y defoliación acelerada. En la última evaluación a los 74 dds, se evaluaron hojas de nuevos brotes, testigo alcanzó mayor severidad (57,27%) comparado con los tratamientos Action FP/Pare y Agromos+Soil set, que obtuvieron 17,2 y 18,49% de severidad (Tabla 5 y Figura 6). Estos resultados coinciden con el reporte de Risco y Mattos (2014) que a los 54 dds alcanzó el valor más alto de severidad en condiciones de La Molina-Lima en var. Pasankalla y en Egipto el pico más alto de severidad se registró a los 70 dds, esto se debió la baja humedad relativa que fue de 35-55% y la T° media 24 °C (Ahmed y Abdel-Wahed, 2018). El tratamiento testigo sin aplicación presentó el valor más alto del ABCPE con 2161,02, seguido de los tratamientos metalosate (0,35 kg) y biosar (1 kg) con 1994,50 y 1945,7 respectivamente y los valores más bajos se obtuvieron con Action FP/Pare y Agromos+Soil set con 939,82 y 1040,73 no habiendo diferencia estadística entre ellos, y los valores más bajos del ABCPE nos señalan que se obtuvo mejor control del mildiu (Figura 7). Los ingredientes activos de Action FP (Fosfito de K), Agromos (Manano oligosacáridos) y de Pare y Soil set (CuSO4.5H2O); son considerados como inductores de defensa de las plantas. Segun, otros autores como Manna et al. (2016); Tkaczyk et al. (2016); Santos et al. (2017); Yáñez-Juárez et al. (2017) indican que los fosfitos de K son utilizados como fuente de P en la nutrición, tienen mayor capacidad de penetrar a través de hojas y los sulfatos de cobre enrequicida con aminoacidos, acilita la asimilación y movimiento del cobre dentro de la planta y activan mecanismos de defensa bioquímica como proteínas PR y fitoalexinas y defensas estructurales (calosa) que inhiben la penetración y colonización en el tejido por los hongos. Los oligosacaridos son macromoléculas, biodegradables inducen resistencia y son protectores del estrés abiótico y bióticos como al ataque de Botrytis cinerea y Plasmopara viticola en el cultivo de vid (Falcón et al., 2015). Posiblemente este modo de acción tuvo los productos aplicados en el control del mildiu en quinua, por ende, se obtuvieron valores bajos en ABCPE. De manera similar, Sanabria (2019), en invernadero y campo con aplicaciones de fosfito de K obtuvo eficiente control de Phytophthora infestans.Soto y Cadenas (2018) con aplicación de oligosacáridos preventivamente indujeron defensa ante Lasiodiplodia theobromae en plantones de vid y Silva et al. (2019) lograron obtener menor severidad del ataque de Elsinoe ampelina en vid. Aminoácido glutamato activó la expresión de genes que sintetiza ácido salicílico y ácido jasmónico en las hojas de arabidopsis (Goto et al., 2020). Extractos de plantas y de algas tuvieron un efecto positivo sobre el vigor de las plantas de tomate inoculadas con Fusarium oxysporum al incrementar la altura y la acumulación de biomasa total (García et al., 2018). Ahmed y Abdel-Wahed (2018) muestran resultados de me nor ABCPE con las variedades Rainbow y American con 225,67 y 309,9 y el valor más alto lo obtuvo con la variedad Black con 2033,44. Dentro de la diversidad genética que tenemos en el Perú, se debe de realizar trabajos de investigación para obtener variedades tolerantes y/o resistentes al mildiu. Al determinar que las semillas de quinua se comportan como fuente de inóculo primario, antes de sembrar se debe de desinfectar las semillas con productos apropiados para evitar la germinación de las oosporas y complementar con las aplicaciones preventivas de los productos permitidos hasta los 30 dds. Los inductores de defensa Fosfito de K y Manano oligosacáridos, son opciones ecológicas que podrían ser incorporados en un paquete de estrategias del manejo de la enfermedad del mildiu.
Tabla 5 Progreso temporal de severidad y comparación de medias de Tukey (α = 0,05) del ABCPE como efecto de los inductores de defensa en el control de mildiu (Peronospora variabilis Gaum.) en el cultivo de quinua (Chenopodium quinoa Willd.) CIPA-UNP
| Trats. | 8-jun | 13-jun | 18-jun | 23-jun | 28-jun | 3-jul | 8-jul | 13-jul | 18-jul | 23-jul | 28-jul | 2-ago | ABCPE |
| 1era | 2da | 3era | 4ta | 5ta | 6ta | 7ma | 8va | 9na | 10ma | 11ma | 12ma | ||
| 19 dds | 24 dds | 29 dds | 34 dds | 39 dds | 44 dds | 49 dds | 54 dds | 59 dds | 64 dds | 69 dds | 74 dds | ||
| Biosar* | 0 | 0 | 0 | 1,01 | 8,11 | 7,37 | 40,97 | 45,05 | 44,50 | 27,42 | 51,91 | 39,64 | 1945,7 c |
| Biosar | 0 | 0 | 0 | 4,65 | 8,17 | 7,94 | 36,38 | 40,56 | 21,43 | 13,22 | 18,55 | 20,55 | 1234,5 b |
| 3 Tac* | 0 | 0 | 0 | 2,7 | 10,35 | 8,23 | 40,23 | 41,21 | 34,92 | 33,23 | 45,59 | 45,39 | 1850,3 bc |
| 3 Tac | 0 | 0 | 0 | 1,84 | 5,25 | 6,19 | 34,16 | 44,23 | 21,51 | 13,37 | 16,29 | 21,48 | 1178,6 b |
| Agromos+Soilset | 0 | 0 | 0 | 0,27 | 2,24 | 4,11 | 24,99 | 42,96 | 17,51 | 15,33 | 13,93 | 18,49 | 1040,7a |
| Action FP/Pare | 0 | 0 | 0 | 0,27 | 2,25 | 4,36 | 28,04 | 40,39 | 16,47 | 7,09 | 14,97 | 17,2 | 939,8 a |
| Metalosate* | 0 | 0 | 0 | 1,05 | 5,77 | 6,4 | 47,81 | 47,91 | 35,22 | 20,78 | 24,33 | 25,26 | 1545,9 b |
| Metalosate | 0 | 0 | 0 | 3,97 | 6,04 | 7,65 | 37,18 | 40,87 | 54,06 | 29,26 | 49,95 | 55,45 | 1994,5 c |
| Testigo | 0 | 0 | 0 | 5,64 | 9,5 | 10,4 | 37,11 | 50,49 | 56,07 | 30,33 | 50,41 | 57,27 | 2161,0 c |
*= Dosis alta de inductores de defensa; dds= días después de la siembra; 1ra, 2da, ……12ma= evaluaciones realizadas.
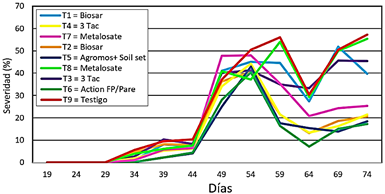
Figura 6 Curva de progreso de la enfermedad causada por Peronospora variabilis G. en el cultivo de quinua (Chenopodium quinoa W.) CIPA-UNP.
Conclusiones
Las semillas de quinua son fuente de inóculo primario de P. variabilis y como síntomas se observó manchas amarillentas en el haz y esporulación grisácea en el envés de las hojas. Los mayores efectos de inducción de defensa en el control de P. variabilis fue con los tratamientos Action FP/Pare y Agromos + Soil set. En el futuro ejecutar trabajos de investigación en la búsqueda de genotipos resistentes y realizar ensayos con otras moléculas en el control de la enfermedad del mildiu en quinua.