1. Introducción
En Ecuador la producción de almendra de cacao es limitada por la presencia de factores biológicos a enfermedades como: a) Mazorca negra, causado por Phytophthora spp; b) Podredumbre de mazorca, Moniliophthora roreri; c) Escoba de bruja, Moniliophthora perniciosa (Aime & Phillips, 2005; Guest, 2006). Este último patógeno interrumpe el equilibrio hormonal del huésped, provocando hipertrofias e hiperplasia seguido de necrosis tisular (Holliday, 1995), siendo clasificado como Marasmius perniciosaStahel en 1915, posterior nombrado como Crinipellis perniciosa en 1956 y hasta el 2005 por estudios de secuenciación al ADN-ribosomal se clasifica como Moniliophthora perniciosa (Stahel) (Aime y Phillips, 2005; Baker y Holliday, 1956; Stahel, 1915). Es un hongo basidiomiceto hemibiotrófico causante de la enfermedad (Escoba de Bruja) en cacao, con la proliferación de brotes verticales, con una gama de síntomas que varían en intensidad al tipo y la edad del tejido involucrado y la constitución genética del árbol (Baker & Crowdy, 1944).
M. perniciosa es hospedero para Theobroma spp, Herrania spp y biotipos específicos que ocasionan infecciones en especies de Solanáceas, Bixáceas y Malpighiaceas, donde su patogenicidad de cada biotipo no ha sido comprobada en T. cacao (Griffith et al., 2003; Griffith & Hedger, 1994b). Los factores que involucran al cambio de biotrófico a necrotrófico en M. perniciosa, depende a la disponibilidad de nutrientes solubles y fuentes de carbono especificas (Meinhardt et al., 2006). Donde las proteínas secretadas por el hongo son de importancia en las interacciones planta-patógeno, especialmente de hongos biotróficos (Allen et al., 2004). Estudios en M. perniciosa determinan una diversidad de síntomas en función de la biodiversidad de los ecotipos, con altos grados de patogenicidad y virulencia al hospedero (Wheeler & Mepsted, 1988). Por lo tanto, es necesario es tudiar y monitorear la variabilidad de M. perniciosa en los sitios de programas de mejora genética y en los sitios donde se introducen cultivares resistentes (Neto et al., 2005).
La caracterización a la variabilidad de M. perniciosa se ha basado en características morfológicas, análisis moleculares y relaciones bioquímicas con T. cacao (Griffith & Hedger 1994a; Lana et al., 2011). Cepas de M. perniciosa son analizados al empleo de polimorfismo de longitud de fragmento de restricción (RFLP), secuenciación del ADN ribosómico y al espacio de transcrito interno (ITS), donde estos han revela una alta variabilidad genética (Griffith & Hedger, 1994a). Esta región ITS es de gran interés para estudios de poblaciones y tipificación genética en M. perniciosa, de diferentes áreas de muestreo. También se ha amplificado las regiones consenso intergénicos repetitivos enterobacterianos (ERIC-PCR) (De Arruda et al., 2003; Osorio et al., 2012).
Este trabajo se enfocó al estudio de la biodiversidad de ecotipos de M. perniciosa con respecto a su distribución de distintos pisos altitudinales de zonas productoras de T. cacao del Ecuador. Información de importancia para entender la dinámica epidemiológica y sus niveles de agresividad de los aislados a su hábitat específico. Orientando el objetivo en caracterizar la biodiversidad de ecotipos y rangos de agresividad de Moniliophthora perniciosa, en Theobroma cacao L.
2. Materiales y métodos
La investigación se ejecutó en el Laboratorio de Microbiología y Biología Molecular de la Universidad Técnica Estatal de Quevedo (UTEQ), localizado en el Campus Universitario “Manuel Haz Álvarez” ubicado en el km 1.5 vía Quevedo - Santo Domingo. Sus coordenadas geográficas 01° 01” de latitud Sur y 79° 47” de longitud Occidental, ubicada a 73 msnm.
Muestreo y caracterización morfológica de M. perniciosa
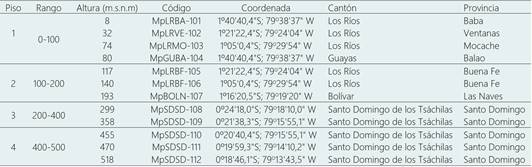
De plantaciones de huertas T. cacao L Nacional, se recolectó material vegetal con síntomas a la enfermedad por M. perniciosa (escobas secas), las muestras de tejido provenían de distintos pisos altitudinales. Se georreferenció y codificó su procedencia (Tabla 1).
El aislamiento del hongo se ejecutó según al protocolo descrito por Rocha & Wheeler (1985), las (escobas secas) se sumergieron en Benomyl al 2% por 24 h. Material vegetal se almacenó en un umbráculo a (8 h de humedad / 16 h de sequía por un mes) para estimular la producción de basidiocarpos y evaluar el Ø de basidiocarpos en los 12 ecotipos. Los experimentos contenían cuatro replicas y cada una con cuatro unidades experimentales.
Los basidiocarpos se extrajeron cuidadosamente y se fijaron desde su píleo al interior de la placa Petri superior para su descarga de basiodiosporas, las placas se agitaron por 24 h a 50 rpm/25 oC en oscuridad. Recuperando las basidiosporas en la solución colectora MES A [(g/L): 2-NMorpholinoethanensulfonic acid, 1,95; glicerol, 160 mL; agua destilada, 840 mL; 0,01% Tween-20 (pH 6,2)]. Estableciendo la concentración de las basidiosporas por la solución colectora (A), para establecer la producción de basidiosporas/ml. Con 10 µL de esta solución se ubicó en cámara de recuento Neubauer, para el conteo en cinco de los cuadrantes de 0,20 mm2, para determinar la concentración de basidiosporas= (número de células x 10.000) / (número de cuadros). 20 µL se ubicaron en portaobjeto para su visualización al microscopio OLYMPUS (ocular 10X y objetivo 40X). Además, se registró longitud y ancho de las basidiosporas en (µm) por el software IScapture. Los experimentos contenían cuatro replicas y cada una con cuatro unidades experimentales. Los valores a cada condición están representados por la desviación estándar promedio individual (±), los tratamientos fueron sujetos al análisis de varianza por ANOVA, y separados por procedimiento de comparación múltiple de Tukey SD, al nivel de significancia de (p ≤ 0,05), empleando Statgraphics.
Caracterización genética por amplificación de la región ITS y la generación de perfiles moleculares por ERIC-PCR
Los basidiocarpos frescos se pulverizaron en N2 líquido, obteniendo entre 400 mg, para iniciar con la extracción de ADNg, siguiendo las intrusiones del fabricante por DNeasy Plant Mini Kit de (QIAGEN-Start EE.UU.), la muestra se diluyó en 50 µL del tampón TE (Ácido tris-etilendiaminotetraacético 10 mM y EDTA pH 8,2). El ADNg se visualizó en geles de agarosa al 0,9 % teñidos en bromuro de etidio. Se realizó la identificación por PCR de los aislados de M. perniciosa empleando los oligonucleótidos universales ITS1 (5'-TCCGTAGGTGAA CCTGCGG-3') e ITS4 (5'-TCCTCCGCTTATTGATATGC-3') (White et al., 1990), que amplifican las regiones ribosomales, ITS (espacios de transcripto interno) que corresponde al gen del ADNr constituido por (ITS1 - 5.8S - ITS2) para su identificación. La PCR se realizó en un volumen de 20 µL con: 4 µL Buffer (1X), 1,2 µL de MgCl2 (6 mM), 1 µL de DNTP`s (0,2 mM), 1 µL / cada primer (0,2 mM), 0,2 µL de Taq pol (Promega®), 1 µL de ADN (60 ng/mL), 10,6 µL de H2O. La reacción de PCR se desarrolló en el termociclador (TECHME®). El perfil térmico de: 94 oC por 2 min; 35 ciclos a 94 oC por 1 min; 60 oC por 1 min; 72 oC por 1 min; extensión final de 72 oC por 10 min. Los productos amplificados se verificaron por electroforesis en gel de agarosa al 2% y teñidos en bromuro de etidio. Los fragmentos se determinaron por comparación con el marcador de peso molecular 100 bp (Invitrogen®). Al producto de amplificación obtenida para M. perniciosa se purificó empleando el kit Invitrogen PureLink™ (GERMANY®), siguiendo el protocolo descrito por el fabricante. El fragmento fue secuenciado por MACROGEN y comparado con la base de datos de GenBank de NCBI (https://www.ncbi.nlm.nih.gov/), empleando Basic Local Alignment Search Tool (BLAST). El árbol filogenético se construyó empleando el método Maximun Likelihood y alineados con múltiples secuencias a M. perniciosa disponible en NCBI. El porcentaje de la réplica del árbol se obtuvo con ‘bootstrap’ de valores de 1000 (Felsenstein, 1985). Se eligió el mejor modelo de acuerdo al criterio de información Bayesian (BIC), con el programa MEGA 6.06 (Tamura et al., 2013).
El protocolo de ERIC-PCR se realizó a lo descrito por Louws et al. (1994), con el empleo de los partidores ERIC-1R (5′ATGTAAGCTCCTGGGGATTCAC-3′) y ERIC-2F (5′AAGTAAGTGACTGGGGTGAGCG-3′), con algunas modificaciones, la PCR se realizó en un volumen de 20 µL con: 4 µL Buffer (1X), 1,2 µL de MgCl2 (6 mM), 1 µL de DNTP`s (0,2 mM), 1 µL / cada primer (0,2 mM), 0,2 µL de Taq pol (Promega®), 1 µL de ADN (60 ng/mL), 10,6 µL de H2O. La reacción de PCR se desarrolló en el termociclador (TECHME®). El perfil térmico de: 94 °C por 3 min; 40 ciclos a 94 oC por 1 min; 37 oC por 2 min; 72 oC por 2 min; extensión final de 72 oC por 10 min. Los productos amplificados se verificaron por electroforesis en gel de agarosa al 2% y teñidos en bromuro de etidio. Los fragmentos se determinaron por comparación con el marcador de peso molecular 100 bp (Invitrogen®). La información binaria de (0 y 1), se reemplazó por las letras (A y T) de los perfiles generados por ERIC-PCR. La historia evolutiva se infirió empleando el método Maximun Likelihood, el árbol filogenético se construyó empleando la distancia evolutiva de Tamura 3-parametro con el programa MEGA 6.06. Los grupos de cada nodo se fortaleció por un análisis de muestreo al ‘bootstrap’ 1000 repeticiones para un dendrograma estadísticamente robusto. Se eligió el mejor modelo de acuerdo al criterio de información Bayesian (BIC), con el programa MEGA 6.06 (Tamura et al., 2013).
Ensayo de agresividad de M. perniciosa en cacao nacional EET-19
El cacao nacional EET-19 se seleccionó por la susceptibilidad a esta enfermedad y evaluar la formación de síntomas producidos por los ecotipos a M. perniciosa. Las semillas se adquirieron de la colección de clones de cacao de la Finca Experimental La María de la Universidad Técnica Estatal de Quevedo. Las semillas se desinfectaron con NaClO al 5% por 3 min y sumergidas en H2O estéril, procediendo a su escarificación. Se ubicaron en contenedores plásticos con papel absorbente con 5 mL de H2O destilada estéril para su incubación a 28°C / 96 h y germinación de semillas. El proceso de infección se realizó a la metodología propuesta por Wheeler & Mepsted (1988), en cada semilla pregerminada se asperjo una suspensión de 5,5 x 104células/mL. El material vegetal se transfirió a contenedores plásticos con 140 g del sustrato con (50 / 50 %) de suelo franco limoso y turba (Novarbo seedling, black C1B), esterilizado por autoclave a 121 oC / 20 min. Se mantuvieron en cámaras húmedas al 90% a 28 ± 2 oC, por un fotoperiodo de (12 h luz / 12 h oscuridad), para asegurar la germinación y penetración del tubo germinativo de M. perniciosa y plántulas control sin el patógeno. A los 60 días de incubación se evaluó: diámetro del hipocótilo; número de brotes; porcentaje de inhibición al peso fresco radicular obtenido por: % inhibición= [crecimiento del testigo (g) - crecimiento del tratamiento (g) / crecimiento del testigo (g)] x 100. Los valores a cada condición están representados por la desviación estándar promedio individual (±), los tratamientos fueron sujetos al análisis de varianza por ANOVA, y separados por procedimiento de comparación múltiple de Tukey SD, al nivel de significancia de (p ≤ 0,05), empleando Statgraphics.
3. Resultados y discusión
Dimensiones de los basidiocarpos y producción de basidiosporas
Se dedujo variaciones morfométricas entre los ecotipos de M. perniciosa, donde se destaca el ecotipo de Los Ríos cepa MpLRBF-105, con mayor Ø del basidiocarpo de 3,1 cm, siendo proporcional al contenido de 6,41 x 107células/mL de basidiosporas (Figura 1). Los ecotipos: (MpLRBA-101, MpLRVE-102, MpGUBA-104, MpSDSD-109, MpSDSD-110, MpSDSD-111 y MpSDSD-112), no superan el Ø de 2 cm. A medida que se incrementa el piso altitudinal de 358 m.s.n.m (Tabla 1), estos ecotipos de Santo Domingo (MpSDSD-109, MpSDSD-110, MpSDSD-111 y MpSDSD-112) disminuyen su Ø al basidiocarpo no superando el 1,8 cm y el contenido de basidiosporas de 1,47 x 106 células/mL (Figura 1).
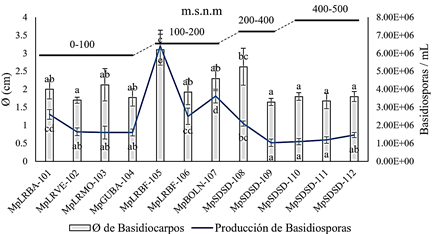
Figura 1 El Ø de basidiocarpos y producción de basidiosporas de M. perniciosa. Distribución respecto a los pisos altitudinales. Las barras de error indican ±DE; diferentes letras indican diferencias significativas entre los promedios a p < 0,05 (Test de Tukey).
Es importante destacar que la distribución geográfica al cultivo de T. cacao nacional ejerce cambios en los parámetros fisiológicos del hongo para su adaptación a estas condiciones climáticas modificando la estructura del hongo (Figura 2). Considerando que las descargas de basidiosporas para los 12 ecotipos de M. perniciosa corresponde a 24 h de recolección a 25 oC y una humedad relativa del 80%, estos son superiores a lo reportado por Mares et al. (2016), donde el promedio aproximado en descargas por basidiocarpo es de 400.000 células/mL de basidiosporas por 12 h de recolección. Estas diferencias en descargas de basidiosporas por M. perniciosa están determinadas por la variabilidad entre los ecotipos, donde el alto número de esporas liberadas por píleo está relacionado con el alto poder de dispersión del hongo (Andebrhan, 1988).

Figura 2 Formación de basidiocarpos de M. perniciosa de material vegetal de T. cacao nacional para los 12 pisos altitudinales del Ecuador. Formación de basidiocarpos de fragmentos de tejidos de (escobas secas), bajo cámaras húmedas.

Figura 3 Morfología del himenio bajo el sombrero de los basidiocarpos de M. perniciosa. a) Formación de láminas que llegan al estípite, b) Formación de lamélulas intercaladas pequeñas que inician al borde del sombrero, pero no llegan al estípite.
Las observaciones al himenio de los basidiocarpos presentan un incremento en formación de lamélulas intercaladas entre láminas, para las cepas (MpLRBF105 y MpBOLN107) de Los Ríos (Figura 3). Esto se explica que la diseminación de esporas en hongos formadores de basidiocarpos se relaciona el incremento de lamélulas adicionales entre láminas, esto optimiza 20 veces más la dispersión de esporas, a diferencias de superficies planas que carecen de lamélulas (Fischer & Money, 2010).
Dimensiones de basidiosporas de M. perniciosa
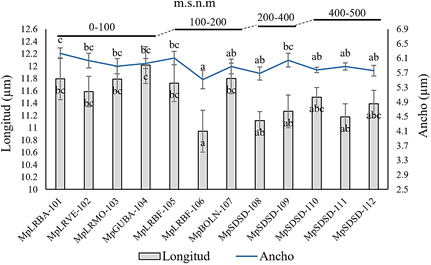
Los ecotipos de M. perniciosa que no superan los 200 m.s.n.m., corresponden las mayores dimensiones en longitudes de basidiosporas entre (11,58 a 12,01 µm) y ancho (6,23 y 5,95 µm), en las cepas (MpLRBA-101, MpLRVE-102, MpLRMO-103, MpGUBA-104, MpLRBF-105 y MpBOLN-107). Los ecotipos de Santo Domingo que superan los 200 m.s.n.m, sus cepas (MpSDSD-108, MpSDSD-109, MpSDSD-110, MpSDSD-111 y MpSDSD-112), no superan en longitud a 11,49 µm y ancho de 6,04 µm. El ecotipo de Los Ríos cepa MpLRBF-106, se verifica la menor dimensión de basidiospora con longitud y ancho de (10,94 y 5,51 µm) (Figura 4). Este carácter morfométrico de las basidiosporas ya difiere a los rangos observado por Rocha & Wheeler. (1985), con longitud y ancho promedios entre (11,9 a 6,4 µm) de las basidiosporas provenientes de plantaciones de cacao de INIAP-Pichilingue-Los Rios-Ecuador, ubicado a 74 m.s.n.m.
Los cambios en los aspectos morfológicos de M. perniciosa se deben a los efectos de las condiciones climáticas de cada ecotipo donde las basidiosporas de mayor tamaño se concentran en las cepas MpLRBA-101, MpLRVE-102, MpLRMO-103, MpGUBA-104, MpLRBF-105 y MpBOLN-107 (Figura 4). A medida que las esporas son más grandes el hongo tendrá mayor suministro de nutrientes, dándole tiempo y capacidad para superar un ambiente hostil (Kauserud et al., 2008). Las basidiosporas de menor tamaño corresponde para los ecotipos MpLRBF-106, MpSDSD-108, MpSDSD-109, MpSDSD-110, MpSDSD-111 y MpSDSD-112 (Figura 4), estas cepas corresponden a un mecanismo de mayor dispersión de la enfermedad. Se puede definir que esa evolución favorece a un compromiso: esporas de un tamaño pequeño para la dispersión expansiva a larga distancia y las esporas de gran tamaño para reservas de nutrientes a corta distancia (Stearns, 1992).
Relación filogenética de los ecotipos de M. perniciosa a su distribución altitudinal del Ecuador
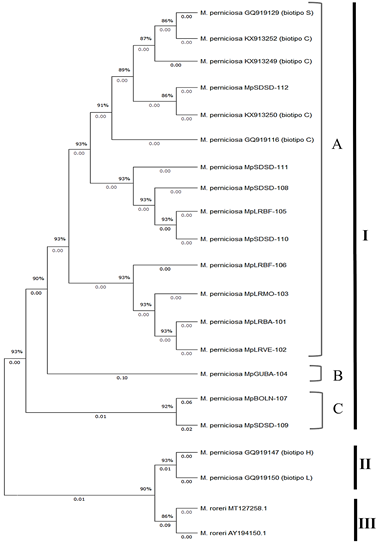
El análisis filogenético por secuenciación a la región ITS1, ITS2 y el gen 5.8S del ADNr de los 12 ecotipos de M. perniciosa se agrupan en tres clados principales con un soporte de bootstrap del 86 al 98 %. El Grupo I reúne al Sub-grupo A, con nueve de los ecotipos M. perniciosa del Litoral Ecuatoriano las cepas (MpLRBA-101, MpLRVE-102, MpLRMO-103, MpLRBF-105, MpLRBF-106, MpSDSD-108, MpSDSD-110, MpSDSD-111 y MpSDSD-112) y cuatro cepas al biotipo C que corresponde a la capacidad patogénica del hongo a T. cacao, obtenidas de NCBI con su número de accesión (Figura 5). La formación del Sub-grupo B, se defiende la hipótesis que la cepa MpGUBA-104 sea el centro de dispersión de la enfermedad, y a partir de ahí, junto con el movimiento de material de siembra se ha diseminado M. perniciosa en Ecuador. La formación del Sub-grupo C, reúne a dos de los ecotipos de M. perniciosa del Litoral Ecuatoriano cepas (MpBOLN-107 y MpSDSD-109). Demostrando la existencia de variabilidad genética por los distintos agrupamientos de M. perniciosa, para cada acopito. A diferencia del trabajo reportado por Maridueña et al. (2019), en la caracterización genética por la región ITS de M. perniciosa de 9 regiones del Ecuador, se ven agrupados en un solo clado no mostrando variabilidad genética. La variabilidad genética encontrada en este trabajo corresponde a la procedencia del patógeno, para sus distintas zonas agroecológicas y plantaciones de T. cacao nacional entre los 40 y 20 años de edad del Litoral Ecuatoriano. Se puede explicar que en algunas regiones geográficas se presume que M. perniciosa ha coevolucionado con su hospedero de T. cacao (De Arruda et al., 2003; Purdy & Schmidt, 1996). Siendo congruente con el desarrollo histórico, de la enfermedad “Escoba de Bruja” se reportó en Ecuador cantón Balao Provincia del Guayas entre (1918 y 1922). En junio de 1923 en la provincia de “Los Ríos”, la principal zona productora de T. cacao nacional (Garces, 1946). Donde trabajos de comparación de secuencias a la región ITS, se evidencia variabilidad genética para M. perniciosa dentro una misma región cacaotera de Bahia-Brasil y también entre años de observación (Gramacho et al., 2007).
Los resultados al análisis filogenético el biotipo-S que infecta a solanáceas está agrupado conjuntamente con el biotipo-C patogénico a T. cacao Grupo I, esto coinciden a los obtenidos por Artero et al. (2017), estos dos biotipos se agrupan en base a su semejanza genética. La distribución de M. perniciosa se extiende desde la cuenca del Amazonas hasta la frontera con Bolivia y registrando como patógeno en una variedad de especies de solanáceas (Lisboa et al., 2020). Estos dos biotipos (C y S) de patógenos son formadores de escobas y están estrechamente relacionadas por exhibir poca variabilidad genética a su estrategia de reproducción homotálico (Artero et al., 2017). Donde se concluye que los biotipos (C y S) no son genéticamente distintos y comparten una expresión similar a la enfermedad: indicando un grado de conservación de los mecanismos de patogenicidad entre los dos biotipos (Marelli et al., 2009).
El Grupo II reúne a los biotipos (H y L), de acuerdo con su adaptación a diferentes hospedantes, donde el biotipo-H infecta a la familia Malpighinaceae; biotipo-L asociado a infecciones a la familia Bignoniaceae (Marelli et al., 2009). La formación de este clado indica un grado de distinción genética dentro M. perniciosa (Figura 6), este resultado representa un grupo ecológicamente distinto para un estilo colonización endofítica no patogénica y siendo variable a su mecanismo de cruzamiento bifactorial, correspondiente al biotipo L (Griffith & Hedger, 1994b). Adicionalmente el Grupo III representa a M. roreri agrupado en un clado separado en el árbol filogenético (Figura 6).
Secuencias de 12 aislados del Litoral Ecuatoriano, siete cepas de M. perniciosa y dos aislados de M. roreri obtenidas de NCBI (indican el biotipo y el número de accesión). Las distancias evolutivas se basaron a Tamura 2-parameter. Las distancias horizontales son proporcionales a las distancias filogenéticas expresadas en sustituciones para un porcentaje de 1000 repeticiones.
La amplificación de secuencias Repetitivas de Consenso Intergénico de Enterobacterias (ERIC-PCR) para los 12 ecotipos de M. perniciosa, generó un perfil genético que varían en tamaño desde 100 a 2500 pb (Figura 6). Los resultados sugieren que la técnica de ERIC-PCR provee un método alternativo válido para la diferenciación de cepas de M. perniciosa.
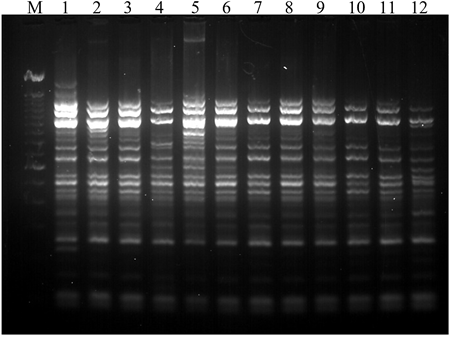
Figura 6 Perfil molecular por ERIC-PCR de M. perniciosa aislados de 12 ecotipos de T. cacao. Del carril 1 - 12 (MpLRBA-101, MpLRVE-102, MpLRMO-103, MpGUBA-104, MpLRBF-105, MpLRBF-106, MpBOLN-107, MpSDSD-108, MpSDSD-109, MpSDSD-110, MpSDSD-111 y MpSDSD-112); M, marcador de masa molecular (Lader 100 bp Invitrogen).
El análisis filogenético por ERIC-PCR genera dos grandes grupos, el Grupo I reúne siete ecotipos distribuidos en tres Provincias (Santo-Domingo, Bolívar y Guayas). El Grupo II, reúne los cinco ecotipos para la Provincia de Los Ríos de M. perniciosa (Figura 7). Esta variación genética ocurre cuando alguna modificación de las condiciones ambientales crea un nicho vacío, activando la selección natural hasta que la población alcanza un nuevo pico de adaptabilidad (González & Rojas, 2014). En este trabajo el producto evolutivo entre M. perniciosa y T. cacao, dependen de su adaptabilidad para evolucionar así resumiendo en un solo concepto: adaptación. Estos resultados también concuerdan con De Arruda et al. (2003), quienes en la evaluación molecular por ERIC-PCR de 50 aislados de M. perniciosa provenientes de T. cacao (biotipo C), H. acutifoliae (biotipo H) y S. lycocarpum (biotipo S) encontraron agrupaciones de acuerdo con el hospedero, mostrando una considerable variabilidad intraespecífica dentro de los aislados provenientes de T. cacao, además la existencia de correlación entre el origen geográfico de M. perniciosa con el polimorfismo de los Grupos.
Origen de escobas axilares e hipertrofia del hipocótilo por infección de M. perniciosa
Los síntomas de mayor grado de agresividad por infección de M. perniciosa dieron origen a escobas axilares de diferentes tamaños con la proliferación de brotes laterales, estos presentaron la formación de escobas cotiledonales con (4 a 11 escobas axilares) para los ecotipos MpLRBF-105, MpGUBA-104, MpLRMO-103, MpLRVE-102, de plantaciones de cacao que no superan los 200 m.s.n.m. A diferencia de los ecotipos MpLRBF-106, MpBOLN-107, MpSDSD-108, MpSDSD-109, MpSDSD-110, MpSDSD-111 y MpSDSD-112 de pisos altitudes superiores a los 200 m.s.n.m., los síntomas a la enfermedad disminuyen en cacao no superando los dos brotes (Figura 8). Las diferencias al grado de agresividad están influenciadas por la variabilidad genética del ecotipo de M. perniciosa, donde los ensayos se mantuvieron bajo las mismas condiciones en invernadero.
Las diferencias observadas en los ensayos de agresividad de infección para los ecotipos de M. perniciosa del Litoral Ecuatoriano coinciden con trabajos de infección de este patógeno en clones de cacao (ICS-1, Sca-6 y SIC-23), con diferentes grados de agresividad y potencial de adaptación de M. perniciosa en diferentes áreas geográficas a la región cacaotera de Bahia-Brasil (Gramacho et al., 2016). Las plantaciones de T. cacao nacional para las provincias de Los Ríos y Guayas (MpLRBF-105, MpGUBA-104, MpLRMO-103, MpLRVE-102), se encuentran aledañas a las mayores extensiones de T. cacao clon CCN-51 con tolerancia a M. perniciosa. A diferencia de la Provincia de Santo Domingo el 56,8 % de la superficie T. cacao corresponde a plantaciones con menos de cinco ha y la asocian con otras especies agrícolas (Anzules et al., 2018). Esto sugiere que probablemente la mayor agresividad de estas cepas se deba al aumento de la presión de selección impuesta por este clon en estas Provincias. Basándonos en este criterio de agresividad de la enfermedad coincide con Santos et al. (2017), los aislamientos de M. perniciosa procedentes de clones de cacao TSH565 y TSH516 (resistentes), resultan tener mayor agresividad hacia los genotipos de cacao.
Los cambios fisiológicos por hipertrofia del hipocótilo se verifican diámetros de 0,97 y 0,905 cm en plántulas EET-19, por inoculación de los ecotipos MpGUBA-104 y MpLRVE-102 respectivamente. A diferencia de la planta no tratada el Ø es 0,66 cm, todos los ecotipos de M. perniciosa causan efectos de hipertrofia en las plántulas de cacao que oscilan en Ø 0,74 a 0,84 cm (Figura 8). Estas alteraciones por la proliferación de brotes laterales y entumecimiento del hipocótilo a causa de M. perniciosa, estaría vinculado con la interferencia directamente del metabolismo hormonal del cacao, donde este patógeno es capaz de producir la hormona vegetal auxina (Teixeira et al., 2015). También la agresividad de la enfermedad se acentúa en plantas jóvenes de cacao donde sus hojas son más susceptibles a la infección por M. perniciosa, para la formación de la escoba de bruja (Purdy & Schmidt, 1996).
Disminución del sistema radicular por infección de M. perniciosa
Los cambios fisiológicos sobre la arquitectura del tejido radicular por efecto de la aplicación de ecotipos de M. perniciosa en semillas de T. cacao (EET-19), el mayor porcentaje de inhibición del peso fresco radicular es del 68 % en presencia del ecotipo MpGUBA-104 (Figura 9). En cierta medida el tejido radicular se vio afectado mayor al 30 % por los ecotipos MpLRBA-101, MpLRVE-102, MpLRMO-103, MpLRBF-105, MpLRBF-106, MpSDSD-110 y MpSDSD-111. En comparación a las semillas sin tratar con el patógeno (Figura 9).
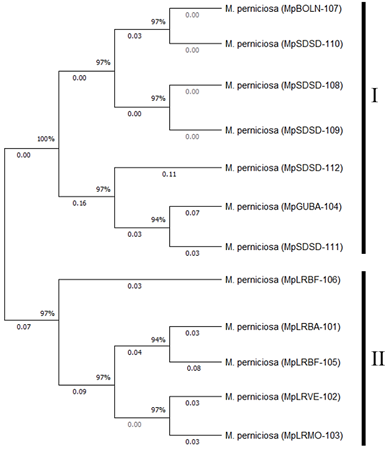
Figura 7 Árbol filogenético basado al método Maximun Likelihood de ecotipos de M. perniciosa. Las distancias evolutivas se basaron a Tamura 2-parameter. Las distancias horizontales son proporcionales a las distancias filogenéticas expresadas en sustituciones para un porcentaje de 1000 repeticiones.
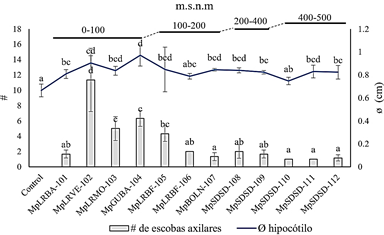
Figura 8 Severidad de infección por ecotipos de M. perniciosa en cacao nacional EET-19. Evaluación del aspecto fisiológico al Ø del hipocótilo y # de brotes. Las barras de error indican ±DE; diferentes letras indican diferencias significativas entre los promedios a p < 0,05 (test de Tukey).
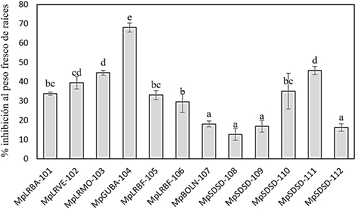
Figura 9 Porcentaje de inhibición del tejido radicular por ecotipos de M. perniciosa en cacao nacional EET-19. Las barras de error indican ±DE; diferentes letras indican diferencias significativas entre los promedios a p < 0,05 (test de Tukey).

Figura 10 Síntomas a la generación de escobas cotiledonales e inhibición del tejido radicular provocados por los ecotipos de M. perniciosa del Ecuador en plántulas de cacao (ETT-19). a) La mayor formación de escobas axilares por MpLRVE-102; b) La mayor incidencia en inhibición radicular por MpGUBA-104.
Generación de escobas cotiledonales e inhibición del tejido radicular por infección de M. perniciosa
Se verificó que todas las cepas evaluadas fueron capaces de inducir síntomas típicos de escobas de bruja, evidenciando la infección por M. perniciosa, donde la severidad de infección inicia a los 60 días después con periodos de drásticas alteraciones morfológicas y fisiológicas. Esto ha llevado a la inhibición del sistema radicular, por los ecotipos de Los Ríos (MpLRVE-102) y Guayas (MpGUBA-104), siendo las más agresivas en relación con los demás ecotipos (Figura 10). Uno de los cambios notables en ETT-19 durante la infección por M. perniciosa es la disminución y/o hipertrofia del sistema radicular. Estos cambios a la reducción de biomasa radicular, puede ser por la alteración del gradiente de auxina que regula la dominancia apical en las plantas (Marelli et al., 2009).
4. Conclusiones
Este trabajo ha permitido corroborar la variabilidad de M. perniciosa con dependencia a los distintos pisos altitudinales que se viene cultivando el cacao en Ecuador, observando cambios en su morfología y distintos grados de agresividad dentro de los 12 ecotipos de M. perniciosa sobre ETT-19. Se debe ampliar la observación en la formación de lamélulas que estarían relacionadas a la dispersión de las esporas y su tamaño. Se definieron dos cepas agresivas MpGUBA-104 y MpLRVE-102 aledañas a las mayores extensiones de T. cacao clon CCN-51. Por consiguiente, se debe plantear el empleo de distintos clones, donde estos aporten genes de diversas fuentes de resistencia para disminuir la presión de selección sobre el patógeno y el desarrollo de cepas más virulentas.