1. Introducción
La semilla es uno de los factores tecnológicos de mayor importancia al ser considerada como el insumo básico en los sistemas de producción agrícola ligado directamente al potencial de rendimiento o productividad de los cultivos (Paliwal, 2001). Asimismo, son el producto final de los programas de fitomejoramiento, los cuales son exitosos solamente cuando ese producto puede llegar y ser efectivamente utilizado por los agricultores a través de un programa eficiente de producción que defina los objetivos y las necesidades específicas de quienes lo utilizan.
En los sistemas de semillas, la calidad entendida desde sus cuatro atributos (fisiológico, genético, sanitario y físico) es fundamental para su producción. Una semilla de baja calidad limita el rendimiento potencial, reduce la productividad (FAO, 2006) e incrementa el riesgo de plagas y patógenos, entre otros problemas; esto ligado a los procesos de obtención y distribución de semilla los cuales poseen elementos adicionales que incrementan la complejidad de estos procesos. Por ende, se requiere de lineamientos claros y definidos para producir semilla de calidad y en cantidad.
La calidad de las semillas se puede ver afectada directa e indirectamente por la contaminación por hongos. En el caso de los primeros dos grupos, las pérdidas causadas pueden ocurrir durante las etapas de desarrollo, almacenamiento o germinación. El daño resulta en la pérdida de la viabilidad de la semilla o en la infección de la plántula después de la germinación. Así mismo condiciones de alta humedad y temperatura en las etapas de cosecha y postcosecha aumentan la incidencia de hongos, que pueden aparecer en la fase de almacenamiento si la temperatura y la humedad no se mantienen adecuadamente (Amza, 2018).
La afectación directa se atribuye al crecimiento y desarrollo del hongo en la semilla y la producción de metabolitos como micotoxinas. Entre las reportadas con mayor frecuencia están las aflatoxinas, obtenidas principalmente del género Aspergillus y las ocratoxinas, producidas por Aspergillus y Penicillium (Omori et al., 2018).
La afectación indirecta está asociada con la transmisión y establecimiento de problemas fitosanitarios que generan reducción en la germinación y vigor de la semilla, o infección de la plántula posterior a la germinación que ocasiona pérdidas en la productividad (Amza, 2018). Desde un punto de vista económico, los hongos transmitidos por semillas se pueden clasificar en tres grupos: (a) patógenos de plantas que son transmitidos por semillas, los cuales invaden la semilla durante su desarrollo o madurez, (b) hongos que reducen la calidad de las semillas y los granos, generalmente hongos saprófitos no especializados que invaden el grano maduro húmedo y (c) hongos que no generan efectos perjudiciales (Martín et al., 2022).
Un patógeno transmitido por semilla puede causar el aborto, la pudrición o necrosis de esta y la reduc ción o eliminación de la capacidad de germinación, así como el daño de las plántulas que resulta en el desarrollo de enfermedades en etapas posteriores del crecimiento por infección sistémica o local (Naqvi & Rehman, 2013, Goko et al., 2021; Hill et al., 2021).
Es así como en los últimos años, el panorama agrícola mundial ha enfrentado una preocupación creciente por la aparición y diseminación de enfermedades destructivas propagadas a través de las semillas (Martín et al., 2022). Este fenómeno subraya el papel crítico que desempeñan las semillas como posibles vectores para la transmisión de varios patógenos capaces de causar daños sustanciales a los cultivos. Esta diseminación ha llevado a riesgos más elevados, ya que estos patógenos encuentran nue vos entornos y hospederos en los que establecerse (Dell’Olmo et al., 2023). Una consecuencia particularmente preocupante de este fenómeno es el potencial de pérdidas de rendimiento de hasta un 50%, atribuidas a la actividad de hongos transmitidos por semillas responsables de provocar enfermedades fúngicas (Erasto et al., 2023). En este contexto, la identificación y caracterización de contaminantes fúngicos es un componente esencial del manejo enfocado a reducir la afectación en la cali dad de semilla (Naqvi & Rehman, 2013).
El objetivo de este trabajo fue identificar y determinar la prevalencia de los contaminantes fúngicos presentes en la semilla de trece variedades vegetales de cuatro especies agrícolas de interés comercial: arroz, soya, maíz y sorgo dulce forrajero producidas en el municipio de El Espinal, Tolima, Colombia.
2. Metodología
Lugar de estudio
Esta investigación se realizó en el 2021, en los Laboratorios de Microbiología Agrícola y Producción Vegetal del Centro de Investigación Tibaitatá de la Corporación Colombiana de Investigación Agropecuaria (AGROSAVIA), ubicado en el municipio de Mosquera del departamento de Cundinamarca (Colombia), latitud N 4º41'43.1349'', longitud W 74º12'18.7666'', y altitud de 2600 m.
Material vegetal
Las semillas usadas para el experimento fueron obtenidas de los campos de multiplicación de semilla ubicados en El Espinal - Tolima durante el primer semestre del 2021 y correspondieron a trece variedades vegetales producidas en cuatro especies agrícolas de interés comercial: arroz (AGRVA1 y AGRVA2); soya (AGRVSY1, AGRVSY2, AGRVSY3, AGRVSY4, AGRVSY5, AGRVSY6 y AGRVSY7); maíz (AGRVM1, AGRVM2 y AGRVM3), y sorgo dulce forrajero (AGRVSR1).
Aislamiento y purificación de los patógenos
Por medio de un blotter test modificado (técnica de diagnóstico de patógenos en semillas) (Agarwal & Gaur, 1997; Tsedaley, 2015) se identificó, caracterizó y determinó la prevalencia de los contaminantes fúngicos presentes en la semilla. En recipientes plásticos herméticos de capacidad de 0,9 L con doble servilleta estéril (toallas absorbentes en Z 24 cm x 25 cm) se generaron condiciones de cámara húmeda con agua destilada estéril. Sobre la servilleta húmeda fueron dispuestas las semillas de cada material por separado con tres repeticiones por material, cada una con 50 semillas que constituyeron la muestra de evaluación. Las semillas dispuestas por recipiente fueron sometidas a condiciones de temperatura entre 25 °C ± 3 C y HR ~ 90% ± 5% por siete días (Ordon et al., 2009).
Siete días después del montaje de las cámaras húmedas se revisaron todos los recipientes con las muestras con el fin de observar el crecimiento micelial de hongos presentes en la semilla (Ordon et al., 2009). El micelio emergente sobre la superficie de las semillas fue sembrado posteriormente en medio PDA pH 4,5 (Ajustado con Ácido Láctico) o PDA + Cloranfenicol. Los aislamientos se incubaron en oscuridad a 25 °C durante 7 días. El micelio generado de los aislamientos de los tejidos se repicó en el mismo medio de cultivo.
Al finalizar el proceso de germinación en cámaras húmedas, siete días después de la siembra para todas las variedades (Ordon et al., 2009; Wain-Tassi et al., 2012; Chrapačienė et al., 2022), se determinó el % de germinación total, % de semillas sanas, % de semillas sanas germinadas y % de prevalencia de hongos contaminantes diferenciado por género de hongo contaminante y semilla germinada o sin germinar (Ordon et al., 2009).
Identificación molecular
Los aislamientos puros fueron identificados molecularmente. Se realizó la extracción de ADN de acuerdo con la metodología propuesta por Griffith & Shaw (1998). Posteriormente, se realizó la amplificación por PCR con los primers ITS1F-ITS4 (ITS1-F 5ʹ-CTTGGTCATTTAGAGGAAGTAA-3ʹ y ITS4 5ʹ-TCCTCCGCTTATTGATATGC-3ʹ). Las secuencias resultantes fueron comparadas con la región ITS1-5.8S- ITS2 correspondiente de las secuencias de la base de datos GenBank del Centro Nacional para la Información Biotecnológica (NCBI, 2022). Los biotipos de hongos aislados se conservaron en medio PDA a -4 °C (tres copias de cada aislamiento) y en Crioviales en solución de crioconservación (Glicerol 20 % y Peptona al 0,5 %) a -80 °C.
Análisis estadístico
Para la determinación de prevalencia de hongos contaminantes en semilla de las diferentes variedades se utilizó un diseño en bloques al azar con trece tratamientos (variedades) tres repeticiones y un recipiente con 50 semillas como unidad experimental. Se determinaron medidas de tendencia central y análisis multivariado con el programa R Studio® (R Core Team, 2020).
3. Resultados y discusión
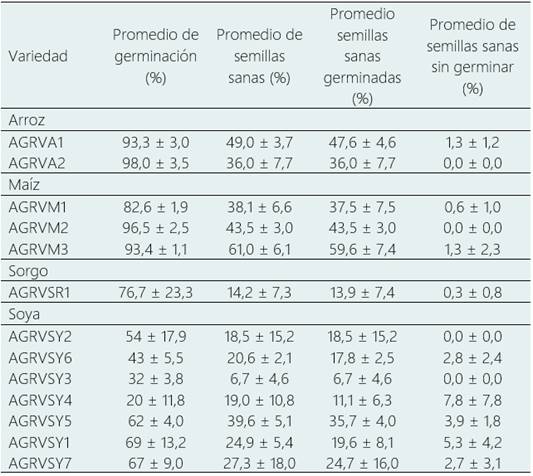
Las variedades de arroz AGRVA1 y AGRVA2 y de maíz AGRVM2 y AGRVM3 presentaron porcentajes de germinación superiores al 90% y esta última mostró el mayor porcentaje de semillas sanas y semillas sanas germinadas. Los porcentajes de germinación más bajos se observaron en las soyas AGRVSY6, AGRVSY3 y AGRVSY4, estas dos últimas con porcentajes más bajos de semillas sanas y sanas germinadas. En general los porcentajes de semillas sanas sin germinar fueron inferiores al 8 % (Tabla 1).
Se obtuvieron en total 65 aislamientos de hongos que, por su morfología macroscópica, microscópica y signos en la semilla fueron agrupados en 28 morfotipos los cuales fueron identificados molecularmente (Tabla 2). En AGRVSY2 se obtuvieron 8 aislamientos. En sorgo (AGRVSR1) se encontraron 7 hongos. En AGRVSY3, AGRVSY4, AGRVSY5, AGRVSY6 y AGRVSY7 se aislaron 6 hongos de cada variedad. Del material AGRVA1 fueron aislados 2 hongos, mientras que de AGRVA2, AGRVSY1 y AGRVSY7 se obtuvieron 3 aislamientos. En los cultivares de maíz AGRVM3, AGRVM2 y AGRVM1 se hallaron entre 2 y 4 aislamientos (Anexos).
A partir del blotter test fue posible distinguir diferentes signos de afectación en la semilla de cada uno de estos materiales, como la presencia de estructuras reproductivas (conidióforos) del género Aspergillus (cabeza negra, verde claro) o el crecimiento de micelio de diferentes colores y morfologías de hongos filamentosos (Figura 1).
Figura 1. Presencia de hongos filamentosos contaminantes en semillas de soya, arroz, sorgo y maíz. De izquierda a derecha y de arriba abajo: Fusarium equiseti en soya, Aspergillus awamori en soya, Diaporthe sp. en soya, Aspergillus flavus en soya, Lasiodiplodia theobromae en soya, Fusarium equiseti en soya, Aspergillus flavus en soya, Fusarium oxysporum en arroz, Curvularia penniseti en arroz, Fusarium proliferatum en arroz, Aspergillus flavus en arroz, Aspergillus niger en maíz, Fusarium verticillioides en maíz, Fusarium verticillioides en maíz, Penicillium sp. en maíz, Aspergillus niger en sorgo, Curvularia lunata en sorgo, Diaporthe melonis en sorgo, Talaromyces pinophilus en sorgo, Aspergillus flavus en sorgo.
Soya
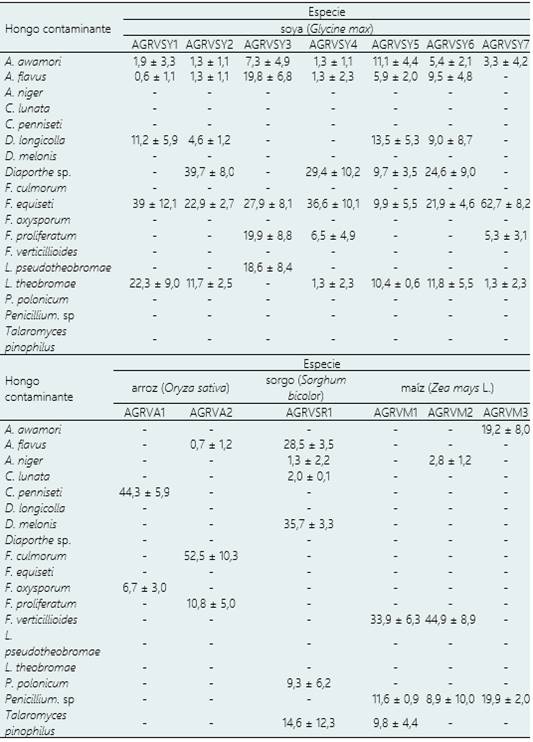
En semilla de soya se identificaron 8 especies de hongos filamentosos. Fusarium equiseti y Diaporthe sp. fueron las más frecuentes en cada uno de los materiales evaluados y las de mayor prevalencia en semillas sin germinar. Algunas especies como A. awamori estuvieron presentes en la semilla de todos los materiales, pero presentaron un porcentaje de prevalencia bajo en semillas sin germinar con respecto a otros hongos (Tabla 3).
Los resultados encontrados en la semilla de soya analizada son similares a otros estudios donde se relacionan a las especies Aspergillus spp. Fusarium equiseti, Diaporthe longicolla y Penicillium citrinum como las más frecuentes (Fresneda et al., 2009; Escamilla et al., 2019).
Fue posible evidenciar que en los tres cultivares de soya existe una relación directamente proporcional entre la prevalencia de especies de Fusarium y de Diaporthe. Esto es similar a los hallazgos de Gally (2006) que indica que Fusarium equiseti ha sido reportado junto con otras especies de este género como F. solani, F. moniliforme, F. oxisporum y F. graminearum en la zona pampeana de Argentina, las cuales se encuentran asociadas a Diaporthe/Phomopsis. En el presente estudio se identificó más de una especie del género Diaporthe en semilla de soya. Esto concuerda con Nishmitha et al. (2021) quienes reportan que en soya, P. phaseolorum, P. longicolla, P. eres y P. helianthi pueden infectar con éxito y causar lesiones.
Se encontró que los patógenos del género Fusarium tienden a presentar una mayor prevalencia en las semillas no germinadas. Esto sugiere que su presencia puede afectar la calidad fisiológica de la semilla de soya. Lo anterior es señalado por Formento et al. (2016) quienes encontraron varias especies de Fusarium en las semillas de soya las cuales ocasionaron podredumbre y muerte de la semilla, y determinaron una correlación negativa y significativa entre la germinación y la incidencia de Fusarium. Los bajos resultados de germinación de semilla (< 70%) se asocian con la mayor prevalencia de Fusarium equiseti. Esto concuerda con Fresneda et al. (2009), quienes encontraron que el género Fusarium se incrementa en la semilla con germinaciones por debajo de 85%, pues en soya es considerado el hongo que produce mayor número de pudriciones, asociado a altas temperaturas y alta humedad al final del ciclo del cultivo.
Tabla 1. Porcentaje de semillas sanas (germinadas y no germinadas) en trece variedades vegetales producidas de arroz, maíz, soya y sorgo
Tabla 2. Resultados de identidad en GenBank de secuencias ITS del ADNr de hongos aislados de semillas
Morfotipo
Especie de procedencia
Identidad en GenBank
Tamaño (pb)
Accesión
D01
Soya
Aspergillus awamori
100,00%
559
KX621965.1
D02
Soya
Aspergillus awamori
100,00%
559
KX621965.1
D03
Soya
Fusarium equiseti
99,78%
530
KU565733.1
D04
Soya
Fusarium proliferatum
99,56%
536
KY848358.1
D05
Soya
Diaporthe longicolla
93,77%
585
MT012104.1
D06
Soya
Diaporthe sp.
99,22%
653
MG976358.1
D07
Soya
Aspergillus flavus
100,00%
552
HQ122936.1
D08
Soya
Lasiodiplodia theobromae
99,79%
520
MT075442.1
D09
Soya
Diaporthe sp.
99,41%
653
MG976346.1
D10
Soya
Fusarium equiseti
100,00%
485
MF993089.1
D11
Soya
Diaporthe sp.
99,18%
486
KF466206.1
D12
Soya
Fusarium proliferatum
99,58%
555
MK817049.1
D13
Sorgo
Diaporthe melonis
86,73%
602
MT422108.1
D14
Sorgo
Aspergillus flavus
100,00%
565
LC106118.1
D15
Sorgo
Talaromyces pinophilus
100,00%
584
MK336630.1
D16
Sorgo
Aspergillus niger
100,00%
568
MN474007.1
D17
Sorgo
Penicillium polonicum
100,00%
578
MT487786.1
D18
Sorgo
Curvularia lunata
100,00%
684
MK204512.1
D19
Arroz
Aspergillus flavus
100,00%
563
MT528892.1
D20
Arroz
Fusarium culmorum
100,00%
506
MK226295.1
D21
Arroz
Fusarium oxysporum
100,00%
511
MN988760.1
D22
Arroz
Fusarium proliferatum
100,00%
553
MT123028.1
D23
Maíz
Aspergillus niger
99,62%
597
MH855928.1
D24
Maíz
Penicillium sp.
99,60%
575
MN093874.1
D25
Maíz
Fusarium verticillioides
99,78%
520
MK790050.1
D26
Maíz
Talaromyces pinophilus
86,34%
576
MK646032.1
D27
Soya
Lasiodiplodia pseudotheobromae
99,57%
531
MN887200.1
D28
Arroz
Curvularia penniseti
99,80%
571
MH858447.1
Tabla 3. Prevalencia (en %) de hongos aislados en semilla de trece variedades vegetales de arroz, maíz, soya y sorgo
La prevalencia de Diaporthe en las semillas de soya no germinadas es similar a lo expuesto por Wallen & Seaman (2011), Petrović et al. (2018) y Lavilla (2019), quienes señalan que las especies de este género afectan negativamente la germinación y la calidad de la semilla, en consecuencia, se generan pérdidas severas en rendimiento. Esto es soportado por Sánchez et al. (2015), quienes señalan que Diaporthe spp es uno de los causantes de varias enfermedades en zonas productoras de soya, este género unido con Phomopsis constituyen un complejo fúngico que generan enfermedades y pérdidas en cultivos de soya.
Arroz
Se identificaron 5 especies de hongos filamentosos en la semilla de los dos materiales de arroz. Los mayores porcentajes de prevalencia, los ocuparon Curvularia penniseti y Fusarium culmorum. Sin embargo, estos presentaron una baja prevalencia en semillas sin germinar, situación que puede ser explicada por la existencia de mayor tejido vegetal susceptible expuesto a la acción de los hongos en la semilla germinada (Tabla 3).
La mayor prevalencia de los géneros Fusarium y Curvularia en semilla de arroz, concuerda con lo reportado por Kwaloe et al. (2018), quien indica que Fusarium equiseti, Fusarium moniliforme, Verticillium cinnabarinum y Curvularia inaequalis son las de mayor incidencia en semillas de arroz. Los resultados concuerdan con estudios previos que reportan a Fusarium spp. como las segundas especies más prevalentes en semillas de arroz después de R. solani, estas especies están asociadas con la pudrición de plántulas en el 50% de los casos (Gaire et al., 2023).
Las especies F. proliferatum y F. culmorum encontradas en la semilla analizada, han sido reportadas como patógenos transmitidos por semilla de arroz, sin embargo, en este estudio no se vio afectada la calidad fisiológica de estas (Chinchilla et al., 2020). Dentro del grupo de especies conocidas como complejo F. fujikuroi, se identificó únicamente la presencia de F. proliferatum en las semillas de arroz. Investigaciones previas han demostrado que entre las especies de este complejo presentes en las semillas de arroz (FFSC), se encuentran F. andiyazi, F. fujikuroi, F. proliferatum y F. verticillioides, las cuales están asociadas con la enfermedad conocida como Bakanae en el arroz. Esta enfermedad puede tener un impacto negativo en la capacidad de germinación de las semillas (Jiang et al., 2020).
El aislamiento de Curvularia penniseti encontrado se trata de un patógeno transmitido por semilla de arroz. Su presencia puede resultar determinante en la aprobación o rechazo de un lote de producción de semilla (Barrios & Pérez, 2005). Se ha reportado la presencia de C. penniseti en semilla de arroz, provocando marchitez del semillero, manchas en las hojas, coloración negruzca del grano, marchitez de la panícula y manchado del grano (Nenínger et al., 2003).
La baja prevalencia total y en semillas no germinadas de arroz de Aspergillus flavus, indica que se trata de un hongo saprófito y no un hongo patógeno que afecta la calidad fisiológica de la semilla. Sin embargo, existe reportes de este hongo como patógeno de semilla (Quintana, 2010).
Probablemente la afectación por los hongos encontrados en estas semillas esté asociada a las características genéticas y físicas de los arroces evaluados; los cuales probablemente presentan algún grado de tolerancia al ataque de estos hongos en la etapa de germinación (Chinchilla et al., 2020).
Sorgo
En el cultivar de sorgo se identificaron 6 especies de hongos filamentosos. El mayor porcentaje de prevalencia total y en semillas no germinadas lo ocupó Diaporthe melonis. En contraste, Aspergillus flavus tuvo una prevalencia total alta pero su frecuencia en semillas no germinadas fue menor al 1% (Tabla 3).
Los géneros Penicillium, Aspergillus y Curvularia encontrados en la semilla analizada han sido previamente reportados (Islam et al., 2009), sin embargo, no se encuentran reportes de D. melonis afectando semilla ni plantas de sorgo (Sorghum bicolor).
La mayor prevalencia de D. melonis en semillas no germinadas sugiere que puede afectar el desarrollo de plántulas normales. Varias especies de Diaporthe se asocian con la presencia de chancros en tallos, manchas foliares e incluso la muerte de estas plantas, por lo que se generan daños económicos considerables (Gao et al., 2017). Debido a que el complejo fúngico Diaporthe/Phomopsis posee un amplio rango de plantas hospederas, es posible que se trate de un patógeno transmitido por semilla.
Durante el aislamiento se evidenciaron presencia de chancros rojizos en la radícula, presentando cierta variabilidad en relación con los dos morfotipos encontrados de la especie D. melonis. Grijalba & Ridao (2014) confirman que el complejo Diaporthe/Phomopsis generalmente se distingue por presentar variaciones morfológicas en sus colonias, ya sea por la formación, el color, el tamaño de los estromas, la velocidad de crecimiento micelar o forma de las ascosporas. Lo anterior también es descrito por Gao et al. (2017) quien señala que el género Diaporthe es parafilético.
Aspergillus flavus, no afecto el potencial germinativo de las semillas de sorgo. Este microorganismo ha sido reconocido como productor de aflatoxinas, que son perjudiciales en plantas y animales. Probablemente la concentración de metabolitos secundarios como aflatoxinas toxigénicas no fue lo suficientemente alta para afectar la calidad fisiológica en términos de germinación y vigor de plántulas (Divakara et al., 2017).
La baja incidencia de Curvularia lunata en la semilla es contrastante con lo señalado por varios autores, quienes reportan a C. lunata como el patógeno con mayor prevalencia en las semillas de sorgo causando una disminución de hasta el 25,3 % de la germinación (Prom, 2004; Girish et al., 2011; Hidayat & Ramadhani, 2019). Probablemente la presencia de este hongo se deba a la ocurrencia de condiciones de altas temperaturas y alta humedad durante la fase de llenado de grano (Montes-García et al., 2010).
Talaromyces pinophilus no ha sido asociado como patógeno en semilla de sorgo, y en este estudio se demostró que tiene mayor prevalencia en semillas germinadas, sin embargo, se ha relacionado en cultivos de trigo Triticum aestivum como estimulante del crecimiento y por su capacidad de fitorremediación (El-Shahir et al., 2021).
Maíz
Finalmente, en los tres cultivares de maíz evaluados fueron predominantes Penicillium sp y Fusarium verticillioides. Este último caracterizado por ser el de mayor prevalencia en semillas germinadas y no germinadas (Tabla 3).
De los hongos encontrados en las semillas evaluadas son los usualmente reportados en otros casos de estudio junto con Alternaria alternata y Fusarium moniliforme (Basak & Lee, 2002). Los resultados presentados concuerdan con Hernández-Delgado et al. (2007) quienes encontraron que tanto en los maíces de grano amarillo como blanco se presenta la mayor incidencia de ataques por hongos de los géneros Aspergillus y Penicillium; mientras que en campo la prevalencia de Fusarium tiende a ser superior. Al igual que en el presente trabajo la concentración en la semilla de estos tres tipos de hongos varía con el genotipo.
La mayor prevalencia de F. verticillioides en los tres materiales de maíz evaluados probablemente se deba a que durante los periodos tempranos de la infección, el hongo adquiera una fase biótrofa lo que lo convierte en un patógeno capaz de sobrevivir como endófito en la semilla y en el tallo de las plantas sin causar daños visibles (Bucio et al., 2001; Luzón et al., 2007). Esto soporta los estudios de Uribe-Cortés et al. (2020) quienes encontraron cepas del género Fusarium (Fusarium subglutinans, F. temperatum y F. verticillioides) en grano de maíz asintomáticos. Esto indicaría que Fusarium es un tipo de hongo con la capacidad de generar cierta coexistencia con la semilla y que la selección visual de los granos no es suficiente para determinar la presencia o ausencia del patógeno.
La transmisión de F. verticillioides a la semilla pudo haberse dado por la presencia del patógeno en los campos de multiplicación. La infección por F. verticilloides, pudo haberse ocasionado desde la fase de plántula, dada la capacidad de supervivencia del hongo y haberse traslocado a otras partes de la planta incluida la mazorca o en el periodo de floración por acumulación de cepas infecciosas en la inflorescencia femenina. Otra posibilidad de infección son los daños mecánicos ocasionados principal mente por insectos como lepidópteros, trips y crisomélidos como Diabrotica sp (de la Torre-Hernández et al., 2014).
Se debe prestar especial atención a los hongos productores de micotoxinas presentes en la semilla como Aspergillus, Penicillium y Fusarium. Reportes previos indican que sembrar semillas infectadas con hongos patógenos productores de micotoxinas contribuye al inóculo de hongos micotoxigénicos en el suelo, los cuales luego contaminan el grano cosechado con diversas micotoxinas en el siguiente ciclo de producción (Erasto et al., 2023).
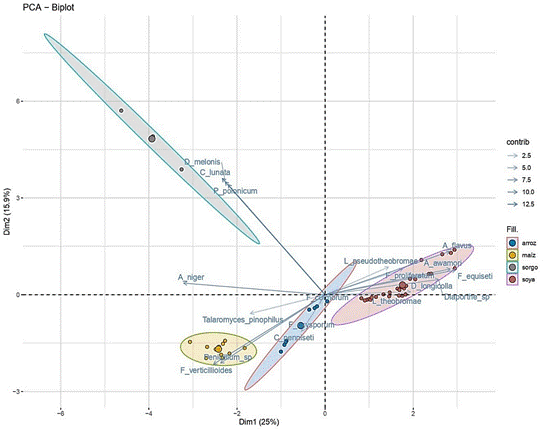
Figura 2. Análisis de componentes principales de variables de prevalencia de hongos contaminantes encontrados en semilla de trece variedades vegetales de arroz, maíz, soya y sorgo.
Los resultados del análisis de componentes principales se presentaron en un BiPlot (Figura 2). La agrupación de las muestras en diferentes regiones dentro del BiPlot indica que existen patrones de similitud y diferenciación en términos de la calidad sanitaria de las semillas. La variabilidad observada entre las muestras parece estar influenciada por la presencia y prevalencia de especies de hongos específicos para cada cultivo evaluado (Martín et al., 2022).
La prevalencia y el grado de infección de hongos dependen en gran medida de las condiciones ambientales durante el desarrollo de las semillas. En general, la humedad prolongada durante la maduración de la semilla aumenta la incidencia de estas enfermedades. Las diferencias en las condiciones climáticas, las fechas de siembra y cosecha, la densidad de siembra y la infestación de insectos pueden influir significativamente. Así mismo, es evidente que existen variaciones considerables entre semillas de diferentes variedades con respecto a la susceptibilidad de la infección por hongos (Martín et al., 2022).
Este estudio en general permitió identificar hongos contaminantes presentes en semillas. Las especies de hongos encontradas incluyen posibles patógenos que afectan la capacidad germinativa de la semilla y hongos saprófitos que son contaminantes habituales en las etapas de post- cosecha y almacenamiento. Las especies identificadas y los valores de prevalencia reportados, pueden servir como referencia para otros estudios complementarios enfocados en estudios relacionados con el aseguramiento de la calidad en las semillas.
4. Conclusiones
Las especies Fusarium equiseti y Diaporthe sp. en semilla soya, Curvularia penniseti en semilla de arroz, Diaporthe melonis en semilla de sorgo y Fusarium verticillioides en semilla de maíz, se pueden considerar como patógenos transmitidos por semilla que ocasionan un efecto negativo en la capacidad germinativa.
La mayor o menor afectación por patógenos en semilla puede estar asociada a las características genéticas y físicas de los materiales. Es así como la semilla de las variedades de arroz AGRVA1 y de maíz AGRVM1 presentaron la menor contaminación por hongos, dado el recubrimiento y dureza de la testa de las semillas.
La prevalencia de hongos en semilla almacenada puede convertirse en una condición relevante para tener en cuenta, principalmente sobre los cuidados necesarios en almacenamiento. Las condiciones no propicias de humedad y temperatura, benefician la proliferación de hongos en etapa de almacenamiento e incrementa la posibilidad de que los patógenos se transfieran a campo y repercutan en la salud animal o humana dependiendo del destino de la cosecha.
Es necesario evaluar el grado de patogenicidad de estos aislamientos y posteriormente evaluar tratamientos físicos o químicos para lograr una reducción significativa de los niveles iniciales en las poblaciones de los hongos. Sin embargo, más allá de la desinfección de semillas, esta debe implementarse junto con otras estrategias preventivas como buenas prácticas agrícolas (limpieza, almacenamiento y manipulación de semillas), buenas prácticas de manipulación y análisis de riesgos.