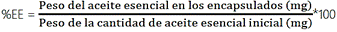1. Introducción
La producción de aceites esenciales cítricos ha aumentado a través de los años por su alta demanda continua en diversos países como Estados Unidos (Agarwal et al., 2022), y con una tendencia creciente esperada del 4,1% para el año 2032 (Fact.MR, 2022). Las cáscaras son el principal residuo del procesamiento de naranjas frescas, y a partir de ellas se pueden obtener aceites esenciales con diversas propiedades, como actividad anti carcinogénica, relajante, ansiolítica, antitumoral, antioxidante, y preservante alimentario (Dosoky & Setzer, 2018). El limoneno es el monoterpeno mayoritario (más del 90%) presente en el aceite esencial de naranja (AEN) (Wang et al., 2019; Torres et al., 2017); sin embargo, otros componentes como sesquiterpenos, alcoholes, y ésteres se han reportado en AEN obtenidas de diversas especies (Razola-Díaz et al. 2021).
La gran desventaja del AEN es la susceptibilidad a la degradación por factores como la luz, el oxígeno y la temperatura, ocasionando una oxidación y pérdida de su actividad (Ferrándiz, 2015) que limita sus aplicaciones. En vista de ello, la encapsulación otorga una protección a la oxidación, deterioro nutricional y pérdida de componentes volátiles; ya que permite cubrir el componente con una matriz o pared polimérica (Durmus et al., 2023). Sin embargo, la selección de la matriz encapsulante y el proceso de encapsulación desempeñan un rol esencial en la protección del AEN y la estabilidad de sus compuestos (Razola-Díaz et al., 2021).
Entre los métodos de encapsulación, se encuentra la inclusión molecular, la cual mediante el uso de ciclodextrinas (CDs), permite mantener las propiedades fisicoquímicas y biológicas del AEN en comparación a otras matrices (Dehghan et al., 2020; Velmurugan et al, 2017), evitando modificaciones en sus componentes (Gonzalez et al., 2021). Dentro de las CDs, la β-ciclodextrina (β-CD) presenta el mayor potencial para encapsular compuestos volátiles debido al tamaño de su cavidad, formado por 7 unidades de glucosas, con una cavidad interna hidrofóbica y una parte externa hidrofílica formando con el aceite un complejo de inclusión (Paiva-Santos et al., 2022; Torres-Alvarez et al., 2020) per mitiendo una aplicación en medios acuosos. Los enlaces no covalentes que permiten la unión entre aceites esenciales y la β-CD suelen ser las fuerzas de enlace de hidrógeno, electrostáticas y de Van der Waal (Liu et al., 2023).
Posterior a la encapsulación, comúnmente la atomización es la tecnología usada para la obtención de partículas finas; sin embargo, una temperatura por encima de 100 °C podría producir pérdidas de componentes sensibles al calor (Cid-Samamed et al., 2022; Mohammed et al., 2020; Durmus et al., 2023). Al respecto, la liofilización y el secado por aire caliente como técnicas de secado no se han investigado, considerando a su vez el efecto que podria tener sobre el aceite encapsulado y las características físicas de las partículas. Por lo expuesto, los objetivos fueron determinar la influencia del método de secado por estufa, liofilización y atomi zación (temperaturas de atomización 160, 180 y 200 °C) sobre las características fisicoquímicas y la estabilidad del complejo AEN: β-CD.
2. Metodología
2.1. Aceite esencial y matriz encapsulante. Se utilizó AEN Brasil Cutrale, mezcla de compuestos aromáticos simples y de origen natural, adquirido de la empresa Esquisa (Perú). Como matriz encapsulante se empleó beta-ciclodextrina (β-CD), proveniente de India, adquirido de la empresa Himedia (Lima, Perú).
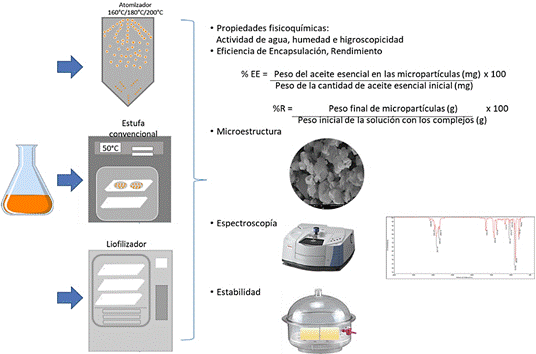
2.2. Formación del complejo de inclusión. Se consideró el método de coprecipitación reportada por Nolazco-Cama et al. (2023) con algunas modificaciones. La β-CD fue disuelta en agua destilada a 50 °C y enfriada para agregar el AEN gota a gota en una ratio AEN: β-CD (1:8,33) (g/g) para la encapsulación. Para la formación del complejo se mantuvo agitación constante a 900 rpm por 210 min (agitador magnético con temperatura Heidolph, modelo MR Hei-Connect, Alemania). Culminado el tiempo, la solución se refrigeró a 4 °C durante 16 h; poste riormente, todas las soluciones fueron secadas: a) Estufa convencional (Mermmet, SN30, Alemania) a 50 °C por 24 h, b) Liofilización a -40 °C con una presión absoluta de 13,33 Pa por 17 h (liofilizador Millrock, Stellar, USA), y c) Atomización a temperaturas de 160, 180 y 200 °C, boquilla de 1 mm y flujo de alimentación igual a 3,35 ml/min (atomizador de laboratorio LabPlant, SD-Basic, Inglaterra) obteniendo un total de cinco tratamientos. Las micropartículas obtenidas se almacenaron en frascos de vidrio transparentes a temperatura ambiente hasta los análisis respectivos (Figura 1).
2.3. Humedad, actividad de agua e higroscopicidad. La humedad se determinó por el método propuesto por la AOAC (1996). La actividad de agua se midió con un equipo medidor de actividad de agua (Aqualab, 4TEV DUO, USA) con compensación de temperatura a 25 °C (Rendón et al., 2010). La higroscopicidad se determinó mediante el método reportado por Atefi et al. (2017). Se pesaron 0,20 ± 0,01 g de micropartículas y se colocaron en una campana desecadora con solución saturada de NaCl (HR: 75%). Después de dos horas, se calculó la higroscopicidad por diferencias de pesos, derterminada como la cantidad de gramos de agua absorbidos (g/100g).
2.4. Eficiencia de encapsulación (%EE) y rendimiento. Todas las micropartículas (0,15 g) fueron diluidas en cloroformo (4 ml) y agua destilada (8 ml), se colocaron en baño maría (Memmert, WNB 14, Alemania) con agitación constante a 100±2°C por 20 min. Luego la solución se separó por decantación y el sobrenadante fue usado para el análisis. Se realizaron 3 lavados en total para extraer la mayor cantidad de aceite de la micropartícula. Posterior a ello, se filtró y realizó las lecturas en un espectrofotómetro UV-visible a 240 nm (espectrofotómetro UV-Vis Thermo Scientific, Genesys 10S, USA). La cuantificación requirió de una curva de calibración con cloroformo entre concentraciones de 1,10 x 10-4 hasta 8,48 x 10-4 g/m. La cantidad de aceite esencial encapsulado y el %EE fue determinado por la siguiente ecuación:
El rendimiento, se determinó mediante diferencia de pesos, entre el valor inicial de la solución con los complejos formados y el final de las micropartículas obtenidas, expresados en porcentaje (%).
2.5. Microestructura de micropartículas. El tamaño y la forma de las micropartículas obtenidas se observaron mediante el microscopio electrónico de barrido (MEB) (Carl Zeiss, Merlin, España), usando el software Phenom Pro suite/particle metric con voltaje de aceleración a 25 kV y con lentes de acercamiento de 4000x y 5000x, de las cuales se escogieron las mejores visualizaciones.
2.6. Caracterización por espectroscopia infrarroja con transformada de Fourier (FTIR). Las micropartículas obtenidas de los diferentes tratamientos se analizaron utilizando un espectrómetro de infrarrojo con transformada de Fourier (FTIR) (Mettler Toledo, ReactIR 45P, Suiza) acoplado con un acce sorio de reflexión total atenuada. Las mediciones se realizaron en un rango de frecuencia de 4000 a 649 cm-1 con una resolución de 4 cm-1. Se utilizó el software OMNIC FTIR para la identificación de los picos.
2.7. Evaluación de la estabilidad. Las micropartículas de todos los tratamientos se colocaron en bolsas de polietileno de alta densidad (PEAD) y se almacenaron en campanas desecadoras de vidrio con solución saturada de nitrato de potasio (HR: 82%), a 20 ± 1 °C. La estabilidad fue evaluada mediante la medición de la humedad, actividad de agua y %EE cada 9 días, en un periodo total de 36 días. Además, se determinó los cambios en la morfología de las micropartículas al finalizar el tiempo de almacenamiento mediante MEB.
2.8. Análisis estadístico. Los tratamientos se evaluaron mediante un Diseño Completamente al Azar (DCA) y la prueba de Tukey, para encontrar diferencia significativa. La evaluación estadística se llevó a cabo usando el programa Statistica version 10, considerando un nivel de significancia p < 0,05.
3. Resultados y discusión
3.1. Humedad, actividad de agua e higroscopicidad de las micropartículas
En la Tabla 1 se observan los resultados de las características fisicoquímicas de las micropartículas de AEN en β-CD.
El menor porcentaje de humedad fue 1,76 ± 0,001%, para las muestras secadas por liofilización, mientras que las de mayor contenido de humedad son aquellas que fueron secadas por atomización a 180°C, con un porcentaje de humedad promedio de 4,85 ± 0,001%. Similares resultados fueron obtenidos por Papoutsis et al. (2018), en los encapsulados de AEN entre liofilizados y atomizados. Según Nowak & Jakubezyk (2020), el proceso de liofilización alcanza una pérdida de humedad mayor al 99% debido a que toda el agua disponible se congela inicialmente para luego ser eliminado durante la sublimación.
En el proceso de liofilización, dependiendo de la composición química, estructura y condiciones, el agua ligada o agua de la monocapa puede ser eliminada (Carpena et al., 2021).
Según Klinkesorn et al. (2006), el contenido de humedad máximo para la mayoría de micropartículas, indistintos del método de secado, puede llegar hasta 4%. Sin embargo, Márquez et al. (2017), consideran un rango de humedad entre 2 hasta 6% en general casi todas las muestras a excepción de las liofilizadas presentaron humedades dentro de este último rango.
Además de la humedad, la actividad de agua (Aw) según Papoutsis et al. (2018) es un valor crucial en la calidad de los encapsulados, al poseer un efecto sobre su vida útil y evitar el desarrollo microbiano. Los resultados obtenidos fueron menores a 0.6 para todos los tratamientos indicando que son microbiológicamente y enzimáticamente estables (Márquez et al., 2017). Al respecto, Esquivel et al. (2015) mencionan, que los valores de Aw no debe ser tan bajas debido a que las muestras pueden sufrir un colapso y disolverse en menor tiempo del esperado.
Referente a la higroscopicidad, el mayor y menor valor fueron 4,89 ± 0,007 y 0,20 ± 0,001%, respectivamente; siendo el primero calculado para secado por atomización a 200 °C y el segundo para liofilizado. Según Yeddes et al. (2022), la higroscopicidad de las micropartículas es baja debido a la naturaleza hidrofóbica del aceite esencial (AE) que no le permite absorber agua, aunque este valor puede aumentar junto al contenido de AE. Por otro lado, existe una relación directamente proporcional ya que las macropartículas secadas a mayor temperatura poseen mayor higroscopicidad esto se debe a que, al incrementar la temperatura de secado, existe una mayor remoción de agua por lo cual al ser sometidos a un ambiente de humedad relativa alta, genera una mayor absorción de agua para alcanzar el equilibrio (Sánchez, 2016). Asimismo, Fang et al. (2013) encontraron que debido al exterior hidrofílico de la β-CD, esta tiende a adsorber moléculas de agua, volviéndola más higroscópica en un medio de mayor humedad.
3.2. Eficiencia de encapsulación y rendimiento
En la Tabla 2 se presenta los promedios de eficiencia de encapsulación y rendimiento obtenidos para cada tratamiento de encapsulados de AEN en β-CD.
Tabla 1 Propiedades fisicoquímicas de las micropartículas AEN: β-CD
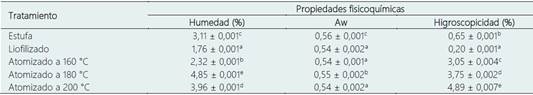
Los resultados se dan como media ± desviación estándar (n = 3). Letras en superíndice diferentes entre columnas indican diferencia significativa (p < 0,05) de las propiedades entre los tratamientos.
Tabla 2 Eficiencia y rendimiento de encapsulación para cada tratamiento
| Tratamiento | Eficiencia de encapsulación (%) | Rendimiento (%) |
|---|---|---|
| Estufa | 86,54 ± 0,70d | 72,85 ± 0,79d |
| Liofilizado | 97,35 ± 0,27e | 70,58 ± 0,98d |
| Atomizado a 160 °C | 42,17 ± 0,72b | 29,63 ± 0,64b |
| Atomizado a 180 °C | 55,70 ± 0,12c | 39,69 ± 0,94c |
| Atomizado a 200 °C | 34,83 ± 0,56a | 25,81 ± 0,93ª |
Los resultados se dan como media ± desviación estándar (n = 3). Letras diferentes en minúscula de superíndices indican diferencia significativa (p < 0,05) entre los tratamientos.
De acuerdo a los resultados, la mayor eficiencia se obtuvo por liofilización con un valor de 97,35 ± 0,27%. Valores cercanos fueron reportados por Santos et al. (2015), al obtener una eficiencia de 91,3% al encapsular carvacrol en β-CD, el cual, al ser un valor superior a 90% es un indicador de buenas condiciones de contacto entre AEN y β-CD durante la formación de complejos; en comparación a los valores de 42,17%, 55,70% y 34,83% encontrados para las macropartículas atomizadas a 160, 180 y 200 °C, respectivamente. Torres (2018) refiere que, la alta eficiencia en la liofilización se debe a las bajas temperaturas y presión de vacío para realizar el proceso, por lo que es menos probable que se volatilicen los componentes.
Según Sandoval et al. (2016), los factores que pueden producir una baja eficiencia al atomizar encapsulados son condiciones no uniformes en el equipo, temperatura demasiada alta a la entrada y salida del aire, flujo de alimentación elevado, e inclusive el tiempo de permanencia en la cámara de secado. Alguno de estos factores guarda relación con lo obtenido, ya que al atomizar a 200 °C se obtuvo la menor eficiencia, esto puede significar que parte del AE se volatilizó durante el secado, sobre todo el aceite superficial que se forma al exterior de la macropartícula. Para el caso del secado por atomización a 160 °C la eficiencia fue menor en comparación del atomizado a 180 °C, debido a que a una temperatura baja no es lo suficiente para secar al producto y solo se recolectarían las macropartículas con humedad más baja del contenedor final y el resto se quedaría adherido al ciclón (Thi et al., 2021).
Por otro lado, los rendimientos obtenidos después de cada proceso presentan similar tendencia con los resultados de eficiencias de encapsulación. Las micropartículas obtenidas por atomización fueron menores al 40%, contrariamente la liofilización y secado en estufa alcanzaron rendimientos cercanos al 70%. Según Dos Passos et al. (2016), el limoneno es el componente mayoritario del AEN, y parte de este compuesto puede quedar retenido en la superficie de las micropartículas por lo que podría ser volatilizado durante el calentamiento; esto explicaría los bajos rendimientos en las micropartículas secadas por atomización.
3.3. Microestructura de las micropartículas
En la Figura 2 se aprecia las vistas microscópicas (5000x) de las micropartículas obtenidas. Las partí-culas secadas por atomización (A, B, C) presentaron un tamaño promedio de 3,15; 3,45 y 2,71 µm para las temperaturas de 160, 180 y 200 °C; las secadas por liofilización (D) de 3,02 µm y estufa (E) de 2,46 µm. La forma de las micropartículas se distingue como ovaladas para los atomizados; romboides y prismas para las liofilizadas y secadas por estufa, respectivamente. Kringel et al. (2017) y Kong et al. (2018) refieren que al produ cirse la complejación con β-CD, es normal que se adopte tamaños y formas irregulares. Torres-Álvarez et al. (2020) señalan que algunos parámetros como el tiempo de agitación puede re ducir las fuerzas repulsivas entre las macropartícu las evitando la aglomeración.

Figura 2 Microestructura de los encapsulados: Atomizado a 160 °C (A), Atomizado a 180 °C (B), Atomizado a 200 °C (C), Liofilizado (D) y Estufa (E).
La forma y tamaño de las partículas obtenidas por atomización se deben a los parámetros empleados en el secado; asimismo el tipo de boquilla (neumático, de presión y disco centrífugo) puede influenciar significativamente en la forma (Piñón-Balderrama et al., 2020). Según Berraquero-García et al. (2023), cuanto menor es el diámetro de la boquilla, las gotas serán de menor tamaño y a su vez, las partículas tienden a ser más pequeñas. En este caso, al emplear una boquilla estándar de 1 mm, favoreció la obtención de la forma ovalada o esférica de las partículas atomizadas y permitieron obtener tamaños intermedios, los cuales varían por pequeñas aglomeraciones de gotas al caer a la cámara de secado. Por otro lado, las partículas liofilizadas y secadas por estufa presentaron un tamaño menor y forma de cristal. Según Guerrero et al. (2022), en el secado por liofilización, el tamaño de partícula es directamente proporcional a la tasa de transferencia de masa desde la superficie de la partícula al entorno; es decir, si el encapsulado es más pequeño, entonces posee un menor contenido de materia seca de la emulsión. Asimismo, Rezende et al. (2018) menciona que la forma de flakes que presentan los encapsulados secados por liofilización se debe a la formación de hielo durante su proceso, lo que a su vez previene la contracción y colapso de la estructura.
Probablemente, la aglomeración también produce la irregularidad en la forma de las micropartículas, y en algunos casos, estas pequeñas imperfecciones que se visualizan pueden ser significado de aceite superficial que no ha sido encapsulado en el interior (Velázquez, 2008). Por su parte, Sánchez (2016) encontró que a mayor temperatura se presentan menos irregularidades en las partículas ya que se suaviza la contracción debido a la expansión térmica del aire dentro de la partícula y que, por el contrario, al ser menor la temperatura de secado la difusión de agua se vuelve lenta y al ser mayor el tiempo de secado, es más probable que se deformen o exista un colapso de partículas.
Anaya-Castro et al. (2017), en su investigación de encapsulado de aceite esencial de clavo de olor y orégano en β-CD, encontraron que la morfología de este encapsulante cambió al formar complejos y que la forma que tenían era romboide y con pequeñas piezas amorfas irregulares, lo cual se asemejan a los encapsulados liofilizados obtenidos. Esto también tiene similitud con lo encontrado por Malapert et al. (2019), en el cual los encapsulados por liofilización poseen estructuras rectangulares irregulares, mientras que en los atomizados tienden a ser esféricas. Adicionalmente, Anaya-Castro et al. (2017) mencionan que, al no poseer fracturas, poros visibles o grietas, implica una buena y adecuada protección; sin embargo, en los tratamientos secados por atomización se observan pequeños orificios en algunas de las partículas, mientras que, en los liofilizados, se observan algunos de los cristales con pequeñas grietas.
3.4. FTIR de las micropartículas
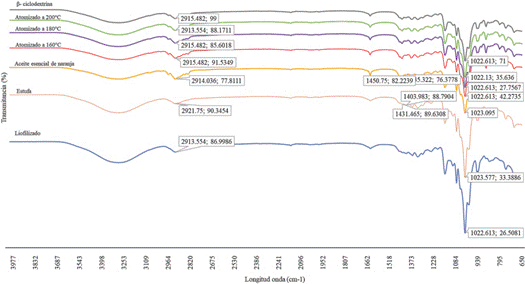
Se aprecia en la Figura 3 los espectros de aceite esencial de naranja, β-CD y micropartículas obtenidas. El espectro del AEN muestra unos picos delgados y muy pronunciados cercanos a 940 cm-1, los cuales tienen un porcentaje de transmitancia menor al de los tratamientos de encapsulados. Asimismo, se presentan los espectros de los encapsulados para los diferentes tratamientos, los cuales son muy parecidas entre sí, desde los picos de menor tamaño hasta los picos más grandes, tienen el parecido tanto en valor de transmitancia como en longitud de onda. Dentro de ellos, los más cercanos entre sí son los encapsulados secados por estufa y atomizado a 160 °C, y los que presentan mayor pico y cercanos son aquellos que se obtuvieron por atomizado a 180 °C y liofilizados. Por otro lado, el espectro inicial de la β-CD es un pico pequeño que se encuentra próximo a una longitud de 1000 cm-1.
Los cambios, desapariciones o atenuaciones que han sufrido los espectros tanto del aceite como de la β-CD se debe a que ambos han sufrido cambios en su estructura. Por ejemplo, la banda a 885,54 cm-1 del AEN no se detectó en ninguno de los complejos obtenidos y la banda 1051,21 cm-1 cambió a más de 1077 cm-1 para cada tratamiento. De igual forma, la banda 1435,52 cm-1 del AEN desapareció totalmente, lo cual puede significar que estas han sido ocultas por alguna banda perteneciente a la β-CD. Estos cambios se deben generalmente a la interacción y formación de enlaces intermoleculares entre el agente encapsulante y la molécula huésped (Restrepo et al., 2009).
Según Li et al. (2018) los picos característicos que presenta el aceite pueden que desaparezcan o se debiliten en las microcápsulas, esto se debe a que han ingresado dentro de las cavidades de la β-CD y que no solo se ha formado una mezcla física, sino que ha habido una interacción química, como la complejación, lo cual redujo el movimiento de las moléculas encapsuladas.
En el caso de la β-CD pura este presenta diversas bandas dependiendo del tipo de enlaces que posee. En este caso se encontró una ligera banda entre 3100 y 3200 cm-1, otra en 1661,44 cm-1 y algunas de absorción en 1022,61 cm-1, 1147,48 cm-1 y 1010,56 cm-1. Según Torres-Alvarez et al. (2020), esto significa que, en el espectro se puede visualizar el enlace CH, CO y las vibraciones de estiramiento para C=O, respectivamente. Además, se considera que las bandas en la región de 940 a 700 cm−1 corresponden a la vibración que ocurre entre los enlaces CH y las vibraciones esqueléticas CC en el anillo de glucopiranosa.
Para las bandas de los distintos tratamientos de los encapsulados, se observan picos pequeños cercanos a 1700 cm−1, los cuales son resultado del estiramiento del grupo aldehído, además, de otros picos también pequeños que oscilan entre 2910 a 2920 cm−1, y entre 1400 a 1300 cm−1. Los primeros son correspondientes a la vibración de carbono-hidrógeno del anillo aromático estructural y los segundos aparecen debido a la vibración de estiramiento del doble enlace carbono-carbono en el anillo aromático (Siva et al., 2020). Esto es similar a lo que se presenta en el espectro del encapsulante puro, lo cual puede entenderse como enlaces que han permanecido luego de la formación del complejo.
3.5. Estabilidad de las micropartículas
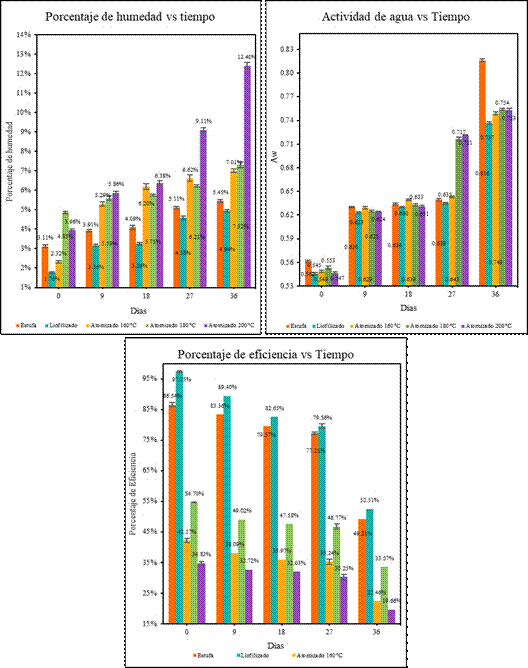
En la Figura 4 se aprecia las variaciones de las propiedades analizadas a través del tiempo de almacenamiento. Todos los tratamientos presentaron una tendencia a aumentar su humedad a través de las semanas (Figura 4A); pero aquel que reportó una variación elevada fue la muestra atomizada a 200 °C, con una diferencia de 9,55% entre el valor inicial (3,96%) y final (12,41%).
Esto significa que el encapsulado ha captado agua, debido a que inicialmente poseía una humedad baja y al ser sometido a un ambiente de humedad relativa alta, se debe encontrar el equilibrio entre el medio y la muestra (Roa et al., 2021), guardando relación con los datos de higroscopicidad determinados anteriormente. Según Muñoz-Shugulí et al. (2022), debido a que el exterior de la β-CD es hidrofílica, las moléculas de agua debilitan la unión del complejo formado, lo cual produce una liberación de los componentes del AEN; por el contrario, cuando mayor sea la humedad relativa del ambiente, en especial cuando es mayor a 50%, existe una tendencia de las micropartículas a perder su eficiencia en el tiempo (Figura 4C).
Por otro lado, el tratamiento por liofilización mostró una menor humedad para la cuarta semana (4,94%). Esto puede suponer que el encapsulante mostró una mejor protección para el AEN; sin embargo, tuvo una pérdida significativa de AEN entre la semana 3 y 4 (Figura 3C), obteniendo al final un porcentaje de 52,53%, esto puede deberse a la temperatura y humedad del medio de almacenamiento durante la última semana. Otro factor que puede afectar la estabilidad del encapsulado es la formación de estructuras porosas, las cuales se forman debido a la presión a la que es sometida la muestra al momento de ser liofilizada, ya que cuando la presión empieza a disminuir, la presión de vapor de la superficie externa del producto también disminuye y aumenta la difusión de vapor junto con la porosidad y tamaño de poro (Vargas, 2015; Merivaara et al., 2021). Esta mayor porosidad trae como consecuencia que el producto final sea más higroscópico, lo que provoca que tienda a absorber más agua al someterlo a un ambiente con una humedad relativa elevada y a su vez, una liberación de parte del AE. A pesar de ello, el método por liofilización presentó la mejor estabilidad a comparación de los otros métodos y aunque las eficiencias en general disminuyeron, aún se encuentran por encima de las reportadas por Kfoury et al. (2015), quienes obtuvieron un rango de 16% a 47% al encapsular aceite esencial de albahaca y estragón en β-CD, esto puede deberse a que usaron una proporción menor de agente encapsulante.
Otro aspecto importante que guarda relación con la eficiencia y conservación de los encapsulados es la Aw. Según Ferreira et al. (2022), esta propiedad influye de manera significativa en la vida útil de los encapsulados, ya que, si estos presentaran una Aw igual o menor a 0,21, favorecería a su estabilidad, por el contrario, si es igual o mayor a 0,74, puede existir un colapso y las partículas pueden disolverse en menor tiempo. Los datos obtenidos presentaron una actividad mayor o cercana a la mencionada anteriormente (Figura 4B), lo cual pudo ser factor para una mayor pérdida en la última semana.
Un factor adicional que puede influenciar en la estabilidad de las micropartículas es el tipo de envase. En este caso, se empleó PEAD, el cual presenta una baja permeabilidad a gases, buena protección contra la humedad y mayor resistencia química a comparación del polietileno de baja densidad. Sin embargo, según Hernández et al. (2014), la actividad de agua de productos encapsulados suele aumentar cuando la temperatura es baja, hasta volverse constante; esto es debido a que la ganancia de vapor de agua se ve influenciada por la permeabilidad del envase y su interacción con la temperatura del medio, lo cual es causado por la humedad relativa del aire junto a la higroscopicidad del producto. Asimismo, Allinson et al. (2001) reportaron que el polietileno es un envase adecuado y protege mejor a compuestos sensibles a la humedad si se encuentran en un medio de humedad relativa de 75% o menos.
Finalmente, con respecto a la morfología, las micropartículas podrían presentar cierto desgaste ya que inicialmente se observó que en todos los tratamientos se presentaron algunas fisuras y orificios que pudieron facilitar la pérdida de AE. Esto se observa con mayor claridad en aquellas muestras tratadas por atomizado (A, B, C), donde presentan manchas, formas irregulares y roturas, lo cual podría significar que parte del AE ha sido liberado o que las micropartículas se han ido deteriorando con el tiempo. Según Pellicer (2016), cuando las partículas presentan irregularidades en su superficie suelen presentar dificultades en las propiedades de flujo e inclusive pueden ser más susceptibles a reacciones de degradación, si se presentaran superficies rugosas. Considerando todo lo mencionado anteriormente, al finalizar la cuarta semana el tratamiento que presentó los mejores resultados fue el liofilizado, obteniendo una eficiencia mayor al 50%, con mínimo incremento de actividad de agua y humedad en el almacenamiento.
4. Conclusiones
Las micropartículas secadas por liofilización presentaron la más baja humedad, actividad de agua e higroscopicidad con una alta eficiencia de encapsulación (97,35%), y buen rendimiento. En cuanto a su estabilidad en el almacenamiento, la liofilización otorgó una mayor estabilidad y una estructura característica. Acorde a los resultados, este método de secado después de la inclusión molecular sería el más adecuado para microencapsulados que posean componentes volátiles en comparación a otros métodos de secado estudiadas; asimismo, se recomienda el estudio de la estabilidad de la micropartícula a temperaturas extremas a fin de evaluar el desenvolvimiento durante y después de un proceso alimentario.