Los coronavirus son un grupo de patógenos que afecta a animales y humanos. Al final del 2019, en Wuhan, China, se identificó un virus que producía una neumonía severa. Esta enfermedad se propagó por toda Asia, afectando posteriormente a otros continentes. En febrero del 2020, la Organización Mundial de la Salud designó a esta enfermedad como Covid-19, y al virus causante de esta enfermedad como coronavirus 2 del síndrome respiratorio agudo severo (SARS-CoV-2) 1,2. La transmisión a través de aerosoles, es un mecanismo importante de diseminación de la enfermedad3. El SARS-CoV-2 se ha detectado en muestras no respiratorias como heces, sangre, secreciones oculares y semen; sin embargo, su rol en la transmisión es incierto4,5.
El SARS COV-2 puede producir una enfermedad grave en un 5% de infectados. Estos pacientes requieren ingreso en la unidad de cuidados intensivos (UCI). Los principales predictores para requerir ingreso a UCI son: saturación de oxígeno <92% con oxígeno ambiental, linfopenia, edad ≥60 años y obesidad. Otros factores de riesgo son: hipertensión arterial, enfermedad renal crónica, y diabetes mellitus. Se consideran como criterios de gravedad los niveles de dímero D superiores a 1000 ng/ml y una puntuación de SOFA elevada al ingreso6,7.
La enfermedad producida por el virus SARS CoV-2, puede producir un cuadro inflamatorio severo, que puede llevar a falla respiratoria, sepsis, disfunción de órganos y muerte8. Por lo que se espera que los medicamentos antiinflamatorios, como los corticoides, sean una alternativa terapéutica. Sin embargo, la evidencia aún no es categórica9-23. En diversos estudios recientes, incluso meta análisis, se han extrapolado resultados de otras enfermedades virales, e incluso bacterianas, a la Covid-1925-28. El presente estudio buscó determinar si existe evidencia que avale el uso de corticoides parenterales en pacientes con Covid-19 grave. Según la estrategia PICO, nuestra Población de estudio fueron los pacientes con Covid-19 grave y/o SRDA; la Intervención a evaluar es el uso de corticoides parenterales; el Comparador, los pacientes con infección Covid-19 que recibieron tratamiento estándar; y el Outcome, la mortalidad en estos pacientes.
MATERIAL Y MÉTODOS
Estrategia de búsqueda: nuestro estudio se llevó en concordancia con la guía PRISMA. La búsqueda se realizó en las bases de datos PubMed, Medline, Cochrane, Embase, y LILACS usando los términos relacionados con nuestra pregunta PICO; entre el de 01 enero al 31 de agosto del 2020. Complementariamente, se realizó una búsqueda secundaria de artículos no incluidos en dichas bases. La expression de búsqueda fue: ("coronavirus" OR "COVID-19", OR "2019-nCoV", OR " SARS-CoV-2 " OR "Acute Respiratory Distress Syndrome") , AND ("corticosteroids " OR " glucocorticoids ", "hydrocortisone " OR "methylprednisolone" OR "dexamethasone" OR "steroid"), AND (“mortality” OR “mechanical ventilation” OR “ICU admission” OR “ICU stay” OR “hospital stay”).
Criterios de elegibilidad. Incluimos sólo estudios primarios [ensayos clínicos (ECs), estudios de cohorte y estudios transversales] que evaluaron corticoides parenterales (dexametasona, metilprednisolona, hidrocortisona, prednisolona) en pacientes adultos con Covid-19 grave y/o SDRA y su efecto en la mortalidad.
Selección de los estudios. Se recopiló artículos primarios y secundarios los cuales cumplieron con los criterios PICO y de selección para el análisis cuantitativo.
Valoración de sesgo. Para los estudios de cohorte y transversales se usó la herramienta Newcastle-Ottawa Scale (NOS); y para los ensayos clínicos aleatorizados, el RoB2 (herramienta de Cochrane).
Extracción de datos y análisis. Para cada publicación seleccionada se extrajo: primer autor; año y mes de publicación; país; tamaño de muestra; covariables relacionadas; tipo, dosis y duración del tratamiento con corticosteroides. La medida de resultado fue el efecto en la mortalidad [RR, OR, HR, e intervalo de confianza (IC) al 95%].
Heterogeneidad. Evaluamos heterogeneidad clínica, metodológica y estadística. La heterogeneidad clínica se evaluó a través de diferencias entre pacientes, tratamientos o desenlaces. La heterogeneidad metodológica, según variabilidad en los diseños, medidas del efecto y control de sesgos. La heterogeneidad estadística se estimó con la determinación de un gráfico forest plot, donde se valoró el efecto de los corticoides a favor, o en contra, del resultado. En el gráfico forest plot, visualmente consideramos que existe poca heterogeneidad cuando los estimados de los estudios se ubican cercanamente entre sí y superponen sus ICs. Consideramos como heterogeneidad significativa un I2 ≥60%, y según el estadístico Chi-cuadrado un p valor ≤0,05. Dada, la significativa heterogeneidad en el forest plot global (considerando todos los estudios) (I2 84% y p <0,00001), estimamos modelos de efectos aleatorios y la prueba Tau2. Sin embargo, cuando analizamos solos los ECAs (excluyendo estudios de cohortes y transversales), obtuvimos que una heterogeneidad estadística no significativa (I2 44% y p = 0,17) por lo que usamos el modelo de efectos fijos.
RESULTADOS
Tras la búsqueda realizada, en las bases de datos mencionadas, durante el 01 de enero al 31 de agosto del2020. Se logró recopilar un total de 287 artículos relacionados con la pregunta PICO (Figura 1). De éstos, 216 artículos se obtuvieron de la búsqueda primaria y 71 de la búsqueda secundaria. Se realizó una revisión por pares, quedando 18 artículos. De estos artículos, finalmente se seleccionaron 9, los cuales cumplieron con los criterios PICO y de selección. Se excluyeron: cartas al editor, serie de casos, correspondencias y revisiones narrativas. Del total de 9 artículos, dos fueron estudios transversales14,19, cuatro cohortes retrospectivas11,13,16,20, y tres fueron ensayos clínicos aleatorizados21-23. Los 2 estudios transversales se realizaron en China; y de los estudios de cohorte, 3 se realizaron en China13,16,21, y uno en Estados Unidos de América11. Los estudios observacionales (transversales y cohortes), se caracterizaron por amplias diferencias en el número de participantes (entre 31 a 416), severidad de la enfermedad; tipo, dosis y tiempo del corticoide administrado). En todos ellos se usó equivalente metilprednisolona en un rango de dosis de 0,5 a 3mg/kg/d11,13,16,21 (Tabla 1).
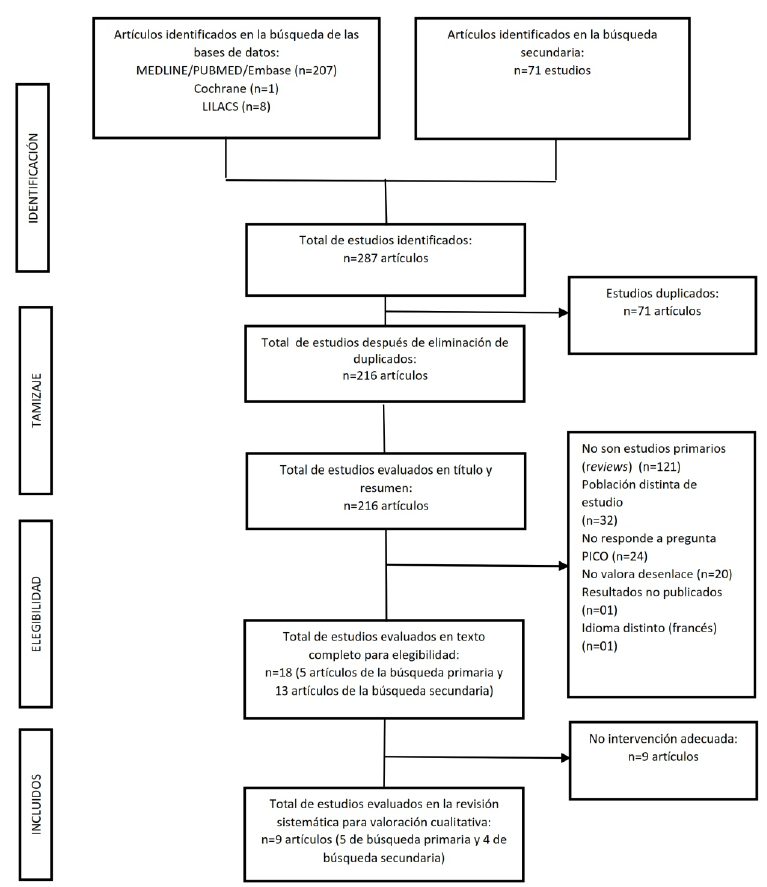
Figura 1 Diagrama de flujo PRISMA de la selección de los estudios primarios sobre el uso de corticoide en pacientes con infección por SARS- CoV-2.
Tabla 1 Características generales de los estudios incluidos sobre el uso de corticoide en pacientes con infección severa por SARS-CoV-2. con infección por SARS- CoV-2.
| Autor | Lugar | Seguimiento (dias) | Tipo de estudio | Diagnóstico de Covid-19 | n | Estadio Severidad | Corticoide | Dosis y duración |
|---|---|---|---|---|---|---|---|---|
| Raef F (11) | EUA | 15 | Cohorte prospectiva | RT-PCR | 213 | Moderado / Severo | MTP | 0.5-1 mg/k, 3 días |
| Wang D (13) | China | 40 | Cohorte retrospectiva | RT-PCR | 115 | Critico / No Critico | MTP | Grupo A: 0.5-1 mg/kg; 3 días Grupo B: 1-3mg/kg; 3 a 10 días |
| Shang J (14) | China | 60 | Transversal retrospectivo multicéntrico | RT-PCR | 416 | No Severo / Critico | MTP | Sobreviviente Severo: 38.7 mg; 2 días. Sobreviviente no severo: 40 mg; 2 días. Muerto: 65 mg; 6 días |
| Wang Y (16) | China | 35 | Cohorte retrospectiva | RT-PCR | 46 | Severo | MTP | 1-2 mg/k/d; 5 días |
| Zha L (19) | China | 30 | Transversal | RT-PCR | 31 | Severo | MTP | 40-80 mg/d; 5 días |
| Horby P (20) | Reino Unido | 28 | ECA abierto | RT-PCR | 6425 | Con O2; Sin O2; Con VMI | DXM | 6 mg/d; 10 días |
| Xu J (21) | China | 60 | Cohorte retrospectiva multicéntrico | RT-PCR | 239 | Severo / SDRA | MTP | 60.9 ± 21.7mg de 3 a 10 días |
| Jeronimo CMP (22) | Brazil | 28 | EC randomizado, doble ciego, controlado con placebo fase Iib | RT-PCR | 393 | Severo / Moderado | MTP | 0.5 mg/Kg/ 12 h por 5 dias. Además, hidrocortisona para pacientes con shock |
| Corral-Gudino (23) | España | No precisa | EC parcialmente randomizado, etiqueta abierta | No precisa método diagnóstico | 85 | Covid-19 con riesgo de SDRA | MTP | 40 mg/12h, 3 días; luego 20 mg/12h, 3 días. |
VMI: Ventilación mecánica invasiva. SDRA: Síndrome de Dificultad Respiratoria Agudo. MTP: metilprednisolona. DXM: dexametasona. EC: ensayo clínico.
Los ensayos clínicos (EC) se realizaron en 3 países: Reino Unido21, España22 y Brasil23. El primero fue un EC aleatorizado, controlado, de etiqueta abierta y adaptativo en 6 425 pacientes en total diagnosticados al100% con PCR-TR; en una proporción aproximada de 1:2 entre el grupo intervención y control; período de seguimiento de 28 días para medir el outcome combinado de mortalidad y necesidad de ventilación mecánica invasiva (VMI) con el uso de dexametasona 6mg/d por 10 días, la cual resulto a favor de disminución del efecto combinado de manera significativa21. GLUCOCOVID fue un EC, parcialmente aleatorizado, etiqueta abierta, adaptativo, contempló análisis por intención a tratar (ITT) y por protocolo (PP) en 85 pacientes en total, diagnosticados al 100% con PCR-TR en una en un proporción aproximada de 2:1 entre el grupo intervención y control; para medir el outcome combinado de mortalidad por todas las causas, necesidad de UCI o VMI con el uso de metilprednisolona 40 mg/d por 3 días seguido de 20 mg/d por días, la cual no resultó en efecto benéfico en los outcomes combinados22. El METACOVID fue un EC aleatorizado (ECA), doble ciego, controlado con placebo fase IIb por ITT en 393 pacientes en total diagnosticados al 81,3% con PCR-TR en una proporción de 1:1; con 28 días de seguimiento y determinación de mortalidad a los 7, 14 y 28 días; lo cual no resultó en efecto en el outcome primario de mortalidad con metilprednisolona 0.5 mg/kg/d por 5 día comparado con solución salina23 (Tabla 1). La proporción de pacientes expuestos y no expuestos entre los estudios no fue uniforme. La medida del efecto en la mortalidad usado fue el OR e IC 95% para los estudios de cohorte, y RR en los 2 primeros EC y HR en el tercero (Tabla 2).
Tabla 2 Características de los estudios incluidos sobre el uso de corticoide en pacientes con infección por SARS- CoV-2 y el efecto en la mortalidad o supervivencia.
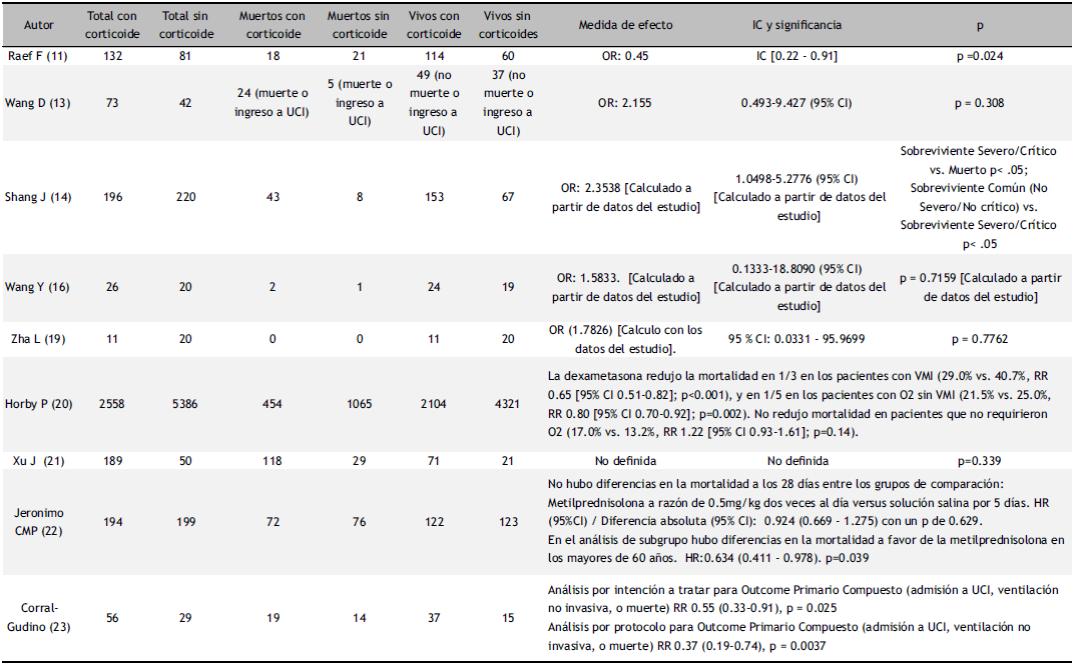
UCI: Unidad de Cuidados Intensivos. OR: Odds Ratio. RR: Risk Ratio. HR: Hazzard Ratio.
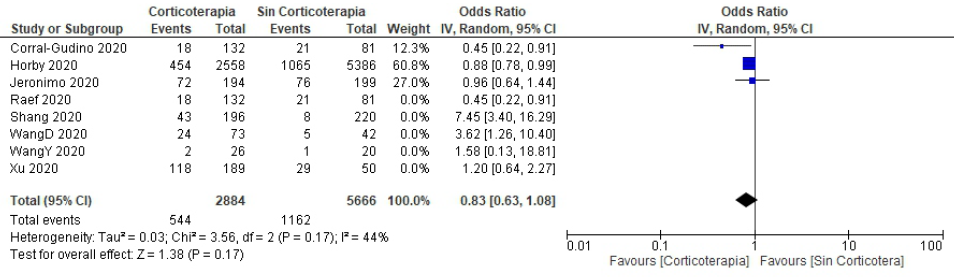
En la evaluación de sesgos se usó la herramienta NOS para cohortes; y para ECAs, se usó el ROB2. Tres de cuatro estudios de cohortes, y los dos estudios trasversales tuvieron riesgo alto de sesgo. Todos los ECAs tuvieron bajo riesgo de sesgo. Al determinar la heterogeneidad clínica y metodológica, en los estudios observacionales y de cohortes resultó alta; y baja en ECAs (Tabla 3). Al determinar el forest plot global (estudios de cohortes, transversales, y ECAs) con efectos aleatorios, la heterogeneidad estadística resultó alta sin efecto en la mortalidad de los corticoides sistémicos. Sin embargo, al analizarlos por separados, sólo los ECAs, con estimación de efectos fijos la heterogeneidad estadística resultó <50% y mostró que los corticoides tienen efecto en la disminución de la mortalidad de manera significativa. Los estudios observacionales y de cohortes tuvieron heterogeneidad clínica, metodológica y estadística alta, sin efecto en la mortalidad (Figura 2 y 3).
Tabla 3 Evaluación de sesgo de los estudios incluidos sobre el uso de corticoide en pacientes con infección por SARS- CoV-2.
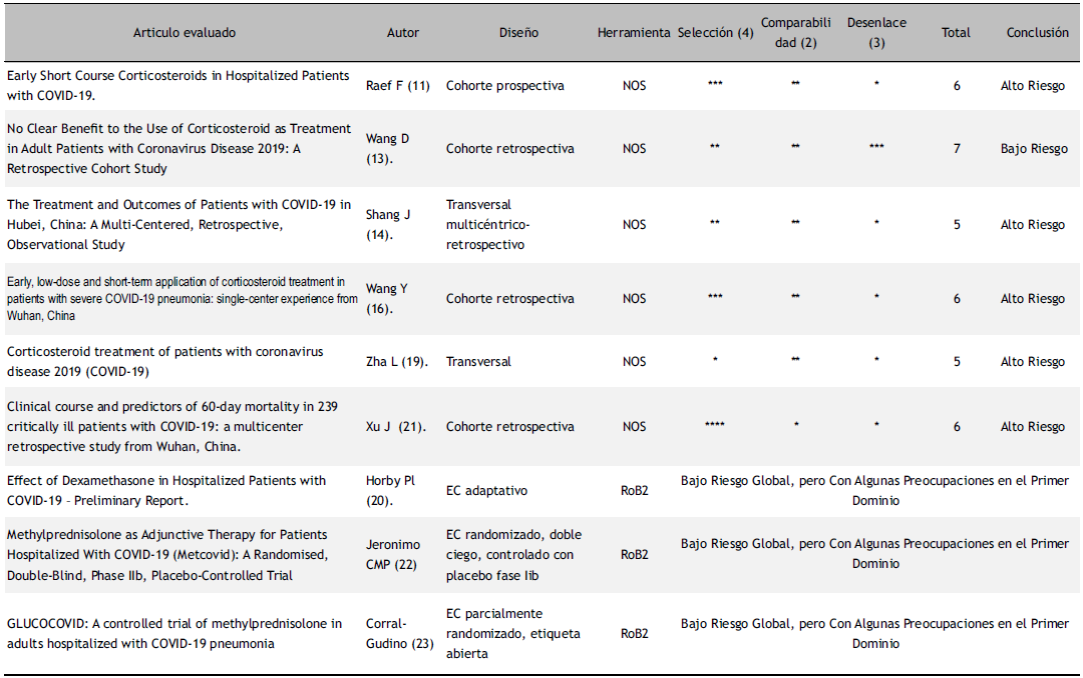
NOS: Score Newcastle-Ottawa para evaluación de estudios observacionales. RoB2: Herramienta de Cochrane para evaluación de riesgo de sesgo de ensayos clínicos. EC: Ensayos Clínicos
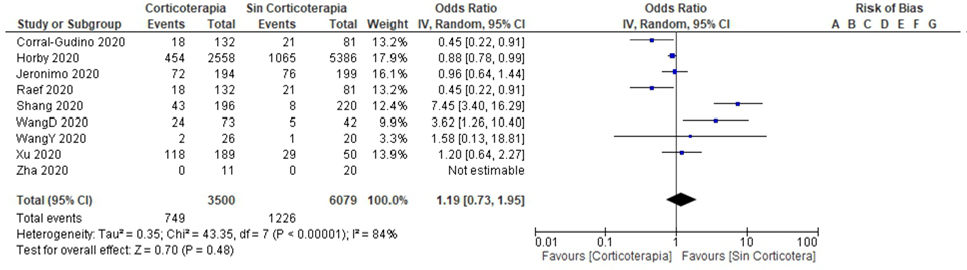
Figura 2 Forest plot global (incluyendo estudios transversales, cohortes y ensayos clínicos) sobre efecto de los corticoides sistémicos en la mortalidad de pacientes Covid-19 severo*
DISCUSIÓN
De acuerdo a nuestros resultados, los corticoides parenterales probablemente tienen un efecto benéfico sobre la mortalidad en pacientes con Covid-19 severo y SRDA [OR 0,83 (IC 95% 0,63-1,08)].
Aunque algunos estudios primarios analizados en nuestra revisión incluyeron outcomes secundarios independientes o combinados (admisión a UCI, ventilación no invasiva, con mortalidad), nosotros no realizamos un metaanálisis de outcomes secundarios, dada la heterogeneidad de estas variables en los estudios incluidos.
Nuestros resultados concuerdan con las conclusiones de otras revisiones sistemáticas y metaanálisis (RSyMETA) previamente publicadas24,25, pero se contraponen con otros estudios26-28. Sin embargo, algunos de los estudios primarios incluidos en estos estudios discordantes con el nuestro se caracterizaron por su tener alto riesgo de sesgo y una gran heterogeneidad. Siemieniuk et al., incluyeron solo pacientes con SARS-CoV-2, y analizaron dos de los estudios21,22 que nosotros también incluimos en nuestro análisis, y concluyeron que los corticoides probablemente reducen la mortalidad y la necesidad de ventilación mecánica en pacientes con Covid-1924. Ye et al., incluyeron varios estudios con etiologías diversas (Covid-19, otros coronavirus, e influenza); solo dos de estos estudios incluyeron pacientes con Covid-19, en uno de los cuales no se precisa dosis, duración, ni tipo de corticoide. Los autores concluyeron que, a pesar que la calidad de la evidencia es muy baja, los corticoides podrían reducir la mortalidad en pacientes con Covid-19 y SDRA25. Lee y col., revisaron estudios con pacientes infectados con SARS, MERS y Covid-19; en los dos únicos estudios que incluyeron pacientes con Covid- 19, no se precisa dosis ni duración del corticoide administrado. Sin embargo, a pesar que este metaanálisis no mostró diferencias en términos de mortalidad, los autores concluyeron que se debería considerar el uso de corticoides en las infecciones por coronavirus, incluyendo Covid-1927. Por el contrario, Yang Z et al., incluyendo estudios con etiologías diversas (SARS-CoV-2, SARS-CoV, MERS-CoV); aunque en ninguno de los dos estudios que se examinó pacientes con Covid-19 se especifica dosis ni duración del corticoide, se concluyó que los corticosteroides se asocian con incremento de la mortalidad en pacientes con neumonía por coronavirus26. Similar resultado mostró el estudio de Li et al., donde incluyeron pacientes con SARS-CoV-2, SARS-CoV, y MERS-CoV; sin embargo, en ninguno de los cuatro estudios primarios que incluyó pacientes con Covid-19 se especifica dosis ni duración del corticoide empleado. Los autores concluyeron que los corticoides en pacientes con infección por SARS-CoV-2, SARS-CoV, y MERS-CoV no mejoran supervivencia, no reduce la estancia hospitalaria, la necesidad de ingreso a UCI o de VMI28.
Principales fortalezas. Encontramos cinco RSyMETs publicadas hasta la actualidad, que incluyeron al menos un estudio primario sobre corticoides y Covid-1924-28. Casi todas estas publicaciones incluyeron también otros coronavirus, e incluso influenza25-27. Así mismo, en varios de los estudios primarios incluidos, no se precisa el tipo de corticoide empleado, la dosis, ni duración de la administración25-27. Si consideramos, sólo estudio primarios sobre SARS-CoV-2 y corticoides, cuatro de estas RSyMETs( 25- 27) incluyeron sólo dos estudios primarios cada una, y una de ellas incluyó cuatro estudios primarios24 sobre SARS-CoV-2 y corticoides.
Nuestro estudio incorpora estudios más recientes, más pacientes, y sólo incluye estudios primarios que únicamente incluyeron pacientes con SARS-CoV-2 y que especificaron el tipo, dosis, y duración de administración de corticoides. Todos esto, proporciona evidencia más robusta respecto al efecto de los corticoides sistémicos sobre la mortalidad en pacientes con Covid-19 severo y SDRA. Así mismo, nosotros empleamos una estrategia de búsqueda muy amplia y sensible, pero sólo incluimos estudios revisados por pares, y excluimos aquellos publicados como preprints. Otra Fortaleza de nuestro estudio es que investigadores independientes (tutores) supervisaron la extracción artículos, el análisis crítico de los mismo, y el análisis de sesgos.
Principales limitaciones. Diseño de estudio y análisis. Esta revisión tiene importantes limitaciones, principalmente respecto a la calidad variable de la evidencia disponible y la heterogeneidad. La mayoría de estudios incluidos son retrospectivos; lo cual limita la capacidad para evaluar variables confusoras y resultados clínicos. Por ejemplo, en la mayoría de estudios retrospectivos no realizaron el ajuste de variables confusoras importantes como la gravedad y grado de comorbilidad del paciente, uso de múltiples medicamentos -además de corticoides-, algunos de los cuales actualmente han sido suspendidos en el tratamiento del paciente con Covid-19 por futulidad terapéutica o por aparente incremento de ventos adversos. Así mismo, se ha reportado en varios estudios, que los pacientes de mayor gravedad, suelen recibir con más frecuencia corticoterapia. Es muy probable que todos estos factores hayan influido sobre el outcome reportado, y el efecto de los corticoides sobre la mortalidad haya sido infra o supra estimado.
Heterogeneidad de resultados. En el análisis acumulado se tomó en cuenta el modelo de efectos aleatorios para explicar la heterogeneidad. La elevada heterogeneidad entre los estudios es explicada en parte por la falta de control confusores y diferencias en tamaño de muestras entre los estudios. Así mismo, al análisis por funnel plot sugería un sesgo de publicación, aunque, debido a que finalmente solo incluimos nueve estudios este tipo de este método no es el más adecuado para evaluar este tipo de sesgo.
Importancia para la salud pública y necesidad de mayor investigación. Nuestros hallazgos podrían tener implicancias en términos de salud pública e influir en las decisiones individuales del clínico tratante. Esto resulta particularmente relevante si consideramos que la pandemia del de Covid-19 continúa en expansión. De acuerdo a la gran heterogeneidad de la evidencia actualmente disponible, y los resultados dispares en relación al beneficio de los corticoides sistémicos sobre mortalidad por Covid-19 severo, resulta evidente que se requieren más estudios con mejor diseño y que tomen en cuenta las limitaciones detectadas en esta y revisiones previas. A diferencia de otras revisiones sistemáticas y meta análisis previos, nuestro estudio incorpora un mayor número de estudios más recientes, solamente incluimos estudios primarios que exclusivamente consideraron pacientes con SARS-CoV- 2, y que precisaron el tipo, dosis, y duración de la administración del corticoide.
La revisión sistemática muestra que los corticoides parenterales podrían disminuir la mortalidad de pacientes con Covid-19 severo y ARDS.