INTRODUCCIÓN
La Enfermedad Tromboembólica Venosa (ETV) es considerada una patología de alta morbimortalidad, debido a que el 70% al 90% de personas que presentan esta patología fallece durante las primeras horas al evento; además, es la tercera causa de muerte cardiovascular, después del infarto de miocardio y el accidente cerebrovascular, presentándose en un diverso espectro de pacientes. Comprende la Trombosis Venosa Profunda (TVP) y el Tromboembolismo Pulmonar (TEP)1,2,3. La TEP se define como la obstrucción o el enclavamiento en las arterias pulmonares de un trombo desprendido de alguna zona del territorio venoso, en la mayoría de las ocasiones (90 - 95 %) se trata de una trombosis venosa profunda de miembros inferiores2. Es una urgencia cardiovascular, teniendo una incidencia por año de 70/100 000 habitantes, cuya frecuencia se incrementa en personas añosas y en presencia de múltiples comorbilidades. Generalmente los casos se manifiestan con clínica poco específica, no obstante, puede presentarse sin manifestaciones clínicas, en acontecimientos de mayor efecto trombótico, generando dificultad diagnóstica4,5.
El síndrome de Down (SD) es el trastorno genético más común y la razón primordial de discapacidad intelectual en el mundo. La Organización Mundial de la Salud estima una prevalencia mundial de 1 en cada 1 000 nacimientos vivos. En la mayoría de los casos es inducido por la presencia de todo o parte de una tercera copia del cromosoma 21. Comprende un múltiple grupo de patologías que implican casi todos los órganos y sistemas6. Si bien, los trastornos vasculares son habituales en el SD, no está claro si dichos pacientes tienen un mayor riesgo de eventos tromboembólicos venosos. Kurokami T. et al (2018), señala que las características del SD incluidos los problemas físicos y de comportamiento pueden causar ETV, indicando que pocos estudios han examinado esta relación7. Además, Girolami A et al (2020), refiere que el SD se halla circunstancialmente asociado con afecciones protrombóticas, como la variante del factor V de la coagulación (factor V de Leiden), deficiencia de metilentetrahidrofolato reductasa, defecto del factor VII (FVII Padua); para los cuales no hay información disponible, demostrando que la relación entre trastornos de la coagulación y SD es sorprendentemente rara8. Pocos estudios han examinado la relación entre SD y la incidencia de ETV. Se presenta el caso de una paciente del sexo femenino, adulto joven con SD que fue diagnosticada con neumonía adquirida en la comunidad (NAC) y Enfermedad Tromboembólica venosa asintomática.
REPORTE DE CASO
Presentamos el caso de una paciente del sexo femenino, adulto joven, de 27 años con SD, natural de Virú-Trujillo, sin comorbilidades asociadas ni uso de medicamentos, sin antecedentes patológicos, familiares y Gineco-obstétricos de importancia; que presentó cuadro de resfrió común, tos con expectoración blanquecina y sensación de elevación térmica, la cual no fue cuantificada. Después de seis días, la clínica se exacerba, asociándose disnea, por lo que es admitida en la emergencia del Hospital Belén de Trujillo. Al examen físico de ingreso se encontraba en regulares condiciones generales, con tensión arterial de 102/64 mmHg, frecuencia cardiaca de 88 lpm, frecuencia respiratoria de 32 rpm, temperatura axilar de 37 °C y saturación de oxígeno al 86% con fracción inspiratoria de oxígeno de 0,21. La paciente media 151 cm y pesaba 54 kg, lo que arrojó un índice de masa corporal de 23,3 kg/m2; se hallaba despierta, tenía discapacidad intelectual moderada, dependiente de familiar con supervisión continua, con piel y mucosas pálidas; en la auscultación de tórax se identificó murmullo vesicular disminuido en los 2/3 inferiores del pulmón izquierdo y crépitos difusos bilaterales; extremidades inferiores simétricas, de tamaño proporcional al cuerpo, de color uniforme con el resto del cuerpo, normotérmicas al tacto, sin presencia de edema. La exploración física de los demás aparatos y sistemas fue de características normales.
Se realizaron los siguientes exámenes de laboratorio, presentando: Hemograma: Leucocitos 8160/mm3, Hemoglobina: 9,9 g/dl, Hematocrito: 29,7%, Volumen corpuscular medio: 82,2 fl, Hemoglobina corpuscular media: 27,4 pg, Concentración de hemoglobina corpuscular media: 33,3 g/dl. Gasometría en sangre arterial: FiO2 0,32, ph: 7,40, Presión parcial de O2: 57.8mmHg, Presión parcial de CO2: 26,8 mmHg, Bicarbonato: 17 mEq/L, índice PaO2/FiO2: 180,6, Gradiente alveolo-arterial de O2: 136,8 mmHg, Potasio: 3,3 mEq/l, Sodio: 134 mEq/l, Lactato: 1 mmol/l. Perfil de coagulación: Tiempo de protrombina:14.2 seg, INR: 1,25, Tiempo parcial de tromboplastina activada: 36,6 seg. Lactato deshidrogenasa: 620 u/L. Glucosa: 96 mg/dl, Urea: 14 mg/dl, Creatinina: 0,74 mg/dl. Perfil tiroideo: TSH: 1,30µU/mL, T4L: 1,42 ng/dl, T3: 1,26 ng/ml. Cultivo de esputo para bacterias se detectó la presencia de Klebsiella oxytoca (K. oxytoca).
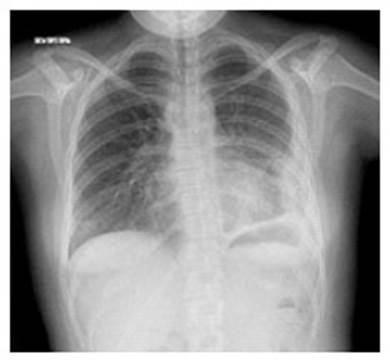
En la radiografía de tórax posterior-anterior se evidenció: condensación en los 2/3 inferiores y obliteración de seno costofrénico del pulmón izquierdo (Figura 1).
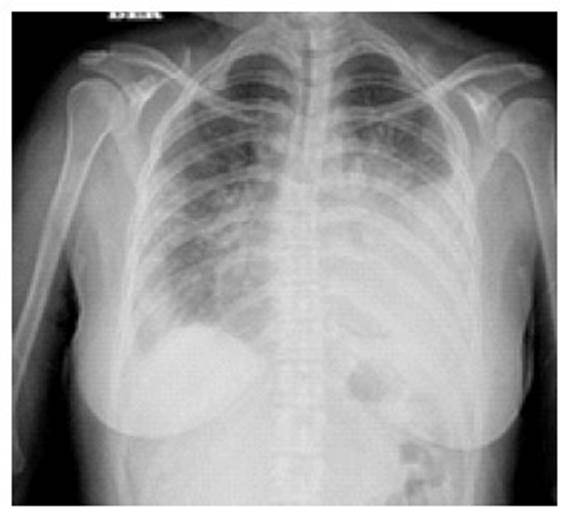
Figura 1 Radiografía postero-anterior de tórax: Imagen de condensación en los 2/3 inferiores del pulmón izquierdo y velamiento de su seno costofréniico.
La paciente es diagnosticada con: Insuficiencia Respiratoria Aguda, NAC causada por K. oxytoca y Síndrome de Interposición Líquida en hemitórax izquierdo, siendo hospitalizada en el servicio de neumología, iniciando tratamiento antibiótico por via endovenosa con: Cefepime (cefalosporina de cuarta generación) a dosis de 2 g cada ocho horas y Ciprofloxacino (quinolona de segunda generación) a dosis de 200 mg cada doce horas; además; hidratación con solución salina fisiológica a 30 gotas por minuto, oxigenoterapia con Macarilla de Venturi, Omeprazol (inhibidor de bomba de protones) a dosis de 40 mg por vía endovenosa cada veinticuatro horas y Metamizol (analgésico y antipirético) a dosis de 1 g por via endovenosa condicional a temperatura mayor a 38°C.
Al noveno día de hospitalización, la paciente presenta una evolución clínica estacionaria, persistiendo síntomas iniciales y requerimiento de oxígeno, que impedía movilización, de igual forma, al examen físico no presentó signos clínicos de TVP; por tal razón, para complementar estudio se le solicita la prueba del Dímero D obteniendo un resultado de 2,90 ug/ml y posterior a ello se le realiza una Tomografía computarizada de tórax, que muestra una imagen sugestiva de émbolo central de gran dimensión en la arteria pulmonar y su rama lobular media del lado derecho; lo cual se confirma por medio de una Angiotomografía donde se evidencia defecto de llenado en bifurcación de la rama derecha; asimismo, focos de condensación pulmonar bilaterales a nivel de bases y vértice hiliar derecho, dando como conclusión: Tromboembolia pulmonar y neumonía basal bilateral (Figura 2A Y 2B).
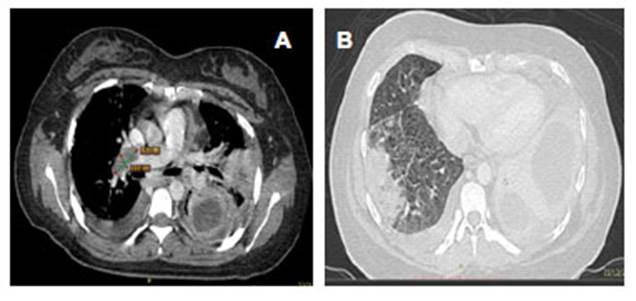
Figura 2 Tomografía de tórax: Tromboembolia pulmonar, embolo (3,11x1.23 cm). en arteria pulmonar y su rama lobular media (A). Condensación pulmonar bilateral a nivel de bases y vértice hiliar derecho (B).
Resultados de estudios complementarios: Ecografía doppler de miembros inferiores, reveló: dilatación del diámetro de la vena femoral derecha, con ecos internos mixtos en lumen movible, fluctuante en luz, parcialmente compresible y con flujo doppler excéntrico; vena poplítea derecha con presencia de flujo doppler y compresible completamente; venas de miembro inferior izquierdo (femoral y poplítea) compresibles totalmente y con presencia de flujo doppler. Concluyendo en TVP de vena femoral común y superficial derecha. Por otra parte, el Electrocardiograma no mostró alteración y la Ecocardiografía evidenció un corazón estructural y funcionalmente normal. Ante la TEP y TVP, se consideró la posibilidad de trombofilia hereditaria y se evaluó a la paciente con un perfil de trombofilia compuesto por proteína C, proteína S, antitrombina III y anticuerpo antifosfolipídico, todos estaban dentro de los limites normales; también, se le solicitud Anticuerpos antinuclerares con resultado negativo. En base a lo descrito, se inició tratamiento anticoagulante con heparina de bajo peso molecular tipo Enoxaparina a dosis de 40 mg por vía subcutánea cada 12 horas y warfarina a dosis de 5 mg por vía oral cada veinticuatro horas. Paciente evolucionó favorablemente, con disminución progresiva de requerimientos de oxígeno, mostrándose asintomática y hemodinámicamente estable; presentando únicamnete pasaje de murmullo vesicular disminuido a niviel basal de pulmón izquierdo, con radiografía de tórax control al día dieciocho de hospitalización (Figura 3) e INR en rango terapeútico (INR: 2,44). Se decidió dar alta médica, indicando continuar con tratamiento antibiótico vía oral y warfarina en casa (se verificó que paciente cuenta con supervisión continua y que tratamiento estaría vajo control de familiar); así como seguimiento por consultorio externo de neumología para control de Tiempo de protrombina e INR.
DISCUSIÓN
La ETV hoy en día sigue manteniendo una incidencia variable y una alta morbimortalidad a causa de la variada forma de presentarse clínicamente; puede afectar a todo individuo que muestre factores de riesgo. Actualmente se considera que la ETV es una consecuencia de la interacción entre los f a c t o r e s d e r i e s g o r e l a c i o n a d o s c o n e l p a c i e n t e (generalmente permanentes) y su contexto (generalmente temporales) (tabla 1)1,3,4. No obstante, hasta 20% de pacientes con TEP, no tiene factores de riesgo identificables (idiopática)9) .
Por tanto, ante la sospecha de TEP, se deben examinar los factores de riesgo y los componentes clínicos; su acoplamiento permite establecer una probabilidad clínica, es así que se emplea el Puntaje de Wells, el cual es el más utilizado, en donde se divide a los pacientes en dos grupos de probabilidad: baja o alta (tabla 2), normando el proceder diagnostico a tomar, mediante el uso de exámenes de laboratorio e imagen. Hecho el diagnóstico de TEP, se estratifica el riesgo, para lo cual se utiliza la escala PESI (Pulmonary Embolism Severity Index), altamente validada, dividendo a los pacientes en 5 grupos de riesgo (tabla 3); contemplando el peligro de muerte, descomposición hemodinámica y sangrado mayor3,4.
De lo antes mencionado, se puede inferir que el diagnóstico de TEP es difícil4, y gran parte de la orientación hacia él se da por la correspondencia entre variables asociadas al historial patológico del paciente; en el presente caso, la paciente presentaba como factores de riesgo: infección respiratoria (específicamente neumonía)1) complicada con sepsis (la cual aumenta la incidencia de ETV en aproximadamente de 3 a 10 veces más)10, inmovilización y reposo en cama mayor a 3 días, los cuales no son los desencadenantes habituales para su desarrollo; además, se señala en un consenso que el sexo masculino y la edad mayor de 80 años son los dos factores más importantes para su presentación, en el caso, no los cumple la paciente4. Asimismo, debido a su comorbilidad genética y poca frecuencia de asociación con ETV7, su presentación clínica relacionada con patología neumónica concomitante que se superpone, se presentó demora para establecer el diagnóstico definitivo.
Si bien, se ha mencionado que los pacientes con SD presentan trastornos vasculares, incluidas afecciones protrombóticas, su asociación con ETV es rara7. Se ha documentado que en los pacientes adultos jóvenes la aparición de TEP es infrecuente10, del mismo modo hay escasos informes previos de TEP en pacientes con SD. En nuestra paciente consideramos que el desarrollo de ETV tuvo como factor de riesgo principal la neumonía causada por K. oxytoca complicada con sepsis. Se sabe que la cascada de inflamación desencadenada por la infección aguda, causa disfunción endotelial, un estado de hipercoagulabilidad transitoria, caracterizada por presentar: trombocitosis, niveles plasmáticos elevados de fibrinógeno, factor VIII e inhibidor del plasminógeno 1, asociados con niveles reducidos de antitrombina III y proteína C, y estasis del flujo sanguíneo debido a inmovilidad causada por compromiso respiratorio10,11,12,13,14, que conllevó a la aparición repentina de trombosis p r o f u n d a d e l m i e m b r o i n f e r i o r d e r e c h o c o n tromboembolismo pulmonar. Además, como se informó en un estudio los pacientes con SD presentan debilidad en la fuerza del músculo extensor de la rodilla, debido a la falta de desarrollo fisiológico de la fuerza muscular característica de estos pacientes; debido a lo cual, tendrían mayor riesgo de estasis venosa en las extremidades inferiores, en comparación con personas sin SD6,7 . Por lo tanto, especulamos que el SD en adultos jóvenes es un factor de riesgo para el desarrollo de dicha patología; de hecho, en un estudio anterior se reportó el caso de un adolescente con SD quien desarrolló Trombosis venosa cerebral sin presencia a l g u n a d e f a c t o r e s d e r i e s g o p a r a trombosis15 . Adicionalmente se descartó la posibilidad de trombofilia hereditaria y enfermedades autoinmunitarias como posibles causas de ETV en esta paciente.
Como se menciona, esta patología generalmente es asintomática debido a que la mayoría de émbolos pulmonares son pequeños16; sin embargo, en el caso la paciente presenta un émbolo central de gran dimensión en la arteria pulmonar y su rama lobular media del lado derecho, que de acuerdo a su correlación clinica, debería generar síntomas marcados, por ejemplo, dolor anginoso de pecho intenso secundario a isquemia de ventrículo derecho; signos clínicos de hipoperfusión tisular, shock manifiesto con hipotensión s o s t e n i d a e i n c l u s o p a r o c a r d i o r r e s p i r a t o r i o 4 . C o n t r a r i a m e n t e , l a p a c i e n t e n o p r e s e n t ó d i c h a s manifestaciones, por lo que se presenta un caso atípico. Una revisión sistemática y un metanálisis estimaron que la prevalencia general de esta afección es del 2,6%, la cual varía del 1,2% al 4% en pacientes ambulatorios y hospitalizados respectivamente, además ésta aumenta con la edad5.
Adicionalmente a esto, la paciente presentó una probabilidad clinica baja (1,5: Inmovilización prolongada), que conllevó a adaptar el diagnóstico de acuerdo a la gravedad de presentación clínica, realizando la prueba de Dímero-D por su alto valor predictivo negativo (95%), la cual resultó elevado, y posteriormente angiotomografía, confirmando el diagnóstico de TEP. El diagnóstico se realizó de acuerdo al algoritmo dado por la Sociedad Europea de Cardiología. Después al estratificar el riesgo, se determinó como bajo (67 puntos), los cuales se benefician con anticoagulación, iniciándose tratamiento4. En nuestra paciente se optó por una terapia con heparina de bajo peso molecular y warfarina con controles periódicos de INR, teniendo evolución favorable. Es importante mencionar también, que los pacientes con sepsis por su estado p r o c u a g u l a n t e , s e b e n e fi c i a r á n c o n e l u s o d e tromboprofilaxis17,18. Así tenemos, que la anticoagulación profiláctica reduce la incidencia de ETV entre un 50% y un 75%, tanto en pacientes quirúrgicos como médicos hospitalizados14. Sin embargo, en pacientes con sepsis también se identifica una alta incidencia de ETV (37,2 %) a pesar del uso de tromboprofilaxis, lo que sugiere que la sepsis con frecuencia desarrollará ETV a pesar de recibir tromboprofilaxis universal recomendada por las guías10.
En este caso, también se encontró, que el cuadro de tromboembolia pulmonar se acompañó de trombosis venosa profunda de miembros inferiores, que es una asociación muy frecuente. Se ha descrito que hasta 50% al 70% de pacientes con TEP la TVP es positiva, peculiarmente de la extremidad inferior en su porción proximal(4).
Otro aspecto que llama la atención en este caso es la presencia de Klebsiella oxytoca como agente causal de neumonía; ya que, es una causa singularmente rara de neumonía adquirida en la comunidad afectando en 1-5% de pacientes. Su origen podría estar relacionada con el déficit inmunitario, considerado un factor de riesgo significativo para su desarrollo, el cual presentan los pacientes con SD. El caso tuvo una presentación clínica típica de este agente, ocasionando enfermedad con infiltrados bilaterales característicos de la enfermedad aguda19.
En conclusión, nuestro caso destaca que la relación entre ETV y SD es poco frecuente en la práctica clínica. Pero especulamos que las características de SD, incluidas su déficit inmunitario que predispone a infecciones agudas por agentes poco frecuentes y problemas físicos, influyen como causa de ETV. Por lo tanto, se requiere mayor investigación, mayor acumulación de casos y estudios prospectivos para confirmar la asociación de SD y ETV, y explorar posibles mecanismos; para lograr una mejor comprensión, abordaje diagnóstico, tratamiento y prevención, con el fin de mejorar la atención y mejorar los desenlaces clínicos de los pacientes. Además, a la vista de nuestro caso también consideramos que, aunque el SD no es necesariamente una patología a de s t a c a r como desencadénate de un evento t r o m b o e m b ó l i c o , s i d e b e m o s t e n e r l a e n c u e n t a . Recomendamos a los médicos mantener la posibilidad de ETV cuando realicen un seguimiento de pacientes con SD, y que i n c l u y a n a l S D en su evaluación de riesgos de tromboembolismo