INTRODUCCIÓN
La anemia es un problema de salud pública en todo el mundo y sigue siendo un problema grave en el Perú1. La anemia está presente en un tercio de la población mundial y está liderada por la deficiencia de hierro2. En Perú, la anemia infantil afecta al 43,6% de los niños y niñas de 6 a 36 meses, siendo más prevalente en los niños de 6 a 18 meses, siendo este un grupo en el que seis de cada diez niños presentan anemia5.
En Perú, el patrón de alimentación es el consumo de hierro de origen vegetal, se observa una ingesta diaria promedio per cápita de hierro de 1.6 mg en las familias de los quintiles más bajos, mientras que en las familias de los quintiles más ricos se observa una ingesta diaria per cápita de 3.6 mg5. Un estudio realizado en Ayacucho, demostró que los niños de 6 a 23 meses tienen una ingesta reducida de hierro, zinc, calcio y niacina. Así, el 90% de los niños no alcanza los niveles recomendados de este nutriente6. Se describen hallazgos similares en Villa el Salvador al sur de Lima en niños de 6 a 11 meses7. En Arequipa, provincia donde se realizó este estudio, la prevalencia de anemia en niños menores de tres años fue del 44,5% en 20164.
Los sistemas de salud están muy interesados en optimizar las reservas de hierro del cuerpo humano en etapas muy tempranas del desarrollo infantil cuando hay un rápido desarrollo cerebral8. El desarrollo infantil es un proceso de cambios continuos. Las áreas del desarrollo infantil en las que se ha reconocido una fuerte asociación con la anemia incluyen el desarrollo mental, motor y conductual del individuo9. Por tanto, se han implementado intervenciones de suplementación con hierro en los sistemas sanitarios de nuestro país1. Sin embargo, la suplementación con hierro y micronutrientes requiere de estudios bien diseñados en Perú, ya que se ha demostrado una baja adherencia y, en consecuencia, una baja efectividad10.
Investigaciones anteriores coinciden en que el enriquecimiento de alimentos es la mejor estrategia a largo plazo en la prevención de la deficiencia de hierro en la población general11. Se sabe que la leche es una de las principales fuente de alimento en la infancia; la leche de vaca tiene una menor densidad y biodisponibilidad del hierro,12,13. Se recomienda lactancia materna exclusiva en los primeros seis meses de vida y su continuación hasta los veinticuatro meses de edad 3). Los productos lácteos podrían ser una opción viable y sostenible para combatir la anemia en niños mayores de dos años Sin embargo, los ensayos clínicos aleatorizados sobre el efecto de los productos lácteos fortificados con hierro y zinc sobre los niveles de hemoglobina son mínimos a nivel local. El estudio pretende cerrar la brecha de información existente para desarrollar una estrategia de control de la anemia en Perú.
En este contexto, nuestro estudio tiene como objetivo evaluar el efecto de la suplementación de una mezcla láctea fortificada con hierro-zinc sobre los niveles de hemoglobina e índices antropométricos en una población infantil de 2 a 10 años con o sin anemia leve.
MATERIAL Y MÉTODO
Diseño
Ensayo clínico aleatorizado, doble ciego y de grupos paralelos, controlado con producto lácteo no fortificado con hierro y zinc.
Participantes
El estudio se realizó en el "Centro de Salud Juan Pablo II" en el distrito de Yura, provincia de Arequipa, un área rural y urbana ubicada a 2.590 metros sobre el nivel del mar (msnm) que cuenta con una población de 18.127 habitantes. En el área rural de Arequipa, solo el 53% de los jefes de hogar tienen educación primaria, el 29% son pobres y el 2% vive en pobreza extrema (14. En la población infantil de menores de cinco años del distrito de Yura, el 68% no cuenta con suplementos de micronutrientes de acuerdo con su edad. Según el Informe “Perú: consumo per cápita de los principales alimentos 2008 - 2009, INEI (2009), en el departamento de Arequipa se evidenció un consumo per cápita de 57.5 kg/persona de papa, 32,7 de pan, 30.2 de arroz, 18,9 de pollo, res 11,6, pescado 3,9 y lácteos 12,5. Siendo el distrito de Yura parte del departamento de Arequipa, podemos corroborar que coincide con los hábitos de consumo reportados por la población estudiada. Cabe mencionar que a la población estudiada se les brindó talleres y charlas de promoción de alimentación saludable. La población en estudio, no cuentan con agua potable ni desagüe.
Se incluyeron en el estudio niños de ambos sexos entre 2 y 10 años. Podían ingresar niños de 2-5 años con corrección de niveles de hemoglobina a 2.590 msnm ≥10 gr/dL y niños de 6-10 años con corrección de niveles de hemoglobina ≥11 gr/dL que también pudieran estar siguiendo tratamiento con hierro. El ajuste de los niveles de hemoglobina según la altura sobre el nivel del mar se realizó mediante la aplicación del factor de ajuste, cuya fórmula es: Nivel de hemoglobina ajustado = hemoglobina observada - factor de ajuste por altitud. Se excluyeron niños con desnutrición crónica, parasitosis intestinal, enfermedades crónicas, enfermedades congénitas, infecciones ocurridas la semana anterior al estudio, trastornos que requirieran una dieta especial (intolerancia o intoxicación alimentaria), dispepsia o estreñimiento, consumo de fármacos que pudieran interferir con la absorción de hierro, alergia o intolerancia conocida a los componentes de los productos lácteos, los que habían recibido otro suplemento nutricional y las familias que planeaban viajar en los primeros siete meses después del tratamiento.
Tamaño de la muestra
El tamaño de la muestra se basó en probar la hipótesis de que los niveles de hemoglobina eran más altos en el grupo que recibió la mezcla láctea fortificada con hierro y zinc que en el grupo que recibió la mezcla láctea no fortificada.
Estimamos que la magnitud de la diferencia para la relevancia clínica identificada fue de 1 gr/dL de hemoglobina para el grupo que recibió la mezcla láctea fortificada con hierro-zinc, con una desviación estándar de 1.2 gr/dL, riesgo de error del 5%, el poder estadístico del 90%, hipótesis unilateral. Con estos parámetros el tamaño de muestra calculado fue de 64 niños. Sin embargo, se tuvo en cuenta un potencial de pérdida del seguimiento del 10%, y finalmente se estimaron 72 participantes para el estudio. La población accesible estuvo constituida por 209 niños de 2 a 10 años, de los cuales 96 cumplieron los criterios de selección. En esta población elegible, 22 padres no aceptaron firmar un consentimiento informado, por lo que finalmente 67 niños fueron incluidos en el estudio.
Aleatorización, ocultación de la asignación y cegamiento
Un total de 67 niños fueron inscritos y asignados al azar a uno de los dos grupos. El grupo experimental (n=32) recibió la mezcla láctea fortificada con hierro y zinc, mientras que el grupo de control (n=35) recibió la mezcla láctea no fortificada. El método utilizado para generar la secuencia de asignación aleatoria consistió en tablas de números aleatorios desarrolladas por un estadístico independiente que no participó en el estudio. Dado que no se podía acceder a la secuencia de asignación aleatoria; ni los participantes ni los investigadores del estudio conocían de antemano la intervención en la que se asignarían los sujetos. Las mezclas lácteas fueron administradas al grupo experimental y de control por nutricionista quien no conocía sobre la asignación de los participantes a los grupos de estudio. También se tuvieron en cuenta las características organolépticas de los productos lácteos, que eran muy similares. Las mezclas lácteas eran de color crema y tenían un olor y sabor característico, así como un aspecto uniforme. La presentación fue un recipiente metálico de 400 gramos para ambos grupos. Los investigadores estaban cegados a los resultados de los niveles de hemoglobina durante todo el estudio. Los familiares de los niños no sabían el tipo de mezcla láctea que estaban tomando sus hijos.
Intervenciones y medidas
La mezcla láctea fortificada con hierro-zinc se administró al grupo experimental y la mezcla láctea no fortificada se administró al grupo de control.
Las dos mezclas lácteas se consideraron alternativas razonables al tratamiento nutricional de los niños, pero queríamos saber si la mezcla láctea enriquecida era superior para mejorar los niveles de hemoglobina.
Además del lácteo, los niños de ambos grupos que presentaban anemia leve al inicio de la intervención recibieron tratamiento con hierro (fumarato ferroso 3mg/Kg), que fue brindado por el personal del Centro de Salud Juan Pablo II en el distrito de Yura, Arequipa.
Las mezclas lácteas utilizadas en el estudio se obtuvieron por el financiamiento de una empresa productora y comercializadora de productos lácteos con registro sanitario otorgado por la Dirección General de Salud Ambiental del Perú.
El estudio de intervención dietética, que tuvo un seguimiento de 24 semanas, comenzó en junio de 2019 y finalizó en diciembre de 2019.
Al grupo experimental (n=32) se le administraron 300 ml (150 gramos de la mezcla láctea enriquecida+150 ml de agua) dos veces al día. Esta mezcla láctea se obtuvo de la combinación de leche entera y otros ingredientes como maltodextrina de maíz, aceite de soja, suero de leche y minerales (pirofosfato de hierro y sulfato de zinc) enriquecidos con Vitaminas A y D.
Al grupo de control (n=35) se le administraron 300 ml (150 gramos de la mezcla láctea no fortificada+150 ml de agua) dos veces al día. Esta mezcla láctea se obtuvo de la combinación de leche desnatada y suero de mantequilla con otros ingredientes como extracto de soja, maltodextrina y aceite vegetal enriquecido con vitaminas A y D y aditivos alimentarios autorizados. Ambas mezclas lácteas fueron pasteurizados, homogeneizados y enlatados en recipientes metálicos sanitarios para alimentos, sellados herméticamente y sometidos a un tratamiento de esterilización térmica para estar disponibles comercialmente. Los perfiles nutricionales detallados de ambos productos se muestran en la Tabla 1.
Tabla 1 Composición nutritiva de las mezclas lácteas fortificada y no fortificada
| Nutrientes | Mezcla láctea fortificada (porción de 100g) | %RD | Mezcla láctea no fortificada (porción de 100g) | %RD |
| Energía (kcal) | 127 | 134 | ||
| Grasa total (g) | 7 | 9 | 7,5 | 12 |
| Grasa láctea (g) | 2,7 | 2,0 | ||
| Grasa vegetal (g) | 4,3 | 5,3 | ||
| Grasa saturada (mg) | 3,8 | 19 | 3,7 | 19 |
| Grasas Trans (mg) | 0,1 | 0,1 | ||
| Colesterol (mg) | 8 | 3 | 10 | 3 |
| Sodio (mg) | 107 | 5 | 80 | 3 |
| Carbohidratos totales (g) | 11,7 | 4 | 12,4 | 4 |
| Fibra dietaria (g) | 0 | 0 | 0 | |
| Azúcares totales (g) | 7 | 8 | 5,7 | |
| Azúcares añadidos (g) | 0 | 0 | ||
| Proteínas (g) | 4,2 | 8 | 3,9 | 8 |
| Calcio (mg) | 153 | 15 | 170 | 17 |
| Fósforo (mg) | 139 | 20 | 103 | 15 |
| Hierro (mg) | 3,3 | 15 | 0 | 0 |
| Zinc (mg) | 2,1 | 15 | 0 | |
| Vitamina A (ugRE) | 240 | 30 | 240 | 30 |
| Vitamina D (ug) | 1,5 | 30 | 1,5 | 30 |
Fuente. Hoja Técnica. “Mezcla láctea compuesta con maltodextrina y aceite vegetal, enriquecida con vitaminas y minerales-Pura Vida”. Hoja Técnica “Mezcla láctea compuesta con extracto de soya, maltodextrina, y aceite de soya-La Pradera” de la empresa fabricante.
Los promotores de salud recibieron capacitación y participaron en talleres demostrativos sobre cómo preparar mezclas lácteas. La capacitación incluyó buenas prácticas de manipulación de alimentos, distribución de dosis, así como instrucciones para el cronograma de administración de las mezclas. La mezclas lacteas se dividieron en dos tomas diarias: por la mañana (entre las 9:30 y las 10:30 horas) y por la tarde (entre las 14:30 y las 15:30 horas). La secuencia de administración de los lácteos fue la misma tanto por la mañana como por la tarde; cada dosis consistió en (150 gramos de mezcla láctea con 150 ml de agua); la mezcla láctea enriquecida aportó (381 Kcal 9,9 mg de hierro y 6,3 mg de zinc) y la mezcla láctea sin fortificar aportó (402 Kcal, sin aporte de hierro ni zinc) por día y se administró cinco días a la semana, durante 24 semanas.
Este procedimiento se registró en tarjetas y luego en un libro de registro dos veces al día. Los nombres completos de los niños, los códigos de identidad, la edad, el sexo, la residencia, los nombres de los familiares, el nombre de la institución educativa, los horarios de las fechas de administración, los efectos secundarios leves, los efectos adversos significativos, los niveles de hemoglobina y las mediciones antropométricas se registraron en las tarjetas al principio y fin del estudio. Para las mediciones antropométricas se utilizó una balanza Seca modelo 803 y una vara de medir estandarizada siguiendo los lineamientos del Instituto Nacional de Salud en Perú. Un antropometrista y un asistente realizaron estas mediciones.
Se realizó una reunión mensual con los padres de los niños para conocer la tolerancia y los probables efectos secundarios. Asimismo, se programaron contactos telefónicos y visitas semanales a los niños y sus familiares. Dos nutricionistas independientes realizaron el suministro de mezclas lácteas en instituciones educativas, y la cantidad requerida se distribuyó mensualmente. Los dos grupos fueron monitoreados de manera similar. La supervisión de la administración de las mezclas lácteas fue realizada inesperadamente por los investigadores en cada punto de distribución tres veces por semana. Se revisaron los libros de registro de los niños de los grupos experimental y de control para evaluar si los dos grupos tenían una buena aceptación de las mezclas lácteas o no.
Desenlaces
Desenlace primario
Se eligió el nivel de hemoglobina en sangre como variable de respuesta o resultado principal. Se completaron tres mediciones de hemoglobina durante el seguimiento. La primera medición tuvo como objetivo determinar la prevalencia de anemia para seleccionar niños con o sin anemia leve para el estudio. Otras mediciones correspondientes al inicio y final del seguimiento se realizaron en julio, septiembre y diciembre. Los niveles de hemoglobina se obtuvieron mediante un muestreo capilar del lado lateral del dedo medio utilizando una lanceta estéril desechable (2 mm de longitud). Las muestras fueron analizadas en el laboratorio del centro de salud de Ciudad de Dios, Arequipa, utilizando una mini centrífuga BOECO HP-240.
Análisis estadístico
Todos los análisis se realizaron mediante el análisis por intención a tratar. Se tuvo en cuenta el efecto de la altitud para la corrección de los niveles de hemoglobina; el presente estudio se realizó a 2.590 msnm; el factor de ajuste para la altitud fue 1,3 utilizando la siguiente fórmula:
Nivel de hemoglobina ajustado = nivel de hemoglobina observado - factor de ajuste por altitud15.
Las variables numéricas se presentan como media y la desviación estándar (DE) y las variables categóricas se presentan como frecuencias y porcentajes. Las comparaciones entre las medias de hemoglobina se llevaron a cabo utilizando la prueba t de Student pareada para comparar las diferencias entre la línea de base y el punto final en cada grupo. Se utilizó la prueba de la t de Student para muestras independientes, cuyo objetivo fue analizar las diferencias entre los grupos de estudio al final del seguimiento. Las comparaciones entre variables categóricas se hicieron con la prueba Chi cuadrado. La significancia estadística tuvo un valor p<0.05. Todos los análisis de datos se realizaron utilizando el software STATA, versión 14.0.
Consideraciones éticas
A los padres de los niños en edad preescolar y escolar que cumplieron con los criterios de selección se les solicitó firmar el consentimiento informado en diferentes aulas de las siete instituciones educativas involucradas en la investigación. El estudio se realizó de acuerdo con los lineamientos de la declaración de Helsinki, y todos los procedimientos que involucraron seres humanos fueron aprobados por el Comité de Ética del Hospital Nacional Alberto Sabogal, Lima, Perú (Carta N ° 185-CIEI-OFI & DGRPS-HNASS-ESALUD -2019). Debido a que este ensayo clínico evalúa un alimento procesado, no se requirió su inscripción en el Registro de Ensayos Clínicos del Perú del Instituto Nacional de Salud.
RESULTADOS
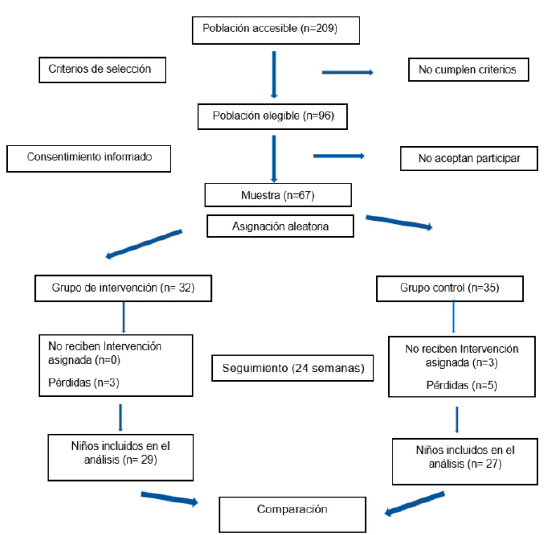
Un total de 67 niños fueron asignados aleatoriamente a los dos grupos de estudio. De ellos, 32 niños fueron incluidos en el grupo experimental, mientras que 35 fueron incluidos en el grupo de control. En el seguimiento, tres y cinco niños no continuaron participando en el estudio debido a efectos secundarios leves como dolor abdominal intermitente y no pudieron asistir regularmente a la institución educativa. Tres niños no recibieron la intervención asignada en el grupo control por motivos personales (Figura 1). La población incluida en la línea de base del estudio tenía características similares en cuanto a edad, sexo, tamaño e índice de masa corporal. La edad promedio de los niños inscritos en el grupo experimental fue de 6,1 años (DE=2,3) y la edad media en el grupo de control fue de 5,5 años (DE=2,4). En cuanto al género, se incluyeron 16 hombres y 16 mujeres en el grupo experimental, mientras que 21 y 14 se incluyeron en el grupo control. Al inicio del estudio, la concentración media de corrección de los niveles de hemoglobina a 2.590 msnm fue de 11,8 gr/dL (DE=0,5) en el grupo experimental y de 11,5 gr/dL (DE=0,7), (p=0,42) en el grupo de control (Tabla 2).
Tabla 2 Características basales demográficas y clínicas para cada grupo
| Variables | Total (n=67) | Experimental (n=32) | Control (n=35) |
| Edad (años) | 5,8 (2,4) | 6,1 (2,3) | 5,5 (2,4) |
| Género (Masculino/Femenino) | 37/30 | 16/16 | 21/14 |
| Peso (Kg) | 21,1 (7,2) | 23,0 (8,2) | 19,3 (5,8) |
| Talla (m) | 1,1 (0,1) | 1,1 (0,1) | 1,1 (0,1) |
| IMC (Kg/m2) | 17,0 (2,0) | 17.5 (2,2) | 16,5 (1,8) |
| Hemoglobina (g/dL) | 11,7 (0,6) | 11.8 (0,5) | 11,5 (0,7) |
Promedio (desviación estándar)
IMC, índice de masa corporal
Se evidenció un aumento de la concentración de hemoglobina en ambos grupos al final de la intervención, estadísticamente significativo. La hemoglobina aumentó en 1,31 gr/dL, (p<0,001) en el grupo experimental, mientras que aumentó en 0,57 gr/dL, (p<0,001) en el grupo de control. Al final de la intervención, la hemoglobina fue de 13,1 gr/dL (DE=0,9) en el grupo experimental y de 12,1 gr/dL (DE=0,8) en el grupo control. Al final del estudio, la diferencias de medias entre ambos grupos fueron a favor del grupo experimental en 1.03 gr/dL, DE=0.21 (p<0.001) (Tabla 3).
Tabla 3 Diferencias basal y al final del seguimiento para las variables de resultado entre los grupos de estudio
| Variables | Diferencia total | Valor pa | Diferencia entre el grupo experimental | Valor pa | Diferencia entre el grupo control | Valor pa | Diferencia entre los grupos al termino de seguimiento | Valor pb |
| Hemoglobina (g/dL) | 0,92 (0,93) | <0,001 | 1,31 (0,92) | <0,001 | 0,57 (0,81) | <0,001 | 1,03 (0,21) | <0,001 |
| Peso (Kg) | 2,49 (2,26) | <0,001 | 3,09 (2,37) | <0,001 | 1,95 (2,04) | <0,001 | 4,84 (2,00) | <0,001 |
| Talla (m) | 0,04 (0,02) | <0,001 | 0,05 (0,02) | <0,001 | 0,04 (0,03) | <0,001 | 0,07 (0,03) | 0,045 |
| IMC (Kg/m2) | 0,56 (1,19) | <0,001 | 0,76 (1,42) | <0,005 | 0,38 (0,93) | 0,019 | 1,28 (0,59) | 0,032 |
Promedio (desviación estándar)
IMC, índice de masa coporal
a t de Student para muestras pareadas
b t de Student para muestras independientes
En cuanto a los índices antropométricos al inicio del estudio, el peso promedio fue de 23 Kg (DE=8,2), talla 1,1 metros (DE=0,1) e índice de masa corporal (IMC) de 17,5 Kg/m2 (DE=2,2) en el grupo experimental, mientras que el peso medio fue de 19,3 Kg (DE=5,8), talla 1,1 metros (DE=0,1) e IMC 16,5 Kg/m2 (DE=1,8) en el grupo control (Tabla 2).
Al final de la intervención, el peso aumentó en 3,09 Kg, DE=2,37, (p<0,001), la talla aumentó en 0,05 metros, DE=0,02 (p<0,001) y el IMC aumentó en 0,76 kg/m2 (DE=1,42) (p <0,005) en el grupo experimental. En el grupo de control, también hubo cambios en las medidas antropométricas. El peso aumentó en 1,95 Kg (DE=2,04) (p<0,001), el tamaño fue el mismo y el IMC aumentó en 0,38 Kg/m2 (DE=0,93) (p<0,001). Al final del estudio, se observaron diferencias en ambos grupos con respecto a las siguientes variables: peso: 4,84 Kg (DE=2,00) (p=0,001), talla: 0,07 metros, DE=0,03 (p=0,045) e IMC: 1,28 Kg/m2 (DE=0,59) (p=0,032). Estas diferencias fueron estadísticamente significativas en el grupo experimental (Tabla 3).
DISCUSIÓN
Este estudio es el primer ensayo clínico aleatorizado, doble ciego y controlado, realizado con niños nutricionalmente vulnerables de 2 a 10 años en un área distante con escasos recursos económicos ubicada a 2.590 metros sobre el nivel del mar en el distrito de Yura, Arequipa, Perú. Nuestros resultados muestran que la ingesta diaria del mezcla láctea fortificada con 9,9 mg de pirofosfato de hierro y 6,3 mg sulfato de zinc dividido en dos tomas diarias durante 24 semanas mejoró los niveles de hemoglobina y los índices antropométricos.
La magnitud del impacto sobre la hemoglobina identificada en nuestro estudio fue consistente con una revisión sistemática de ensayos controlados aleatorizados que demuestran que la suplementación con hierro fortificado las fórmulas a base de leche aumentan significativamente los niveles de hemoglobina en los niños, con un aumento en la concentración de hemoglobina16.
Una revisión sistemática evaluó el efecto de mezclas lácteas fortificadas mostrándose que tuvo efectos mínimos sobre el aumento de peso; el riesgo de anemia se redujo en los grupos de leche fortificada y no hubo efectos significativos sobre el aumento de altura, los cambios en la composición corporal o la concentración de hemoglobina17. Otra revisión sistemática de ensayos clínicos demostró que en Asia, África y el Caribe la fortificación con micronutrientes en el hogar en comparación con ninguna intervención o placebo redujo el riesgo de anemia y la deficiencia de hierro en bebés y niños pequeños18. En contraste una revisión sistemática incluyó 24 ensayos controlados aleatorizados donde se encontró un aumento muy pequeño pero no significativo de los valores de hemoglobina con los productos lácteos enriquecidos con micronutrientes en la salud de los niños y adolescentes (5-15 años)19.
Se observó una diferencia positiva entre los grupos experimental y control al final de la intervención con respecto a los índices antropométricos. Una revisión sistemática que utilizó un producto lácteo fortificado con hierro, zinc y otros nutrientes informó efectos mínimos sobre el peso; sin embargo, se observó un pequeño aumento en comparación con el grupo de control y no se observaron efectos significativos sobre el aumento de estatura17. Nuestros resultados positivos probablemente estén influenciados por la duración de la intervención y el bajo nivel socioeconómico de la población de estudio. Tras la intervención, el peso aumentó en ambos grupos de estudio, mostrando mayores proporciones en el grupo experimental. Una posible causa del aumento más significativo en el grupo experimental podría ser que, en este grupo, la mezcla láctea fortificada con zinc ha mejorado la función biológica del sentido del gusto y el apetito20.
La absorción de hierro de los alimentos enriquecidos con hierro debe estar regulada por el estado nutricional del hierro en el niño. En este estudio, incluimos niños con riesgo de presentar anemia y niños con anemia leve para evitar el riesgo potencial de sobrecarga de hierro. La mezcla láctea fortificada se reconstituyó con agua sin alterar la biodisponibilidad de los micronutrientes21. Las mezclas lácteas administradas se fortificaron con 3,3 mg Fe y 2,1 mg Zn por cada gramo de producto lácteo. En este sentido, un estudio dirigido a determinar el efecto del zinc sobre la absorción de hierro de la leche fortificada concluye que la adición de zinc a 20 mg/L no inhibe significativamente la absorción de hierro de la leche fortificada con 10 mg/L de hierro22. Asimismo, otro estudio afirma que la relación entre hierro y zinc no debe ser mayor a dos para evitar una reducción de la biodisponibilidad del zinc. En nuestro estudio, la relación entre el hierro y el zinc fue de 1,5723.
El enriquecimiento de alimentos es uno de los métodos más efectivos para prevenir la deficiencia de hierro en los niños; por lo tanto, para su implementación se debe seleccionar un alimento específico (vehículo) que el grupo destinatario pueda consumir con mucha frecuencia. Las mezclas lácteas son un excelente vehículo para la suplementación de hierro en los niños. En este ensayo clínico, se administró a niños una mezcla láctea fortificada con hierro y zinc con buena aceptación sensorial, que estaba disponible comercialmente en Perú. Un estudio realizado en Turquía informa que la suplementación láctea con micronutrientes puede ser preferible debido a su fácil uso y bajo costo23.
La deficiencia de hierro es la principal causa de anemia en todas las edades, principalmente prevalente en niños escolares de familias pobres de Indonesia 24. En nuestro país también es más prevalente especialmente en las familias pobres de las zonas rurales5.
En cuanto a la adherencia, el vehículo utilizado para la suplementación mostró niveles adecuados de adherencia en ambos grupos de estudio. En este sentido, experiencias previas con otros vehículos utilizados para la suplementación no demostraron efecto sobre los niveles de hemoglobina. En un estudio realizado en Apurímac, Perú, la suplementación con micronutrientes administrada en sobres denominados Chispitas no encontró asociación entre el número de sobres recibidos o tomados y la anemia. Los autores concluyeron que la dispensación o ingesta de la cantidad necesaria de micronutrientes no es suficiente, pero se debe garantizar un proceso de ingesta equitativo para reducir la prevalencia de anemia. Este punto de vista debe tenerse en cuenta para mejorar esta intervención25. Los gestores sanitarios de nuestro país deben considerar que la leche fortificada podría ser una nueva alternativa para planificar políticas públicas relacionadas con la suplementación con hierro y zinc en niños por sus altos valores nutricionales y buena calidad sensorial.
Nuestro estudio tiene limitaciones, durante el seguimiento, hubo tres abandonos en el grupo experimental y ocho en el grupo control porque los niños no pudieron asistir a la escuela por problemas personales. A pesar del pequeño tamaño de la población de estudio, nuestros hallazgos son consistentes con los hallazgos de estudios anteriores. Debido al uso de una población en situación de pobreza, nuestros resultados no son generalizables a otras partes del país. Sin embargo, más estudios deberían intentar romper estas limitaciones.
En conclusión, nuestro estudio demuestra que la administración de mezclas lácteas fortificadas con hierro-zinc es una opción viable que provoca un efecto positivo en los niveles de hemoglobina en niños en edad preescolar y escolar.